噻吩并吡啶并嘧啶衍生物抗鼻咽鳞癌活性的3D-QSAR研究与分子设计
秦正龙,杨伟华,冯长君
(1.江苏师范大学 化学与材料科学学院,江苏 徐州 221116;2.徐州工程学院 材料与化学工程学院,江苏 徐州 221018)
近年来发现吡啶并嘧啶衍生物是一类具有良好抗肿瘤活性的杂环化合物,并对多种肿瘤细胞均有较强的抑制作用。噻吩并嘧啶衍生物是具有杀菌、抗过敏、除草、抗惊厥等良好生物活性的稠杂环化合物,其抗癌活性也引起了人们的重视。基于药效团叠加原理,把噻吩并嘧啶、吡啶并嘧啶合成在同一分子中,将会展现出良好的抗肿瘤活性。据此,王胜红等[1]虽然合成了25个新的化合物(简称“噻吩并吡啶并嘧啶衍生物”),并以四甲基偶氮唑蓝(Methylthiazoletrazolium,MTT)法测定了这些化合物的抗鼻咽鳞癌细胞CNE2活性,但尚未给出此活性的数学模型。
研究结构与性能之间数量关系的学科,称为物质构效学[2-7]。狭义的物质定量构效关系(Quantitative structure-activity relationship,QSAR)研究化合物分子结构与生物活性之间的因果关系,揭示其量变规律,并利用规律估算与预测活性,以及探讨生物作用机理等[8,9]。目前主要分为二维定量构效关系(2D-QSAR)和三维定量构效关系(3D-QSAR)[6],后者引入分子的三维空间构象,通常能够获得更优的QSAR模型。上述方法已在化学、药学、医学、环境科学等领域得到广泛应用[2-14]。本文采用比较分子力场分析(Compara-tive molecular field analysis,CoMFA)方法[10-14]建立噻吩并吡啶并嘧啶衍生物抗鼻咽鳞癌活性[1]的3D-QSAR模型,以揭示影响抗癌活性的微观结构因素,探讨其体外抗肿瘤作用的分子机理。
1 研究方法
1.1 数据来源
王胜红等[1]合成的25种噻吩并吡啶并嘧啶衍生物分子的基本结构见图1。其中取代基R1、R2为分子中可变部分,具体分子结构见表1。王胜红等[1]测定抗鼻咽鳞癌细胞的半数抑制浓度以“IC50”表示,单位为μmol·dm-3。
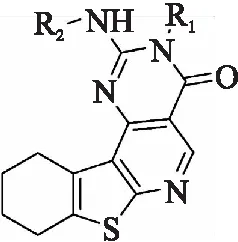
图1 噻吩并吡啶并嘧啶衍生物分子的基本结构图
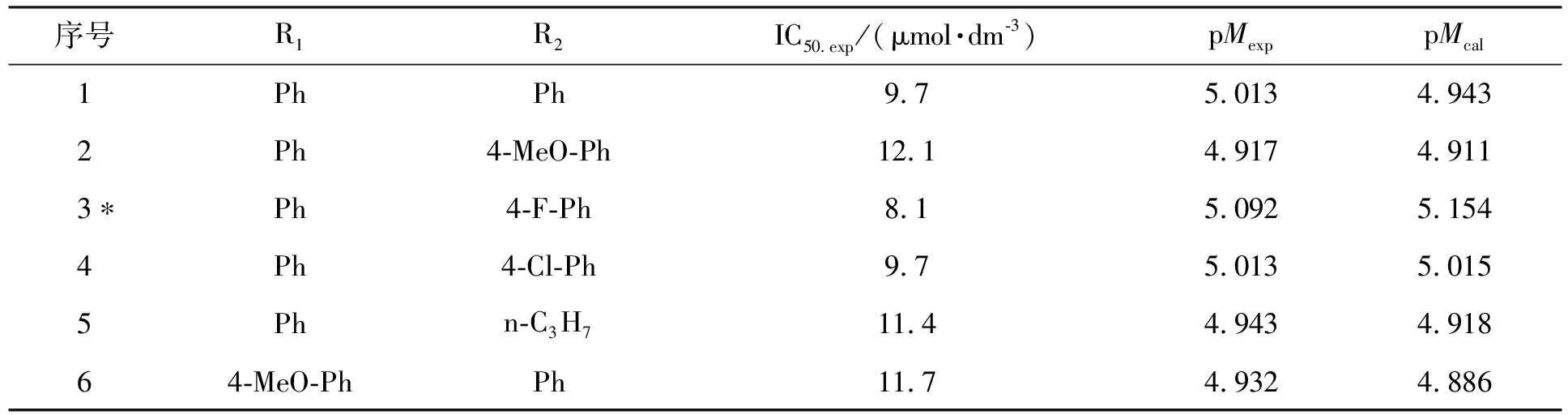
表1 噻吩并吡啶并嘧啶衍生物分子结构与抗鼻咽鳞癌活性(pM)表
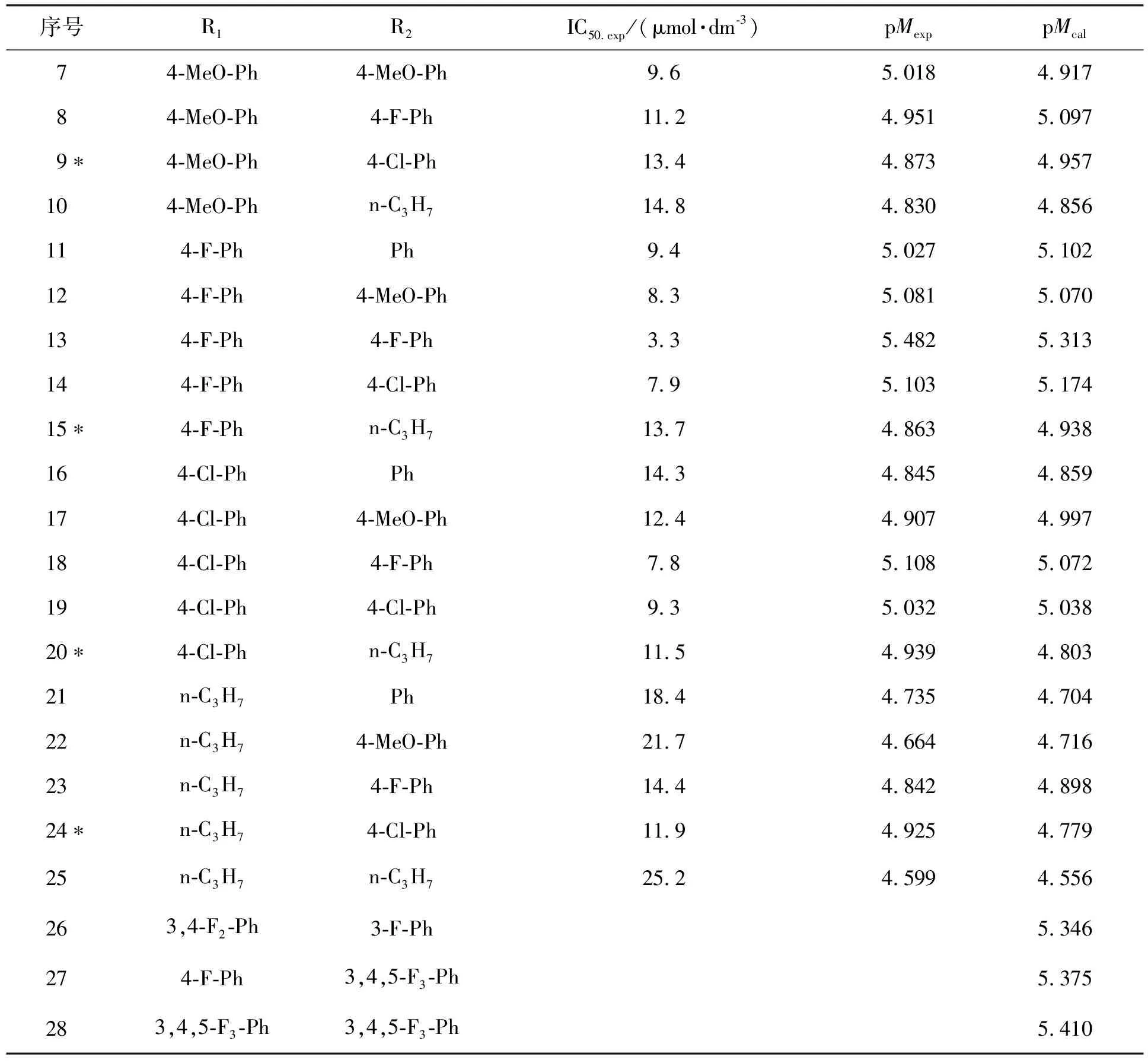
续表1
考虑化学反应自由能变与平衡浓度为对数关系[15],故令
pM=-lg(IC50/mol·dm-3)
(1)
它们的IC50及pM数据见表1。
1.2 建模方法
本文使用Tripos公司Sybyl-x2.0分子模拟软件完成3D-QSAR[10-14]分析,使用的模块包括Sketch、Minimize、Database-alignment以及QSAR等,各项参数除特别指明外均采用缺省值。
1.2.1 确定化合物的活性构象及分子叠合
分子的最低能量构象可以用来代替其药效活性构象。使用Sybyl-x2.0软件中的Sketch molecule模块先构建25个噻吩并吡啶并嘧啶衍生物分子以及新设计3个分子的初始三维空间结构。然后,通过Minimize模块,选取Tripos力场,加Gasteiger-Huckel电荷,将最大迭代次数(Max iterations)定为1 000,将Gradient降低到0.005等,对上述28个分子进行分子力学能量最低优化,通过全构象搜索得到能量最低构象,并以此最低能量构象作为分子叠合的生物活性构象。
按照5∶1原则,随机选取分子3、9、15、20、24,以及新设计3个分子和13号分子(模板分子),共9个分子组成测试集(Test set),为表1中带“*”的分子,余下20个分子作为训练集(Training set),亦含模板分子。所谓模板分子是指样本中生物活性最强的分子。Align database模块基于原子契合的公共骨架叠合方式,尽量保证所有分子取向一致,使分子间相互重叠的均方根偏差最小。运用Align database模块,以13号分子中的公共骨架,分别对训练集、测试集进行叠合。训练集的叠合图见图2。测试集的叠合图与其非常相似不予列出。
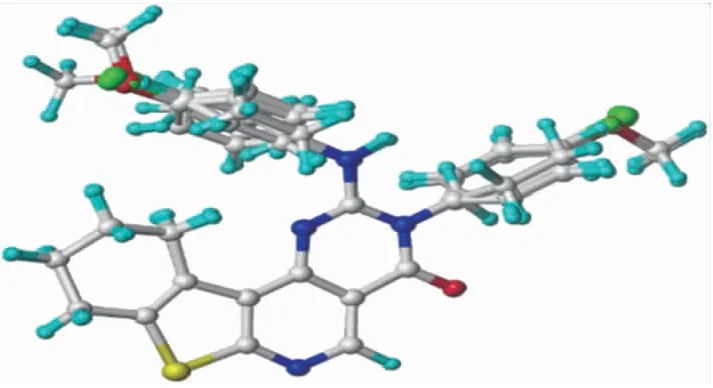
图2 训练集的三维叠合图
1.2.2 建立CoMFA模型
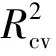
2 结果与讨论
2.1 CoMFA模型
训练集的CoMFA模型:
(2)非交叉验证部分R2=0.853>0.8,显示良好的拟合性[18]。R2又称为削减误差比例,意为该模型包含影响噻吩并吡啶并嘧啶衍生物抗鼻咽鳞癌活性85.3%的因素,仅有不足14.7%属于未知因素。
(3)在95%可靠性下,F临界值F0.05(4,15)=3.06。该模型的F=21.79,是其临界值的7倍多,表明模型为密切相关。该模型具有较低的估计标准偏差SE,仅为0.081。利用训练集模型的外部预测能力对测试集中分子的pM计算值进行衡量。测试集的pM预测值见表1,与相应实验值基本吻合,其平均绝对误差只有0.101,显示良好的预测能力。
2.2 CoMFA等势图
图3为以训练集中抗鼻咽鳞癌活性最高的13号分子为模板建立的CoMFA模型的三维等势图。

图3 13号分子的CoMFA模型的三维等势图
图3(a)为立体场等势图,在R2中苯环的4-位及R1中苯环的3-位各有1个较大绿色区域,在此区域引入较大体积的基团,有助于提高噻吩并吡啶并嘧啶衍生物抗鼻咽鳞癌活性。在R1相同时,R2为4-Cl-Ph、-Ph、n-C3H7的体积依次减小,其pM逐渐增大。例如:pM按化合物序号14>11>15,24>21>25递降。图3(a)中有3个黄色区域,由于它们离苯环较远,对噻吩并吡啶并嘧啶衍生物抗鼻咽鳞癌活性影响很弱,可以不考虑。
图3(b)为化合物周围的静电场分布,在2个苯环的4-位各有1个较大的红色区域,在此区域引入带负电荷的基团对活性有利。在R1相同时,4-F的吸电子能力比4-Cl强,其pM亦是4-F较强。例如3与4、8与9、13与14、18与19、23与24,均是前者pM大于后者。在R2中苯环的3-位有个蓝色区域,此区域内增大基团正电性有利于抗鼻咽鳞癌活性增强。
3D-QSAR模型显示立体场对pM的贡献稍强于静电场,依次为53.7%和46.3%。由于CoMFA的立体场包含疏水性和空间位阻,静电作用一般包含库仑力、氢键及配位。因此,影响pM的主要作用力是分子的疏水性和空间位阻,而库仑力、氢键及配位稍弱,即噻吩并吡啶并嘧啶衍生物分子与鼻咽鳞癌细胞靶标作用的基元反应中,疏水性和空间位阻是影响反应速率的决定因素,而库仑力、氢键及配位作用为非控速因素。
2.3 分子设计
QSAR研究目的之一是根据所建模型中隐含的影响生物活性的主要结构信息进行分子设计。由2.2节分析可知,在R1、R2中苯环的4-位上引入大体积的负电性基团,有利于增强噻吩并吡啶并嘧啶衍生物的抗鼻咽鳞癌活性。据此设计3个化合物(表1中第26~28号化合物),3D-QSAR模型给出较大的pM预测值,为5.346~5.410,均优于13号分子pM预测值(5.313)。这3个分子的抗鼻咽鳞癌活性,有待生物医学实验确认。
3 结束语
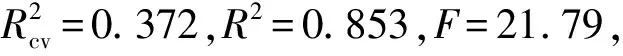
(2)CoMFA模型三维等势图显示影响抗鼻咽鳞癌活性(pM)的主要因素是取代基的疏水性和空间位阻,其次是取代基的库仑力、氢键及配位。
(3)CoMFA模型三维等势图显示,在R1、R2中苯环的4-位上引入大体积的负电性基团,有利于增强噻吩并吡啶并嘧啶衍生物的抗鼻咽鳞癌活性。据此设计的3个化合物,具有良好的抗肿瘤活性,有待生物医学实验确认。

