氮硫掺杂石墨烯量子点荧光探针测定葡萄酒中铜离子的含量
邱競瑶,何 岗,李 欣,白文凤**,金 丽*,张建坡*
(1.吉林化工学院 化学与制药工程学院,吉林 吉林 132022;2.吉林石化公司 精细化学品厂,吉林 吉林 132021)
铜(Ⅱ)是哺乳动物所需营养中最重要的微量元素之一,正常人体铜的总含量约为100~150 mg[1],每天摄入1.5-2.0 mg铜是必不可少的.但是,如果大量摄入并堆积在组织中,反而会对人体产生毒性,通常测定血清和尿液中的铜水平可用于某些疾病的早期诊断.目前有多种方法可检测铜或者铜离子[2-4],但是大部分检测方法存在灵敏度低的问题,因此,最近发展起来的荧光检测方法由于其操作简便、成本低等优点而备受关注.制备具有优良发光性能的荧光探针是提高传感器性能的关键,故而各类荧光发光材料(量子点、氨基酸、有机发光材料、稀土等[5-9])被相继报道.
石墨烯是一种以sp2杂化连接的碳原子形成的厚平面片层二维(2D)晶体结构材料,由于其非凡的性能和潜在的应用而引起了广泛的关注.理论上,原始石墨烯的零光学带隙可防止其发出光,但将零能带石墨烯切割成纳米带时,它呈现出令人难以置信的边缘效应和量子限制,这些物理特性也适用于石墨烯量子点(GQDs),并且随着其尺寸的减小,性能会变得更强.除此之外,GQDs还具有其他出色的化学和物理特性,可应用于光学、生物、能量、电化学、催化和光伏设备[10-15].当在材料中掺杂杂原子时,如:硼(P)、氮(N)、氟(F)和硫(S),可有效修改电子密度、提升光化学性能[16],并显示出半导体的特性和更优的光吸收率.本论文以氮硫掺杂石墨烯量子点(N,S-GQDs)作为荧光探针,探讨了铜离子与其的相互作用,并通过优化实验条件、机理讨论、干扰离子分析和实际样品分析,开发出了一种新的定量分析铜离子含量的方法.
1 实验部分
1.1 试剂与仪器
硫酸铜购于国药集团化学试剂有限公司.N,S-GQDs为自制.所有试剂均为分析纯,使用前未做任何处理.水为双蒸水(>18 MΩ·cm).
采用天津港东的F-280荧光分光光度计测得荧光发射光谱,以氙灯为光源,比色皿宽度1 cm.
1.2 实验过程
N,S-GQDs与铜离子的相互作用:用移液枪取一定量的N,S-GQDs和缓冲溶液(pH=7)于离心管内,最终体积为2 mL,摇匀.倒入石英荧光比色皿中,然后放入荧光分光光度计中,测出其荧光强度F0.接着,向离心管中依次加入10 μL的被分析溶液,充分摇匀,测其荧光强度F.记录并保存上述数据,计算荧光强度变化.
2 结果与讨论
2.1 优化实验条件
不同时间和pH对铜离子和N,S-GQDs体系的猝灭作用的影响如图1~2所示.反应时间在2 min后,随着时间的推移,F0/F(F0表示未添加铜离子的荧光强度,F表示添加铜离子后的荧光强度)值几乎没有变化,故反应时间选择在2 min.查表可知Cu(OH)2的Ksp=2.2×10-22,计算得出铜离子在pH=7.77时开始产生沉淀.由图2可知pH=4时,N,S-GQDs处于酸性条件,体系不太稳定;当pH=7时,Cu2+对N,S-GQDs的猝灭程度最大,这也与上述计算条件相符,因此选择pH为7作为实验最佳pH进行进一步的应用.
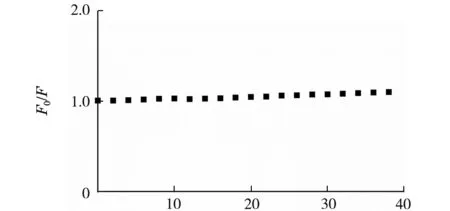
t/min图1 时间对铜离子和氮硫掺杂石墨烯量子点体系荧光强度的影响
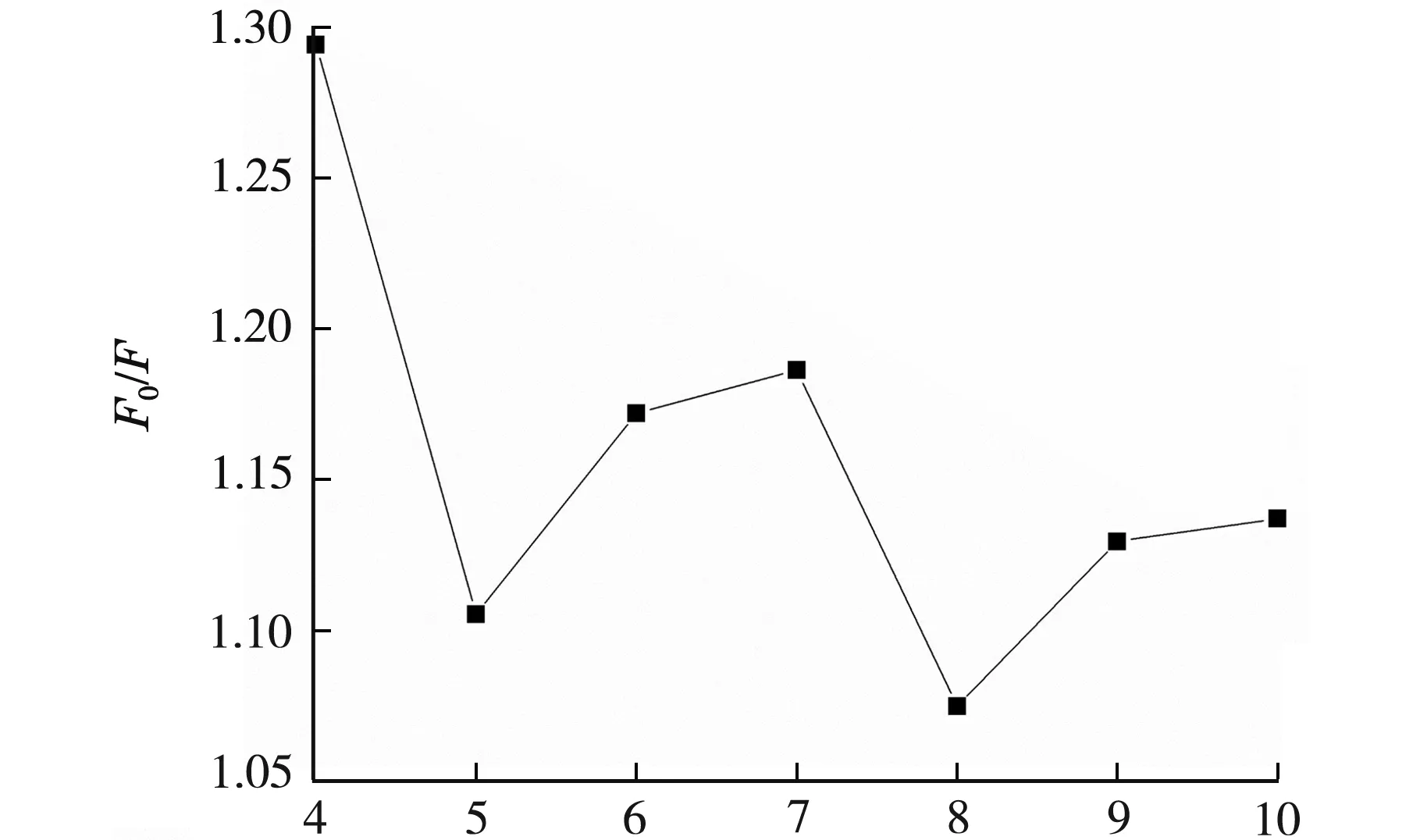
pH图2 pH对铜离子和氮硫掺杂石墨烯量子点体系荧光强度的影响
2.2 检测范围与检出限的测定
在最佳实验条件下,将不同浓度的Cu2+添加到2 mL的缓冲溶液(pH=7)和260 μL N,S-GQDs混合液中,随着铜离子浓度的增加,N,S-GQDs的荧光发射强度逐渐降低,如图3所示.
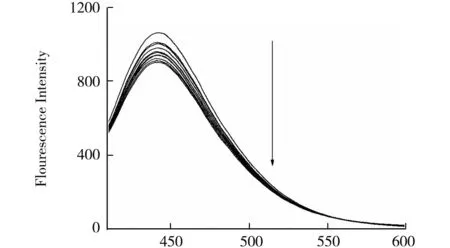
Wavelength/nm(a) N,S-GQDs的荧光强度变化关系图
当铜离子浓度在0.02~0.2 mmol·L-1(即0.004 4~0.044 g·L-1)范围内,铜离子浓度和N,S-GQDs荧光强度变化之间呈线性,其线性方程为F0/F=0.874 8[C]+1.335 9,检出限为0.032 27 mmol·L-1.研究发现铜离子的检测范围和检出限具有可调性.铜离子浓度为0.006~0.2 mmol·L-1(1.327~4.425 mg·L-1)范围内,线性方程为F0/F=4.313 8[C]+1.022,其相关系数R2=0.996 2,检出限为0.973 6 μmol·L-1;在0.2~2.0 μmol·L-1(即0.0442 5~0.442 5 mg·L-1)范围内,线性方程为F0/F=0.047 3[C]+1.002,其相关系数R2=0.991,检出限为0.118 0 μmol·L-1;在0.02~0.2 μmol·L-1(即0.004 425~0.044 25 mg·L-1)内线性方程为F0/F=0.634 9[C]+0.996 9,其相关系数R2=0.997 8,检出限为5.859 nmol·L-1;进一步稀释铜离子浓度,在0.004~0.02 μmol·L-1(即0.885 0~ 4.425 μg·L-1)内呈线性范围,F0/F=4.397 8[C]+0.993,其相关系数R2=0.963,最低检出限为2.708 nmol·L-1,如图4所示.说明了铜离子对该体系的检测范围具有可调性,并可根据测试要求调节检测范围.
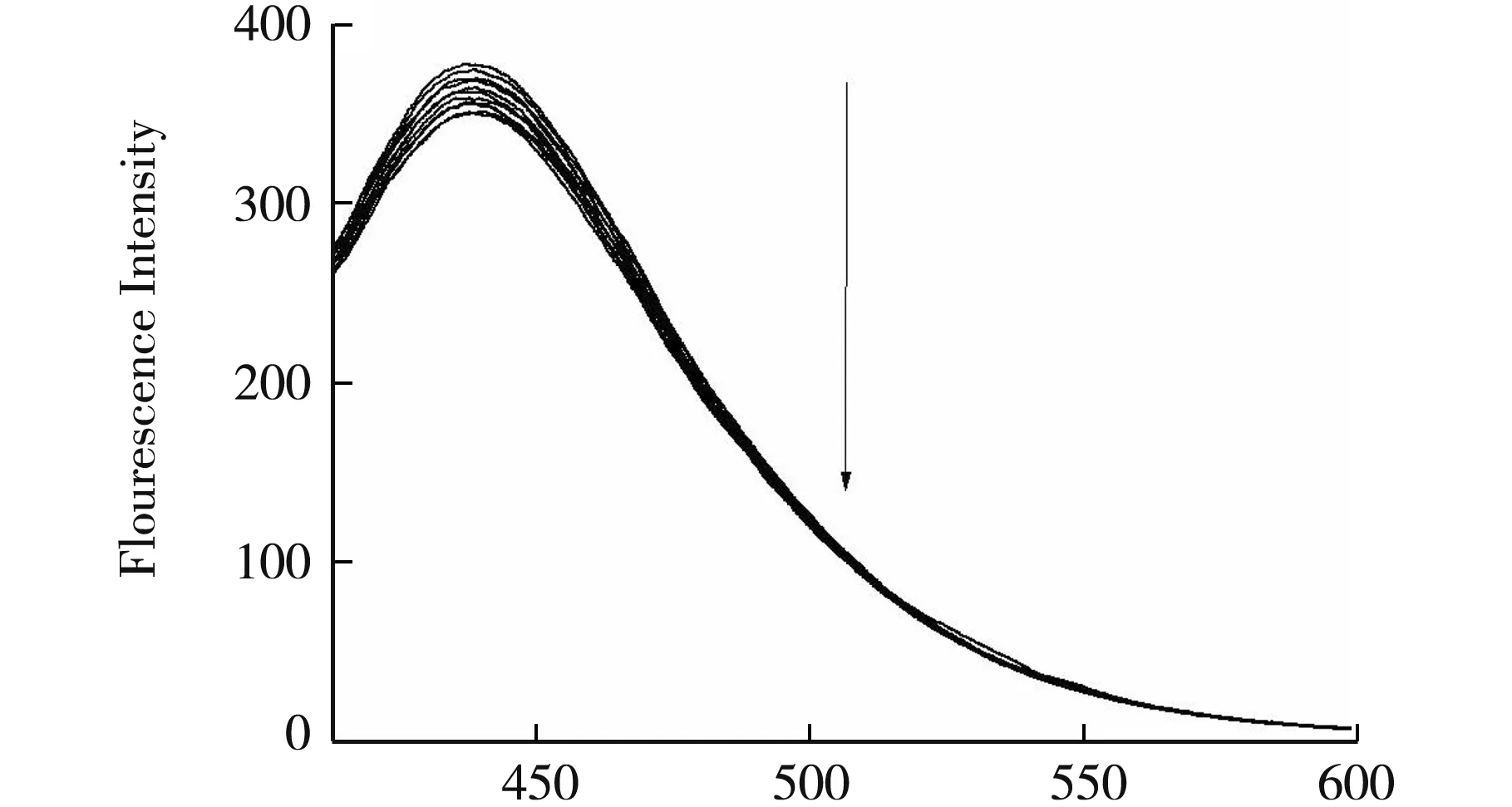
Wavelength/nm(a) N,S-GQDs的荧光强度变化关系图
2.3 实际样品的检测
为了进行实际样品分析(葡萄酒中铜离子含量),研究了Ca2+、K+、Na+、葡萄糖和乙醇对检测荧光系统的影响.如图5所示,可以看出上述物质对体系的干扰很小,而实际样品中其含量都很低,故可以忽略不计,可以应用于实际样品分析.
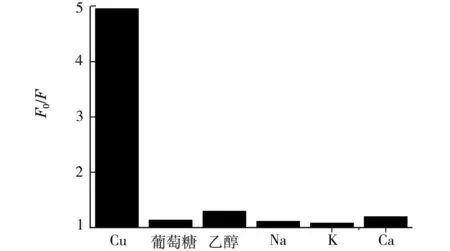
Interfering Substance图5 各种离子对猝灭体系的荧光强度影响
采用标准加入法对实际样品(葡萄酒)中铜离子含量进行了分析.向葡萄酒样品中加入氮硫掺杂石墨烯量子点和一系列浓度的铜标准溶液(0.02~0.2 mmol·L-1),测得荧光光谱,以F0/F为纵坐标,以铜离子的浓度为横坐标,绘制工作曲线.F0表示单纯N,S-GQDs的荧光强度,F表示加入铜离子和样品后的荧光强度,线性关系式为F0/F=0.640 6[C]+1.004.
而由之前的实验可知,相同铜标准溶液的回归方程为F0/F=0.634 9[C]+0.996 9,二者联立,同时使F0/F=0,分别带入对应的关系式,可以得出待测溶液此时含有的铜离子浓度为1.567 3 μmol·L-1,而0.001 g·L-1的铜离子标准液对应的铜离子浓度为1.570 1 μmol·L-1,由此可以得出葡萄酒中的铜离子含量应为2.8 nmol·L-1.经过3次重复实验后,可以计算出其回收率在102.4%~113.7%,如表1所示,说明该方法可以应用到实际样品分析中.平行测定11次空白样(不添加Cu2+)的荧光强度,发现RSD=0.2%,说明该实验具有良好的精密度.
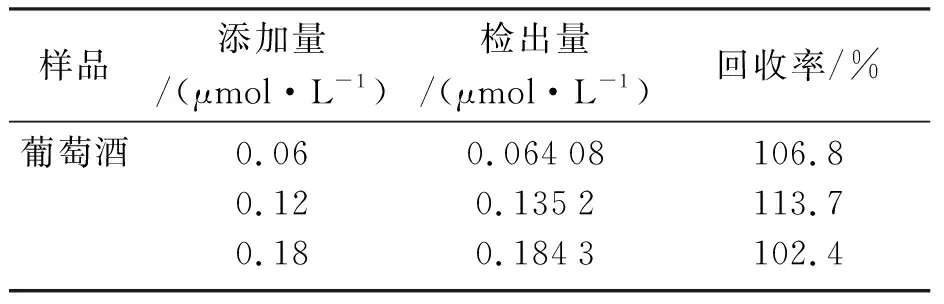
表1 葡萄酒中铜离子含量分析
2.4 铜离子对氮硫掺杂石墨烯量子点体系荧光猝灭的反应机理
许金钩将荧光猝灭过程分为动态和静态猝灭过程[14].动态猝灭过程是基于猝灭剂与激发态荧光材料之间的碰撞作用,静态猝灭过程是猝灭剂与荧光材料之间形成了非发光基态配合物.动态和静态猝灭均符合Stern-Volmer方程F0/F=1+Kqτ0[C]=1+Ksv[C],Kq为荧光猝灭速率常数,它反映了该体系的相互扩散和相互碰撞的反应效应,Ksv是猝灭常数(标准曲线线的斜率).Kq=Ksv/τ0,τ0为无猝灭剂的荧光分子的平均荧光寿命.
如图6所示,N,S-GQDs荧光强度的变化F0/F与Cu2+浓度具有良好的线性关系,斜率(Ksv)随着温度的升高而减小,这符合静态猝灭过程的特点.静态猝灭过程主要是因为分子之间形成了复合物,随着温度的增加,复合物的稳定性降低,猝灭率也减小,斜率也逐渐变小,所以高温Ksv比低温Ksv小,根据Kq=Ksv/τ0(N,S-GQDs的平均荧光寿命为τ0=(5.05 ns)的方程,在293、303、313 K处的Kq分别为3.02×1013、2.269×1013、1.809×1013mol·L-1·s-1,明显比2×1010mol·L-1·s-1(最大动态猝灭常数)大,这也符合动态静态过程的特点.
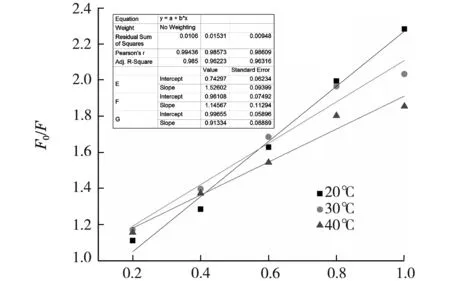
The consentration of Cu2+/(mmol·L-1)图6 不同温度下猝灭体系荧光强度变化拟合图
3 结 论
基于铜离子浓度与N,S-GQDs荧光强度变化之间的线性关系,以N,S-GQDs为荧光探针,建立了一种定量分析铜离子含量的方法,并对反应机理进行了详细讨论,证明铜离子引起的猝灭为静态猝灭过程.通过改变N,S-GQDs的浓度,该检测方法的检测范围具有可调性,可以适应不同浓度样品的分析.并应用该方法对葡萄酒中铜离子的含量进行了分析,计算出其回收率为102.4 % ~ 113.7%,RSD=0.2%,说明该实验具有良好的精密度.

