急性心肌梗死合并室间隔穿孔的诊治及预后分析
张良 徐涵 王珏
室间隔穿孔(ventricular septal rupture,VSR)是急性心肌梗死(acute myocardial infarction,AMI)后一种潜在并发症,由急性梗死区域室间隔心肌缺血导致。VSR一旦发生,可引起严重的血流动力学改变,进而导致心力衰竭、恶性心律失常等严重后果,许多患者因此丧失手术修补时机而导致短期内死亡[1-3]。AMI的溶栓治疗数据表明,VSR的发生率为0.2%[4]。目前VSR主要有3种诊疗方案:药物保守治疗、内科介入性封闭治疗以及外科开放性手术治疗。应用血管活性药物可以减少心腔血液机械性的左向右分流,从而增加心输出量,但同时会导致平均动脉压(mean arterial pressure,MAP)降低及冠脉血流量减少的严重后果。随着介入技术的发展,内科介入性封闭治疗也是可选择的方法[5],但由于目前内科介入性封闭治疗的患者数较少,其安全性及对心功能的改善效果仍有争议。外科开放性手术治疗被认为是VSR的标准治疗方法[6-7],目前指南建议无论血流动力学状态如何,均应紧急关闭VSR,但部分学者认为外科手术修补应在AMI后4~6周进行[8],即待坏死组织逐渐形成瘢痕后再行修补。本研究分析AMI合并VSR患者的临床特征,比较其治疗方式及预后情况,现将结果报道如下。
1 对象和方法
1.1 对象 选择2006年12月至2020年5月温州医科大学附属第一医院收治的AMI合并VSR患者37例,其中男 19 例,女 18 例,年龄 50~87(72.3±9.8)岁。根据患者接受治疗出院后30 d内生存情况,分为存活组7例和死亡组30例。存活组男4例,女3例,年龄52~76岁,中位年龄65岁;死亡组男15例,女15例,年龄50~87(74.0±9.7)岁。存活组年龄小于死亡组,差异有统计学意义(P<0.05)。纳入标准:(1)AMI参照世界卫生组织的诊断标准:典型胸痛持续时间达30 min;相邻2个导联ST段抬高超过1 mm;心肌酶水平明显升高。(2)VSR诊断标准:胸骨左缘第3~4肋间听诊可闻及响亮的全收缩期杂音,偶可扪及震颤;超声心动图检查显示室间隔回声连续性中断,由左向右分流,需除外腱索断裂;左心室造影发现VSR,对比剂从左心室分流至右心室[9]。排除标准:(1)合并先天性心脏病、动静脉畸形、重度瓣膜病;(2)合并恶性肿瘤;(3)存在认知功能障碍及神经系统病变。本研究经医院医学伦理委员会审批同意(批准文号:2018-066)。两组患者均签署知情同意书。
1.2 方法
1.2.1 治疗方法 均给予AMI规范药物治疗,包括阿司匹林、氯吡格雷抗血小板治疗,低分子肝素抗凝,他汀类药物调脂;根据血流动力学情况,选择性应用血管紧张素转换酶抑制剂、血管紧张素受体阻滞剂、β受体阻滞剂、正性肌力药等。同时根据患者病情及意愿选择相应的治疗方式,包括主动脉内球囊反搏(intraaortic balloon pump,IABP)支持治疗、内科介入性封闭治疗、外科开放性手术治疗等。
1.2.2 两组患者一般资料的收集 收集两组患者吸烟史、高血压、糖尿病、MAP、WBC、TBil、尿酸、肌酐、脑钠肽(brain natriuretic peptide,BNP)、肌钙蛋白、肌酸激酶同工酶(creatine kinase isoenzyme,CK-MB)、左心室射血分数(left ventricular ejection fraction,LVEF)、左心室舒张末期内径(left ventricular end diastolic diameter,LVEDd)、超声 VSR 直径、梗死部位、Killip分级、AMI至确诊VSR的时间、是否合并室壁瘤、是否应用IABP以及是否行外科开放性手术治疗等。
1.2.3 AMI血管分支闭塞情况及VSR特点的分析 结合心电图(上海光电ECG2250心电图机)及冠脉造影(荷兰飞利浦FD10数字血管造影机)结果,判断AMI血管分支闭塞情况。结合超声心动图(美国GE Vivid E9型超声诊断仪,探头频率2.0~4.0 MHz)及术中检查,分析VSR特点(包括穿孔位置、个数、是否合并心脏破裂、穿孔直径、发生穿孔时间等)。
1.2.4 死亡组病例分析 对死亡组病例的年龄、MAP、TBil、WBC等进行多因素logistic回归分析,判断死亡病例的独立危险因素。
1.2.5 随访 根据是否进行外科开放性手术治疗分为手术患者8例和非手术患者29例,随访方式包括电话随访、门诊复查等,以患者死亡为终点事件,比较两组患者500 d生存率。
1.3 统计学处理 采用SPSS 25.0统计软件。正态分布的计量资料以表示,组间比较采用两独立样本t检验;偏态分布的计量资料以M(P25,P75)表示,组间比较采用秩和检验;计数资料组间比较采用χ2检验;多因素分析采用logistic回归;用Kaplan-Meier法绘制生存曲线,组间比较采用log-rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 死亡组患者基本情况 死亡组30例患者中,采用单纯药物保守治疗25例(83.33%),药物治疗同时应用IABP支持治疗3例(10.00%);内科介入性封闭治疗后发生感染性休克1例(3.33%);外科开放性手术治疗后发生心源性休克1例(3.33%)。
2.2 两组患者一般资料比较 存活组患者WBC、TBil、KillipⅢ~Ⅳ级比例均低于死亡组,MAP、外科手术治疗比例均高于死亡组,差异均有统计学意义(均P<0.05),两组其他指标比较差异均无统计学意义(均P>0.05),见表1。
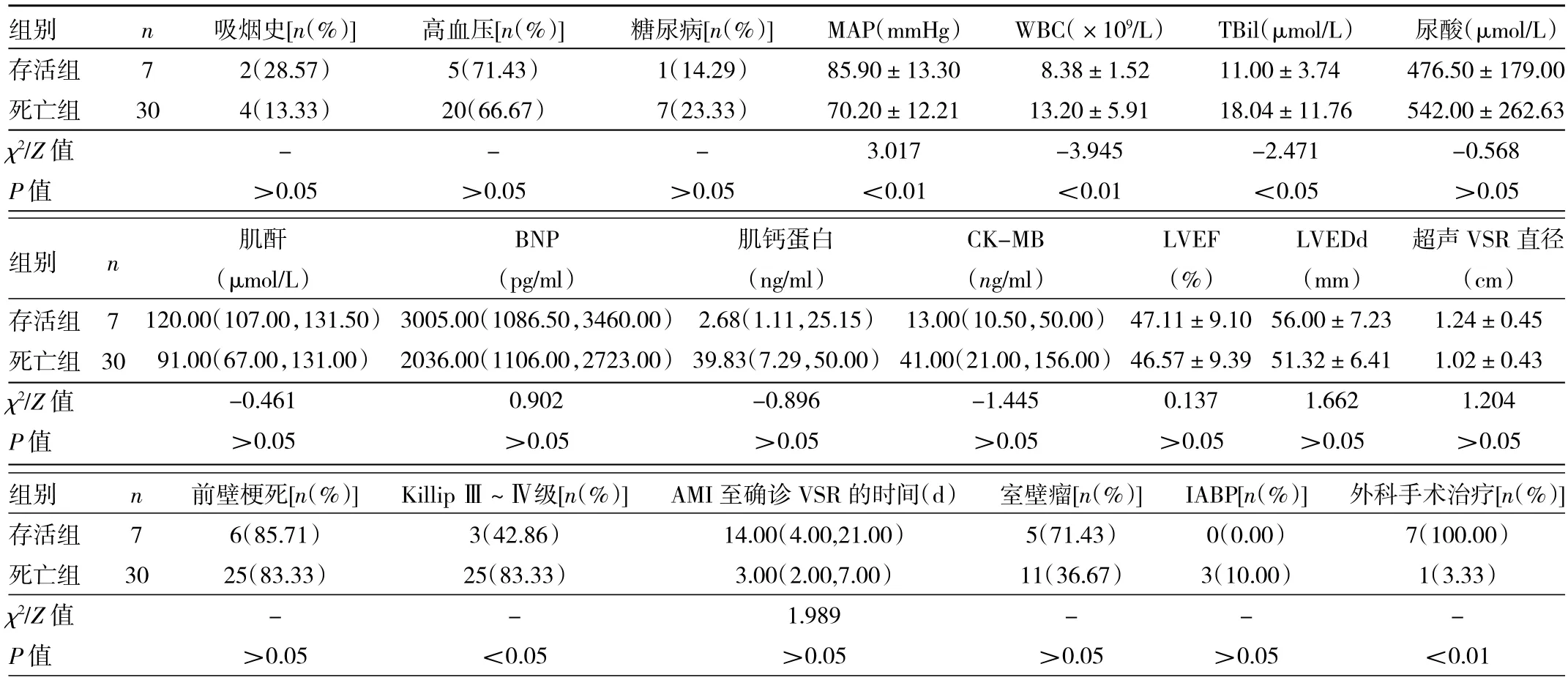
表1 两组患者一般资料比较
2.3 AMI血管分支闭塞情况及VSR特点 37例患者中,12例(32.43%)完成冠状动脉造影和左心室造影,其中罪犯血管为前降支11例(91.67%),右冠脉1例(8.33%)。VSR位于室间隔近心尖部26例(70.27%),后间隔10例(27.03%),肌部 1例(2.70%)。室间隔多个穿孔 2例(5.41%),其中合并心脏破裂1例(2.70%);VSR 直径范围为(10.0±0.3)mm,其中,5~10 mm 22例(59.46%),>10 mm 13例(35.14%),<5 mm 2例(5.41%)。AMI后24 h内发生穿孔者6例(16.22%),2~7 d内发生穿孔者21例(56.76%),>7 d发生穿孔者10例(27.03%)。
2.4 死亡组患者危险因素分析 年龄和WBC是患者30 d内死亡的危险因素(均P<0.05),见表2。
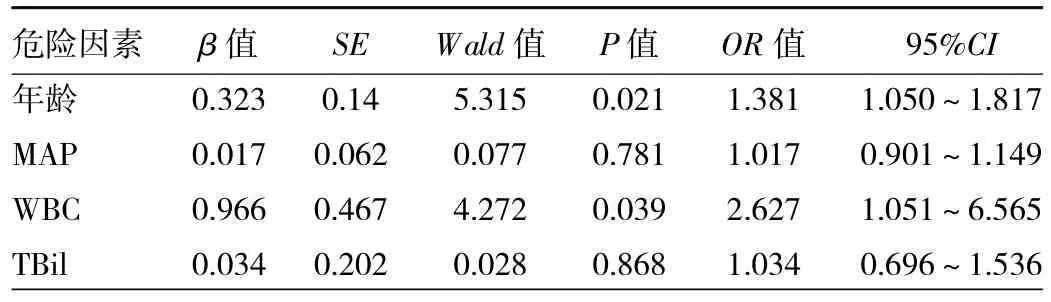
表2 死亡组患者危险因素分析
2.5 手术患者与非手术患者生存率比较 手术患者的500 d累计生存率(87.5%)明显高于非手术患者(0.00%),差异有统计学意义(P<0.01),见图1。
3 讨论
AMI合并VSR因其较大的血流动力学改变,会很快导致右心衰竭以及心源性休克,因此在循环的稳定方面显得尤为重要,必要时需联合IABP治疗[10]。在临床中采取及时有效的外科手术治疗,实施有针对性的治疗方案以及合理的循环和呼吸支持可较大程度地降低该疾病的死亡风险。随着溶栓和介入技术的发展,AMI合并VSR的发生率有了显著下降[4],但是目前尚无关于建立适用性标准的共识,该方案对于患者的选择性较高,VSR孔径大小可能相差很大,且经常存在多个VSR,当前的介入封堵方案未能减少分流导致的严重结果。
本研究37例患者中有11例完成了冠脉造影,罪犯血管多为前降支,未能建立良好的侧支循环,导致梗死面积较大。目前比较一致的认同VSR相关因素有:女性、高血压、高龄、前壁或大面积梗死、无侧支循环等[11]。本研究的37例患者平均年龄(72.3±9.8)岁,其中合并高血压25例,前壁梗死31例,这与较高的VSR发生率相一致。药物保守治疗的效果差,患者病死率极高,本研究中25例单纯保守治疗的患者均在短期内死亡。据文献报道仅仅采取药物保守治疗病死率1 d内为24%,7 d内为46%,2个月内高达67%~82%,不能逆转左心室向右心室分流的结果,患者因为病情急剧恶化而导致心功能衰竭甚至死亡。本研究中1例患者行室间隔缺损伞堵术后仍有束宽5~6 mm的分流,后发生感染性休克伴心源性休克而死亡。但是介入性封闭可以避免或延迟手术修复,从而可为高危VSR患者提供可能挽救生命的方法。
美国胸外科医师学会的数据统计提示,不同时间手术者病死率差异较大。在穿孔后7 d内接受手术的患者病死率为54.1%,而7 d后则为18.4%[12]。延迟手术使结局改善可能与心肌梗死的发展和组织稳定性的改善相关,这种延迟为心脏修复提供了充足的时间,而早期手术通常是针对血流动力学不稳定和循环异常的个体进行的妥协,许多患者因存在严重心力衰竭和器官功能障碍的风险而无法推迟手术,在这些情况下诊断出VSR后立即手术是合乎逻辑的。此外,对于仅发生血流动力学受损的患者,可以考虑在术前使用心室辅助装置、IABP来推迟手术。因此,临床医生必须权衡早期手术的已知风险与推迟手术后病情恶化的未知风险。
针对本研究的8例手术患者,术者均采用梗死区域隔绝旷置的方法,即应用心内补片将梗死区域旷置,同时保持心室的几何结构。在VSR早期,由于发生炎症的组织水肿明显,加之坏死的心肌组织缝合困难,直接修补往往达不到预期效果。对于前部缺损,选择将补片固定于缺损下方正常的室间隔及前侧方正常的心内膜上;对于后部缺损,将补片固定于二尖瓣环、正常的室间隔及左心室后壁,范围直达后乳头肌的边缘并加用垫片。除了术中撕脱的坏死心肌以外,对梗死心肌不做过多清除,防止术后低心排以及室间隔再次破裂,也可避免脆弱的心肌组织张力过大降低术后出血的概率。
总之,目前认为AMI合并VSR的整体预后仍较差,及早发现并监测梗死区域的发展,动态观察穿孔的发生,在条件允许的情况下积极完善冠脉造影,尽可能实现循环及呼吸支持,在血流动力学指标恶化前施行手术修补,才能降低该病发生、发展的风险。

