改良Kraske术治疗巨大骶前囊肿(附1例报告)
严美悦, 杨向阳, 戴亭亭, 张书信, 李京向
(北京中医药大学东直门医院肛肠科,北京 100700)
骶前囊肿是生长在骶骨和直肠间隙内的囊性肿物,临床发病率低,以女性为主,约占70%以上[1-2]。早期多无明显症状。当囊肿体积进一步增大,可出现邻近脏器的压迫症状,且伴随较高的感染风险。故其治疗应以彻底切除为原则[3]。骶前囊肿的位置特殊,邻近组织结构复杂,手术入路方式的选择对于结局影响较大[4]。本文结合我院1例巨大骶前囊肿的临床诊疗过程,探讨改良Kraske术经骶尾后入路手术方案的临床疗效,为临床术式的选择提供参考,结合相关文献及治疗经验进行介绍。
病例:男,59岁,因排便困难1年余,近期明显加重而入院。病人自诉1年前出现排便困难,无便血、无里急后重等症状,未见明显诱因,未予治疗。入院前症状明显加重,排便时长半小时以上,需甘油辅助排便,量少质硬。口服通便药物(具体不详)效果不明显。无腹胀、腹痛、发热,饮食和睡眠正常。小便澄清、色淡黄,每天尿量1 000~1 500 mL。本院东区于2017年11月8日CT检查提示:骶前巨大囊性病变,体积9.1 cm×9.6 cm×10.0 cm,增强CT扫描无强化,边界清楚,直肠受压向前移位,局部与肿块分界不清。既往有慢性肾炎、肝囊肿、肾囊肿、二尖瓣关闭不全、前列腺增生病史。否认手术、药物过敏及家族遗传病史。入院后腹部体格检查:未见明显阳性体征,侧卧位查看肛周皮肤,未见肛瘘、肛裂,未见红肿,骶尾部外观正常,无隆起及包块,无按压疼痛。肛门指诊触及直肠后壁距肛缘3 cm处巨大肿物,质韧,上极不可触及,退指指套无染血。电子肠镜检查提示距肛缘40 cm降结肠可见带蒂息肉1枚,直径约0.6 cm。电凝切除送病理检查,提示管状绒毛状腺瘤Ⅰ级。2017年11月14日盆腔增强MRI检查结果提示盆腔直肠后方10.0 cm×10.0 cm×8.5 cm占位,边缘较光滑,边界清晰,以T1、T2稍长信号为主。直肠明显受压、移位。显示腹股沟区多发肿大淋巴结影。骶尾部皮下软组织内可见条片状长T2信号。增强扫描见盆腔内直肠后方类圆形病变轻度强化(见图1、2)。

图1 盆腔矢状位增强MRI
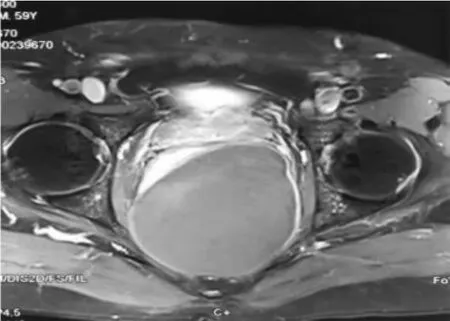
图2 盆腔横断面增强MRI
结合病人症状体征、辅助检查及专科检查,临床诊断为骶前肿物,性质待查。本例骶前囊肿巨大,占据小骨盆,压迫直肠,排便困难。梗阻趋势明显,已影响病人情绪及生活,无保守治疗可能。目前诊断明确,有手术指征。术前请骨科医师会诊,进一步明确囊肿与骶骨关系。根据CT及MRI检查,发现肿物边界较清,与骶骨粘连不明显,暂不考虑来源于骶骨。术式选择上,腹腔镜探查手术切除具有创伤小、并发症少的优点,但手术个人费用高。剖腹探查具有直视下手术、操作方便的优势,但创伤大、恢复慢、术后并发症多。骶腹联合入路虽充分暴露术野,但术中需更换体位及分步消毒,创伤大、感染风险高。骶前囊肿经骶尾后入路摘除具有不进入腹腔、创伤小、术后恢复快、并发症发生少的优点,但手术视野差、操作空间小,需截断部分尾骨以更好地暴露。综合病人经济能力、个人意愿及术后转归,遂拟行改良Kraske经骶尾后入路骶前囊肿摘除术。
病人取俯卧折刀位,全身麻醉成功后,常规消毒铺无菌巾,碘伏消毒肠腔。在距肛缘2.5 cm处沿肛门后缘弧度做弧形切口约10 cm,随后沿臀沟左侧(或右侧,该病人笔者选择左侧)约2 cm,自骶骨旁向肛门方向作约15 cm纵行切口,与前切口汇合。电刀+超声刀逐层切开,切除尾骨末段2节,以充分暴露术野。术中探察囊肿约12 cm×13 cm,占据整个盆腔,囊肿下端与直肠及提肛肌粘连紧密。解剖过程中分破囊肿下极,发现内容物为灰褐色豆腐渣样,考虑表皮样囊肿的可能性大,在示指引导下将囊皮完整剥除(见图3、4)。术中未损伤直肠,出血约100 mL。创面放置硅胶引流管,切口引出接负压引流瓶。骶尾部切口以1号减张线水平褥式间断全层缝合,4号丝线间断垂直褥式V-Y缝合皮肤切口。肿物病理检查结果为表皮样囊肿。术后予禁食禁水、肠外营养、抗感染、换药等治疗。骶前负压引流出血性液体由多到少。病人于术后第8天拆除肛周及骶尾部切口缝线及减张线。暴露骶尾部创面,拔除引流管。为预防创面感染,予康复新液浸润纱布填塞,乳酸依沙吖啶溶液浸润纱条每天湿敷换药处理。术后15 d创面肉芽组织填充,血供良好,从较多渗出及分泌物到基本无渗出,从填塞4块纱布减少至1块,并于术后24 d出院。出院2周后复查,骶尾部创面愈合良好,无相关并发症发生。术后1年电话随访,病人自诉排便症状明显改善。大便每天1次,排出通畅,余无明显不适。
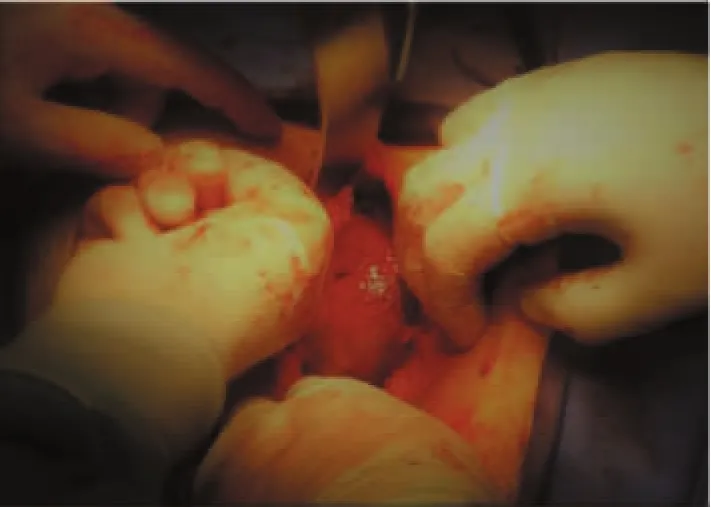
图3 术中暴露囊肿
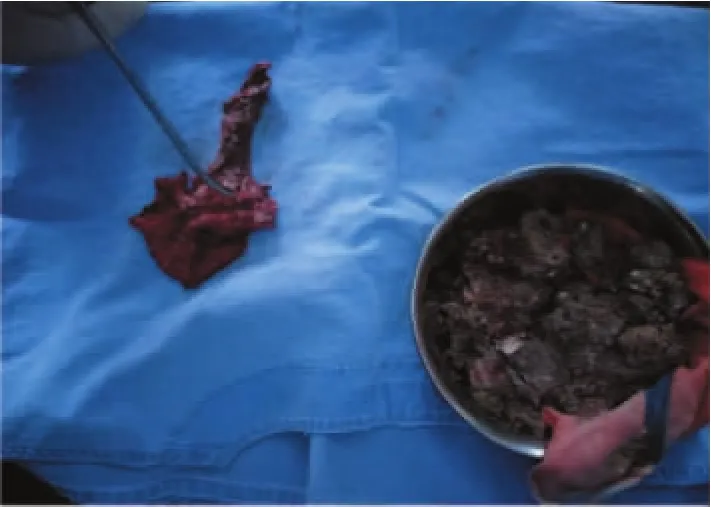
图4 囊壁及豆渣样内容物
讨论:骶前囊肿是一种成人直肠后肿瘤,多为良性病变。起病隐匿,发病率低,发展迟缓,临床症状不典型,且易发生继发感染。表现为骶尾部坠胀、隐痛或肛周瘘道,与肛周脓肿、肛瘘极相似。年轻医师首诊时由于临床经验不足,误诊率较高[5]。当囊肿体积增大时,可出现邻近脏器的压迫症状。后期囊肿合并感染时,可引起肛门、骶尾部和腰腿部不适或疼痛[6]。直肠指检为临床常规检查,是一种既简便易行而又行之有效的检查方法。文献报道该检查对骶前肿块的阳性诊断率为67%~96%[7]。影像学检查是必不可少的辅助诊断,对术前评估至关重要。据报道骶尾骨X线显示骶前钙化灶、牙齿有助于诊断。经直肠超声检查操作简便、价格低廉、阳性率高,可作为初步诊断的首选影像检查[8]。对于盆腔内肿块,CT、MRI检查的阳性诊断率为85.7%[9]。两者相比,MRI检查在骶前囊肿的术前诊断中存在一定优势,能更好地显示肿块及其周围毗邻关系,对手术入路的选择至关重要[10-11]。由于骶前囊肿位置的特殊性,其定性诊断可行性较小,且易致破裂感染、组织损伤,故不宜行穿刺细胞学检查。
骶前囊肿虽多为良性病变,但随着其体积的增大,会对周围组织产生压迫,且其感染风险较高,故应以手术切除为治疗原则。由于其位置特殊,邻近组织结构复杂,目前对于治疗骶前囊肿的手术入路有3种,即经骶尾部、经腹和经骶腹联合入路。国外学者提出以骶骨与骶前囊肿的位置关系为标准选择手术入路,若囊肿上界低于骶3平面,可采用经骶尾部入路方式[12]。国内对骶前囊肿入路的选择缺乏统一标准。国内近6年有3篇病案报道以及回顾性分析[13-17]。合计65例病人中,男11例,女54例,年龄18~74岁,直肠指检阳性诊断率为67.4%~76.9%。无明显临床症状而在常规体检中发现者为8.7%~20.0%。表现为骶尾部肿胀疼痛者为44.6%~52.2%,表现为直肠、膀胱的压迫症状,如排便困难、排尿不畅者占21.7%~23.1%,表现为肛周和(或)骶尾部的破溃流脓者占12.3%~17.4%。65例均采取经骶尾入路,其中40例切除尾骨甚至部分骶骨。术后3例切口感染,感染率为6.5%~9.1%。术后2例在1年内复发,复发率为2.2%~5.3%。近半年我院成功治疗骶前囊肿2例,均为男性,入院后MRI检查,术前请骨科医师会诊,进行肠道清洁。在脊椎麻醉下行骶尾后入路骶前囊肿切除术。术中切除部分尾骨,直视下完整剥离囊肿。这2例囊肿上界均处于S3~S4水平以下,囊肿下界均与肛缘相距5 cm以上,与国内报道基本一致。
骶尾入路在腹膜外侧进行,走行于括约肌上端,既不会造成腹腔内感染,又保护了肛门肌肉的功能。手术风险可得到有效控制,必要时切除尾骨,甚至部分骶骨。该术式又称改良Kraske术[18]。改良Kraske术野暴露较多,对于大多数骶前囊肿切除已足够。手术时可根据影像学检查确定囊肿位置,选择偏左或偏右手术切口。手术切口不推荐使用骶尾部正中直行切口,不利于皮肤愈合。建议改行旁后弧形切口,囊肿较大时可采用斜“倒 Y”形切口[19]。分离过程中应仔细辨认正常组织与病变组织的间隙。避免对机体的损伤,尽量采用钝性分离。当囊肿与直肠后壁粘连紧密时,可用示指在肛门内作引导。在游离囊肿过程中,应尽量完整切除,以防破裂而污染创面。行Kraske术切除骶前囊肿后,骶前会出现较大的残留空腔,以致骶尾局部张力大、缝合困难。对皮损较大的伤口,建议行“Z”形或 “V-Y”皮瓣覆盖缺损区域。切口张力大小是皮肤愈合的关键[20]。术后可留置负压引流管,以缩小空腔,预防感染。
采用骶尾后入路治疗骶前囊肿,具有术野显露好、操作简易、安全性高、损伤少、恢复快的优点。改良Kraske术经骶尾后入路可有效切除巨大骶前囊肿,并发症发生少,安全性高,值得临床应用。

