透视引导下逆向穿刺技术在股腘动脉硬化闭塞症治疗中的应用
牛振凯,曹立华,孙岩
(1.滨州市中医医院外科,山东滨州256600;2.山东第一医科大学附属省立医院血管外科,山东济南250021)
下肢动脉硬化闭塞症(atherosclerosis obliterans,ASO)是最常见的外周动脉疾病(peripheral arterial disease,PAD),随着人口老龄化进程的加快,发病率逐年攀升,至2020年中国PAD患者达4 113万[1]。ASO以肢体缺血为主要病理基础,可表现为肢体发凉、间歇性跛行、静息痛甚至合并溃疡,严重者需行截肢手术,影响患者的生活质量[2]。随着诊疗技术的进步,腔内治疗已成为ASO的首选治疗方案[3],其常规途径是沿血流方向顺行开通闭塞管腔,但是当股浅动脉起始端被累及时顺行开通的成功率会大大降低[4]。近年来,逆穿技术在ASO腔内治疗中的应用逐渐增多,已成为顺行开通失败的重要补救措施之一[5]。2019年3月至2021年3月我院应用逆穿技术辅助治疗ASO股(腘)动脉闭塞病变35例,效果显著,报道如下。
1 资料与方法
1.1 临床资料
选择2019年3月至2021年3月在滨州市中医医院外科应用逆向穿刺技术治疗的ASO股(腘)动脉闭塞病变患者作为研究对象。纳入标准:①符合下肢动脉硬化闭塞症诊断标准[6],且临床症状符合Rutherford分级[7]3级及以上者;②术中顺行无法开通闭塞段,或导丝位于动脉内膜下,无法返回真腔者;③术前CT血管造影或术中血管造影提示膝下动脉(胫前动脉、胫后动脉、腓动脉)至少有一支通畅。排除标准:①合并髂动脉重度狭窄、闭塞者;②病变累及双侧股总动脉,或合并腹股沟区病变无法穿刺股总动脉者;③膝下动脉(胫前动脉、胫后动脉、腓动脉)全闭塞者;④合并严重心、肺等器官功能不全,不能耐受手术者。
共35例患者纳入本研究,其中男29例(82.86%),女6例(17.14%);年龄52~76岁,平均(64.23±6.88)岁;病程6~51个月,平均(25.94±14.26)个月。患者均行术前评估,测量踝肱压力指数(ankle brachial index,ABI)以及患侧足部温度:术前ABI 0.00~0.40,平均(0.23±0.12);术前患侧足部温度29.26~34.77℃,平均(31.95±1.56)℃。Rutherford临床分级:3级10例(28.57%),4级11例(31.43%),5级13例(37.14%),6级1例(2.86%)。合并冠心病9例(25.71%),高血压13例(37.14%),糖尿病7例(20%)。病变部位:单纯累及股动脉16例(45.71%);单纯累及腘动脉6例(17.14%);累及股-腘动脉13例(37.14%)。所有患者均签署手术知情同意书。
1.2 手术方法
患肢疼痛不明显或可耐受术中患肢疼痛者,行局部浸润麻醉;不能耐受术中患肢疼痛者,行腰丛和坐骨神经阻滞麻醉。患者取仰卧位,术区常规消毒铺无菌巾,同侧顺行或对侧逆行穿刺股总动脉,置入短血管鞘,造影明确病变位置、病变范围以及膝下流出道情况。造影定位下,交换长血管鞘,单弯导管配合0.035'超滑导丝或V18导丝尝试开通闭塞段。若反复尝试无法开通,造影定位逆向穿刺部位,局麻后,在造影或透视引导下用微穿刺针逆向穿刺远端流出道。穿刺成功后,置入V18导丝,配合支撑导管,逆向沿真腔或经内膜下返回真腔后,开通闭塞病变,选入单弯导管后引出体外,建立逆向穿刺路径。经长血管鞘沿逆向穿刺路径置入合适直径的球囊导管、支架实施治疗(图1)。

图1 逆向穿刺开通股浅动脉闭塞病变
1.3 术后处理
逆向穿刺点予弹力绷带加压包扎;股总动脉穿刺点予缝合器缝合并用弹力绷带加压包扎。术后平卧24小时,给予抗凝、抗血小板、水化等治疗。术后第1、2天超声评估各穿刺点有无出血、皮下血肿、假性动脉瘤等并发症;术后第3天复查ABI及患侧足部温度;合并溃疡者术后常规换药治疗。
1.4 统计学处理
采用SPSS26.0统计软件进行数据分析。计数资料以“例(%)” 表示。符合正态分布的计量资料以(x±s)表示,治疗前后比较采用配对样本t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 技术成功率
35例患者中,13例(37.14%)逆穿股浅动脉远端,8例(22.86%)逆穿腘动脉远端,6例(17.14%)逆穿胫后动脉,4例(11.43%)逆穿胫前动脉,4例(11.43%)逆穿足背动脉。所有患者均穿刺成功,其中22例在造影引导下完成穿刺,10例在路径图(road map)引导下完成穿刺,3例在管壁钙化显影引导下完成穿刺(图2)。24例患者导丝经真腔通过病变部位,11例患者导丝经内膜下返回真腔通过病变部位。30例患者行支架置入术,5例患者单纯行球囊扩张术。术后彩超检查未见出血、皮下血肿、假性动脉瘤等并发症。
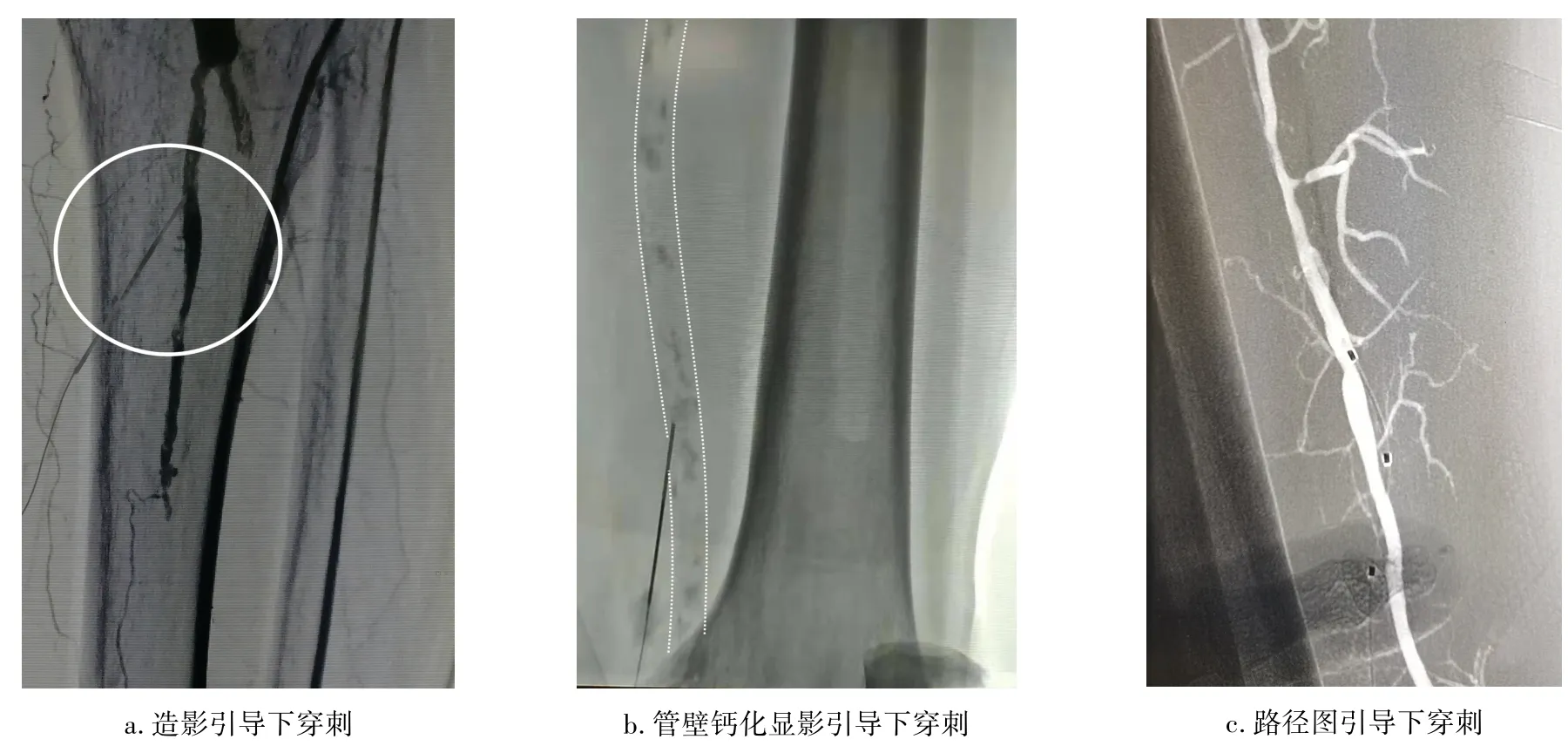
图2 透视引导下逆向穿刺
2.2 术后ABI和患侧足温
术后第3天复查ABI及患侧足温,见表1、图3。结果显示,术后ABI及患侧足部温度均较术前显著升高,差异均有统计学意义(P<0.05)。
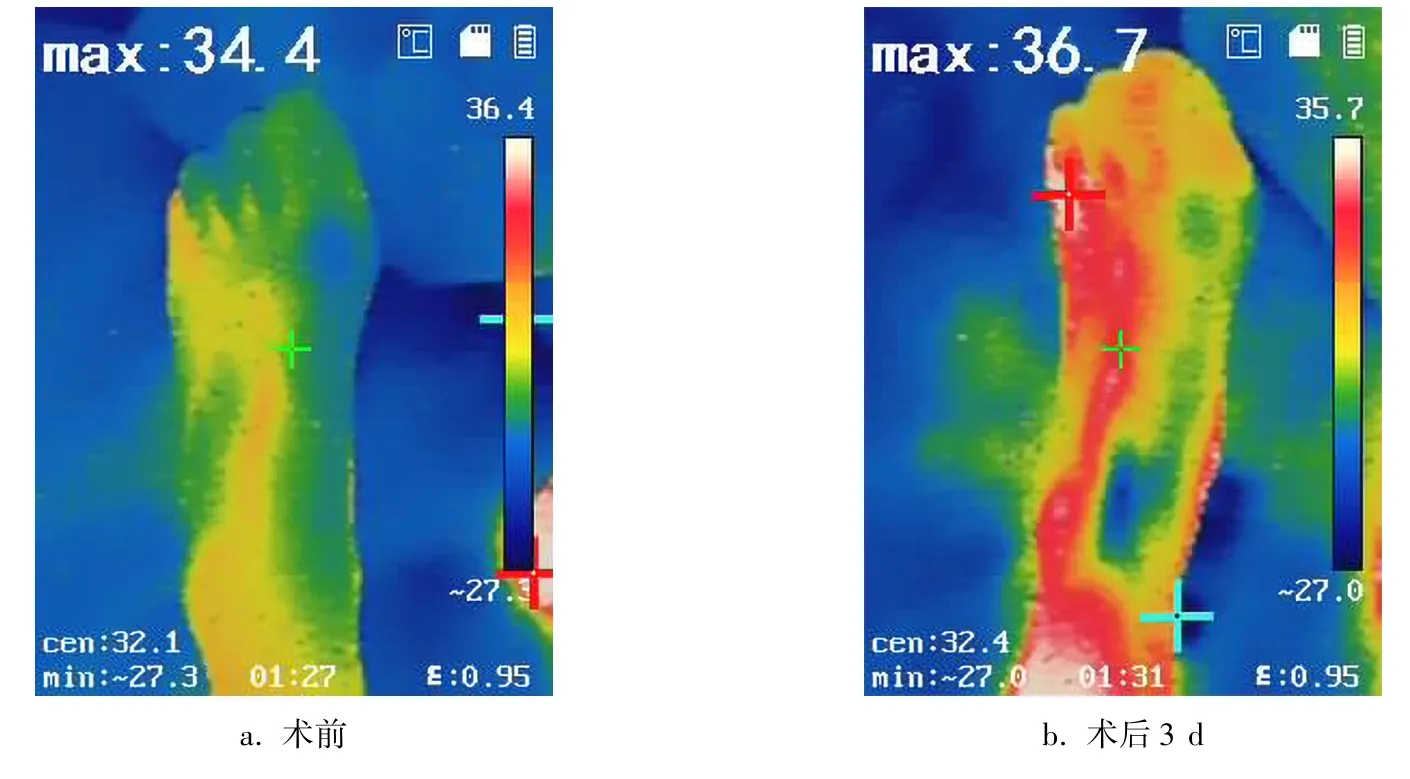
图3 手术前后患侧足部温度变化

表1 手术前后ABI和患侧足温比较(¯x±s)
3 讨 论
如何顺利通过闭塞病变一直是ASO腔内治疗的目标和难点。随着新的临床问题的发现和技术的进步,腔内器械已有了长足发展,但ASO慢性长段病变的治疗仍存在巨大挑战。随着动脉粥样硬化的进展,动脉中的胶原含量和纤维帽厚度增加[8],影像学研究证实,钙化是纤维帽的主要病理改变[9]。在ASO慢性长段病变中,坚硬的纤维帽多位于病变近心端,顺行开通时导丝难以通过,或导丝进入内膜下难以返回真腔,导致治疗失败[10]。在病变的远心端,纤维帽的钙化组织较近心端疏松,使得逆向开通病变的成功率大为增加[11]。逆向穿刺多在靠近病变的靶血管进行,操作距离较短[12]。同时,下肢动脉多向远端发出分支,与主干形成锐角,逆向穿刺不易进入分支[13]。上述两方面因素可以增加导丝、导管的可操作性和径向支撑力,提高开通病变的成功率。
逆向穿刺的方法主要包括彩超引导下穿刺、透视下穿刺、切开直视下穿刺等。直视下穿刺需在靶血管走行处做手术切口,损伤较直接穿刺大[14]。超声引导下穿刺具有造影剂使用量小、定位准确、可避开动脉钙化斑块等优势,但对操作者要求较高,且ASO病变多呈节段性狭窄或闭塞,探头施加的压力也会影响管腔的直径[15]。本组35例患者中,22例在造影引导下穿刺,10例在路径图引导下穿刺,3例在管壁钙化显影引导下穿刺,透视引导下穿刺成功率达100%。笔者总结透视引导下逆向穿刺的要点:①为减少术中造影剂的使用量,造影引导下逆穿时可将使用的造影剂用肝素水2~3倍稀释,使用大容量注射剂缓慢推注,同时放大图像,能够判断逆穿靶血管的走行及进针的角度即可。②路径图引导下穿刺成功的基础是减少患者移动时伪影的干扰,操作前应与患者充分沟通,取得患者的配合。③对于合并静息痛的患者,可采用腰丛和坐骨神经阻滞麻醉,以减轻患者术中的痛苦,提高患者的配合度。④膝下动脉多有同名静脉与其伴行,穿刺时应注意根据穿刺针尾部返血的色泽辨别针尖位置,避免误入静脉。
良好的导丝径向支撑力是开通闭塞病变的关键。支撑导管有直径小、推送力及跟进性能好、支撑力强等优点,能够为导丝提供强有力的径向支撑力,且支撑导管的材质柔顺性好,不会影响导丝的走行,临床应用广泛[16]。本研究中,35例患者均采用导丝配合支撑导管的方法开通闭塞病变,并且均采用无鞘化操作(逆穿部位不置入血管鞘)。有学者建议,逆向实施球囊扩张或支架置入时,应在逆穿部位置入4F甚至更大直径的血管鞘,便于操作[17],但在撤出血管鞘后,多需应用球囊贴壁止血,对于管径较小的膝下动脉,球囊扩张可增加血管痉挛的风险。笔者体会,对于闭塞病变的治疗,应首选股总动脉入路,若需行双向内膜下血管成形术开通闭塞病变,应选择位置较为表浅的动脉逆穿,术后压迫止血。
综上所述,透视引导下逆向穿刺技术有助于ASO闭塞病变的开通,显著改善ASO患者肢体的血流供应,可作为顺行开通失败的首选补救措施。但逆向穿刺技术对靶血管的选择有较高的要求,在实施前应充分评估下肢动脉的状态,术中根据造影的结果选择合适的靶血管,降低血管痉挛、血肿等并发症的发生率。
——导丝概述及导丝通过病变技巧

