吡非尼酮治疗类风湿关节炎伴肺间质病变的临床观察及其对肺泡细胞表面抗原KL-6的影响*
姜丽丽,尚可
江西省人民医院风湿免疫科(江西南昌330006)
类风湿关节炎(rheumatoid arthritis,RA)是以慢性破坏性、多关节滑膜炎为特征的自身免疫性疾病,除关节表现外,近50%的患者可出现关节外表现,其中肺间质病变(interstitial lung disease,ILD)是RA最常见的关节外表现之一,也是RA患者的主要死亡原因之一。有研究报道类风湿关节炎相关肺间质病变(RA-ILD)患者的病死率比单纯RA患者高3倍,与普通人群相比病死率增加13%[1-2],严重影响RA的总体预后。随着改善病情抗风湿药(diseasemodifying antirheumatic drugs,DMARDs)和生物制剂的应用,RA的总体病死率明显改善,但是RA-ILD的病死率却在上升,目前尚缺乏有效控制RA-ILD进展的药物。吡非尼酮是少数获批准治疗特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)适应证的药物之一,多项随机对照试验研究证实其可以减缓肺功能下降的速度和延长无进展生存期[3-5]。鉴于RA-ILD在影像学和组织病理学上和IPF有一定相似性,目前尚无充分循证医学证据证实吡非尼酮在RA-ILD中的疗效。我们尝试在常规治疗的基础上联用吡非尼酮,以观察真实世界中吡非尼酮能否改善或延缓RA-ILD患者肺功能下降,并观察及其对肺泡细胞表面抗原KL-6的影响,为RA-ILD患者选择合适的抗纤维化药物提供依据。
1 资料与方法
1.1 一般资料 2018年1月至2019年1月在江西省人民医院风湿免疫科住院治疗的RA-ILD患者。入组程序符合我单位负责人体试验的伦理委员会所制定的伦理学标准并得到伦理委员会的批准(编号2017-43),同时取得受试对象的知情同意。纳入标准:符合2010年ACR发布的RA分类标准[6],肺高分辨CT(HRCT)证实存在ILD。排除标准:(1)合并RA以外的其他自身免疫性疾病史;(2)合并ILD以外的其他严重肺部疾病史,如肺结核、肺部肿瘤、肺动脉高压等;(3)药物(如胺碘酮)导致的肺部病变;(4)伴慢性心、肝、肾功能不全,或其他系统肿瘤;(5)妊娠或准备妊娠;(6)对吡非尼酮过敏。借鉴Collard等[7]对IPF病情进展定义:(1)用力呼气肺活量(FVC)占预计值%较基下降≥10%或一氧化碳弥散量(DLCO)占预计值%较基下降≥15%;(2)胸部HRCT提示间质性病变较基线进展(原有ILD病变范围较基线增大或出现新的ILD病灶)。满足上述任意1项认为患者出现ILD病情进展。
1.2 试验分组 连续纳入30例符合入组条件的RA患者应用吡非尼酮治疗(吡非尼酮组),同期经年龄和性别匹配的未应用该药物的RA-ILD患者30例作为对照(对照组),两组患者性别比例(男性23.3% vs23.3%)、年龄[(55.4±11.7)岁vs(55.6±10.8)岁]及中位病程(36月vs24月)均差异无统计学意义(P>0.05)。
1.3 检查和治疗方案 所有入选患者均常规给予非甾体抗炎药或小剂量激素及DMARDs抗风湿治疗,两组患者激素用量均≤15 mg/d;DMARDs包括:来氟米特、艾拉莫德、环磷酰胺、柳氮磺吡啶、硫酸羟氯喹、吗替麦考酚酯、他克莫司/环孢素等,除艾拉莫德、柳氮磺吡啶、硫酸羟氯喹作为联合用药方案之一外,其他DMARDs均为单药治疗。吡非尼酮组在此基础上联合吡非尼酮治疗:第1周,300 mg/d,分3次口服,此后每周加量300 mg/d,直至1 800 mg/d或不能耐受更高剂量。所有患者入组时均行肺部HRCT扫描和肺功能以及KL-6检查,每6个月复查上述指标,至少随访6月,并记录临床症状变化。
1.4 统计学方法 采用SPSS 23.0统计软件,非正态分布的计量资料采用M(P25,P75)表示,正态分布的计量资料采用±s表示;两组独立样本比较:非正态分布的计量资料的比较采用Mann-whitney U检验,正态分布的计量资料的比较采用独立t检验,计数资料的比较采用χ2检验;配对计量资料比较采用配对样本的Wilcoxon符号秩检验。以P<0.05为差异有统计学意义。
2 结果
2.1 入组患者基线情况 两组在吸烟比例、疾病活动度、基线水平肺功能指标及6 min步行距离(Sixminute walk distance,6MWD)、DMARDs用药等均差异无统计学意义(P>0.05)。见表1。
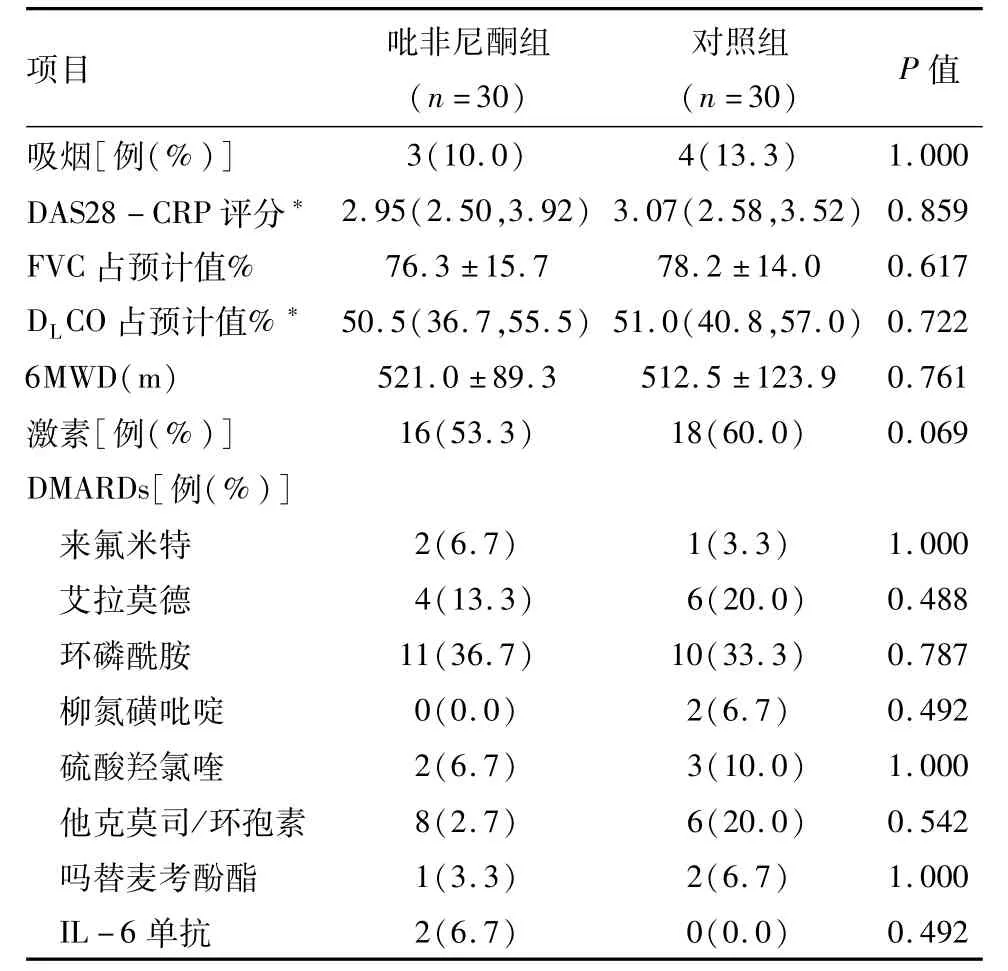
表1 两组患者基线资料
2.2 两组患者治疗前后肺功能及6MWD变化 受经济条件及药物相关不良反应影响,吡非尼酮组30例患者仅2例达到药品说明书推荐的600 mg,3次/d的剂量,22例患者最终维持剂量为400 mg,3次/d,另外6例最终维持剂量为300 mg,3次/d。入组患者最短随访6个月,最长随访12个月,中位随访时间7个月。因完成12个月随访的患者例数较少,仅对治疗后6个月的数据进行统计分析。吡非尼酮组患者治疗后FVC占预计值%、DLCO占预计值%以及6MWD均有不同程度改善,而对照组上述指标有不同程度恶化,差异有统计学意义(P<0.05);吡非尼酮组治疗后上述指标显著优于对照组,差异有统计学意义(P<0.05);治疗组病情进展患者例数(5例,16.7%)少于对照组(10例,33.3%),但差异无统计学意义(χ2=2.222,P=0.136)(表2)。
表2 两组治疗6个月后肺功能及6MWD变化 ±s
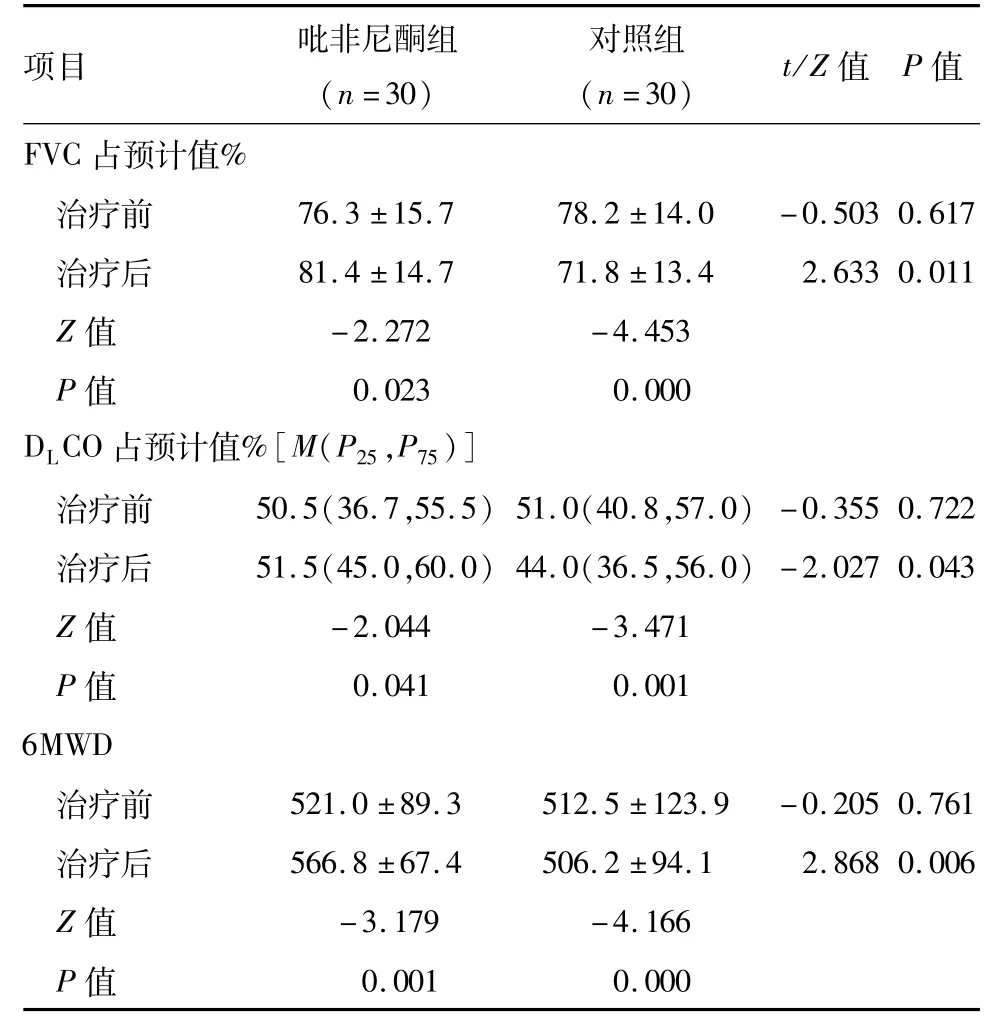
表2 两组治疗6个月后肺功能及6MWD变化 ±s
项目 吡非尼酮组(n=30)对照组(n=30) t/Z值 P值FVC占预计值% 治疗前 76.3±15.7 78.2±14.0 -0.503 0.617 治疗后 81.4±14.7 71.8±13.4 2.633 0.011 Z值 -2.272 -4.453 P值 0.023 0.000 DLCO占预计值%[M(P25,P75)]治疗前 50.5(36.7,55.5)51.0(40.8,57.0)-0.355 0.722 治疗后 51.5(45.0,60.0)44.0(36.5,56.0)-2.027 0.043 Z值 -2.044 -3.471 P值 0.041 0.001 6MWD 治疗前 521.0±89.3 512.5±123.9 -0.205 0.761 治疗后 566.8±67.4 506.2±94.1 2.868 0.006 Z值 -3.179 -4.166 P值0.001 0.000
2.3 两组患者治疗前后血清KL-6变化 两组患者治疗前KL-6水平差异无统计学意义,治疗后KL-6水平呈下降趋势,但差异均无统计学意义(P>0.05),见表3。

表3 两组治疗后6个月血清KL-6变化 M(P25,P75)U/mL
2.4 吡非尼酮不良反应及转归 吡非尼酮组共10例患者出现可能与吡非尼酮相关的不良反应,均在剂量滴定过程中出现,服药剂量在900~1 500 mg/d。其中胃肠道不适5例,皮肤瘙痒2例,头晕1例,ALT升高1例,但不良反应轻微,均未中断治疗,胃肠道不适患者予对症治疗、改为餐中服药或减少服药剂量后缓解,皮肤瘙痒患者建议做好皮肤防晒后逐渐缓解,头晕患者随服药时间延长逐渐耐受,ALT升高患者予口服护肝药物并降低服药剂量后恢复正常。
3 讨论
本研究是一项观察性研究,观察在常规抗风湿基础上联用吡非尼酮治疗RA-ILD的疗效。结果表明,在常规治疗基础上联用吡非尼酮治疗6个月可以一定程度上改善RA-ILD患者肺功能指标FVC占预计值%和DLCO占预计值%,提高6WMD,且有降低血清KL-6水平的趋势。
RA-ILD和IPF在发病机制、形态学表型(包括胸部HRCT以及肺活检组织病理学表型)等方面均有类似之处:如两者均有TGF-β介导的成纤维细胞、肌成纤维细胞的活化和肺内聚集;两者在胸部HRCT上均可表现为网格影、蜂窝影等寻常型肺间质病变(usual interstitial pneumonia,UIP)的典型表现;两者肺组织病理中均可出现肺间质纤维化、成纤维母细胞灶形成等[8]。吡非尼酮是一种吡啶类的小分子化合物,其抗纤维化作用主要是通过抑制致纤维化因子转化生长因子(TGF-β)、血小板衍化生长因子(PDGF)和碱性成纤维细胞生长因子(bFGF)的过度表达,从而减少成纤维细胞的增殖和胶原纤维的合成,降低细胞外基质的沉积[9-11],多个随机对照试验研究证实吡非尼酮治疗IPF有效。本研究在RA常规治疗的基础上联合使用吡非尼酮,在疗程满6个月的患者中观察到肺功能FVC占预测值%和DLCO占预计值%的改善以及6MWD的增加,提示吡非尼酮在RA-ILD同样有效。目前国内外尚无大样本的吡非尼酮治疗RA-ILD的随机对照试验研究,仅小样本临床研究及个案报道吡非尼酮对RA-ILD治疗有效,安全性较好[12]。国内研究[13]发现,吡非尼酮在RA中抗纤维化的机制可能是通过下调转录激活因子3(activating transcription factor 3,ATF3),从而抑制人原代肺成纤维细胞向肌成纤维细胞转化。
KL-6为由Ⅱ型肺泡上皮细胞和细支气管上皮细胞表达的一种高分子量黏蛋白样糖蛋白,其在细胞损伤和(或)再生后表达增加。在IPF患者的研究中发现,基线KL-6水平显著升高,且与不良预后相关[14]。KL-6在结缔组织病(connective tissue disease,CTD)相关肺间质病变中的作用也越来越受到关注:有研究证实KL-6对肺成纤维细胞具有促纤维化和抗细胞凋亡作用,系统性硬化症(systemic sclerosis,SSc)相关肺纤维化的患者的KL-6血清水平明显高于单纯的SSc,且对SSc-ILD的诊断和严重程度有提示作用[15-16];Chen等[17]在多发性肌炎/皮肌炎(polymyositis/dermatomyositis,PM/DM)患者的研究中发现,KL-6可预测新发ILD的出现[17]。Fotoh等[18]研究发现KL-6水平和RAILD严重程度及不良预后相关。本研究在治疗后观察到血清KL-6水平呈下降趋势,但差异无统计学意义(P>0.05),可能与样本数相对较小、随访周期较短等因素有关,未来需要设计更严格的随机对照试验进一步验证。
作为观察性研究,本研究不可避免存在一些不足:对入组患者的合并用药及剂量没有严格限定,虽然统计结果显示两组在DMARDs和激素用药构成比方面无显著差异,但药物的剂量个体差异较大,无法进行统计分析,因此不能除外激素及DMARDs剂量对ILD转归及KL-6水平的影响,研究结果需谨慎解读;此外,大部分患者未进行肺组织活检,而肺HRCT不能对ILD具体类型进行精准判断,因此无法评估不同类型ILD对吡非尼酮的治疗反应。目前国外有一项吡非尼酮治疗RA-ILD的随机对照试验研究正在进行中(TRAIL1:NCT02808871),我们期待更有说服力的结果。
RA-ILD的发病机制尚未完全阐明,治疗药物选择有限,本研究在真实世界的有限样本中观察到吡非尼酮可一定程度上延缓RA-ILD的肺功能下降,期待未来能开展更多的多中心随机对照试验研究及真实世界研究,为RA-ILD患者合理用药提供更多证据支持。

