酮肟钾盐与18-冠醚-6在有机溶剂中的配位反应与消毒性能的关系
孔令策,陈文明,张 旭,吴 遥,辛 毅,左言军,习海玲*
(1.国民核生化灾害防护国家重点实验室,北京 102205;2.军事科学院防化研究院,北京 102205)
消毒是指使用专用消毒剂对染有毒剂或生物战剂的人员、装备、地面等实施洗消的行动。化学消毒剂按照化学成分与性质,可分为活性氯、活性氧、醛类、杂环类、醇类、酚类、季铵盐及其他类8类消毒剂[1-3]。其中,酮肟盐类消毒剂是以碱金属酮肟盐为消毒活性成分的一类高效、广谱、无毒、无刺激性的消毒剂[4-6]。目前,国外唯一商品化的一种酮肟盐类消毒剂是1993年加拿大研制的反应型皮肤消毒液(RSDL)。该产品主要用于沾染沙林、梭曼、维埃克斯和芥子气等典型化学毒剂以及T-2毒素的人员皮肤的应急消毒,并于1995年装备北约国家部队。
在跟踪国外研究进展的基础上,中国从2006年开始酮肟盐皮肤消毒剂的研究工作[7-10]。目前,已研制出基于酮肟盐的皮肤消毒液配方和人员应急消毒包的样包。但是,酮肟盐消毒剂配方中相转移催化剂(冠醚)对酮肟盐的活化机制的相关研究极少。美国E-Z-EM有限公司的一篇关于酮肟盐消毒剂的专利[9]提到,二乙酰单肟(DAM)及其盐(如KBDO)含有3个潜在的亲核性原子:羰基氧、肟氮和程度更低的肟氧。亲核性原子能够攻击并中和多种有毒化学品。并在一个实施例中提到了配方里可含有18-冠醚-6和其他杂环化合物,但未说明其作用原理。
目前,碱金属酮肟盐的金属阳离子与配方中相转移催化剂如何形成配合物、酮肟阴离子稳定性与消毒剂的消毒反应性能及反应动力学存在什么联系等问题还没有弄清楚。因此,开展酮肟盐与冠醚在有机溶剂中的配位反应以及对消毒性能的影响规律研究,对于优化酮肟盐类消毒剂配方和设计新型酮肟盐消毒剂产品,从而实现酮肟盐类消毒剂的实际应用具有十分重要的军事意义。
近年来,文献报道的冠醚金属配合物稳定常数的测试方法主要有电极电位法[11]、电导率法[12-14]、吸收光谱法[15]、核磁共振法[16-17]和极谱法[18]等。其中,电导率法对检测仪器要求比较低,操作简单,适用范围比较广。现拟采用电导法研究两种酮肟钾盐分别与18-冠醚-6在四乙二醇二甲醚、N-甲基吡咯烷酮、乙醇和乙腈等溶剂中的配位反应,计算配合物的稳定常数和摩尔电导率。并测试四种配合物在4种主溶剂配方中对2-氯乙基乙基硫醚(2-CEES)的消毒动力学规律,尝试建立配合物稳定常数与其消毒性能之间的内在关系。
1 实验部分
1.1 主要试剂与仪器
试剂:N-甲基吡咯烷酮、四乙二醇二甲醚、乙腈、无水乙醇,分析纯,国药集团化学试剂有限公司。
仪器:DDSJ-308F型电导率仪,上海仪电科学仪器股份有限公司。
1.2 实验步骤
1.2.1 测试配合物的在不同溶剂中的电导率变化
溶液配制:测试有机溶剂体系分别为四乙二醇二甲醚、N-甲基吡咯烷酮、乙腈和乙醇,分别配制0.5 mol/L的18-冠醚-6溶液25 mL和5 mmol/L的KBDO溶液250 mL。
试验步骤:首先,取50 mL的KBDO溶液加入配有磁力搅拌器的50 mL广口瓶中,用装有电导率电极的塞子密封,开启恒温水浴和磁力搅拌;然后,用移液器每次加入定量的冠醚溶液,直到冠醚总浓度为钾离子总浓度的5倍以上。每次加入冠醚后,需要持续搅拌,待反应和温度平衡后,测试电导率值。每次加入冠醚溶液的体积分别为0.1、0.1、0.1、0.1、0.1、0.25、0.25、0.25、0.25、0.25、0.25、0.25和0.25 mL,总体积为2.5 mL。
1.2.2 稳定常数的计算方法
根据张强等[13-14]的方法,采用MATLAB软件自行编写了计算程序,利用程序计算配合物的平衡常数(KML)和摩尔电导率(ΛML)。MATLAB计算程序如下。
deltam=deltaexp(1);
cm=0.005;
cl=cm*clcm;
km1=0.1:0.0001:10;
km=10.^km1;
alpha=((km.*(cm-cl)-1)+((km.*cl+1-km.*cm).^2+4*km.*cm).^0.5)./(2*km.*cm);
deltamL=(sum((1-alpha).*deltaexp)-sum(alpha.*(1-alpha)*deltam))./(sum((1-alpha).^2));
u=sum((deltaexp-alpha*deltam-(1-alpha).*deltamL).^2);
temp=find(u==min(u))
kmL=km1(temp)
deltaca=alpha*deltam+(1-alpha).*deltamL;
deltamL(temp)
deltaca(temp)
alpha(temp);
1.2.3 消毒动力学试验方法
(1)消毒液配制。分别以四乙二醇二甲醚、N-甲基吡咯烷酮、乙腈和无水乙醇为主溶剂,按照如下配比:酮肟盐(8%)+主溶剂(52.7%)+相转移催化剂(15.3%)+助溶剂(20%)+促渗剂(4%),配制4种消毒液,每种消毒液10 g。每种溶液混合后,超声震荡10 min,形成均一的消毒剂溶液。
(2)试验过程。分别取4 mL消毒液置于25 mL试管中,加入40 μL的2-CEES,2-CEES的浓度为10 mg/mL,将试管放入恒温震荡器中,25 ℃条件下反应,并分别在2.5、5、10、15、20、30、45和60 min等时间点取出50 μL反应液,加入取样管中,取样管内提前加入2 mL萃取剂二氯甲烷和50 μL中止剂10%盐酸,之后震荡取样管,用长针从取样管下层抽取萃取液,进行气相-火焰光度检测(gas chromatography-flame photometric detector,GC-FPD)分析,测试2-CEES的残余浓度,并计算对2-CEES的消毒率。
2 结果与讨论
2.1 18-冠醚-6与KBDO在不同溶剂中配位过程的电导率测定
除乙腈溶剂外(对KBDO溶解度较小),其他溶剂中KBDO浓度为0.005 mol/L,乙腈溶剂中KBDO浓度为0.001 mol/L。电导率测试结果见表1和图1。在四乙二醇二甲醚中,体系的摩尔电导率整个过程变化不大,初始值很小,随着冠醚的加入逐渐减小,滴加结束时摩尔电导率略有升高。在N-甲基吡咯烷酮和乙醇中,体系的摩尔电导率整个过程变化也不大;在N-甲基吡咯烷酮中,随着冠醚的加入,体系的摩尔电导率先下降后逐渐升高;而在乙醇中,体系的摩尔电导率先下降,后逐渐升高,最后又逐渐下降。在乙腈中,体系的摩尔电导率变化幅度很大,先减小后逐渐增大,并趋于平衡。
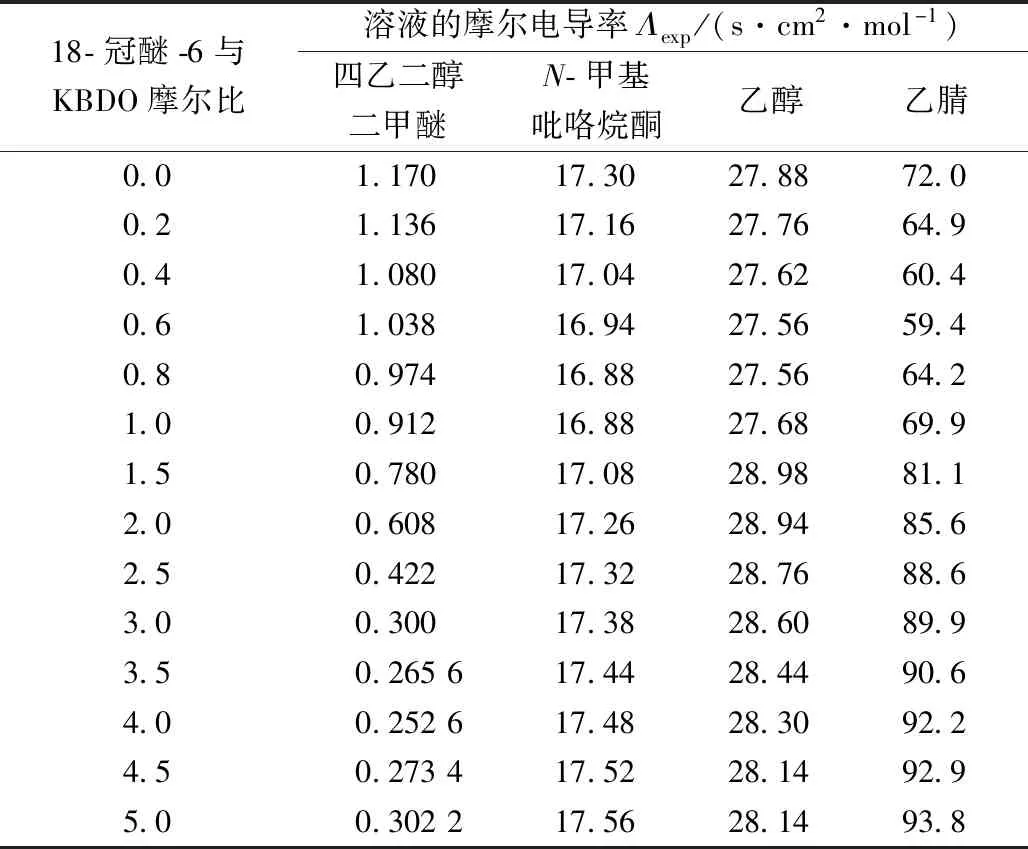
表1 18-冠醚-6加入KBDO溶液形成配合物过程中的电导率测试数据Table 1 Conductivity test data of 18-crown-6 in the process of adding KBDO solution to form a complex
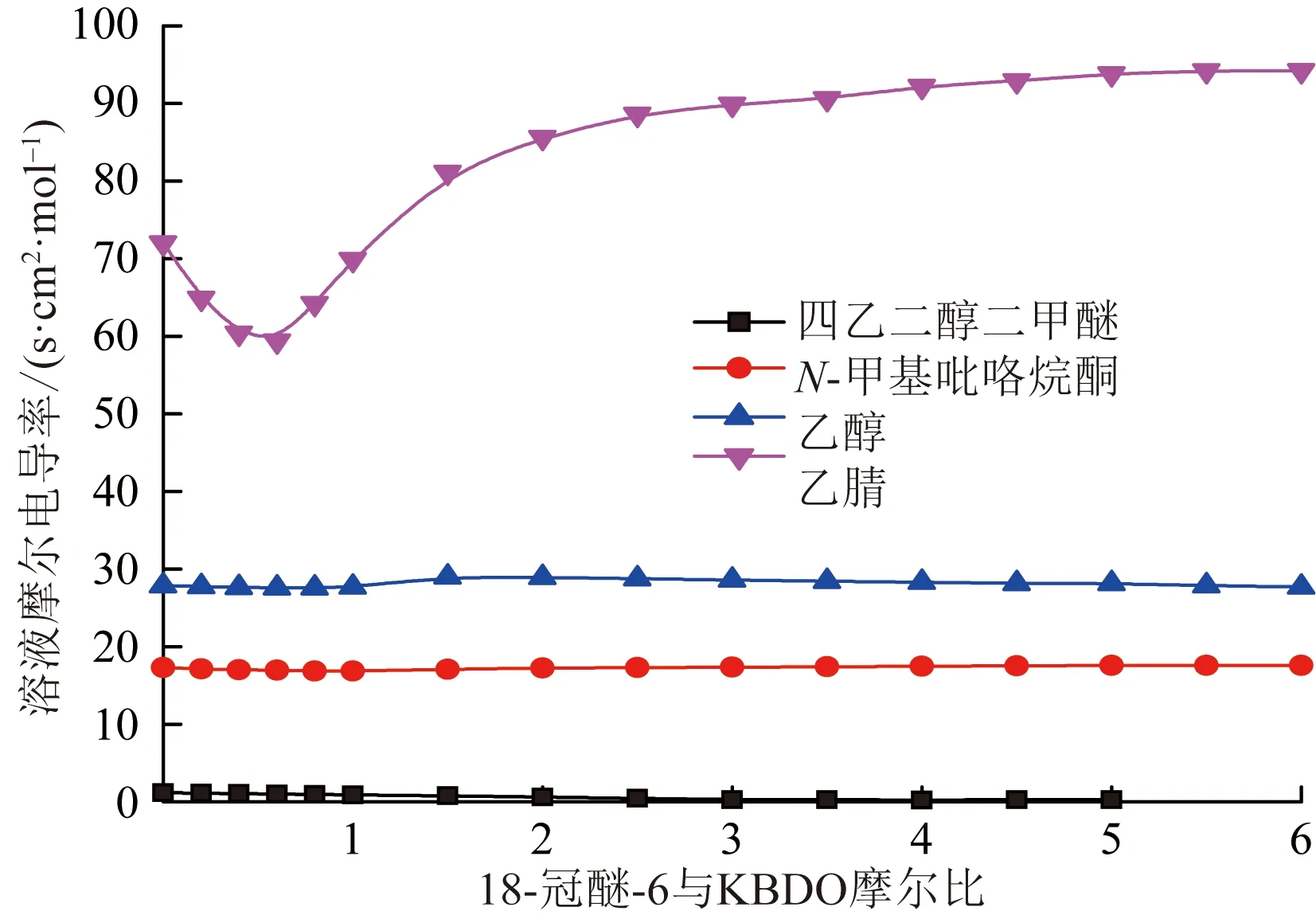
图1 KBDO溶液电导率随18-冠醚-6加入量的变化曲线Fig.1 The change curve of KBDO solution conductivity with 18-crown -6 added amount
2.2 18-冠醚-6与K-DMKO在不同溶剂中配位过程的电导率测定
除乙腈溶剂外(对K-DMKO溶解度较小),其他溶剂中K-DMKO浓度为0.005 mol/L,乙腈溶剂中K-DMKO浓度为0.001 mol/L。电导率测试结果见表2和图2。在四乙二醇二甲醚中,体系的摩尔电导率整个过程变化不大,初始值很小,随着冠醚的加入逐渐逐渐升高。在N-甲基吡咯烷酮中,随着冠醚的加入,体系的摩尔电导率变化较大,呈逐渐升高,并趋于平衡。在乙醇中,体系的摩尔电导率整体变化不大,先逐渐升高,后逐渐下降。在乙腈中,体系的摩尔电导率变化幅度很大,体系的摩尔电导率前期快速上升,后期上升速度减缓。

表2 18-冠醚-6加入K-DMKO溶液形成配合物过程中的电导率测试数据Table 2 Conductivity test data in the process of adding 18-crown-6 to K-DMKO solution to form a complex
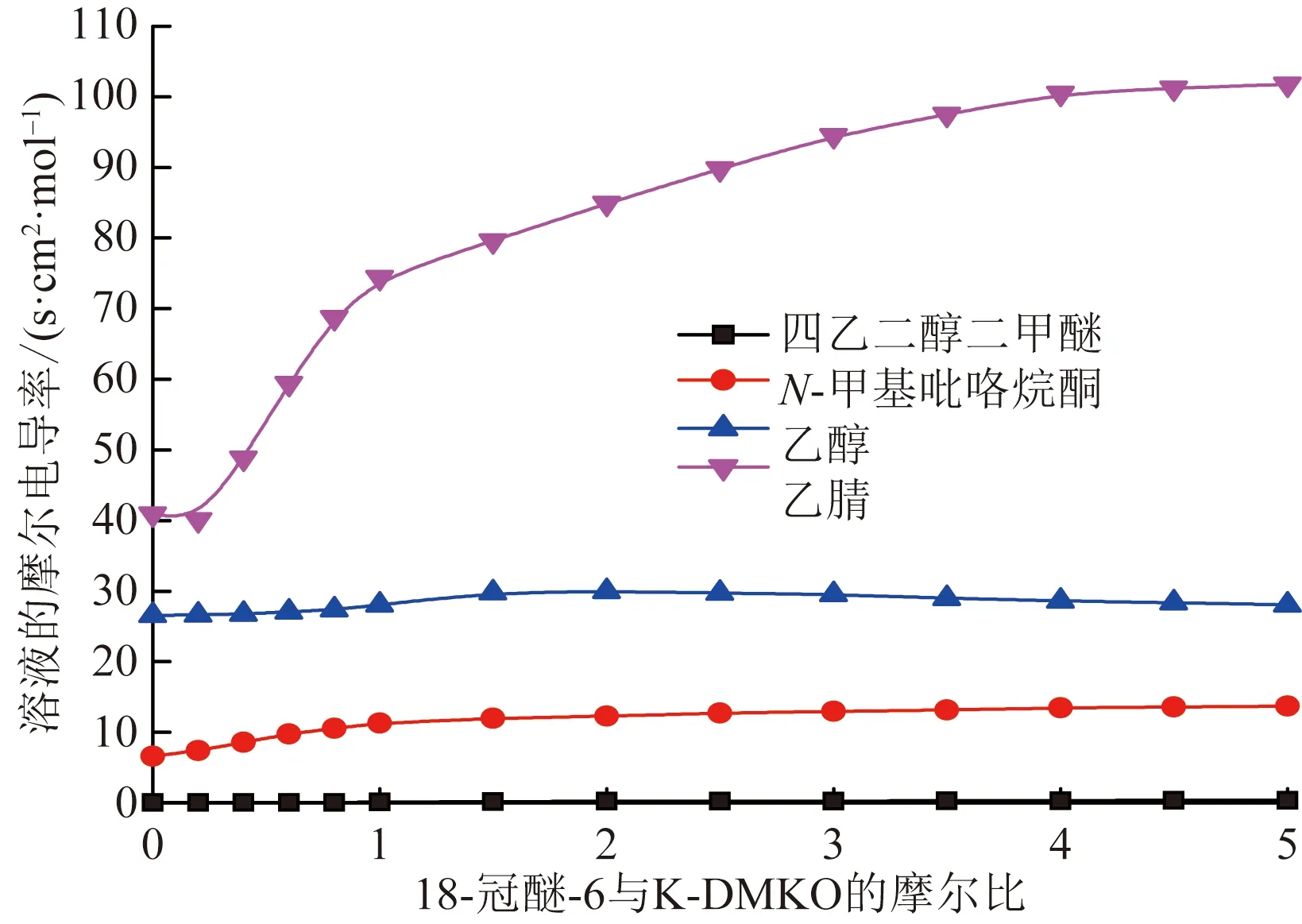
图2 K-DMKO溶液电导率随18-冠醚-6加入量的变化曲线Fig.2 The change curve of the conductivity of K-DMKO solution with the added amount of 18-crown-6
2.3 配合常数计算
假定在有机溶剂中18-冠醚-6与钾离子形成1∶1的配合物,则反应方程可表示为

(1)
式(1)中:CM和CL分别为金属离子和冠醚的总浓度;α为游离金属离子分数。则稳定常数为
KML=[1-α]/α[CL-(1-α)CM]
(2)
溶液的表观摩尔电导率Λ为
Λ=1 000κ/CM
(3)
式(3)中:κ为电导率。假定电导率为下列两项之和,即
(4)
则
Λ=1 000κ/CM=(1-α)ΛML+αΛM
(5)
式中:ΛM、ΛML分别为盐和配合物的摩尔电导率。利用表1和表2数据,采用自编程序计算得到稳定常数lgKML和ΛML,结果列于表3和表4。

表4 几种溶剂中18-冠醚-6与酮肟盐配合物的表观摩尔电导率Table 4 Apparent molar conductivity of complexes of 18-crown-6 and ketoxime salt in several solvents
由表3分析可知,在溶剂四乙二醇二甲醚、N-甲基吡咯烷酮、乙醇和乙腈中,KBDO和18-冠醚-6配合物的稳定常数大小顺序为乙醇>四乙二醇二甲醚>乙腈>N-甲基吡咯烷酮;K-DMKO和18-冠醚-6配合物的稳定常数大小顺序为乙醇>N-甲基吡咯烷酮>乙腈>四乙二醇二甲醚。综合分析,2种配合物中在乙醇中的稳定常数最大,在乙腈中稳定常数最小。
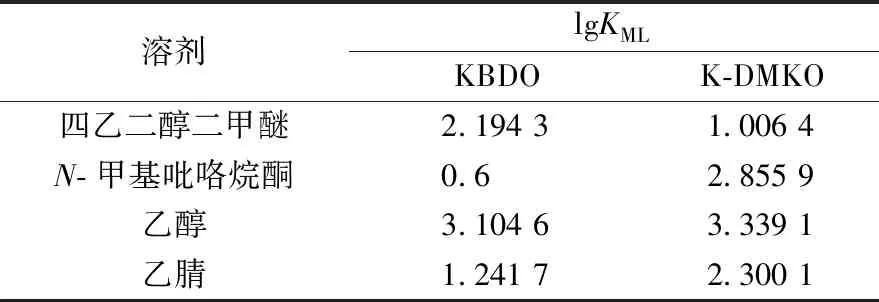
表3 几种溶剂中18-冠醚-6与酮肟盐配合物的稳定常数Table 3 Stability constants of complexes of 18-crown-6 and ketooxime salts in several solvents
由表4分析可知,对于不同的溶剂来说,配合物在极性较大的溶剂中表观摩尔电导率的数值较大。本实验中所用的溶剂极性大小顺序依次为乙腈>乙醇>N-甲基吡咯烷酮>四乙二醇二甲醚,不同溶剂中同一酮肟盐的ΛML大小顺序与此是一致的。这是由于冠醚配合物在极性较强的溶剂中电离程度较大,因而表观摩尔电导率也较大。
2.4 酮肟盐和冠醚配合物形成的消毒剂配方对2-CEES消毒动力学
2.4.1 18-冠醚-6与KBDO配合物的配方体系对2-CEES消毒动力学
4种消毒剂溶液对2-CEES的消毒动力学曲线见图3。由图3可知,以乙醇为主溶剂的配方对2-CEES基本没有消毒效果;由其他3种主溶剂形成的配方对2-CEES的消毒率均随时间增加而逐渐增大,四种溶剂配方对2-CEES的消毒性能顺序依次为四乙二醇二甲醚>N-甲基吡咯烷酮>乙腈>无水乙醇。对4个体系的消毒结果进行一级动力学拟合结果见表5。结果表明,该配方对2-CEES的消毒基本符合一级反应动力学规律。
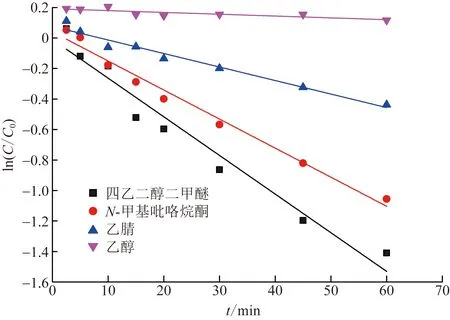
C0、C分别为2-CEES的初始浓度和反应过程中的浓度图3 4种主溶剂形成的消毒剂溶液对2-CEES的消毒动力学拟合曲线Fig.3 Fitting curve of decontamination kinetics of solution formed by four main solvents to 2-CEES

表5 18-冠醚-6与KBDO配合物的不同主溶剂配方对2-CEES消毒动力学结果Table 5 Decontamination kinetics results of 2-CEES by different main solvent formulations of 18-crown-6 and KBDO complexes
2.4.2 18-冠醚-6与K-DMKO配合物的配方体系对2-CEES消毒动力学
4种消毒剂溶液对2-CEES的消毒动力学曲线见图4。由图4可知,以乙腈为主溶剂的配方对2-CEES基本没有消毒效果;由其他3种主溶剂形成的配方对2-CEES的消毒率均随时间增加而逐渐增大,4种溶剂配方对2-CEES的消毒性能顺序依次为N-甲基吡咯烷酮>四乙二醇二甲醚>无水乙醇>乙腈。对4个体系的消毒结果进行一级动力学拟合结果见表6。结果表明,该配方对2-CEES的消毒也基本符合一级反应动力学规律。
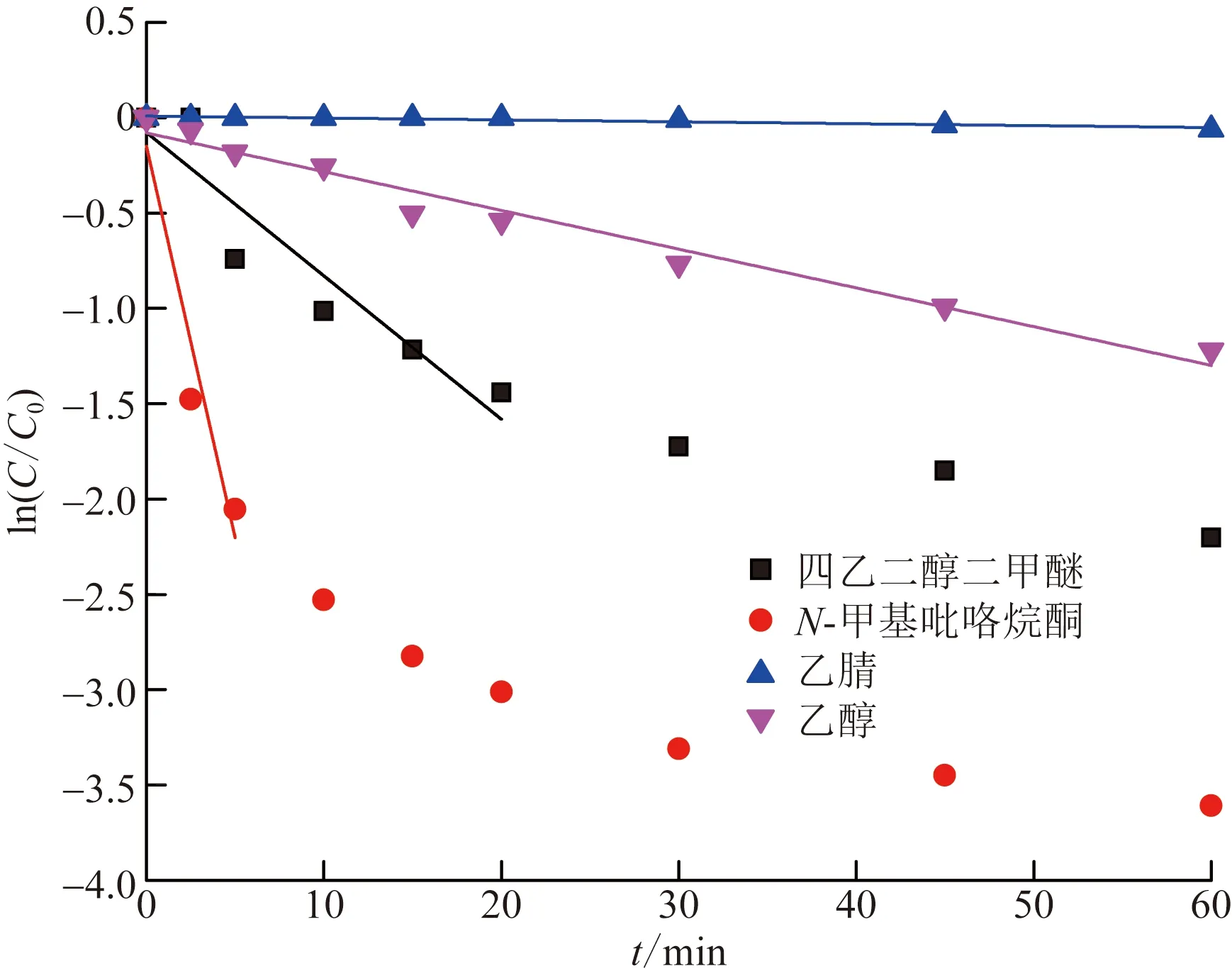
C0、C分别为2-CEES的初始浓度和反应过程中的浓度图4 4种主溶剂形成的消毒剂溶液对2-CEES的消毒动力学拟合曲线Fig.4 Fitting curve of decontamination kinetics of solution formed by four main solvents to 2-CEES
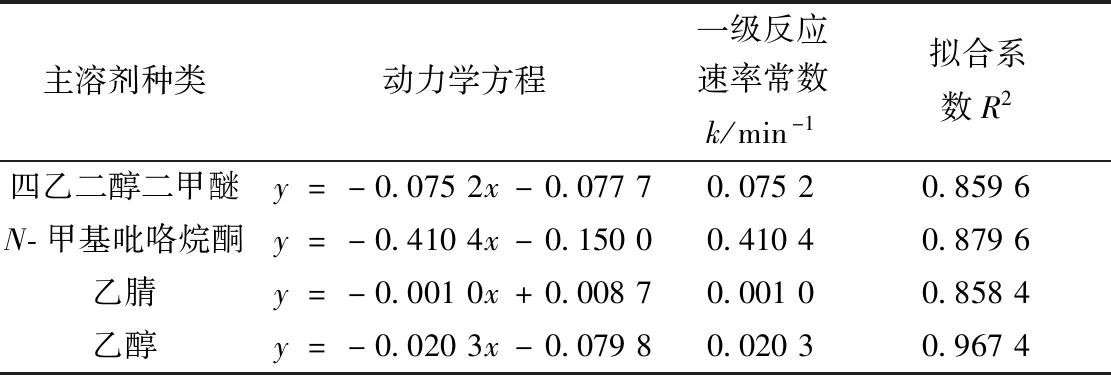
表6 18-冠醚-6与K-DMKO配合物的不同主溶剂配方对2-CEES消毒动力学结果Table 6 Decontamination kinetics results of 2-CEES by different main solvent formulations of 18-crown-6 and K-DMKO complexes
2.5 配合物稳定常数与消毒性能的关系分析
将酮肟盐与冠醚形成的配合物在不同溶剂中的稳定常数与配方对2-CEES的消毒性能进行关联分析可知,在几个溶剂体系中,乙醇溶剂中配合物的稳定常数基本是最大的,但是2种配合物在乙醇溶剂中的一级消毒反应速率常数k基本为最小值;N-甲基吡咯烷酮溶剂中配合物的稳定常数中等偏小,但是2种配合物在N-甲基吡咯烷酮溶剂中的一级消毒反应速率常数k基本为最大值。
根据文献报道[5],酮肟盐消毒剂配方中加入冠醚后,可以形成酮肟钾和冠醚的配合物,有利于酮肟阴离子的暴露而促进亲核消毒反应的发生。而当前实验结果表明,乙醇溶剂体系中配合物稳定常数最大,但消毒反应反应速率最慢。可能的原因是,乙醇作为一种极性质子溶剂能够提供质子,质子与配合物中的酮肟阴离子以氢键相结合而变得稳定,从而降低了酮肟阴离子的亲核进攻性能,从而导致消毒反应速率的降低。
综合分析认为,酮肟盐消毒剂配方消毒速率不仅与配合物在溶液中的稳定常数有关,还与配合物在溶剂中的溶解度有关。一般而言,配合物在溶液中溶解性越好,溶液中消毒活性成分的浓度越高,从而对目标物的消毒速度越快。在消毒液配制过程中发现,配合物在N-甲基吡咯烷酮溶剂配方中溶解度最佳,而在乙腈溶解度最差。因此,2种配合物在4种不同主溶剂中形成的消毒剂配方对目标物的消毒反应动力学规律是以上两种主要影响因素共同作用的结果。
3 结论
(1)2,3-丁二酮单肟钾与18-冠醚-6配合物的稳定常数大小顺序为:乙醇>四乙二醇二甲醚>乙腈>N-甲基吡咯烷酮;丙酮肟钾盐与18-冠醚-6配合物的稳定常数大小顺序为:乙醇>N-甲基吡咯烷酮>乙腈>四乙二醇二甲醚。两种酮肟盐冠醚配合物的摩尔电导率值大小顺序均为:乙腈>乙醇>N-甲基吡咯烷酮>四乙二醇二甲醚。
(2)配合物稳定常数与消毒性能的关系。在不同的溶剂体系中,乙醇溶剂中配合物的稳定常数基本是最大的,但是2种配合物在乙醇溶剂中的一级消毒反应速率常数k基本为最小值;N-甲基吡咯烷酮溶剂中配合物的稳定常数中等偏小,但是2种配合物在N-甲基吡咯烷酮溶剂中的一级消毒反应速率常数k基本为最大值。2种配合物在4种不同主溶剂中形成消毒剂配方的消毒反应动力学规律基本符合一级反应动力学规律。酮肟盐消毒剂配方消毒速率不仅与配合物在溶液中的稳定常数有关,还与配合物在溶剂中的溶解度有关,是以上两种主要影响因素共同作用的结果。

