MBfR去除对氯硝基苯的影响因素研究
杨文婷,李海翔
(1.广西建设职业技术学院,广西 南宁 530001;2.桂林理工大学,广西 桂林 541004)
1 氢基质自养生物去除对氯硝基苯
对氯硝基苯(p-NCB)是化工生产过程中化学合成的一种中间产物,是硝基氯苯中毒性最大的化合物,具有三致效应和遗传毒性,对人体有潜在致癌作用。对氯硝基苯的化学性质稳定,极易在生物、水体沉积物或土壤有机质中富集,难降解易挥发,排放到环境中具有极大的毒害作用,被列为优先控制的有机污染物[1]。
有研究指出,通过硝基还原和还原脱氯,生成易生物降解和低毒性的苯胺类,是氯代硝基苯生物转化或矿化的重要途径[2]。在好氧条件下,p-NCB苯环上的硝基和氯原子具有吸电子特性,很难被降解,因此,p-NCB的生物转化要采用厌氧还原的方式。p-NCB氢基质自养生物处理的主要降解过程见图1。从图1可以看出,氢气作为电子供体,洁净无残留,无二次污染,氧化还原电位低。p-NCB为电子受体,氢自养还原菌利用H2,将对氯硝基苯还原脱氯,先使p-NCB还原成对氯苯胺(p-CAN),再通过对位还原脱氯,p-CAN进一步将苯环上的氯原子取代,生成低毒和易生化降解的苯胺(AN)[3]。因此,氢基质自养生物对p-NCB的还原转化,不仅能降低毒性,还能提高p-NCB的可生化降解性。
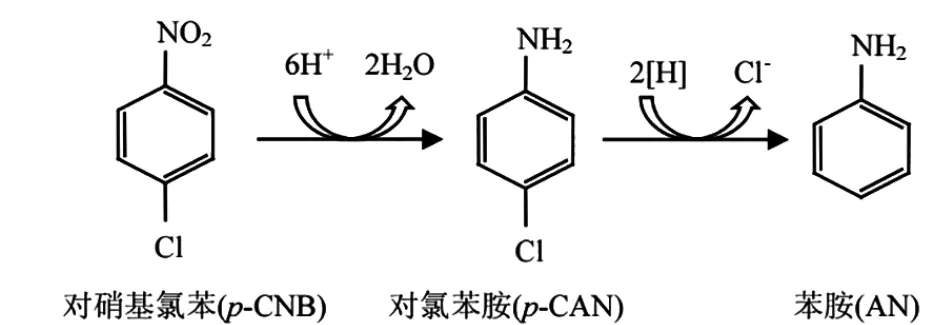
图1 p-NCB的生物转化过程
2 氢基质生物膜反应器
早期的氢基质自养生物还原技术使用氢气进行曝气,造成氢气的利用效率低,且溢出水面的氢气易发生爆炸[4-5]。氢基质生物膜反应器(MBfR)将微孔膜和氢气自养工艺有机结合。H2在中空纤维膜的膜内外无泡曝气,以浓度差为传质动力,降低了曝气能耗,大大提高了H2的利用效率,还有效防止了H2爆炸的发生[6]。中空纤维膜具有较大的比表面积,可为微生物提供附着和生长的场所,保证反应器内维持较高的微生物量,既提供了载体,又加强了气液传质。
对氯硝基苯很难在水体中自行降解,MBfR反应器可用于去除水中的对氯硝基苯。反应过程中,H2在膜内通过中空纤维膜上的微孔,在压力的作用下,以无泡方式从纤维膜内壁扩散到外壁的生物膜,被附在膜上的氢自养还原菌利用。膜表面的微生物利用外部进水中的氧化性污染物进行新陈代谢,将p-NCB降解为低毒或无毒产物,从而达到净化水质的目的。
3 实验方法
把接种菌置于MBfR反应器中进行一段时间的驯化,中空纤维膜的外表面会聚集一层黄褐色的生物固体,反应器生物驯化和富集出理想细菌,挂膜完成。人工配制模拟实验污水,采用缓冲液(KH2PO4+Na2HPO4)调节进水的pH,同时在反应器进水中投加营养元素,以满足微生物的生长代谢需要,以便更准确地模拟实际水质背景下,各影响因素对p-NCB还原降解效果的影响。
本文基于氢基质生物膜反应器的生物降解展开研究,选择反应时间为4d,系统考察对氯硝基苯生物降解过程中的氢气压力、对氯硝基苯浓度、硝酸盐浓度等因素对降解p-NCB的影响。设置对氯硝基苯初始浓度为 0.5~5 mg·L-1,氢分压为 0.04~0.07 MPa,硝酸盐浓度为 0.5~50 mg·L-1,水样经 0.45 μm滤膜过滤后,采用高效液相色谱法测定。
4 实验结果与讨论
4.1 对氯硝基苯初始浓度的影响
为了评价不同的对氯硝基苯负荷对反应器性能的影响,以及过高的对氯硝基苯负荷是否会产生负面作用,确定反应器在不同的对氯硝基苯进水负荷对p-NCB去除效果的影响,实验选择氢分压为0.04 MPa,进水 p-NCB 浓度分别为 0.5、1、2、5、10 mg·L-1,考察反应器中p-NCB的去除情况。
图2是不同的p-NCB初始浓度下,氢自养菌生物还原p-NCB的情况。整个反应周期内,随着进水p-NCB的浓度增加,出水p-NCB的浓度逐渐降低,去除率逐渐增加,各浓度条件下p-NCB的生物降解效果均较好,去除率均高于89%。进水p-NCB浓度由0.5 mg·L-1升高到10 mg·L-1,去除率从进水浓度为0.5 mg·L-1时的89%升高到2 mg·L-1的94.2%,进水浓度为10mg·L-1时,出水中p-NCB去除率减小为92%。总体来说p-NCB的去除率随进水负荷的增加呈逐渐上升趋势,在进水浓度为2 mg·L-1时,达到最大94.2%。本实验条件下,对氯硝基苯的负荷升高并未明显影响其去除率,p-NCB的去除率并不完全随进水中p-NCB的增大而升高。理论上可通过增加p-NCB的进水负荷来提升去除率,从而提升反应器的去除效能。就本实验装置而言,设置p-NCB进水浓度为2mg·L-1,既能使反应器对p-NCB处理速度达到较高水平,又能满足排放标准。
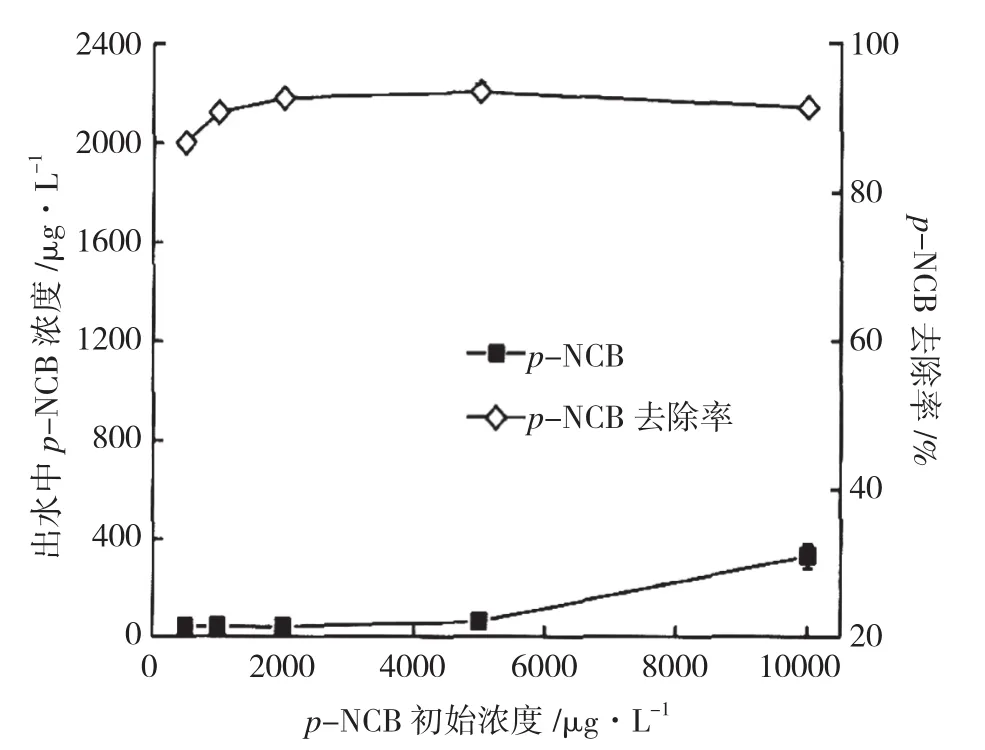
图2 p-NCB进水浓度对其去除率的影响
4.2 氢气压力的影响
H2作为p-NCB还原的电子供体,将直接影响p-NCB的还原效果。反应器生物膜中,过低的H2分压可能会导致电子供体不足,使反应器发挥不出其性能,但H2分压过高又会造成浪费,还存在潜在的危险。因此,设置合理的H2分压,为反应器提供较多的可被利用的H2显得尤为重要。实验选择进水p-NCB浓度为2mg·L-1,H2分压分别设置为0.04、0.05、0.06、0.07MPa,考察在不同 H2分压下反应器中p-NCB的去除情况,结果见图3。
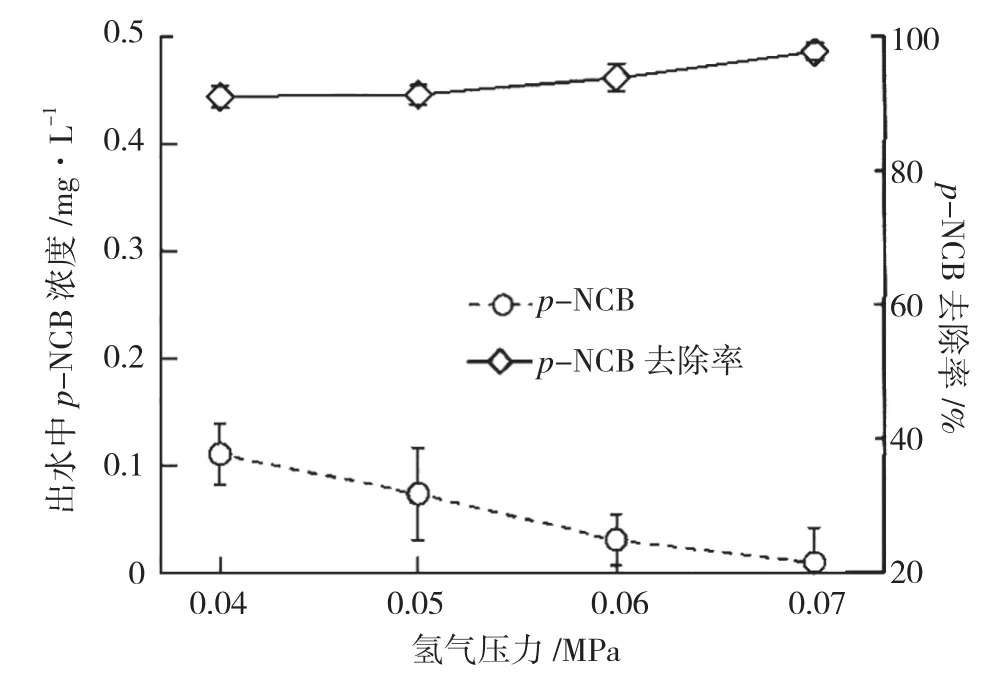
图3 氢气压力对p-NCB去除的影响
由图3可见,随H2分压的升高,出水中p-NCB的浓度逐渐降低,p-NCB去除率由94.2%升至98%。结果表明提高H2分压对p-NCB的去除有促进作用,增加氢气压力对p-NCB的还原有正面效应,原因可能是相对增加了生物膜的活性层厚度。p-NCB的去除率虽有升高,但升幅较小,说明过多地升高氢气压力,并不能使去除率呈线性增加。氢气压力对去除效果的促进作用,随H2分压的增加逐渐变小,并不能带来p-NCB去除量的线性增长,过高的H2分压可能会造成浪费。根据本实验结果,在保障去除率和经济成本要求的前提下,控制氢气压力为0.04 MPa。
4.3 硝酸盐的影响
硝酸盐是地下水中含有的常规氧化性污染物。在厌氧条件下,硝酸盐进行反硝化反应时,会被微生物作为电子受体消耗H2,从而对p-NCB的还原产生电子供体的竞争。有研究表明,反硝化还原过程中产生的中间产物如NO2-、N2O等,对氯代有机物的还原脱氯作用有抑制效应。由于硝酸盐是p-NCB生物还原降解的潜在抑制因子,因此,有必要进一步考察硝酸盐对p-NCB还原的影响。选择氢分压为0.04 MPa,进水p-NCB浓度为2 mg·L-1,硝酸盐浓度分别为 0.5、5、10、20、50mg·L-1,考察硝酸盐对p-NCB还原的影响,结果见图4。
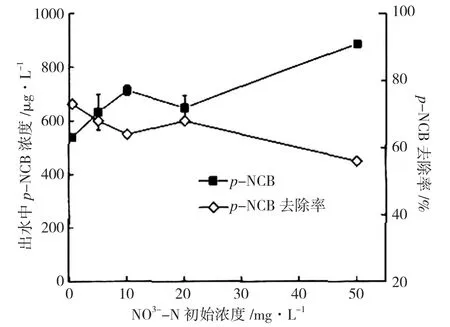
图4 硝酸盐浓度对p-NCB还原的影响
由图4可知,进水硝酸盐浓度的改变,对p-NCB的生物还原效果有较明显的影响。随着硝酸盐的浓度升高,p-NCB的出水浓度升高,去除率逐渐降低,p-NCB的去除效果变差。进水硝酸盐浓度为0.5mg·L-1时,p-NCB的去除率最高,达到73.1%以上;进水硝酸盐浓度升高至50 mg·L-1时,p-NCB的去除率最低,为55.6%;硝酸盐浓度高于5 mg·L-1后,对p-NCB的还原产生了明显的抑制效应,表明硝酸盐的浓度升高对p-NCB的去除有明显的抑制效应。Nelson等人[8-9]研究发现,硝酸盐浓度高于4.4 mg·L-1时,对四氯乙烯的还原脱氯作用有明显的抑制,这可能是因为硝酸盐的中间还原产物NO2-和N2O,会对p-NCB还原菌产生毒害作用,反硝化过程中产生的中间产物积累,对还原脱氯微生物有毒性作用,进而抑制其降解。同时,硝酸盐作为第一电子受体,反硝化细菌会优先将氢气作为电子供体,还原p-NCB,氢气的供应量不变时,p-NCB的生物还原会受到NO3-还原过程中电子供体的竞争性抑制。进水硝酸盐的浓度增加,即反应器中电子受体的总量增加,需要消耗更多的电子供体,在电子供体总量受到限制的条件下,硝酸盐比p-NCB更具有电子竞争优势,导致氢气的可利用率降低,从而限制了p-NCB的生物降解。
5 结论
1)MBfR生物膜中的氢基质自养微生物,能够以氢气为电子供体,有效还原降解水中的p-NCB,通过微生物的逐步还原转化,使p-NCB降解或降低毒性。反应过程中,p-NCB的去除率最高达94.2%。MBfR可提高p-NCB的可生化降解性,对p-NCB有较大的去除潜力。
2)增加进水的p-NCB浓度,并未明显影响其去除率,各浓度条件下的p-NCB去除率均在89%以上。随着进水p-NCB的浓度增大,MBfR氢自养菌对p-NCB的生物还原作用仍有提高,p-NCB的去除率也随之增加。本实验中,适宜的p-NCB进水浓度为 2mg·L-1。
3)氢气压力对p-NCB的还原有正面效应,但过多地升高氢气压力,并不能使去除率呈线性增加,过高的H2分压可能会造成浪费。为了满足反应器的去除性能和经济成本要求,本实验中,p-NCB还原最适宜的氢气分压为0.04MPa。
4)水中共存的硝酸盐对p-NCB的生物还原有抑制作用,硝酸盐会消耗更多的氢气,会对p-NCB还原产生电子供体的竞争性抑制。此外,反硝化-还原的毒性中间产物对还原脱氯微生物有毒性,因此在实际的地下水处理工艺中,必须考虑硝酸盐的因素。

