基于层次分析法结合Box-Behnken响应面法优选陈皮麻黄饮水提工艺*
谭娥玉,王贤儿,林信亨,马少锋,关琴笑,唐兴荣
(江门市五邑中医院,广东 江门 529000)
陈皮麻黄饮是名中医唐兴荣在临床上实践多年的验方,该方由二陈汤和三子养亲汤加减化裁而成,由陈皮、苦杏仁、紫苏子、桔梗、麻黄、干姜、甘草、五味子、金荞麦9味中药组成,具有温肺化饮、止咳平喘的功效,主要用于日久不愈的咳嗽诸证,现拟将其制备为合剂。为确保制剂质量的稳定性及有效性,本实验以苦杏仁苷、橙皮苷、迷迭香酸、甘草酸及总黄酮含量为综合评价指标,采用层次分析法(AHP)确定各指标权重系数,结合Box-Behnken响应面法优选陈皮麻黄饮的水提工艺,为进一步完善该制剂的制备工艺提供可靠依据。
1 仪器与材料
1.1 材料陈皮、苦杏仁、紫苏子、桔梗、麻黄、干姜、甘草、五味子、金荞麦饮片均购自广州市集芝宝中药有限公司,经我院药学部李燕晖副主任中药师鉴定为正品;橙皮苷对照品(批号:MUST-19030701,纯度:98.46%)、苦杏仁苷对照品(批号:MUST-19042820,纯度:99.28%)、迷迭香酸对照品(批号:MUST-19053107,纯度:99.02%)、甘草酸单铵盐对照品(批号:MUST-16113011,纯度:99.10%)(成都曼思特生物科技有限公司);磷酸为分析纯,水为超纯水,甲醇为色谱纯。
1.2 仪器1260 InfinityⅡ型HPLC仪[美国Agilent公司,包括四元泵(G7111A)、自动进样器(G7129A)、柱温箱(G7129A)、DAD检测器(G7117C)、色谱工作站(OpenLAB CDS Chem-Station)];WH-800型超声波清洗机(济宁万和超声电子设备有限公司);HH-3A型数显恒温三温水浴锅(金坛市精达仪器制造有限公司);XS205DU型电子分析天平(梅特勒-托利多仪器上海有限公司);T6型紫外可见光-分光光度计(北京普析通用有限责任公司);Best-S30型超纯水机(芷昂仪器上海有限公司)。
2 方法与结果
2.1 高效液相色谱法同时测定陈皮麻黄饮中苦杏仁苷、橙皮苷、迷迭香酸、甘草酸的含量
2.1.1 色谱条件 色谱柱:Infinity Lab Poroshell 120 EC-C18(4.6 mm×250 mm,5 μm);流动相为甲醇(A)-0.2%磷酸(B)梯度洗脱:0.00~5.00 min,10%A,5.01~6.00 min,10%~18%A,6.01~16.00 min,18%A,16.01~17.00 min,18%~20%A,17.01~32.00 min,20%A,32.01~33.00 min,20%~50%A,33.01~45.00 min,50%A,45.01~50.00 min,10%A。检测波长:苦杏仁苷207nm,0~16min;橙皮苷283 nm,16~25 min;迷迭香酸330 nm,25~30 min;甘草酸250nm,35~50min。流速:1.0mL/min;柱温:35℃,进样量:5 μL。
2.1.2 对照品溶液配制
2.1.2.1 对照品贮备液配制 精密称取苦杏仁苷16.55 mg,置5 mL量瓶中,加甲醇制成每1 mL含3.31 mg苦杏仁苷的贮备液;精密称取橙皮苷16.40 mg,置5 mL量瓶中,加甲醇制成每1 mL含3.28 mg橙皮苷的贮备液;精密称取迷迭香酸4.41 mg,置10 mL量瓶中,加甲醇制成每1 mL含0.441 mg迷迭香酸的贮备液;精密称取甘草酸单铵盐9.34 mg,置5 mL量瓶中,加甲醇制成每1 mL含1.868 mg甘草酸单铵盐的贮备液。
2.1.2.2 混合对照品溶液配制 分别精密量取苦杏仁苷贮备液4 mL、橙皮苷贮备液2 mL、迷迭香酸贮备液1 mL、甘草酸单铵盐贮备液1 mL,置10 mL量瓶中,加甲醇制成每1 mL含苦杏仁苷1.324 0 mg、橙皮苷0.656 0 mg、迷迭香酸0.044 1 mg、甘草酸单铵盐0.186 8 mg的混合对照品溶液。(甘草酸质量=甘草酸单铵盐质量/1.020 7)
2.1.3 供试品溶液配制 精密量取陈皮麻黄饮水提液20 mL,水浴蒸干,加甲醇20 mL超声30 min,转移至20 mL量瓶中,加甲醇稀释至刻度,摇匀,经0.45 μm微孔滤膜过滤,即得。
2.1.4 阴性对照品溶液配制 取缺少苦杏仁、陈皮、紫苏子、甘草的阴性对照样品,按上述供试品溶液的制备方法制备,即得阴性对照品溶液。
2.1.5 系统适应性试验 取上述混合对照品溶液、供试品溶液、阴性对照品溶液适量,按“2.1.1”项下色谱条件进样测定,记录色谱,见图1。由图1可知,供试品溶液色谱图中,在与对照品色谱相应位置上有相同的色谱峰,且阴性对照对测定无干扰,说明该方法可行。
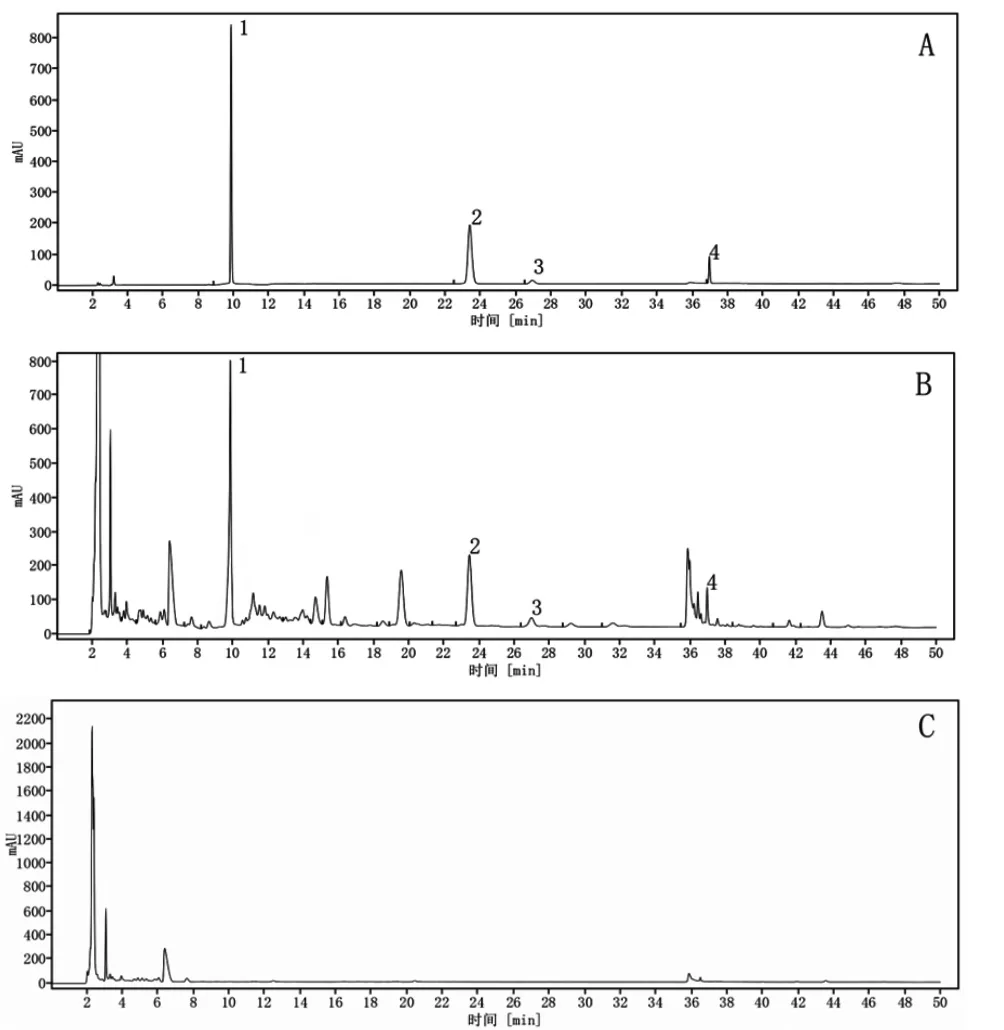
图1 HPLC色谱图
2.1.6 线性关系考察 将混合对照溶液稀释为系列对照品溶液,按“2.1.1”项下色谱条件进样分析,测定峰面积,以峰面积为纵坐标,对照品溶液浓度为横坐标,进行线性回归计算,即得苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单铵盐的回归方程、相关系数及线性范围。结果表明4种指标成分在各自含量范围内线性关系良好。(见表1)
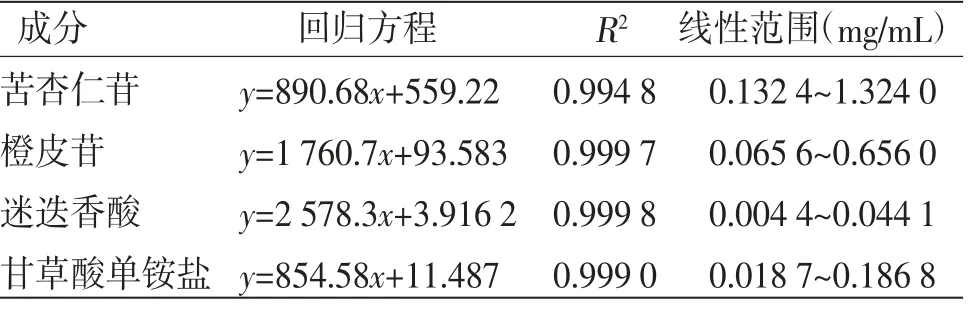
表1 线性关系考察结果
2.1.7 精密度试验 精密吸取混合对照品溶液5 μL,按“2.1.1”项下色谱条件连续进样测定5次,以峰面积指标计算RSD(n=5)。结果显示苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单铵盐峰面积的RSD分别为0.92%、1.02%、1.03%、0.97%,表明仪器精密度良好。
2.1.8 稳定性试验 取同一供试品溶液,分别于制备后0、2、4、8、24 h,按“2.1.1”项下色谱条件进样,测定峰面积,计算苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单胺盐峰面积RSD,RSD分别为1.02%、1.05%、1.23%、2.69%(n=5),表明供试品溶液在24 h内的稳定性良好。
2.1.9 重复性试验 取同一水提液适量,按“2.1.3”平行制备6份供试品溶液,按“2.1.1”项下色谱条件,同时测定苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单铵盐的峰面积,计算其峰面积RSD,RSD分别为0.94%、0.45%、0.67%、2.16%(n=6),表明方法重复性良好。
2.1.10 加样回收率试验 精密吸取已知含量的供试品溶液10 mL,共6份,分别置于20 mL量瓶中,分别精密加入各对照品溶液,加水定容至刻度,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件进样,测定苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单铵盐峰面积,由回归方程计算,计算平均加样回收率和RSD。苦杏仁苷、橙皮苷、迷迭香酸、甘草酸单铵盐平均加样回收率分别为95.32%、96.64%、96.09%、95.87%,其RSD分别为4.63%、3.05%、4.89%、2.80%,均小于5%。
2.2 紫外-分光光度法(UV)测定陈皮麻黄饮中总黄酮的含量
2.2.1 供试品溶液的制备 取20 mL浓缩水提液置于蒸发皿中,水浴蒸干后加入20 mL甲醇,超声30 min,置于20 mL容量瓶中,定容,得甲醇提取液。精密吸取甲醇提取液1 mL,置于10 mL容量瓶中,定容,即得供试品溶液。
2.2.2 对照品溶液的配制 准确称量橙皮苷对照品7.03 mg,置于20 mL容量瓶中,用甲醇定容到刻度,摇匀,即得0.351 5 mg/mL的对照品溶液。
2.2.3 显色剂的配制 称取ZrOCl2·8H2O固体2 g置于100 mL容量瓶中,加甲醇溶解并定容至刻度,摇匀,配成2%ZrOCl2·8H2O甲醇溶液。
2.2.4 测定方法及波长的选择 参考相关文献[1-2],准确吸取供试品溶液、对照品溶液各1 mL,置于20 mL容量瓶中,分别加入1 mL 2% ZrOCl2·8H2O甲醇溶液进行显色,再加入甲醇定容至刻度,摇匀。用2% ZrOCl2·8H2O甲醇溶液作为空白对照,放置15 min后,用紫外-可见分光光度计在200~600 nm波长处进行全波段扫描,结果显色的供试品溶液、对照品溶液在313 nm波长处有最大吸收,故选择总黄酮的测定波长为313 nm。
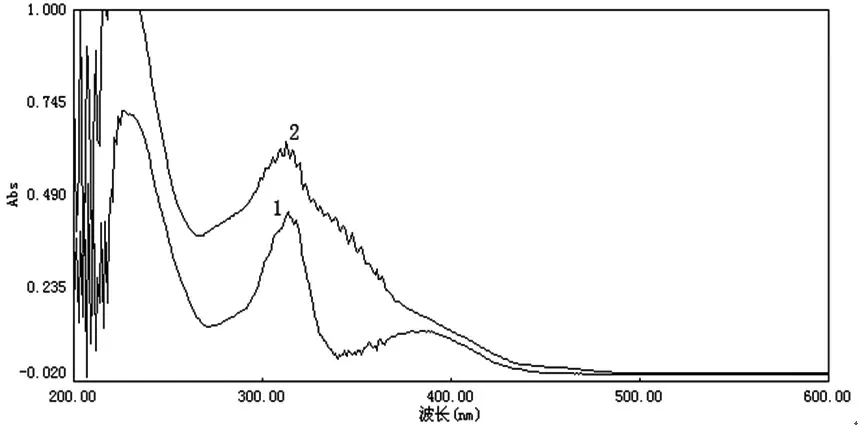
图2 全波段扫描光谱图
2.2.5 线性关系考察 取0.351 5 mg/mL对照品溶液0.6、0.8、1、1.2、1.4 mL分别置于20 mL容量瓶中,加入1 mL 2%ZrOCl2·8H2O甲醇溶液,用甲醇定容至刻度,摇匀。在313 nm波长处进行检测,结果在0.021 09~0.049 21 mg/mL范围内具良好线性,回归方程y=15.092x+0.011 1,R2=0.999 6。
2.3 层次分析法(AHP)确定各考察指标的权重系数 参考相关文献[3-5],根据本方的配伍特点、各药材的实际配比及药理作用强弱,采用AHP法将橙皮苷、苦杏仁苷、迷迭香酸、甘草酸、总黄酮含量这5个指标的重要程度予以量化,确定各指标优先顺序:橙皮苷>苦杏仁苷=迷迭香酸>甘草酸>总黄酮,具体判断矩阵见表2。采用几何平均法计算得橙皮苷、苦杏仁苷、迷迭香酸、甘草酸、总黄酮含量权重系数分别为0.449 8、0.193 7、0.193 7、0.105 0、0.057 7,随机一致性比率(CR)<0.1,说明指标优先比较判断矩阵满足一致性要求,权重系数有效、可行。

表2 各指标5个层次的优先矩阵
2.4 Box-Behnken响应面法优化水提工艺
2.4.1 水提工艺 称取处方量1/10药材,置于500 mL具塞三角烧瓶,加适量纯水,浸渍30 min后,加热煮沸,调至慢火,静置,抽滤,滤液浓缩至100 mL。
2.4.2 响应面设计及结果 本制剂是以原药材饮片进行投料煎煮的传统剂型,方中含有较多根茎类及种子类坚实药材,水提过程中扩散较慢,为利于成分充分浸出,参考相关文献[6-9],并根据前期单因素实验结果,以溶媒用量、提取次数和提取时间为影响因素,确定优化范围,以5个指标含量作为水提工艺的考察指标,设计3因素3水平Box-Behnken响应面实验(见表3),按照实验安排表(见表4)平行称取17份药材按照“2.4.1”项下方法进行实验,按照“2.1.1”项下方法测定苦杏仁苷、橙皮苷、迷迭香酸、甘草酸含量,按照“2.2.4”项下方法测定总黄酮含量,结合归一化法和权重系数计算总分,总分=(苦杏仁苷含量×0.193 7/最大苦杏仁苷含量+橙皮苷含量×0.449 8/最大橙皮苷含量+迷迭香酸含量×0.193 7/最大迷迭香酸含量+甘草酸含量×0.1050/最大甘草酸含量+总黄酮含量×0.057 7/最大总黄酮含量)×100,结果见表4。

表3 Box-Behnken实验设计因素水平表
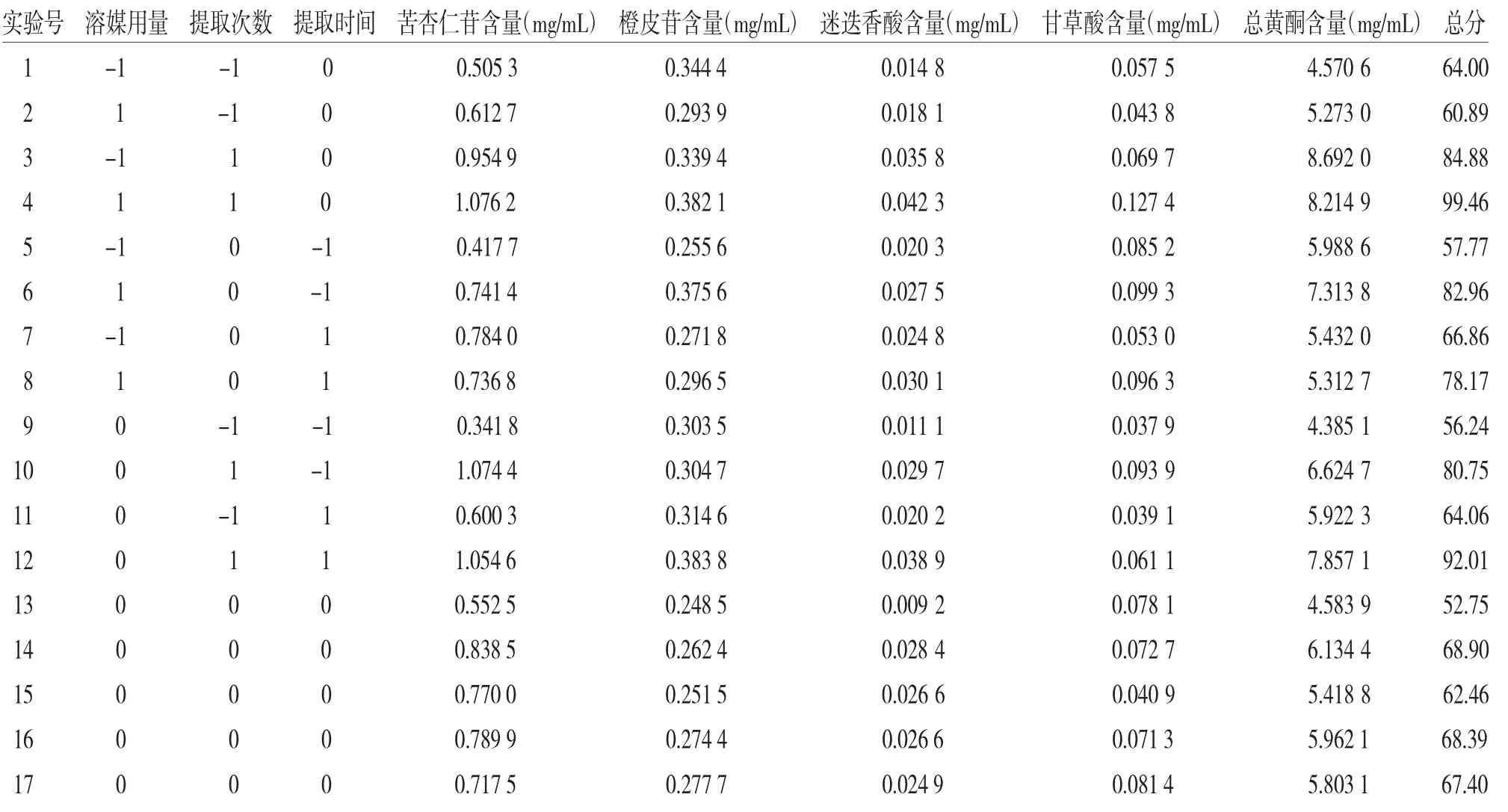
表4 响应面实验安排及结果
2.4.3 实验结果分析 利用方差分析对各因素进行多元二次回归,得到的回归方程Y=64.70+6.00A+13.99B+2.92C+4.42 AB+5.84A2+7.67B2,响应面结果的方差分析见表5,结果显示,水提工艺考察的3个因素中,溶媒用量(A)为显著项,提取次数(B)为极显著项,提取时间(C)为不显著项;二次项中,B2为显著项,表明考察因素与响应面值之间并非简单的线性关系。模型整体具有极显著性(P=0.000 6),且失拟合程度不显著(P=0.705 3),表明模型能较好地反映溶媒用量(A)、提取次数(B)、提取时间(C)与评价指标加权得分(Y)之间的变化关系,能够预测和分析该水提工艺。按照所得模型绘制的溶媒用量、提取次数、提取时间的交互作用对陈皮麻黄饮的水提工艺影响的3D响应面图和等高线图见图3,从图3中可以看出,考察的3个对象3者交互作用不明显。软件Design Expert 12得出陈皮麻黄饮的水提工艺为溶媒用量12倍,提取次数3次,每次提取时间1 h。
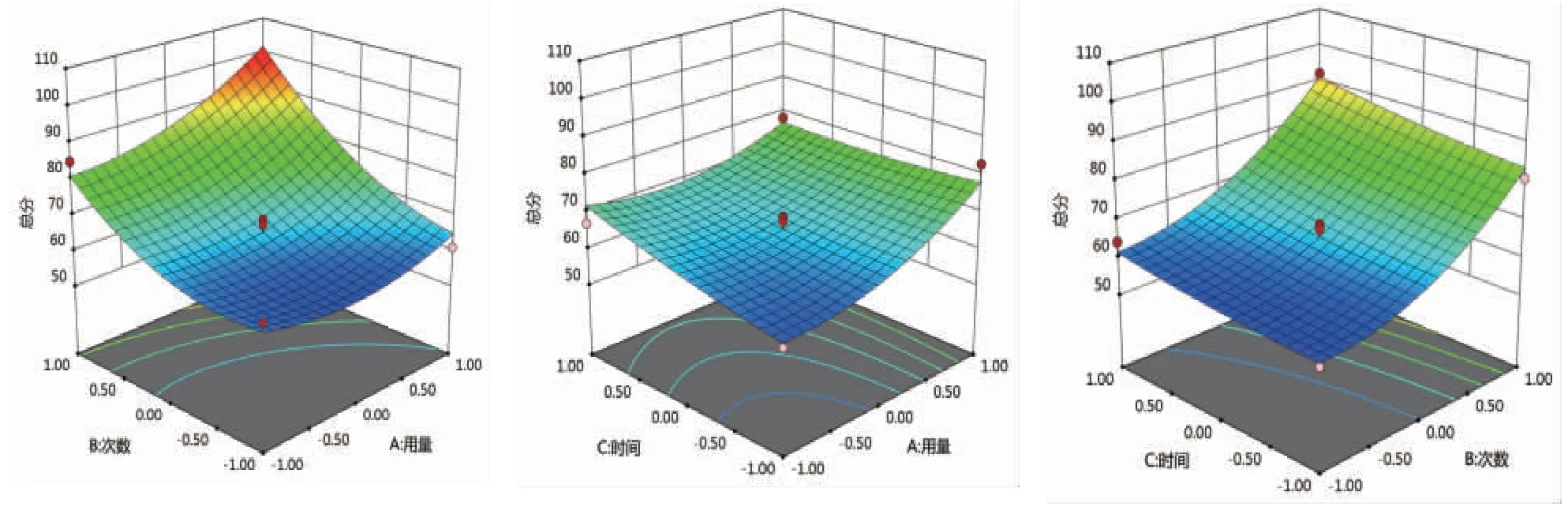
图3 溶媒用量(A)、提取次数(B)、提取时间(C)交互作用的三维响应面图
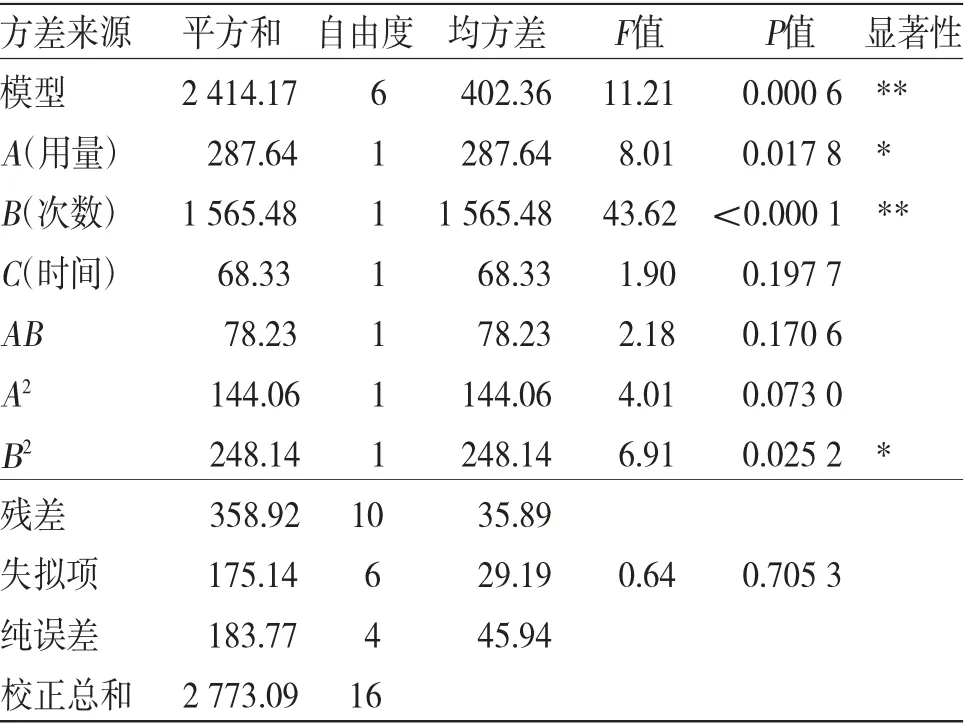
表5 综合得分回归模型方差分析表
2.4.4 验证实验 按照优选工艺,进行3次平行验证实验,结果见表6,综合评分说明优选的提取工艺合理可行。苦杏仁苷、橙皮苷、迷迭香酸、甘草酸、总黄酮平均含量分别为1.060 7、0.454 6、0.034 7、0.105 6、8.203 6 mg/mL,RSD分别为4.05%、4.70%、1.36%、2.65%、1.18%,预测综合得分102.61,实际综合得分(101.28±3.10),RSD为3.06%,与预测值差异较小,且在合理范围内,表明提取工艺结果稳定,预测结果可信。
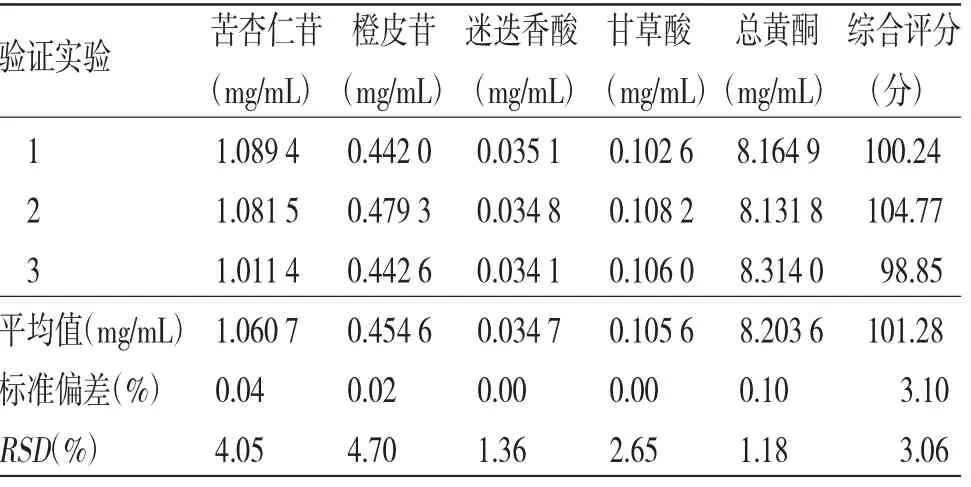
表6 验证实验结果
3 讨 论
陈皮麻黄饮的组方为9种常见的中药,处方来源为二陈汤和三子养亲汤加减化裁而成。本研究根据其组方配伍特点,选择制剂中有效成分和组分作为评价指标进行研究。方中陈皮为君药,研究表明橙皮苷为陈皮的主要活性成分,具有抗氧化、抗炎、抗细菌、抗病毒、抗肿瘤、抗过敏、调节免疫力等药理作用[10];苦杏仁中的苦杏仁苷具有止咳、平喘、抗肺纤维化等药理作用[11];迷迭香酸为紫苏子主要的酚酸类活性成分[12];甘草酸为甘草中主要活性成分之一[13-14];黄酮类化合物是植物中重要的次生代谢产物,在抗病毒、抗炎、降血脂、降血糖、抑菌和抗癌等方面发挥着重要的作用[15]。从有效成分充分提取的角度考虑,结合该方的君、臣、佐、使配伍关系,将橙皮苷、苦杏仁苷、迷迭香酸、甘草酸及总黄酮的含量作为考察指标,采用AHP法对指标赋权并结合归一化法计算各组实验总分,同时也兼顾处方的配伍特点及药效物质基础,既能有效保障提取的全面性,又符合中医整体论治的指导原则[16]。
中药复方提取液中黄酮类物质种类繁多,理化性质也存在差异,而UV法的专一性较差,本课题组在预实验中采用直接UV法测定总黄酮含量,由于存在较强的背景吸收而导致测定值偏高。陈皮麻黄饮中以陈皮为君药,其主要的有效成分为橙皮苷,属于二氢黄酮类化合物,在硝酸铝显色体系中不能产生特征吸收峰,因此,本实验最终采用ZrOCl2比色法,利用水提液中的黄酮类成分与ZrOCl2络合反应后,在313 nm波长处吸光度值发生显著变化,所测得的吸光度值与水提液中的黄酮类组分在0.021 09~0.049 21 mg/mL范围内具良好线性关系,而水提液中的其他组分在该波长下无吸收,因此可较好避免背景吸收的干扰。
本实验采用的Box-Behnken是响应面设计中常用方法,与正交法相比,响应面法优点在于精确度更高、模拟程度更好,更适合于多因素、多水平共同影响的实验,也兼顾了影响因素及各因素间的交互作用,通过二项式能更准确地获取与真实实验接近的最优条件[17]。本次优化的提取工艺简便易行,预测效果好,可以为进一步的制剂研发提供理论依据。

