低流量医院行“全腹腔镜下胰十二指肠切除术”临床研究
满泉 庞慧芳 郭雅明 邵志远 陈艳哲 祁向军
通辽市医院肝胆胰外科028000
0 引 言
1992年,Gagner和Pomp[1]首次成功开展腹腔镜下胰十二指肠切除术(laparoscopic pancreaticoduodenectomy,LPD),从此奠定了LPD的应用基础。LPD手术过程复杂、学习曲线长,与胃肠道微创手术相比发展缓慢。经过二十余年的发展,腹腔镜胰十二指肠切除术在国内外较大胰腺中心已广泛开展,甚至已成为常规开展术式[2-5]。国内外常规开展LPD的胰腺中心研究结果表明,LPD具有创伤小、住院时间短、出血少、术后并发症少等优点,并且病死率及肿瘤学治疗效果相近甚至优于开腹手术[6-9]。目前LPD的手术入路以传统入路为主,而多个胰腺中心在探索中开展动脉先行入路、钩突先行技术、No-touch等方式[10-12]。而在低流量医院(年手术量少于25例)安全开展LPD为当今热点问题。2020年通疗市医院肝胆胰外科对3例患者行全腹腔镜(3D)下“结肠后入路,钩突先行”胰十二指肠切除术,获得了良好的临床效果。
1 资料与方法
1.1 临床资料
病例1,女性患者,56岁。因“间断性腹痛1月,皮肤及巩膜黄染10 d”于2020年1月11日入院。否认高血压、心脏病史,否认糖尿病史,否认肝炎、结核病史,否认脑血管疾病史,否认吸烟、饮酒史,否认手术史。甲胎蛋白(AF P):4.63 ng/ml,癌胚抗原(CEA):5.69 ng/ml,糖类蛋白(CA19-9):896.40 U/ml;谷草转氨酶(ALT):361.00 U/L,谷丙转氨酶(AST):247.00 U/L,总胆红素(TBIL):182.00μmol/L,直接胆红素(DBIL):176.70μmol/L。胃镜结果显示:慢性浅表性胃炎,十二指肠球部溃疡。腹部增强磁共振成像(MRI)结果:考虑胰头占位性癌变(CA)伴梗阻性黄疸改变。
病例2,男性患者,51岁,农民。因“皮肤及巩膜黄染3个月,加重伴皮肤瘙痒0.5个月”于2020年2月15日入院。既往有间断性转氨酶升高2年,有饮酒史二十余年,白酒每日约0.2 kg,否认吸烟。否认高血压、心脏病史,否认糖尿病史,否认肝炎、结核病史,否认食物、药物过敏史,否认手术史。AF P:5.04 ng/ml,CE A:2.33 ng/ml,CA19-9:203.30 U/ml;AL T:131.00 U/L,AST:65.00 U/L,TBIL:162.40μmol/L,DBIL:158.50μmol/L,胃镜提示:慢性萎缩性胃炎伴十二指肠乳头癌变。胃镜病理报告:十二指肠乳头高分化腺癌。腹部增强CT显示:梗阻性胆管扩张,梗阻平面在胆总管下段,考虑壶腹CA可能。
病例3,男性患者,60岁。因“皮肤及巩膜黄染3周”于2020年8月13日入院。否认高血压、心脏病史,否认糖尿病史,否认肝炎、结核病史,否认脑血管疾病史,有饮酒史40年,白酒每日约0.25 kg,5年前曾行阑尾切除术。AF P:3.30ng/ml,CEA:3.51ng/ml,CA19-9:64.92 U/ml;ALT:53.00 U/L,AS T:43.00 U/L,T BIL:171.50μmol/L,DBIL:149.00μmol/L。腹部增强MRI显示:梗阻性胆管扩张,胆总管下段及十二指肠乳头处占位,考虑壶腹CA可能。
3例患者术前血尿常规、肾功能、血糖、血凝均未见异常;心肺功能无明显异常。
1.2 方法
全麻生效,患者平卧分腿位,常规消毒皮肤,铺无菌巾,于脐下2 cm处纵行切口约1 cm,气腹针穿刺腹腔,建立气腹,10 mm戳卡穿入腹腔作为观察孔,气腹压力为14 mmHg(1 mmHg≈0.133 kPa),进腹常规探查腹腔,腹腔、盆腔、肝胆未见异常结节;腹腔镜下右侧腋前线与右侧肋缘交界处、右侧锁骨中线与脐水平线交界处各做5 mm、10 mm切口作为主操作孔,与对侧再打两孔作为辅助操作孔。
将横结肠向头侧提起,横结肠下十二指肠降段与水平部交界处外侧分离系膜,打开十二指肠降段及胰头钩突后腹膜,显露下腔静脉、左肾静脉,左肾静脉汇入下腔静脉处左肾静脉上缘寻找肠系膜上动脉(SMA),探查肿瘤未侵及肠系膜上动脉,术中决定行腹腔下胰十二指肠切除术。沿下腔静脉向头侧游离,与肝脏脏面打通,显露肝尾状突(图1A)。
轻提十二指肠水平部,打开融合筋膜,解剖、显露肠系膜上静脉(SMV)及第一支空肠静脉(J1V),沿SMV向头侧游离肠系膜上静脉,并结扎、切断胃结肠干(Helen干),显露、保护结肠中静脉。打开横结肠系膜,沿SMV主干游离至胰颈下缘。再显露Treitz韧带,提起空肠起始端,显露肠系膜下静脉(IMV),十二指肠旁陷凹处打开十二指肠升部后腹膜,对侧打开Treitz韧带,于Treitz韧带远端10 cm肠系膜无血管处打开系膜,应用腔镜切割闭合器切断空肠,向内侧游离、切断十二指肠系膜,显露J1V,并保护J1V,游离、切断J1V与空肠间小分支。十二指肠及空肠起始端向小肠系膜孔内侧移位至SMV右侧;游离胰头钩突与SMV之间分支,游离、切断胰十二脂肠下静脉(IPDV),再沿SMV游离、切断胰十二指肠上后静脉(PSPDV)。再沿SMA游离,显露空肠第一支动脉(J1A),并予以保护,沿J1A游离出胰十二指肠下动脉(IPDA),结扎、切断IPDA。SMA与胰头钩突间小分支应用超声刀切断,游离至胰腺颈部,显露门静脉、肠系膜上静脉右侧缘,骨骼化SMA右侧缘。将结肠放下,应用超声刀打开胃结肠韧带,向左游离至胃网膜左血管,向右游离、切断胃网膜右动静脉,打开胃结肠系膜融合处,并向右继续游离打开Kocher切口,打开十二指肠降段后侧腹膜与对侧汇合,顺行切除胆囊。
将胃大弯侧胃网膜血管交界处无血管处游离、切断大网膜,对侧小网膜处打开小网膜,应用切割闭合器切断胃;沿胰腺上缘清扫8区淋巴结,显露肝总动脉,沿肝总动脉左侧游离,清扫第7组淋巴结,显露胃左动脉、冠状静脉;沿肝总动脉游离处肝固有动脉,显露、结扎胃十二指肠动脉(GDA)、胃右动脉,清扫12a淋巴结。
显露胰上三角,超声刀打开胰上三角处系膜,显露门静脉,贯通胰颈后隧道。应用超声刀于门静脉左缘切断胰腺颈部,游离门静脉与十二指肠之间疏松组织,完全游离,并清扫12p、12b淋巴结;与左右肝管汇合下方切断肝总管,将整块标本(enbloc)切除(图1B)。
消化道重建应用Child法:胰肠吻合应用黏膜对黏膜吻合法将远端空肠在结肠后与胰腺断端行端侧吻合,应用4-0prolene线将胰腺断端与空肠后壁浆肌层吻合,胰管置入支撑管,长约15 cm,并用4-0prolene先固定1针,胰管对空肠侧开口,行胰管、空肠黏膜吻合,前壁再行空肠浆肌层缝合(图1C)。距胰肠吻合口远5 cm处行胆肠端侧吻合,应用刀刺线连续缝合;胰肠吻合口远端45 cm处行胃肠吻合。
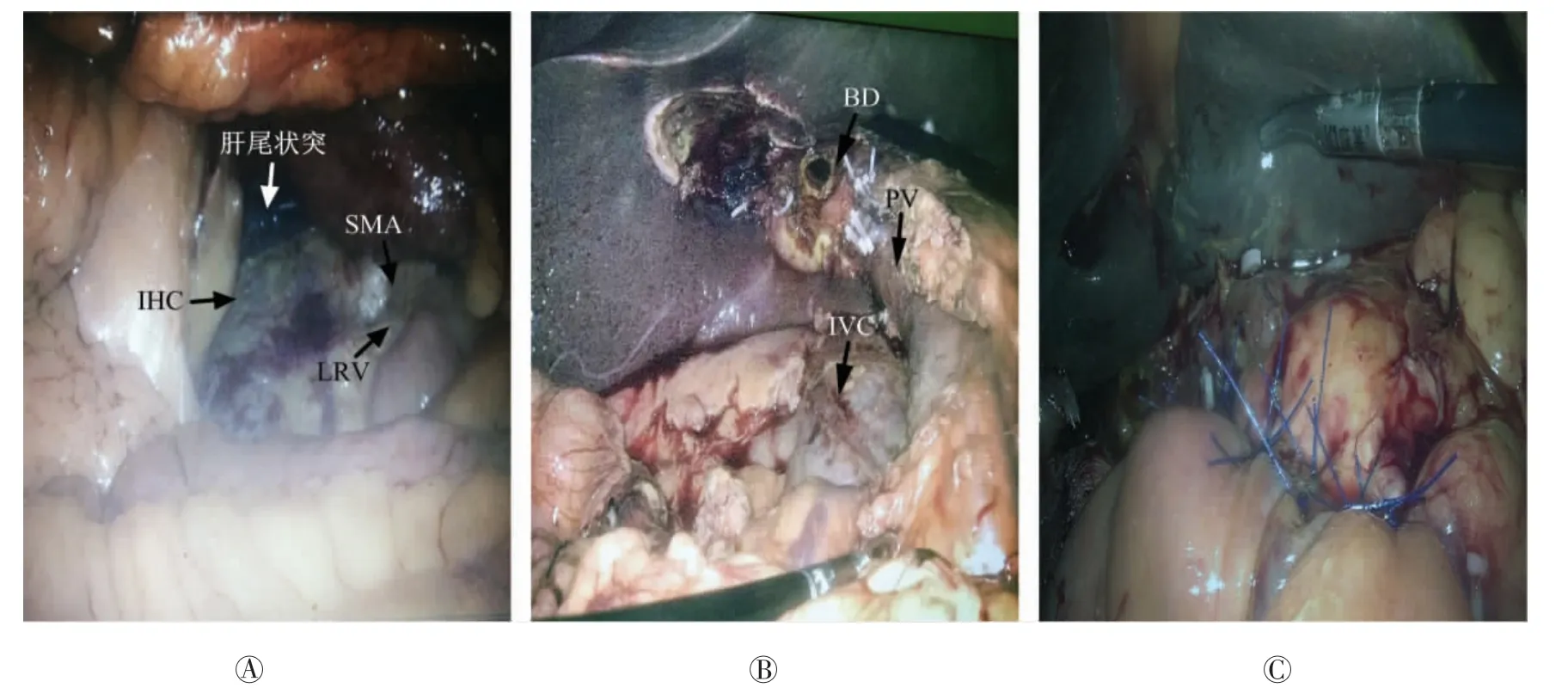
图1 手术方法
取出标本,腹腔镜下胰肠吻合口前方、胆肠吻合口后方以及肠系膜上静脉右侧壁分别留置引流管,自腹壁的戳口引出固定。
2 结果
手术前患者均未进行减黄治疗。术中平均出血量为(456.67±81.45)ml,平均手术时间为(413.33±24.66)min。术后患者均未见胰瘘、胆漏、肠瘘。术后均未见胃排空障碍,排气时间为术后第4天、第5天、第5天,均于术后第6天拔出胃管及进流食,腹腔引流管拔出时间均为第7天、第7天、第9天;术后恢复均良好,术后住院时间各为18、15、16 d。病理结果:1例为胰头高-中分化导管腺癌,清扫淋巴结结果4/18;1例为十二指肠壶腹高-中分化腺癌,清扫淋巴结结果0/11;1例为十二指肠乳头高分化腺癌,清扫淋巴结结果0/7。
3 讨论与结论
胰十二指肠切除术是治疗胰头及壶腹周围肿瘤的唯一可能治愈的方法。随着微创技术的发展及腹腔镜器械的改革,目前腹腔镜胰十二指肠切除术(LPD)发展迅速,国内外较大的胰腺中心已广泛开展该手术。LPD为风险高、难度大、学习曲线长,被誉为“外科手术的珠穆朗玛峰”[13]。研究表明,手术质量与手术数量密切相关[14]。美国癌症数据库资料显示,胰十二指肠切除术年手术量少于25例的低流量医院开展LPD的质量和安全性较大流量中心差距明显[15]。LPD难度大、过程复杂和学习曲线长,低流量医院开展LPD较缓慢,且低流量医院开展LPD安全性和手术质量正处于探索阶段[16]。目前国内低流量医院开展LPD报道较少。
笔者自2020年1月至8月顺利完成“结肠后入路,钩突先行”技术3例,均取得满意的效果。有团队自2015年开展“结肠后入路,钩突先行”技术行LPD手术,取得了满意的临床疗效[17]。总结该技术要点和优势如下:①传统的PD和LPD手术首先打开Kocher手法分离十二指肠及胰头后方间隙,暴露下腔静脉及腹主动脉,而此法开始于横结肠系膜根部右侧的十二指肠下曲,利用腹腔镜背侧视角,打开十二指肠降部及水平部移行部外侧打开系膜,游离十二指肠后腹膜,显露下腔静脉、左肾静脉,进而显露肠系膜上动脉(SMA),早期探查肿瘤与SMA根部的关系,可明确肿瘤的可切除性。②“结肠后入路,钩突先行”技术利用腹腔镜背侧视角,自胰腺钩突的后方,沿SMV的右侧壁自下而上游离胰腺钩突,保护空肠静脉第一支,离断IPDA,完整游离胰腺钩突。③该技术适用于胰十二指肠区的良性及交界性肿瘤、早期的胆管末端癌、十二指肠乳头癌、十二指肠癌、未侵犯肠系膜血管的胰头癌及胰头钩突癌。④早期即切断胰十二指肠区血供(IPDA、GDA以及胰十二指肠上、下静脉等),使术中出血量明显减少,术野更加清晰。⑤与开放手术相比,最大限度降低了开放手术对肿瘤的挤压及刺激,并早期阻断肿瘤的血行及淋巴转移途径,从而最大限度避免了手术操作造成的肿瘤转移。
本组术后病理结果:1例为胰头高-中分化导管腺癌,4/18;1例为十二指肠壶腹高-中分化腺癌,0/11;1例为十二指肠乳头高分化腺癌,0/7。术后均未出现吻合口瘘、胃排空功能障碍等并发症,恢复良好。
通过笔者团队于低流量医院开展LPD经验总结如下:①熟练掌握解剖知识是手术操作的必备条件。笔者团队成员多次通过进修学习,线上、线下视频、手术演示等多种途径了解、熟练掌握理论及解剖知识。而胰十二指肠切除术中胰头钩突处理是手术最易出血部位,也是手术之难点[18]。因此了解十二指肠、胰头血管解剖是重中之重。②具有扎实的腹腔镜技术是完成LPD的技术支撑。消化道重建,尤其是胰肠吻合是LPD的关键环节,是LPD发展缓慢和阻碍其普遍开展的重要因素之一,亦是导致手术时间较长的重要因素之一[4]。笔者团队具有多年的普外科微创治疗工作经验,并熟练完成如熟练操作腹腔镜胆囊切除、腹腔镜腹股沟疝修补、腹腔下胆总管缝合、腹腔镜下胃肠恶性肿瘤切除、腹腔镜下肝门部胆管癌切除术(bismuth-corletteⅠ,Ⅱ型)、腹腔镜下左半肝切除术、腹腔镜下保脾胰体尾切除术,并能完成开腹胰十二指肠切除术等技术,掌握了镜下分离、缝合、止血等技术。③笔者医院具备3D腹腔镜、超声刀、腔镜下切割闭合器等器械,为完成LPD创造了硬件设备和器械。3D腹腔镜具有视角灵活及立体视野放大的优势,有助于辨别解剖结构,保护重要血管,使血管骨骼化及淋巴结清扫更精准[19]。④笔者有良好团队配合精神,有多年的团队配合经验、配合默契,为手术安全操作、缩短手术时间、手术质量提供了很好的保障。
综上所述,胰腺外科的微创治疗模式是新时代医学发展的大趋势。LPD已在国内外较大的胰腺中心已成为常规术式,必将进一步推广普及。依照“严于术前,慎于术中,勤于术后”的原则,从术前患者选择、手术入路规划、术中标准化流程操作,LPD会像腹腔胆囊切除术一样在全国普及、常规化。通过笔者团队经验,壶腹部周围良恶性肿瘤、胆总管下段肿瘤及胰头早期肿瘤可在低流量医院(具有丰富的开腹胰十二指肠手术经验、娴熟的腹腔镜操作技能、默契的手术团队)推广普及LPD,初学者可选择“结肠后入路,钩突先行”入路方法。LPD在全国普及可为基层患者带来交通方便及经济实惠,深受低流量医院肝胆胰外科医生的青睐,将给广大患者带来福音。
利益冲突所有作者均声明不存在利益冲突

