厚朴煎剂对白色念珠菌及其生物膜影响的初步研究
向晓波 严履冰 周艳萌
(1. 遵义医科大学附属口腔医院口腔外科,贵州遵义563000;2.遵义医科大学2017级,贵州遵义563000;3.遵义医科大学微生物学与免疫学实验室,贵州遵义563000)
高效广谱抗生素的广泛使用、免疫抑制剂滥用、艾滋病及血液系统恶性肿瘤等因素,造成真菌感染率和致死率不断增长,其中白色念珠菌(Candidaalbicans)就是真菌性感染的常见病原体之一[1],同时也是最常见的医院获得性真菌感染的病原体,常在植入的医疗器械上形成生物膜,导致致命的播散性疾病[2]。目前唑类和多烯类抗生素是治疗白色念珠菌感染的主要药物,这些药物均存在一定的毒性,且长期使用可导致白色念珠菌耐药性不断增强[3]。白色念珠菌的一个关键毒力因子是其在酵母和菌丝体两种形态之间可以进行形态转化,此能力在组织入侵、抵抗吞噬和生物膜形成中起着重要作用。生物膜具有引发或延长感染的潜力,并对传统抗真菌治疗产生高水平的耐药性[4-5]。近来研究[6-8]显示,中药及中药提取物在抗生物膜方面具有较好的作用。中药厚朴(Mangnolia officinalis)为木兰科木兰属植物厚朴或凹叶厚朴的干燥干皮、根皮及枝皮。现代药理试验[9]证明,厚朴具有广谱抗菌、抗肿瘤、抗炎、保护心脑血管、抗溃疡以及抗凝血等作用。田玉珠等[10]发现和厚朴酚对白色念珠菌黏附及其生物膜的形成及厚度均有抑制作用。笔者前期的研究[11-12]显示,厚朴冷浸液对白色念珠菌早期黏附和中期生物膜形成有抑制作用,厚朴酚通过抑制白色念珠菌的早期黏附而有效降低其致病性,并对已形成的生物膜具有明显的抑制作用。本课题组拟在前期研究的基础上,进一步探讨厚朴煎剂抗白色念珠菌的作用机制,为厚朴用于临床抗真菌感染提供基础实验依据。
1 材料与方法
1.1 材料
1.1.1 菌种
白色念珠菌 (Candidaalbicans10231,C.albicans,10231) 标准株由遵义医科大学医学微生物学与免疫学实验室馈赠。
1.1.2 药物与试剂
芽管液体培养基按照参考文献[13]制备;厚朴购于遵义医科大学附属医院中药局;酵母蛋白胨葡萄糖 (yeast peptone glucose,YPG) 液体培养基依据文献[14]配制;沙氏琼脂培养基(sabouraud agar medium,SDA)购于杭州滨和微生物试剂有限公司;LIVE/DEAD细菌活力检测试剂盒(L13152)购于赛默飞世尔公司;异硫氰酸荧光素标记的刀豆蛋白 A(FITC-conA)购于美国Sigma公司;SYBR Premix Ex.TaqTM荧光定量 PCR试剂盒、反转录试剂盒购于日本TaKaRa公司;CFX96型实时荧光定量PCR仪。
1.2 方法
1.2.1C.albicans菌悬液的制备
白色念珠菌划线接种于SDA上,培养后挑取单个菌落再划线接种于SDA培养基分离纯化3次,然后挑取单个菌落转种于YPG液体培养基中,37 ℃、90 r/min 摇床培养过夜活化2次,血细胞计数板计数并调整菌液浓度至2× 106个/mL,备用。
1.2.2 药物的配制
60 g厚朴粉末加入1 600 mL三蒸水中,煎煮3次,收集3次的液体混合并浓缩至400 mL获得厚朴煎剂(0.15 g/mL)保存液,无菌滤器过滤并分装放入-20 ℃冰箱保存备用。使用时,将厚朴煎剂稀释成 250、125、62.5、31.25、15.625 mg/L。
1.2.3 芽管形成试验
实验组以2×106个/mL的菌液1 mL与上述各浓度药液1 mL混合,空白对照组以1 mL菌液与1 mL芽管液体培养基混合,每组3支复管,37 ℃培养30 h离心去上清,用100 μL 0.9%(质量分数)氯化钠注射液(以下简称生理盐水)重悬,每管取10 μL 涂片革兰染色,显微镜下计数100个菌中正常芽管数和受抑制芽管数(正常芽管长度一般超过菌体直径 2 倍及以上,受抑制芽管长度小于或等于菌体直径),计算均值和芽管生成率(芽管生成率=带芽管的白色念珠菌数目/100)[13]。实验重复3次。
1.2.4 厚朴煎剂对白色念珠菌早期黏附基因1(agglutinin-likesequencefamily,ALS1)、ALS2、ALS3的影响
1.2.4.1 样品的制备
白色念珠菌转种于YPG液体培养基中37 ℃摇床培养过夜,离心收集菌体,用芽管液体培养基调整菌浓度为2×106个/mL,以每瓶80 mL分装于克氏瓶中,37 ℃恒温培养箱静置90 min,吸弃上清,无菌PBS洗3次,实验组分别加入31.25、15.625、7.812 5 mg/L厚朴煎剂,空白对照组加入等量的芽管液体培养基,37 ℃ 静置培养1 h,吸弃培养基,用生物膜刮刀刮下黏附在瓶壁上的菌体,收集后离心去上清,用DEPC水洗1次,离心弃上清备用。
1.2.4.2 提取RNA
取沉淀用Novelase消化液悬重,室温消化10 min后,每管沉淀中加入1 mL Trizol,按照Trizol试剂说明书提取总RNA,紫外分光光度法测定RNA 的浓度。
1.2.4.3 引物及其合成
根据文献[15]中ALS1、ALS2、ALS3的基因序列,采用Primer Premier 6.0 软件设计检测白色念珠菌ALS1 mRNA、ALS2 mRNA、ALS3 mRNA 和 18 S-RNA 的实时荧光定量PCR(quantitative real-time PCR,qRT-PCR)引物(表1),各引物由上海生工生物工程公司合成。

表1 特异引物序列和PCR产物长度
1.2.4.4 qRT-PCR定量分析
以1 μg总 RNA 为模板,反应参数:95 ℃30 s;95 ℃5 s、60 ℃ 10 s,39个循环。每个基因6个复管,实验重复3次。实验以18S RNA 为内参,qRT-PCR 数据采用2-ΔΔCt方法评估管家基因和ALS1、ALS2、ALS3的表达水平。
1.2.5 荧光显微镜观察厚朴煎剂对白色念珠菌成熟期生物膜的影响
无菌1 cm×1 cm的盖玻片用胎牛血清浸泡12 h备用。盖玻片放入24孔板,每孔加入上述菌液1 mL,37 ℃静置培养72 h,形成白色念珠菌成熟期生物膜,用 PBS 洗3次去除浮游菌,实验组每孔加入0.5 mL上述浓度厚朴煎剂和0.5 mL芽管液体培养基,空白对照组加入1 mL芽管液体培养基,继续培养24、48、72 h,用无菌PBS 洗3次去除浮游菌,每孔加入20 μL FITC-conA室温避光染色1 h,冷PBS洗3次,荧光显微镜下观察。
1.2.6 扫描电镜(scanning electron microscope,SEM)观察厚朴煎剂对白色念珠菌成熟期生物膜的影响
生物膜制备同上,15.625 mg/L厚朴煎剂处理48 h,PBS 洗3次去除浮游菌后,3%(体积分数)戊二醛固定4 h,PBS 洗4次,每次15 min;去除PBS,加入1%(质量分数)四氧化锇于旋转器上固定1.5 h,再用蒸馏水漂洗4次,每次10 min;以梯度乙醇脱水后,样本先放于临界点干燥仪中干燥,再将样本放于真空镀膜机中喷金,然后于扫描电镜下观察。
1.2.7 激光共聚焦显微镜观察厚朴煎剂对白色念珠菌成熟期生物膜内菌活力的影响
按照上述方法制备72 h生物膜,15.625 mg/L厚朴煎剂处理48 h,PBS洗3次去除浮游菌后,每孔加10 μL SYT09/PI室温避光染色30 min,用激光共聚焦显微镜488 nm氩激光进行激发,PI发射波长635 nm,镜下为红光;SYT09发射波长500 nm,镜下为绿光。
1.3 统计学方法
2 结果
2.1 不同浓度厚朴煎剂对白色念珠菌芽管形成的影响
白色念珠菌革兰染色呈阳性,显微镜下空白对照组(0 mg/L)白色念珠菌以交织成网的真菌丝为主,同时伴有少量的圆形或卵圆形的芽生孢子及假菌丝;各浓度厚朴煎剂均可抑制白色念珠菌的芽生孢子、假菌丝及真菌丝的形成,且抑制作用具有浓度依赖性(图1A)。芽管计数结果显示,随厚朴煎剂浓度的升高受抑制芽管数量增加,与空白对照组比较差异有统计学意义(P<0.05)(图1B)。

图1 不同浓度厚朴煎剂对白色念珠菌芽管形成的影响Fig.1 Effect of Magnolia officinalis decoction with different concentrations on germ tube formation of Candida albicansA: effects of different concentrations of Magnolia officinalis decoction on germ tube formation of Candida albicans(Gram staining),scale bar=5 μm; B: inhibitory rate of Magnolia officinalis decoction at different concentrations on germ tube of Candida albicans; *P<0.05 vs control group(0 mg·L-1).
2.2 厚朴煎剂对白色念珠菌早期黏附基因相对表达量的影响
黏附早期,空白对照组ALS3基因的表达最高,ALS2基因其次,ALS1基因表达最低,实验所用3个浓度厚朴煎剂均能使ALS1、ALS2、ALS3 mRNA的表达下调,且具有浓度依赖性,与空白对照组比较差异均有统计学意义(P<0.05),详见表2,图2。
表2 厚朴煎剂对白念珠菌黏附基因相对表达量的影响
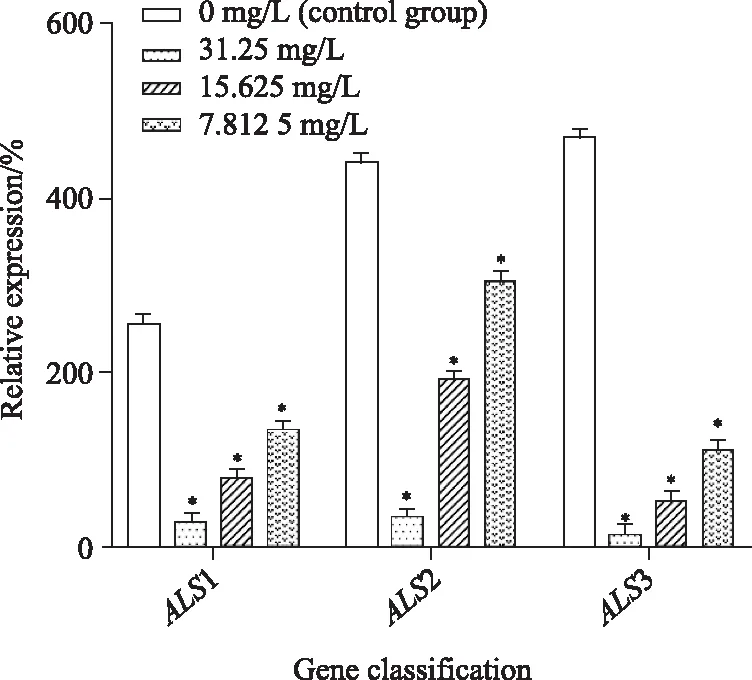
图2 厚朴煎剂对白色念珠菌早期黏附基因相对表达量的影响Fig.2 Effect of Magnolia officinalis decoction on relative expression of early adhesion gene of Candida albicans *P<0.05 vs control group;ALS: agglutinin-like sequence family.
2.3 不同浓度厚朴煎剂对白色念珠菌成熟生物膜的影响
FITC-conA与生物膜中的胞外多糖结合,荧光显微镜下呈绿色荧光。空白对照组随培养时间的延长生物膜不断增厚,而厚朴煎剂作用24、48和72 h后白色念珠菌生物膜结构被破坏,72 h镜下主要见散在的孢子相白色念珠菌,未见片状生物膜(图3~图5)。SEM观察15.625 mg/L厚朴煎剂作用48 h后对生物膜的影响,空白对照组白色念珠菌生物膜由分泌物包裹芽体、交织成网的菌丝形成,药物组生物膜的结构被破坏,镜下白色念珠菌以孢子相为主,孢子失去典型形态,大小不均,表面有分泌物包裹,同时可见少量被抑制的菌丝(图6)。

图3 不同浓度厚朴煎剂作用24 h对白色念珠菌生物膜的影响Fig.3 Effect of Magnolia officinalis decoction on Candida albicans biofilm for 24 hours (scale bar=20 μm)
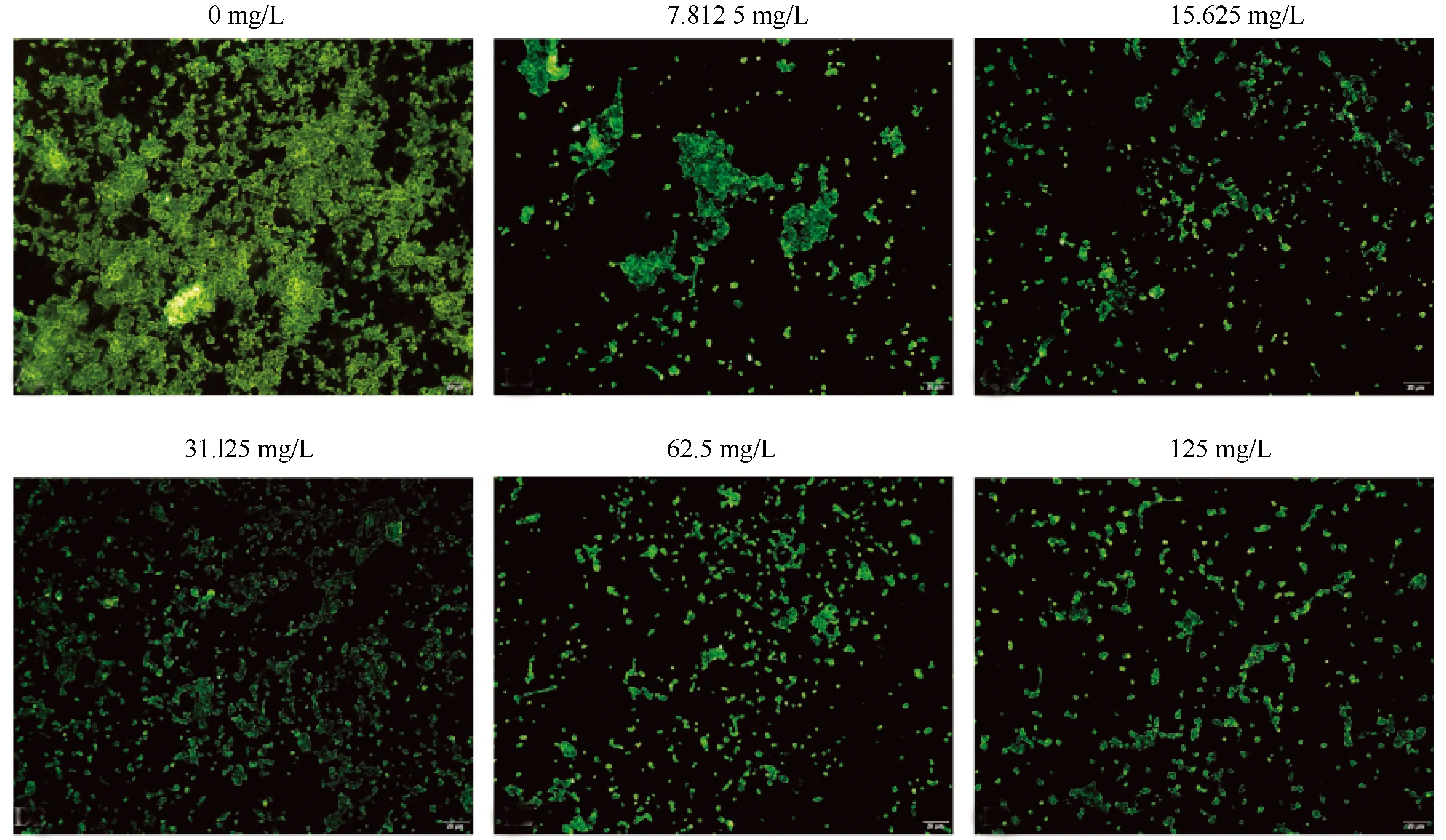
图4 不同浓度厚朴煎剂作用48 h对白色念珠菌生物膜的影响Fig.4 Effect of Magnolia officinalis decoction on Candida albicans biofilm for 48 hours (scale bar=20 μm)

图5 不同浓度厚朴煎剂作用72 h对白色念珠菌生物膜的影响Fig.5 Effect of Magnolia officinalis decoction on Candida albicans biofilm for 72 hours (scale bar=20 μm)

图6 扫描电镜观察厚朴煎剂作用48 h对白色念珠菌生物膜的影响Fig.6 Effect of Magnolia officinalis decoction for 48 hours on Candida albicans biofilm was observed by SEMSEM: scanning electron microscope.
2.4 厚朴煎剂对白色念珠菌成熟期生物膜内菌活力的影响
共聚焦显微镜下,死菌被PI 染色发红色荧光, 活菌被SYT09染色发绿色荧光,橙色为死活菌重叠所致。空白对照组白色念珠菌主要为交织成网的菌丝,以活菌为主,仅见少量死菌;15.625 mg/L厚朴煎剂作用48 h后,白色念珠菌以孢子相为主,死菌数量明显增加,可见少量被抑制的菌丝(图7)。
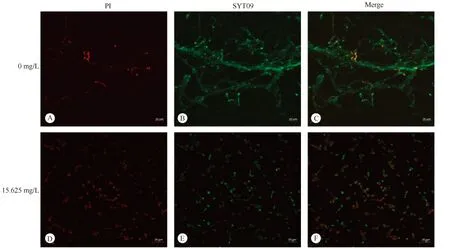
图7 厚朴煎剂作用48 h对白色念珠菌生物膜内菌活力的影响Fig.7 Effect of Magnolia officinalis decoction for 48 h on bacterial activity in Candida albicans biofilm (scale bar=20 μm)A-C: Candida albicans is mainly mycelium; D-F: Candida albicans is mainly spore phase
3 讨论
中药汤剂是我国应用最多、最早的一种剂型,其制法简单,用水为溶剂,起效较快,目前在中医临床仍然广泛使用,而中药浓煎剂则是在中药汤剂的基础上发展起来的,它是将单方或复方的中草药经水煎煮,浓缩成一定容量的液体制剂[16]。本研究制备中药厚朴煎剂,探讨其对白色念珠菌的芽体、菌丝及生物膜的作用。念珠菌病是最常见的侵袭性真菌感染,目前在全球医院中侵袭性真菌感染排第三至第四位,而白色念珠菌仍然是念珠菌病的主要病因[17]。白色念珠菌是一种二相性真菌,从形态上分为酵母相和菌丝相,在一些因素的诱导下,酵母相可以向菌丝相转换[18],菌态转换是白色念珠菌由定殖菌向致病菌转变的一种标志,与白色念珠菌致病性和生物膜形成密切相关[19-20]。本研究用芽管形成试验观察厚朴煎剂对白色念珠菌菌态转换的影响,结果显示通过抑制白色念珠菌芽管、假菌丝和真菌丝的形成以及酵母细胞的增殖,从而抑制白色念珠菌发生菌态转换,芽管计数结果提示厚朴煎剂对白色念珠菌芽管的抑制作用具有浓度依赖性。白色念珠菌生物膜的发育过程可分为四个主要阶段:黏附、增殖、成熟和扩散[17],黏附阶段是其形成生物膜与致病的基础,因此抑制黏附是抗白色念珠菌生物膜感染的关键措施,而芽管的形成可以提高白色念珠菌的组织侵袭性和黏附力,厚朴煎剂抑制芽管形成说明其可以抑制白色念珠菌的黏附[21]。白色念珠菌黏附性主要由其细胞表面蛋白黏附素完成,白色念珠菌ALS基因家族编码的黏附素参与了该菌对宿主的黏附和生物膜的形成。以往的研究[22]表明ALS1、ALS2、ALS3在白色念珠菌体外生物膜形成过程中呈优势表达。因此本实验进一步检测了厚朴煎剂对ALS1、ALS2、ALS3基因的影响,qRT-PCR结果提示厚朴煎剂作用后可下调3个基因的表达,说明厚朴煎剂可能是通过下调白色念珠菌早期黏附基因的表达从而影响其早期黏附;同时ALS1还是菌丝形成关键基因之一,厚朴煎剂作用后ALS1的下调导致白色念珠菌菌丝形成受到抑制。
真菌生物膜是指真菌黏附于惰性或活性实体的接触表面,分泌多糖基质、纤维蛋白、脂质蛋白等物质,将其自身包绕其中而形成的大量真菌聚集膜样物,主要组成为菌丝[1]。本研究制备的白色念珠菌成熟期生物膜,在荧光显微镜下空白对照组生物膜由大量菌丝交织呈片状,而厚朴煎剂作用后随着药物浓度的增加及作用时间延长,未见大片状生物膜,镜下主要为孢子相白色念珠菌;扫描电镜观察生物膜发现空白对照组生物膜以分泌物包裹菌丝为主,15.625 mg/L 的厚朴煎剂作用48 h后,生物膜结构被破坏,镜下多见孢子相白色念珠菌,在菌体表面也包裹有分泌物,菌体大小不一。进一步在共聚焦显微镜下观察厚朴煎剂对成熟期生物膜中菌活力的影响,发现空白对照组以菌丝和活菌为主,而15.625 mg/L的厚朴煎剂组以孢子相为主,且死菌数量明显增加。共聚焦显微镜和芽管形成试验说明厚朴煎剂可能是通过破坏成熟期生物膜的结构,然后进入生物膜内抑制芽管的形成从而发挥杀菌作用的。
综上所述,厚朴煎剂早期可通过下调ALS1、ALS2、ALS3基因抑制白色念珠菌发生菌态转换和生物膜的形成,同时可以破坏成熟期生物膜的结构从而促进药物进入生物膜内抑制芽管形成并发挥杀菌作用。但是实验中没有进一步检测影响菌丝形成的基因、影响生物膜形成的信号通路等,因此厚朴煎剂对白色念珠菌菌丝形成及其生物膜的作用机制还需进一步验证。

