迷人的化学火焰彩虹
张嘉麟 张笑瑜 郑慧娴


九年级化学第二单元《氧气》,让我们观察到了硫在氧气中燃烧的现象。硫在氧气中燃烧会产生非常好看的蓝紫色火焰,看到这一现象,我们产生了一个疑问:平常见到的火焰颜色一般是蓝色或者黄色的,那么有没有什么物质燃烧时会产生其他颜色的火焰?
带着疑问,我们查阅了资料,询问了老师,了解到:不同的金属元素在燃烧时的确会产生不一样的火焰颜色,如钠燃烧是黄色火焰,钙燃烧是砖红色火焰,铜燃烧是绿色火焰。因此,我们想设计一个实验,探究不同金属元素燃烧时会产生什么颜色的火焰。
资料显示,在实验室里,化学家将不同种类的金属或它们的化合物进行灼烧,产生了五光十色的火焰。这是因为每种金属元素都有自己特定的光谱。这个原理被称为“焰色反应”。五颜六色的烟花正是利用了这一原理,将夜空装点得璀璨美丽。我们还找到了高中课本,发现高中教材里有一个蘸取少量金属盐溶液后在火焰上燃烧的实验。经过实践,我们发现这个实验的效果不够明显,因此我们萌生了改变这些金属燃烧的介质,使实验效果更显著、能够真正看到不同颜色火焰的想法。
◎实验仪器及方法
1.实验药品:酒精溶液,硫酸铜,氯化钙,氯化钾,氯化钠,氯化钡和氯化铁。
2.实验用品及仪器:棉花,餐巾纸,滤纸,蒸发皿(小),蒸馏水,酒精灯,玻璃棒,烧杯,石棉网,镊子。
3.实验方法:
实验一:在酒精溶液中燃烧。
实验步骤:分别取一勺硫酸铜、氯化钙、氯化钾、氯化钠、氯化钡和氯化铁放于小烧杯中,再分别加入约10 ml 95%的酒精溶液和3 ml水,用玻璃棒搅拌液体使其充分溶解。
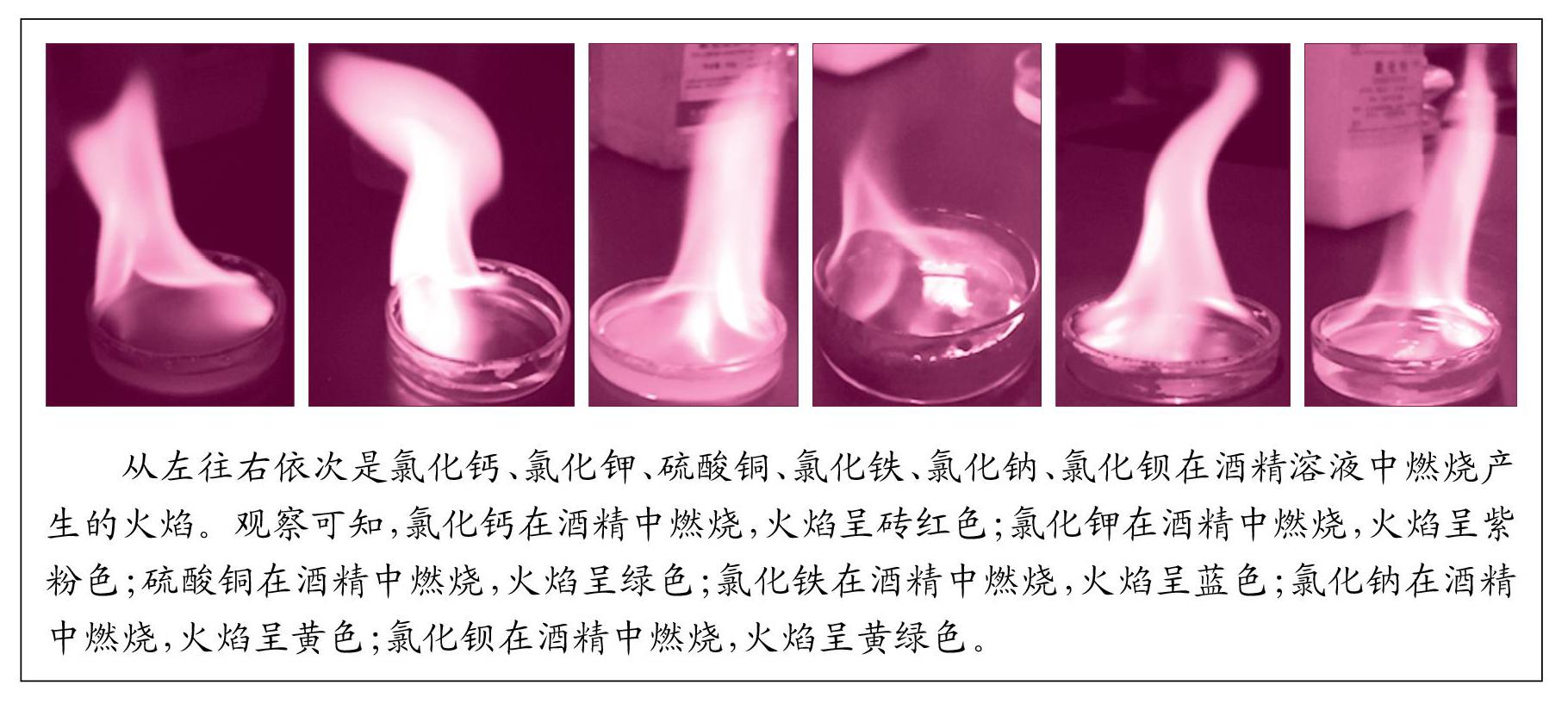
从左往右依次是氯化钙、氯化钾、硫酸铜、氯化铁、氯化钠、氯化钡在酒精溶液中燃烧产生的火焰。观察可知,氯化钙在酒精中燃烧,火焰呈砖红色;氯化钾在酒精中燃烧,火焰呈紫粉色;硫酸铜在酒精中燃烧,火焰呈绿色;氯化铁在酒精中燃烧,火焰呈蓝色;氯化钠在酒精中燃烧,火焰呈黄色;氯化钡在酒精中燃烧,火焰呈黄绿色。
实验二:在滤纸上燃烧。
实验步骤:分别取一勺硫酸铜、氯化钙、氯化钾、氯化钠、氯化钡和氯化铁均匀铺在滤纸上,再将滤纸置于石棉网上,点燃滤纸,观察火焰颜色。
从左至右分别为氯化钠在滤纸上燃烧、硫酸铜在滤纸上燃烧、空白滤纸燃烧对照。观察可知,将氯化钠放在滤纸上燃烧,得到较弱的黄色火焰,与空白滤纸燃烧现象区别不大;放在滤纸上燃烧的硫酸铜,虽然也可以看到绿色火焰,但不明显。氯化钙、氯化鉀、氯化钡与氯化铁在滤纸上燃烧的效果不明显,故不展示。
实验三:在纸巾上燃烧。
实验步骤:(1)将撕碎的纸巾置于石棉网上,取一勺硫酸铜粉末均匀撒在纸上,点燃,观察火焰颜色;(2)将硫酸铜换成氯化钙、氯化钾、氯化钡和氯化铁,再分别重复步骤(1)。
从左至右分别为氯化钠在纸巾上燃烧、硫酸铜在纸巾上燃烧、空白纸巾燃烧对照。观察可知,将氯化钠放在纸巾上燃烧得到了黄色火焰,而放置了硫酸铜的纸巾火焰边缘仅有小部分地方出现了绿色。氯化钙、氯化钾、氯化钡、氯化铁在纸巾上燃烧效果不明显,故不展示。
◎实验结论
经过三个实验对比,我们发现,直接将可溶性的金属化合物加在酒精溶液中燃烧效果最佳,且可以几个容器同时展示。
(指导老师:利海媚 张 智)

