电针内麻点对乳腺癌术后镇痛效果及疼痛介质的影响
罗守江,杨鹤,杨波,李立伟
河南省鹤壁市人民医院南院区 河南鹤壁 458030
乳腺癌现已成为威胁女性健康常见的恶性肿瘤之一,手术切除是治疗该疾病的重要手段,相关研究显示[1],行乳腺癌手术患者在术后约2/3会发展为慢性疼痛,而术后急性疼痛是向慢性疼痛转变的主要危险因素。故采取合理的镇痛方案是关键。临床常规镇痛主要以阿片类药物静脉自控镇痛为主,但乳腺癌术后疼痛由多方面因素所致,导致其镇痛效果不佳[2]。而术前予以电针内麻点在手术创伤未产生前通过针灸刺在内麻点后施加不同程度的刺激电流,以产生镇痛效应。但其确切的镇痛机制尚不清楚,故本研究观察电针内麻点对乳腺癌术后镇痛效果及疼痛介质的影响,旨在探究电针内麻点的镇痛机制,现将结果报道如下。
资料与方法
1 诊断标准
1.1 西医诊断标准 符合《2016年NCCN乳腺癌临床实践指南(第1版)》中关于乳腺癌诊断标准且经病理检查确诊[3]。
1.2 中医诊断标准 符合《中医症候的临床研究指导原则》[4]中的相关标准,拟定为气虚血瘀的证候。
2 纳入和排除标准
2.1 纳入标准 ①符合中西医关于乳腺癌的诊断;②卡氏评分60分以上[5];③麻醉分级Ⅰ~Ⅱ级[6]。
2.2 排除标准 ①术前接受放化疗者;②乳腺癌复发或转移者;③合并其他癌症;④阿片类药物成瘾者;⑤经络部位皮肤感染。
3 一般资料
经医院伦理委员会批准(批准文号:20170819),患者及家属同意后,将我科2017年8月—2020年8月86例行手术治疗的乳腺癌患者分组,按照组间基线资料匹配原则分为对照组(n=43)和观察组(n=43)。其中对照组年龄40~59岁,平均年龄(45.26±5.69)岁;病程1~4年,平均病程(2.26±0.28)年;体重指 数 21~ 23kg/m2,平 均 体 重 指 数(22.05±0.52)kg/m2;麻醉分级:Ⅰ级20例,Ⅱ级23例;肿瘤直径2~ 5cm,平均直径(3.23±0.15)cm;TNM 分期:Ⅰ期21例,Ⅱ期22例。观察组年龄40~56岁,平均年龄(46.01±5.56)岁;病程2~4年,平均病程(2.31±0.26)年;体重指数 21~23kg/m2,平均体重指数(22.09±0.51)kg/m2;麻醉分级:Ⅰ级 19 例,Ⅱ级24例;肿瘤直径2~5cm,平均直径(3.26±0.16)cm;TNM分期:Ⅰ期20例,Ⅱ期23例。上述资料2组比较无统计学差异,具有可比性。
4 治疗方法
2组均予以静脉全身麻醉,予以0.03~0.05 mg/kg咪达唑仑(江苏恩华药业;H19990027;10ml:50mg)、0.3~ 0.5μg/kg舒芬太尼(宜昌人福药业;H20054172;2ml:100μg)、2 ~ 3 mg/kg 丙泊酚(西安力 邦 制 药;H19990282;20ml:200mg)、0.4mg/kg 顺 式阿曲库铵(江苏恒瑞医药;H20060869;10mg/支)静脉注射进行麻醉诱导。麻醉维持以丙泊酚及瑞芬太尼进行靶控输注,然后跟据脑电双频指数调控靶控浓度。2组均观察术后48h。
4.1 观察组 术前予以电针内麻点:在麻醉诱导前取双侧内麻点(小腿内侧,胫骨后缘0.5寸内踝上7寸),对该穴位皮肤进行消毒处理后,采用一次性毫针经该部位垂直进针,得气后留针。然后接治疗仪(G6805Ⅱ型),设置参数:频率:4~100次/min,输出电压正脉冲12.5V以上,负脉冲20V以上,负载:250Ω,刺激30min。
4.2 对照组 予以常规静脉自控镇痛:在手术结束前15min,经静脉连接镇痛泵[配制:50μg舒芬太尼+10mg地佐辛(扬子江药业;H20080329;1ml:5mg)+0.9%NaCl稀 释 至 100ml],锁 时 15min,PCA 每 次0.5mL,连续使用 48 h。
5 观察指标
观察2组各时间点疼痛程度及疼痛介质水平。
5.1 疼痛程度 电针刺激前(T0)、术后2h(T1)、术后 12 h(T2)、术后 24 h(T3)和术后 48 h(T4)采用视觉模拟评分[7](Visual Analogue Scale,VAS,总分10分,分高疼痛严重)评价疼痛程度。
5.2 疼痛介质水平 与T0、T4时间点抽取静脉血4ml采用全自动生化仪(型号:迈瑞2800)采用依据酶联免疫吸附测定(ELISA)法试剂盒(生产批号:A2016011)测 量 5-羟 色 胺(5-hydroxytryptamine,5-HT)、去 甲 肾 上 腺 素(Noradrenaline,NE)、亮 脑啡 肽(leucine-enkephalin,L-ENK)及 β-内 啡 肽(β-endorphin,β-EP)水平。操作严格按照说明书进行。
6 统计学方法
数据录入SPSS22.0软件中分析,计数资料用%表示,采用χ2检验,计量资料用()表示,采用t检验,P<0.05表示差异具有统计学意义。
结 果
1 2组各时间点疼痛程度比较
2组T0时间点VAS评分比较差异无统计学意义(P>0.05);T1~T4时间点2组均先升高后降低,但观察组T1~T4时间点VAS评分均较对照组低(P<0.001),见表 1。
表1 2组各时间点疼痛程度比较()

表1 2组各时间点疼痛程度比较()
组别 例数 T0 T1 T2 T3 T4观察组 43 2.23±0.36 3.25±1.02 2.54±0.45 2.12±0.37 1.48±0.28对照组 43 2.26±0.34 4.69±1.09 3.59±0.54 3.41±0.51 2.28±0.36 t 0.397 6.325 9.795 13.425 11.503 P 0.692 <0.001 <0.001 <0.001 <0.001
2 疼痛介质水平比较
2组T0时间点β-EP、5-HT、NE及L-ENK比较差异无统计学意义(P>0.05),T4时间点2组5-HT、NE水平均降低,但观察组5-HT、NE水平较对照组低(P<0.001),L-ENK、β-EP水平均升高,但观察组L-ENK、β-EP 较对照组高(P<0.001),见表 2。
表2 2组疼痛介质水平比较()
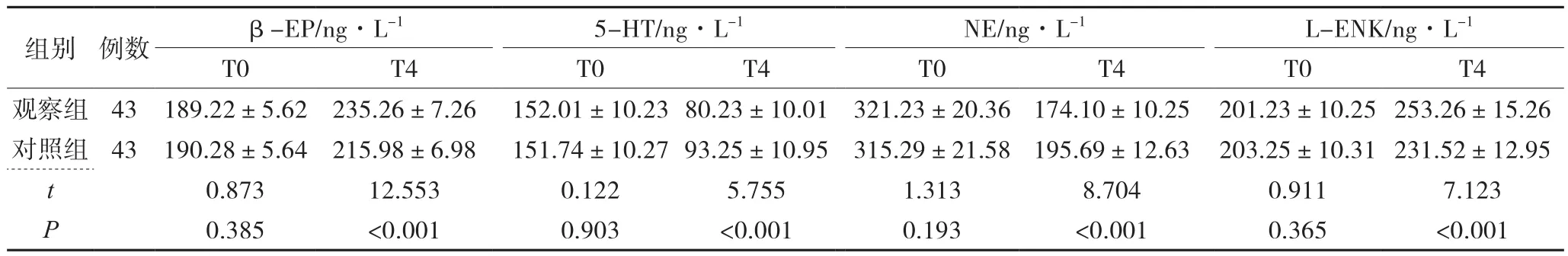
表2 2组疼痛介质水平比较()
组别 例数 β-EP/ng·L-1 5-HT/ng·L-1 NE/ng·L-1 L-ENK/ng·L-1 T0 T4 T0 T4 T0 T4 T0 T4观察组 43 189.22±5.62 235.26±7.26 152.01±10.2380.23±10.01 321.23±20.36 174.10±10.25 201.23±10.25253.26±15.26对照组 43 190.28±5.64 215.98±6.98 151.74±10.2793.25±10.95 315.29±21.58 195.69±12.63 203.25±10.31231.52±12.95 t 0.873 12.553 0.122 5.755 1.313 8.704 0.911 7.123 P 0.385 <0.001 0.903 <0.001 0.193 <0.001 0.365 <0.001
讨 论
疼痛是第5大生命体征,术后疼痛为机体受到手术创伤后所致的组织损伤,进而引起一系列生理病理反应,乳腺癌手术创伤大且术后常伴有剧烈疼痛,若镇痛不完善,易影响患者恢复[8],故合理的镇痛可改善机体多系统功能。术后静脉自控镇痛是以往常规的镇痛方案,但乳腺癌患者在术后多存在一定程度疼痛不适,加之手术创伤等因素,会进一步加重机体疼痛,导致该镇痛方案往往达不到患者镇痛需求[9,10]。为此探讨合理的镇痛方案以缓解乳腺癌术后患者疼痛程度成为当前研究方向。
内麻点是经外奇穴,位于小腿内侧,为足三阴交汇之处(任督二脉)[11],十二经脉必需经过督、任二脉的综合调节以发挥主治作用,而电针是将传统针刺联合电刺激的方法,可发挥针、电双重刺激作用,电针内麻点可通过抑制炎症病灶神经末梢合成,抑制炎症介质释放,同时可通过刺激机体β-EP的合成与释放,导致其前体物质的消失,产生具有吗啡样活性,阻断疼痛信号传导通路,以提高镇痛效果。
和麻醉领域相关的是手术创伤引起的疼痛,该疼痛属于急性疼痛的一种,为术后引起的多系统、多环节参与的病理生理反应[12-14]。尽管术后急性疼痛和乳腺癌的慢性疼痛具有一定的差异,但两种类型的疼痛都涉及到组织损伤或炎症反应所致的外周、中枢敏感化反应,进而放大机体对刺激所产生的应激反应,导致术后疼痛产生,不利于患者快速恢复。VAS评分为评价疼痛程度的简易量表,其评分高低和疼痛严重程度呈正比。本研究中,观察组T1~T4时间点VAS评分均较对照组低(P<0.05),提示电针内麻点可提高乳腺癌术后镇痛效果。因电针内麻点可激活脊髓的α2受体,通过抑制γ-氨基丁酸参与的突触后,阻断神经冲动的传导,抑制交感神经活性,避免疼痛信号向脊髓后角传递,进而产生镇痛作用。同时电针刺激过程可产生大量内源性阿片肽物质参与,可结合中枢和外周阿片类受体,抑制疼痛信号的表达,发挥镇痛效果。
疼痛产生与致痛物质参与痛觉信息的传递有关[15-17]。外周组织损伤后,该损伤部位将释放大量致痛物质,如5-HT、NE等,这些物质会直接作用于感受器神经末梢,激活痛觉感受器,造成中枢敏感化,同时可通过伤害性冲动在传入纤维分叉口传向其他末梢,兴奋感受器,还能继发性激活相邻的伤害性刺激[18,19]。β-EP则为抗伤害性感受递质,其水平与疼痛程度呈负相关,本研究中,观察组T4时间点5-HT、NE水平较对照组低,L-ENK、β-EP水平较对照组高(P<0.05),提示电针内麻点可改善乳腺癌术后患者疼痛介质水平。因电针刺激可调节机体机械性痛敏阈值和热痛阈值,促使大脑L-ENK、β-EP、吗啡样物质释放,增加脊髓中脑啡肽水平,从而引起外周阿片前体信使核糖核酸表达,以抑制5-HT、NE水平释放。同时电针内麻点可通过增加阿片肽的释放,导致前体物质消失,增加阿片肽基因的表达以弥补这种损失,发挥长期镇痛效应。且一项动物实验指出[20],电针刺激可通过抑制脊髓神经元活化和P物质的释放,以改善疼痛早起神经的病理性可塑性,进而调节致痛介质水平。
综上所述,电针内麻点可通过改善乳腺癌术后患者疼痛介质水平,提高术后镇痛效果。本研究不足之处在于样本量相对较少且观察时间短,其可能导致研究结果存在偏倚,拟扩大样本量延长观察时间以进一步研究。

