卡瑞利珠单抗治疗复发或转移性食管鳞癌的临床疗效及安全性
张桂枫,刘振华,钟江鸣,李德育,林 莉
(福建医科大学省立临床医学院、福建省立医院肿瘤内科,福建 福州 350004)
食管癌是世界上最常见的恶性肿瘤之一,发病率居第7位,死亡率居第6位[1]。中国食管癌的发病和死亡人数占全世界的一半。中国食管癌多以食管鳞癌为主,占90%以上[1-2]。早期食管癌症状不明显,发现率极低,多数患者初次就诊时已经是局部进展期甚至发生远处转移,只有20%~30%的患者才有机会接受手术治疗,术后患者复发及远处转移风险仍然很高。复发或转移性食管鳞癌患者的一线治疗,主要是以紫杉烷类、顺铂和氟尿嘧啶为基础的化疗,但由于不良反应及耐药等因素,生存获益有限。对于进展或不能耐受一线标准化疗的复发或转移性食管鳞癌患者,尚无标准的二线治疗方案[3]。一项Ⅲ期的临床研究Keynote-181[4]证实,在中国队列中,派姆单抗与化疗组对比,总有效率和总生存时间(overall survival,OS)均有明显改善,特别是程序性死亡配体1(programmed cell death-Ligand 1,PD-L1)联合阳性评分≥10分者OS获益尤为显著,且安全性良好。2019年美国食品和药品管理局批准并公布了帕博利珠单抗用于治疗PD-L1联合阳性评分≥10分食管鳞癌的二线及以上治疗。一项Ⅲ期的临床研究Attraction-03[5]证实,纳武单抗组与化疗组对比,OS明显改善,且重度不良反应明显减少。2020年美国食品和药品管理局批准了纳武单抗用于食管鳞癌的二线及以上治疗,中国的一项Ⅲ期临床研究ESCORT 研究[6]证实,卡瑞利珠单抗组与化疗组对比,总有效率和OS均有明显改善,2020年国家药物监督管理局批准了卡瑞利珠单抗用于食管鳞癌的二线及以上治疗。本研究对一线及以上化疗失败的复发或转移性食管鳞癌患者应用卡瑞利珠单抗治疗并随访,讨论其治疗复发或转移性食管鳞癌的临床疗效和安全性。
1 资料与方法
1.1 一般资料回顾性分析2019年11月至2020年11月于福建省立医院应用卡瑞利珠单抗治疗的20例一线及以上化疗失败的复发或转移性食管鳞癌患者。纳入标准:1)经病理组织活检证实为食管鳞癌;2)至少有1个可客观测量的病灶;3)既往接受一线及以上化疗方案治疗失败;4)ECOG评分0~1分;5)年龄18~75岁。排除标准:1)5 a内伴发其他恶性肿瘤;2)心、肝、肾等多器官功能不全;3)自身免疫性疾病史;4)免疫缺陷;5)活动性肝炎;6)既往使用过程序性死亡受体1(programmed cell death-1,PD-1)或及其配体(programmed death-ligand 1,PD-L1)抑制剂;7)有脊髓压迫或癌性脑膜炎病史,或经CT或MRI证实脑部转移。年龄45~74岁,中位年龄57岁;男18例,女2例;既往放疗史:有7例,无13例;既往化疗史:一线14例,二线6例;既往手术史:有8例,无12例;ECOG评分:0分7例,1分13例。
1.2 治疗方法所有患者用药前均评估血常规、肝功能、肾功能及凝血功能。应用卡瑞利珠单抗200 mg静脉滴注,2周1次,直至疾病进展(progressive disease,PD)或出现不可耐受的不良反应。
1.3 疗效评价及随访随访至2021年2月5日,治疗每2个周期后进行影像学检查,评价近期疗效,并进行不良反应评价。根据实体瘤疗效评价标准RECIST 1.1[7]评价近期疗效,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stabled disease,SD)和PD。以CR+PR+SD计算疾病控制率(disease control rate ,DCR)。疾病无进展生存期(progression-free-survival, PFS)定义为首次使用卡瑞利珠单抗治疗到PD、死亡或末次随访的时间间隔,以先发生者为准。OS定义为首次使用卡瑞利珠单抗治疗到死亡或末次随访的时间间隔,以先发生者为准。根据CTCAE 5.0标准评价不良反应,分为0~Ⅳ度。
1.4 统计学处理采用SPSS 21.0进行统计分析,计数资料用百分数表示,比较用χ2检验及Fisher确切概率法,用log rank检验进行生存差异性检验,检验水准α=0.05。
2 结果
2.1 近期疗效20例患者中,CR 0例,PR 2例,SD 10例,PD 8例,DCR为60.00%(12/20)。其中出现反应性皮肤毛细血管增生症(reactive cutaneous capillary endothelial proliferation ,RCCEP)组CR 0例、PR 2例、SD 9例、PD 3例、DCR 78.57%,未出现RCCEP组CR 0例、PR 0例、SD 1例、PD 5例、DCR 16.67%,出现RCCEP组DCR高于未出现RCCEP组(P=0.018)。
2.2 远期疗效所有患者的中位PFS为2.00个月,中位OS为6.75个月。出现RCCEP组患者PFS优于未出现RCCEP组(χ2=6.487,P=0.011);2组患者OS比较差异无统计学意义(χ2=0.569,P=0.451)。见图1、2。
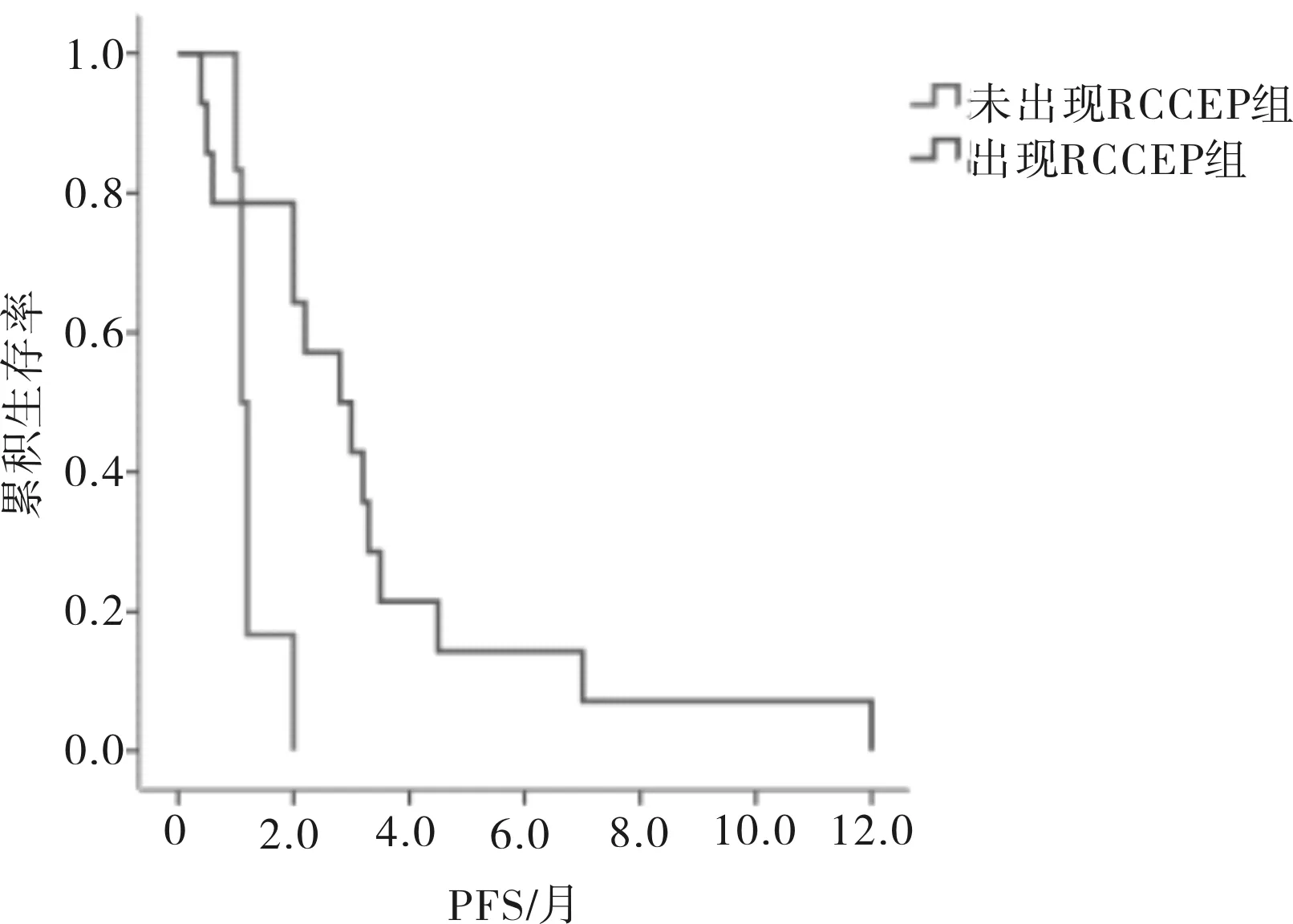
图1 2组患者PFS生存曲线比较
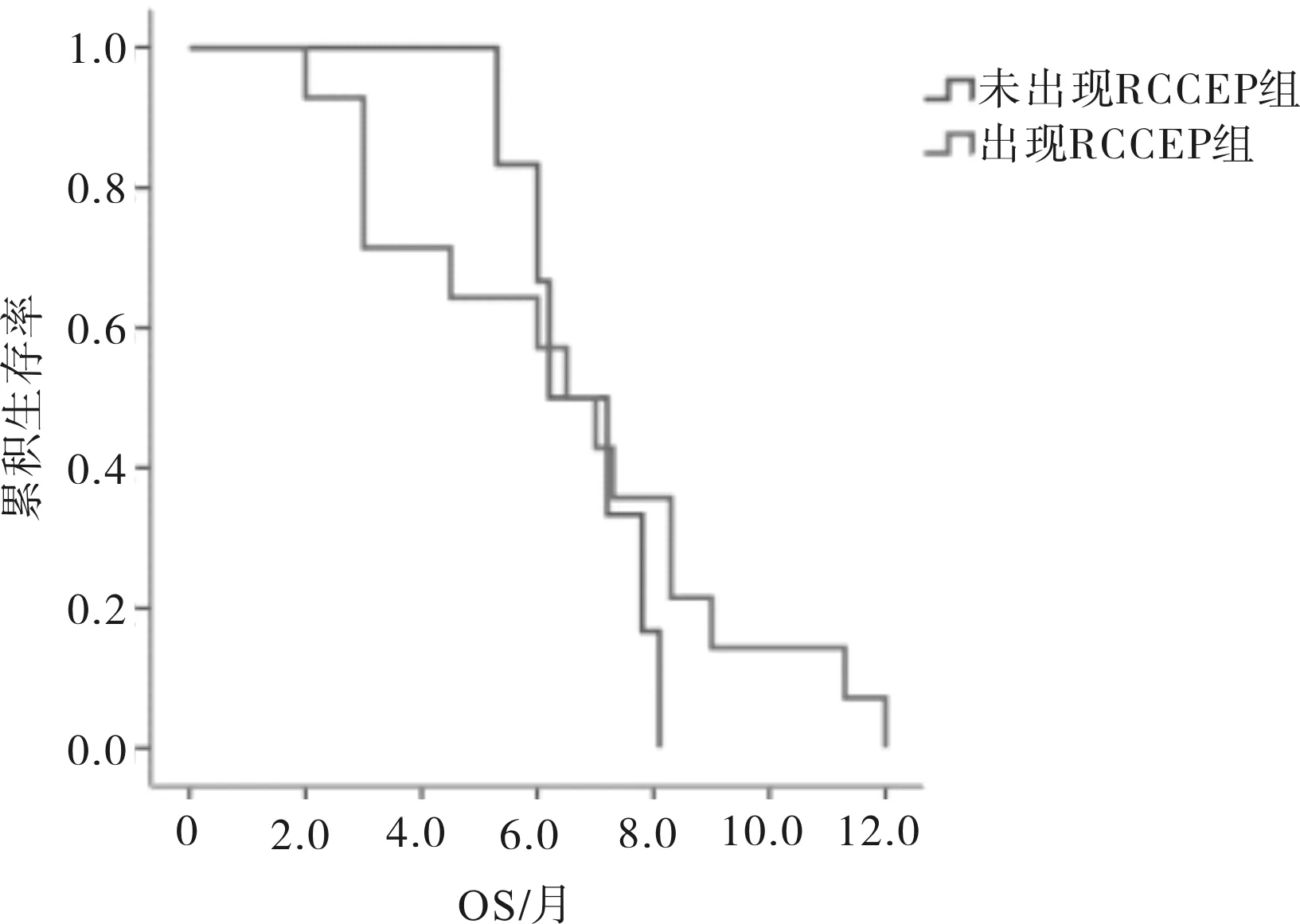
图2 2组患者OS生存曲线比较
2.3 不良反应常见不良反应为RCCEP[14例(70.00%)]、免疫性肝炎[5例(25.00%)]、腹泻[4例(20.00%)]、甲减[4例(20.00%)]、肺炎[3例(15.00%)]、白细胞减少[2例(10.00%)]、甲亢[1例(5.00%)]、肾炎[1例(5.00%)],且大部分为Ⅰ、Ⅱ度,予以处理恢复后可续用药。
3 讨论
在复发或转移性食管鳞癌患者中,免疫治疗通过激活自身免疫细胞产生抗肿瘤作用,能延长PFS和OS,患者耐受性良好。PD-1、PD-L1是免疫治疗肿瘤的重要新靶点,无论是单药应用还是联合用药,PD-1、PD-L1抑制剂在食管癌中都显示出良好的治疗反应,为食管癌患者带来了更多的希望[8]。PD-1免疫治疗是通过PD-1或PD-L1抑制剂阻止PD-1和PD-L1的识别过程,部分恢复T细胞功能,从而使T细胞可以杀死肿瘤细胞,多项二线及以上的研究证实,相较于化疗,其可以延长食管癌患者OS。一项一线治疗晚期食管癌Ⅲ期临床研究[9]证实,相较于化疗,免疫联合化疗在总有效率、PFS、OS方面有优势。免疫治疗有望在食管癌的一线治疗中获得更多疗效。研究[10]证实,食管癌是突变频率较高的瘤种,这可能是免疫治疗有效人群更多的原因之一。鉴于食管鳞癌的高度异质性和地域差异,在实施一线治疗时,应慎重解读。对于免疫治疗的预测因子,PD-L1的高表达及微卫星高度不稳定或错配蛋白修复缺失在别的实体瘤中展示了良好的治疗反应,比如肺癌、胃肠道肿瘤等[11-13]。在食管癌中,PD-L1的高表达及微卫星高度不稳定或错配蛋白修复缺失是否能作为预后因子,可能是未来研究的方向。
本研究中,大部分不良反应为Ⅰ、Ⅱ度,可耐受,但70.00%的患者出现了毛细血管增生的不良反应。一项Ⅱ期的临床研究[14]中发现66.7%的患者出现RCCEP,这与本研究的70.00%相近,该研究发现,卡瑞利珠单抗可能促进血管增殖。在另一项I期的临床研究[15]中发现,出现RCCEP的患者比未出现RCCEP的肿瘤应答率更高,可能提示RCCEP与肿瘤反应有潜在的关系。Ⅱ期临床研究[14]中还发现,出现RCCEP患者和未出现RCCEP患者的总有效率分别为19.3%和5.6%。此外,还观察到RCCEP的发生与PFS和OS延长显著相关。本研究中出现RCCEP组DCR明显高于未出现RCCEP组,出现RCCEP组患者PFS优于未出现RCCEP组,但2组OS比较差异无统计学意义,可能与本研究样本量较少、随访时间较短,出现RCCEP组的OS尚未达到有关,RCCEP的出现与否有可能与卡瑞利珠单抗的疗效成正相关。
综上所述,卡瑞利珠单抗治疗复发或转移性食管鳞癌安全有效,能够有效控制疾病进展,改善患者生存,且安全性较高,尤其是出现RCCEP患者。但由于本研究样本量小,随访时间短,OS尚未成熟,可能存在一定的偏移,仍需进一步的大样本随机对照研究进行验证。
——中国居民收入分配中的逆向调节机制

