双(2-羟基-1-萘甲醛)缩N,N'-二(3-氨基丙基)哌嗪Schiff 碱的合成、表征及抑菌活性
佟 萍,刘泽含,刘春风,王 瑞,李凡凡,杨 杨,杨迎晨,许瑞波,3
(1. 江苏海洋大学药学院,江苏,连云港 222005; 2. 江苏绿源工程设计研究有限公司, 江苏,连云港 222007;3.江苏省海洋资源开发研究院.,江苏,连云港 222005)
Schiff 碱是一类含有亚胺基(-HC=N-)的重要含氮化合物,结构独特而易于合成。Schiff 碱特征官能团结构使其与天然生物体系的结构类似[1-3],且其氮原子上存在孤对电子, 赋予了Schiff 碱优良的配位性能和生物活性[4]。由于Schiff 碱及其金属配合物具有良好的抑菌、杀菌、抗肿瘤、抗病毒的生物活性及光学、催化活性,使得它们在化学、医药、材料等领域有着广泛的潜在应用前景[5-8]。因此,设计合成结构新颖、性能各异的Schiff 化合物具有重要意义。
含哌嗪环化合物通常显示出广泛生物活性,如抗肿瘤、抗高血压、镇痛、抗炎及抗过敏等[9-10],它们是医药、农药等药物的重要结构片段。以含有哌嗪环的伯胺为原料,通过与结构各异的含活泼羰基化合物的反应,能制备出含哌嗪环及其他官能团的席夫碱,从而改善化合物的一些理化性质、药理活性[11]。目前,国内外对哌嗪席夫碱的研究较少,国内主要是我们课题组进行含哌嗪环席夫碱及其衍生物的研究工作,并取得了一定的成果[10-17]。近期,课题组首次研究了双(2-羟基-1-萘甲醛)缩N,N'-二(3-氨基丙基)哌嗪Schiff 碱(简称为BNO)的最佳合成工艺条件。本研究报道BNO 合成(见Scheme 1)、结构表征及其对金黄色葡萄球菌和大肠杆菌的抑制作用,为设计、开发具有优良生物活性的含哌嗪环化合物提供一定参考。
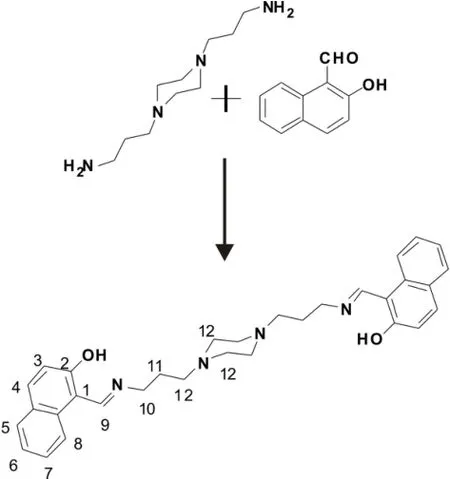
Scheme 1 Synthesis route for the title compound方案1 标题化合物的合成路线
1 实验部分
1.1 仪器与试剂
试剂:N,N'-二(3-氨基丙基)哌嗪(BAPP))是由东京化成工业株式会生产,购于北京百灵威化学技术有限公司;2-羟基-1-萘甲醛、无水乙醇、正丁醇等均为市售分析纯,用前皆未做任何处理。
仪器:SGW X-4 型显微熔点测定仪,温度未校正;Nicolet-is10 型傅里叶红外光谱仪(KBr 压片),Thermo Fisher Scientific 公司;UV-Vis 2550 型紫外分光光度计,日本岛津公司;Brucker DRX300 核磁共振仪(CDCl3为溶剂,TMS 为内标)。
1.2 双(2-羟基-1-萘甲醛)缩N,N'-二(3-氨基丙基)哌嗪Schiff 碱(i.e.BNO)的合成
准确称取1.033 g(约6 mmoL)2-羟基-1-萘甲醛于100 mL 三口烧瓶内,加入10 mL 溶剂搅拌溶解;再准确称取0.601 g(3 mmoL)BAPP,用5 mL溶剂溶解在烧杯里。将三口烧瓶置于恒温水浴锅内,持续加热搅拌,同时将烧杯中液体滴加至三口烧瓶中,在某温度范围内反应一段时间,冷却至室温,过滤,滤渣用少量无水乙醇冲洗,烘干后称重。
产物BNO为黄色粉末,产率约92 %;m.p.176~178 ℃; UV (EtOH) λ / nm : 230 (K), 307 (K),400-418(R);1H NMR (500 MHz, CDCl3) δ:14.32 (s,2H),8.73(s,2H),7.82(d,J=8.3 Hz,2H),7.66(d,J=9.3 Hz, 2H), 7.59 (d, J = 7.8 Hz, 2H), 7.41 (s, 2H),7.22(d,J=7.5 Hz,2H),6.90(d,J=9.3 Hz,2H),3.67(d, J=5.2 Hz, 4H), 2.46 (t, J= 6.8 Hz, 12H), 1.90(d,J=6.8 Hz, 4H); IR δ /cm-1:1058,1159,1214, 1 227,1256, 1277, 1346, 1361, 1401, 1417, 1463, 1492,1629, 3439. Anal. calcd for C32H36N4O2: C 75.56, H 7.13,N 11.01;found C 75.67,H 7.38,N 11.32。
1.3 BNO 的表征
主要采用熔点测定、红外光谱、紫外可见光谱、核磁共振氢谱进行产物结构表征。
1.4 BNO 最佳合成工艺条件的考察
本研究通过单因素实验分别考察了溶剂、反应温度和反应时间对BNO产率的影响,获得了最佳合成工艺条件。
1.5 抑菌活性实验方法
参考文献[10]的抑菌实验步骤和方法,测定了产物BNO对二种受试细菌大肠杆菌、金黄色葡萄球菌的抑制作用。取34 g营养琼脂,加1.0 L蒸馏水,溶解后置于高压灭菌锅内,120℃灭菌30 min。冷却至50~60℃制成平板,取0.1 mL活化菌液,在平板上涂抹均匀,以等距离均匀、垂直放置牛津杯。在牛津杯中加入0.1 mL样品液,盖好平皿,置于37℃生化培养箱中培养24 h。取出后,测量每个牛津杯周围所产生的透明抑菌圈直径(mm)。
2 结果与讨论
2.1 最佳合成工艺条件的的确定
2.1.1 溶剂的影响
称取5 份2-羟基-1-萘甲醛1.033 g,溶剂分别使用无水乙醇、正丁醇、乙酸乙酯、四氢呋喃和丙酮,按照1.2 的操作步骤,在60℃下反应2.5 h,考察溶剂对BNO 产率的影响,结果见表1。
从表1 可以看出,以四氢呋喃作为反应溶剂时,BNO 的产率最低,为13%。可能是因为产物在四氢呋喃中具有良好的溶解度,故析出的固体产物较少;当乙醇、乙酸乙酯作溶剂时,BNO 的产率分别为89%、87%,相差很少,考虑到乙醇价格低,故本实验选择乙醇作为最佳反应溶剂。

表1 溶剂对BNO 产率的影响Table 1 The effect of solvents on the yield of BNO
2.1.2 温度的影响
按照1.2 的操作步骤,以乙醇为溶剂,在一定温度下(50、55、60、65、70℃)加热反应2.5 h,考察反应温度对BNO 产率的影响,结果见图1。

图1 温度对BNO 产率的影响Fig.1 The effect of temperature on the yield of BNO
由图1 可知,随着反应温度的升高,BNO 的产率先增大后降低,在60 ℃时产率最高,继续升高反应温度,BNO 的产率逐渐减小。有可能是因为温度较高,反应原料发生了氧化反应,同时有利于亚胺水解的副反应进行,导致产率降低。故确定60 ℃为最佳反应温度。
2.1.3 时间的影响
以乙醇为溶剂,按照1.2 的操作步骤,在60℃加热反应一定时间(分别是2、2.5、3、3.5、4、4.5、5 h),考察反应时间对BNO 产率的影响,结果见图2。
从图2 可以看出,随着反应时间的延长,BNO的产率先逐渐增加,然后迅速减少,当反应为4 h时收率达到最高,约为92%。因为随着反应时间的延长,原料转化率增加,产物增多,反应时间为4 h时,基本达到反应平衡,再延长反应时间,促进原料的氧化和产物的水解,使产率下降,故确定4 h为最佳反应时间。
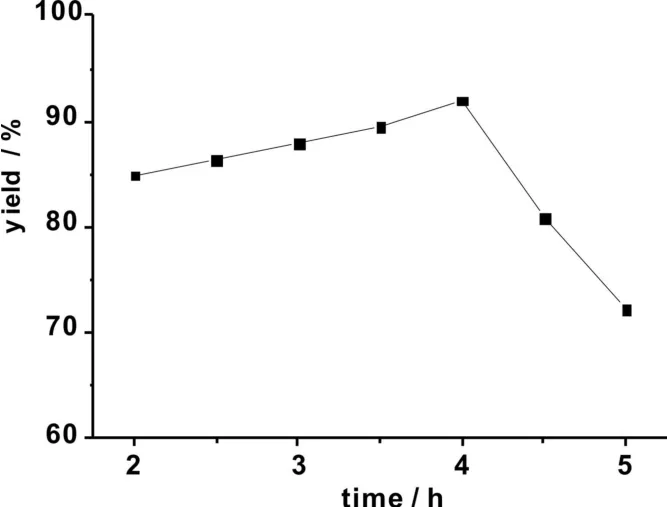
图2 反应时间对BNO 产率的影响Fig.2 The effect of time on the yield of BNO
2.2 BNO 的表征
2.2.1 熔点测定
常温常压下BAPP 为液体,原料2-羟基-1-萘甲醛的熔点为82~85 ℃,经测定得固体产物的熔点为176~178 ℃,与固体原料2-羟基-1-萘甲醛的熔点不同,由此,初步判断生成物可能是目标产物BNO。
2.2.2 红外光谱分析
BNO 的红外光谱如图3。从图中可以看出,在3439 cm-1处存在一个较宽的吸收峰,可归属为O-H的特征峰[18];在1629 cm-1处有一个强吸收峰,可归属为Schiff 碱典型的C = N 伸缩振动峰;1300-1544 cm-1吸收峰可能是萘环骨架C=C 的伸缩振动引起[19];在2941、2814、1463 cm-1附近的峰可能是由于-CH2-伸缩振动、变形振动引起的;1200-1300 cm-1的吸收峰可归属为萘环C-O 的伸缩振动[18];在1159 cm-1和1058cm-1处的吸收峰可归属为哌嗪环C-N 的伸缩振动。此外图中没有出现氨基NH2-、醛基CHO-典型吸收峰,说明该产物红外光谱符合目标产物的结构特征,且反应比较彻底。
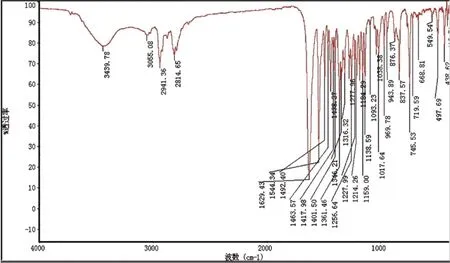
图3 BNO 的红外图谱Fig.3 IR spectrum of BNO
2.2.3 紫外光谱分析
图4 是产物BNO 与原料2-羟基-1-萘甲醛(简写为HNA)的紫外光谱图。从图中可以看出,NHA和BNO 在200~280 nm 区间出现较为复杂吸收峰,峰形比较相似,可归属为萘环骨架π-π*跃迁[18-19];二者在300~380 nm 出现的较强宽峰可归属为萘环C=C、醛基C=O 或亚胺基C=N 引起的π-π*跃迁,可能是由于助色基团-OH 的存在导致波长红移[18-19];此外HNA 在大于400 nm 有一弱吸收,而BNO 在400、418 nm 处有较强宽峰,可分别归属为醛基HC=O、亚胺基C=N 的n-π*跃迁产生的R 带,二者峰强的显著差别可能是以下二个原因引起的:一是杂原子不同,O 的电负性比N 强,给电子能力要弱;二是N-上的烃基与共轭体系产生较强的超共轭效应。
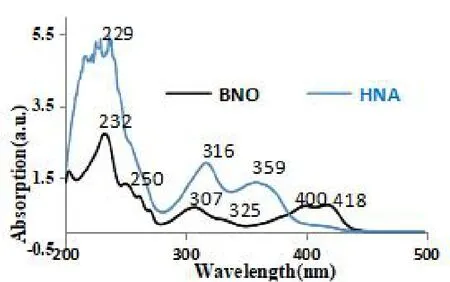
图4 BNO 和HNA 的紫外光谱Fig.4 UV-Vis spectra of BNO and HNA
2.2.4 核磁共振氢谱分析
由1H NMR 图谱(见图5)可以看出,在14.32 处有一单峰,可归属于萘环的羟基;在8.73 处的双峰为亚胺CH=N 上的质子;萘环上12 个质子峰出现在6.89~7.83 区间;3.67 处的峰可归属为C10上的质子;1.90 处的峰可归属为C11上的质子;2.46 处的三重峰可归属为C12上的质子。该1H NMR 进一步证明产物与目标产物BNO 结构一致。
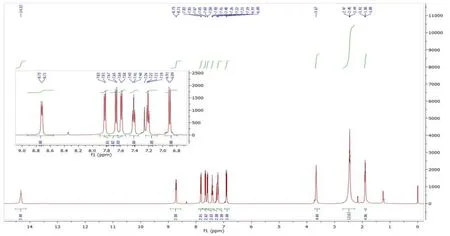
图5 BNO 的核磁共振氢谱图Fig.5 1H NMR spectrum of BNO
2.3 BNO 的抑菌活性
初步研究了产物BNO 浓度为1、5 mg/mL 时对大肠杆菌和金黄色葡萄球菌的抑制作用,实验发现:BNO 对大肠杆菌和金黄色葡萄球菌都具有一定的抑制作用,对大肠杆菌后续实验的抑菌活性略好(见表2)。有关抑菌活性的进一步实验正在后续实验进行中。

表2 BNO 的抑菌实验结果Table 2 The results of antibacterial activities of BNO
2.4 溶解度测试
称取7 份BNO,每份100 mg,加入7 只试管。在每只试管中分别加入氯仿、二氯甲烷、丙酮、乙醚、甲醇、乙醇、乙酸乙酯各1.0 mL,发现BNO在氯仿中全部溶解,在乙醚中几乎不溶,其他溶剂中少量溶解;加热后,在二氯甲烷中全部溶解,乙醚中仍旧几乎不溶,其他溶剂中溶解度有所增加;再在试管中分别加入1 mL 相应溶剂,丙酮中全部溶解,乙醇、甲醇中部分溶解,乙酸乙酯中少数溶解,而乙醚依旧几乎不溶,故可以得到BNO 在个溶剂中的溶解性难易顺序为:三氯甲烷> 二氯甲烷> 丙酮> 乙醇> 甲醇> 乙酸乙酯> 乙醚。
3 小结
以N,N'-二(3-氨基丙基)哌嗪和2-羟基-1-萘甲醛为原料,采用简单易行的加成-消除反应,设计合成了一个Schiff 碱化合物即双(2-羟基-1-萘甲醛)缩N,N'-二(3-氨基丙基哌嗪)Schiff 碱。由于2-羟基-1-萘甲醛分子中的羟基、醛羰基与萘环会分别发生p-π、π-π共轭效应,使得羰基碳正电性减弱,反应活性降低,因此,至少需要对反应温度和反应时间二个因素进行考察。结合有关参考文献,本研究选取了反应温度、反应时间、溶剂种类三个因素进行了单因素实验,并且获得了目标化合物的最佳合成工艺条件,产率高达92%。利用熔点、红外光谱、紫外光谱、核磁共振氢谱等手段对产物结构进行表征,证明为目标化合物。
该Schiff 碱分子中含有6 个配位原子,分别是2 个羟基O、2 个亚氨基N 和哌嗪环上的2 个N,由于哌嗪环可以以船式和椅式二种构象存在,以及哌嗪环上的柔性手臂丙基,使得该分子是一个很好的配体。下一步我们将对该席夫碱的金属配合物的合成、性质及活性等展开深入研究,为设计具有良好生物活性、光学性能的哌嗪等杂环衍生物[20-21]提供一定的理论和实验经验。

