Na3AlF6-SiO2熔盐中Si(IV)的电化学行为
何 林,高运明,秦庆伟,李光强
(1. 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2. 武汉科技大学钢铁冶金新工艺湖北省重点实验室,湖北 武汉,430081)
熔盐电沉积法制备硅因具有操作简单、工艺流程短、能耗低、环境污染小等优点而备受关注[1-2]。迄今为止,有关硅电沉积的研究工作大多在氟化物熔盐体系中进行,特别是Na3AlF6熔盐体系,其不仅对自然界中大量存在的SiO2有较高的溶解度,而且在铝电解中已获得成功应用,有望成为理想的熔盐体系而应用于硅制备。但目前,有关在Na3AlF6熔盐中利用溶解的SiO2电沉积硅的研究,主要采用石墨坩埚作为辅助电极或阳极,Pt作为准参比电极,由此引入因碳参与反应而带来的COx等污染气体排放,以及熔盐电子导电性所导致的CV曲线峰位不明显、有关电位不稳定等问题[3-7]。基于此,本文拟利用Y2O3稳定的ZrO2固体电解质(YSZ)管集成构建Pt,O2(air)│YSZ作为参比、辅助电极的三电极新型电化学池[8],采用循环伏安、计时电流等电化学测试技术,在完全无碳条件下研究了1323 K下Na3AlF6-5%SiO2熔盐体系中Si(IV)的电化学还原行为,以期为硅的绿色电沉积技术开发提供依据。
1 实验
1.1 熔盐与电极制备
将分析纯试剂SiO2和Na3AlF6置于真空干燥箱中,在473 K下分别烘干12 h后,配制成95%Na3AlF6-5%SiO2(质量分数,下同)的混合物,充分混匀后压制成块,在Pt坩埚内于1373 K下保温熔化3 h;随后,将熔盐倾倒于置于冰水上的不锈钢盘中急冷凝固,得到Na3AlF6-5%SiO2预熔盐碎块备用。研究显示,1253 K温度下SiO2在Na3AlF6中的溶解度为3.0%[9],1273 K时其溶解度为5.9%[10],故本研究选择在1323 K熔体中添加5%的SiO2。
1.2 实验方法
本文构建的电化学池示意图与文献[8,11]的装置类似。所用YSZ管含8 mol%Y2O3(全稳定型),YSZ管内外径分别为8、10 mm,长度为100 mm。为密封与操作方便,将YSZ管与刚玉管(内外径分别为11、15 mm,长度420 mm)通过高温水泥密封连接。
将质量约1.8 g的Na3AlF6-5%SiO2预熔盐(或纯Na3AlF6试剂)装入YSZ管,通过与YSZ管相连的刚玉管,将YSZ管封闭端放入硅碳管管式炉内恒温区。高温炉以5 K/min的速率升温,在673 K及923 K各保温1 h,除去盐中自由水和结合水,同时以25 mL/min流速向YSZ管内通入经硅胶干燥的高纯Ar气进行保护;YSZ管外(炉内)通入流速为200 mL/min的空气,形成稳定的氧分压气氛,构建Pt,O2(air)丨YSZ参比电极。如无特别说明,本文后续提到的电位均指相对Pt,O2(air)|YSZ参比电极的还原电位。当温度升至1323 K,恒温10 min,Ar气流速调整为17 mL/min。将电化学池装置的各电极联接到Ivium型电化学工作站,通过开路电位法确定熔盐液面,Ir丝工作电极在熔盐中插入深度为7 mm(对应表观面积为0.112 cm2),随后进行循环伏安(CV)和计时电流(CA)电化学测试。此外,将装有Na3AlF6-5%SiO2熔体的YSZ管在1323 K下静置30 min后,随炉冷却到室温,切割装有熔盐的YSZ管并制成金相样品,利用Nova 400 Nano型场发射扫描电镜(SEM)结合其配备的INCA IE 350PentaFET X-3型能谱仪(EDS),对凝固盐的微观组织及微区成分进行表征。
2 结果与讨论
2.1 循环伏安法测试结果
图1为Na3AlF6-5%SiO2熔盐于不同扫描速率v下的CV曲线,此外,图中还显示了Na3AlF6(空白渣)的CV曲线作为对照组。由图1可见,Na3AlF6在扫描过程中(v=30 mV/s),电流值维持在0附近,表明此范围Na3AlF6的电化学稳定性高,未发生化学反应。不同扫描速率下,Na3AlF6-5%SiO2熔盐的还原峰C清晰可见,且峰电位在-1.6~-1.7 V之间。热力学计算结果显示,SiO2在1323 K的还原电位为-1.70 V,结合本实验采用的熔盐体系,可判断C峰对应于Si的一步还原,即Si(IV)→Si,这不同于Sokhanvaran等[3]得出的Si(IV)还原是Si(IV)→Si(II)→Si分步进行的结论,并且该文献中,所测熔盐的CV曲线峰形并不明显。图1中,C峰前-1.20~-1.42 V电位对应的小电流,可归因于Si在Ir工作电极上轻微的欠电位沉积;C峰后的还原峰(峰位约为-1.8 V)则对应Al的合金化析出。A峰是对应C峰的Si的再氧化峰,具有典型的不可溶沉积产物氧化剥离的特征。Si、Al的析出电位已另行通过-1.4、-1.6、-1.8 V等恒电位下的电解实验证实(将在另文中详细介绍),本文主要研究Si(IV)的电化学还原行为,因此,下文主要分析对应于Si(IV)的还原峰C及Si的再氧化峰A。
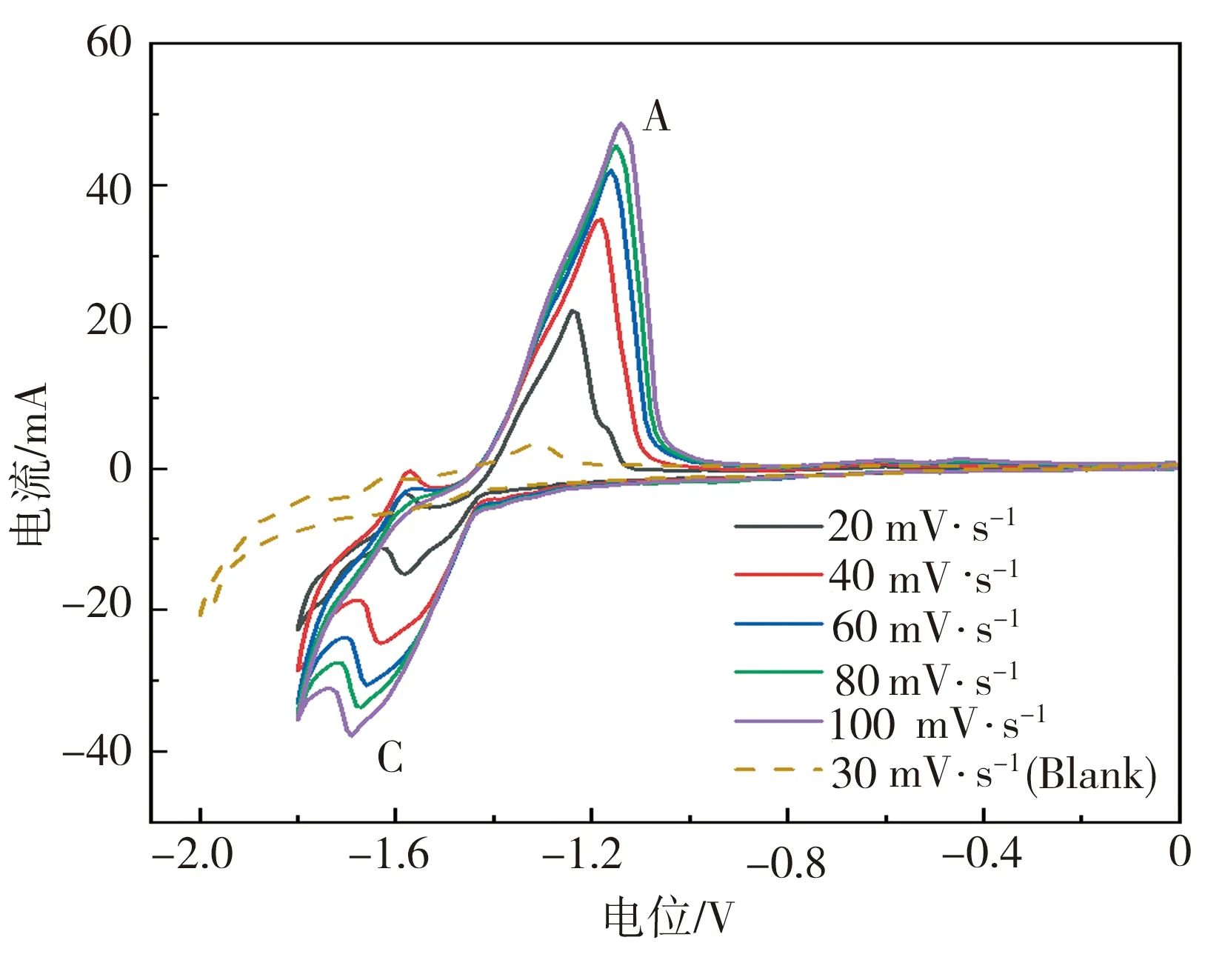
图1 Na3AlF6及Na3AlF6-5%SiO2熔盐的循环伏安曲线
从图1中提取相关电化学参数列于表1,表中Ipc为还原峰电流,Epc为还原峰电位,Epa为氧化峰电位,Epc/2表示半峰(I=Ipc/2)处的电位,ipc为电流密度(ipc=Ipc/A,A表示电极面积,取0.112 cm2),α表示传递系数(表中显示为式(3)的计算值)。
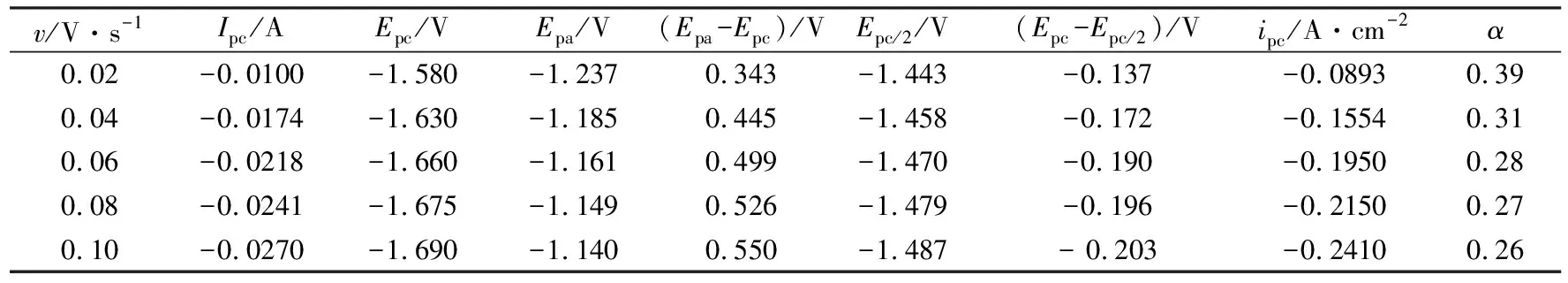
表1 图1中提取的还原峰C和氧化峰A的相关电化学参数
根据表1数据,可作还原峰C的Epc-lgv和ipc-v1/2关系图如图2所示。由表1可见,氧化峰与还原峰电位差(Epa-Epc)始终大于2.303RT/(nF)的计算值(0.0656 V);结合图2可知,Epc和lgv呈线性关系且斜率不为0,表明Si(IV)的还原不是可逆过程[12-14];此外,扫描速率范围内,ipc与v1/2也呈现线性关系且拟合直线过原点,表明Si(IV)的还原并非准可逆过程[13],同时说明该反应是受溶解的Si(IV)在熔盐中扩散控制的[12,15]。由此可见,Si(IV)的还原是受扩散控制且产物不可溶的不可逆过程,其扩散系数D一般由下式(1)和式(2)(Delahay公式)计算[12-14]:
(1)
ipc=0.4958nFC0(αnαFD)1/2(RT)-1/2v1/2
(2)
上述式中:T为温度,T=1323 K;R为气体摩尔常数,R=8.314 J/(mol·K);F表示法拉第常数,F=96 485 C/mol;n为电极反应交换电子数;nα表示多电子电极反应还原过程中,电子传输到速率控制步骤并包含速率控制步骤的电子数,这里C峰对应于Si的一步还原,取n=nα=4;C0为电活性Si(IV)的体积浓度,mol/cm3。
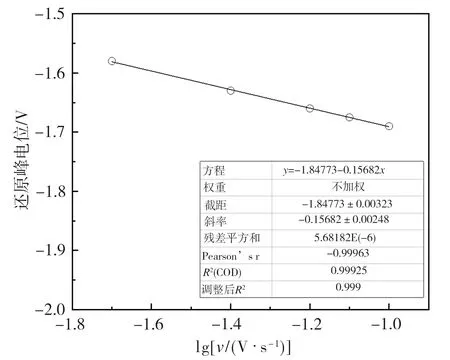
(a)Epc-lgv
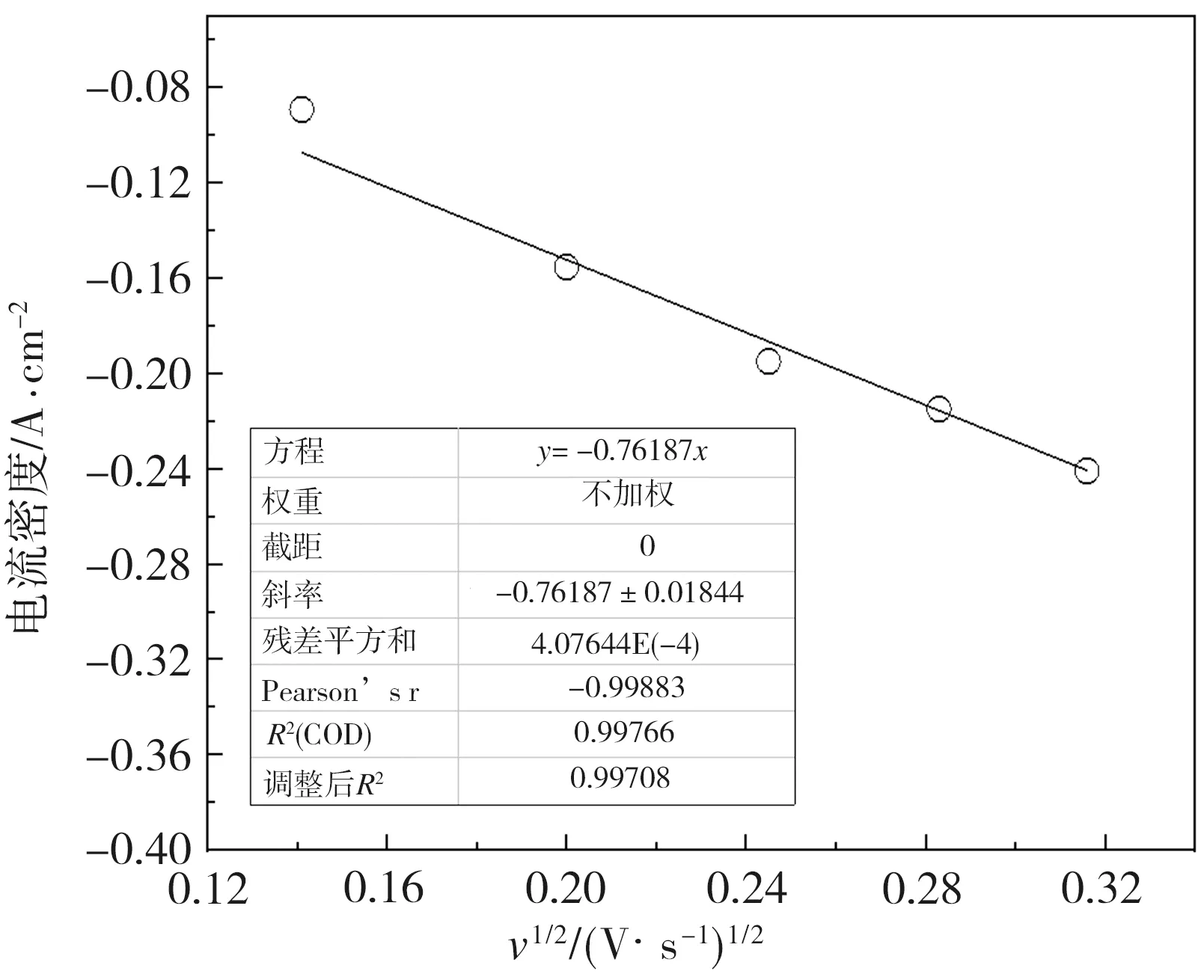
(b)ipc-v1/2
参考Korenko[16]和Grjotheim等[17]的研究工作,取Na3AlF6-SiO2熔盐体系在1323 K时密度为2.05 g/cm3;本文熔盐总质量约为1.8 g,体系中SiO2的质量分数为5%,计算得到本文熔盐中Si(IV)的初始浓度C0=0.0017 mol/cm3。将图2中斜率值分别带入式(1)和式(2),即得到Si(IV)在1323 K时的扩散系数D=7.2×10-7cm2/s,传递系数α为0.21。值得注意的是,这里Si(IV)并不代表SiO2在熔盐中均以简单Si4+离子形式存在,实际往往很可能以含Si、O的复合离子形式存在[10,18]。
此外,对于不可逆体系,利用式(3)与式(2)组合,可计算得到其扩散系数D[14]:
(3)
此情形下,D的计算值处于4.0×10-7~6.0×10-7cm2/s,α为0.26~0.39,D和α均与前文计算结果相近,处于同一数量级,且扫描速率越大,α的计算值越接近前文的计算结果(0.21)。
2.2 计时电流法测试结果
图3为Na3AlF6-5%SiO2体系在不同阶跃电位下初期的CA曲线。由图3可见,当给工作电极施加阶跃电位时,电流持续降低直至稳定,未发现双电层的充电效应,表明此熔盐体系下工作电极与熔盐之间的双电层未对CA曲线产生明显影响。当施加的阶跃电位在-1.0~-1.4 V范围时,极限电流均很小,接近于0(背景电流),表明在此阶跃电位范围内,所施加的电位未能使Si元素沉积,这与前文的循环伏安法所得结果一致;当阶跃电位负移至-1.5 V和-1.6 V时,电流明显增大,表明此条件下有电子转移发生,二者的CA曲线较为相似,电流相差较小,到达极限电流的时间接近,结合前文的CV分析可知,此阶跃电位范围工作电极上有Si开始沉积。当阶跃电位负移至-1.7 V及以上时,CA曲线形状开始改变,到达稳定电流的时间相对更长,表明很可能有新的沉积反应发生。由于该过程所涉及的离子反应较多,沉积机理也更为复杂,故本文仅针对-1.5、-1.6 V阶跃电位下Si的沉积规律进行分析。
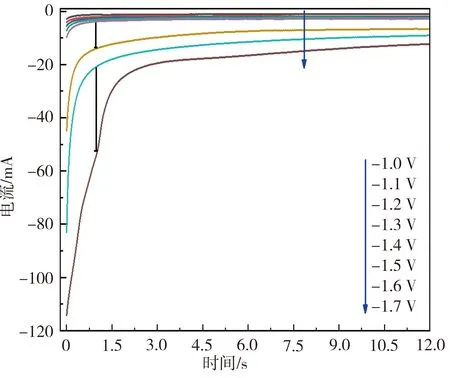
(a)-1.0~-1.7 V
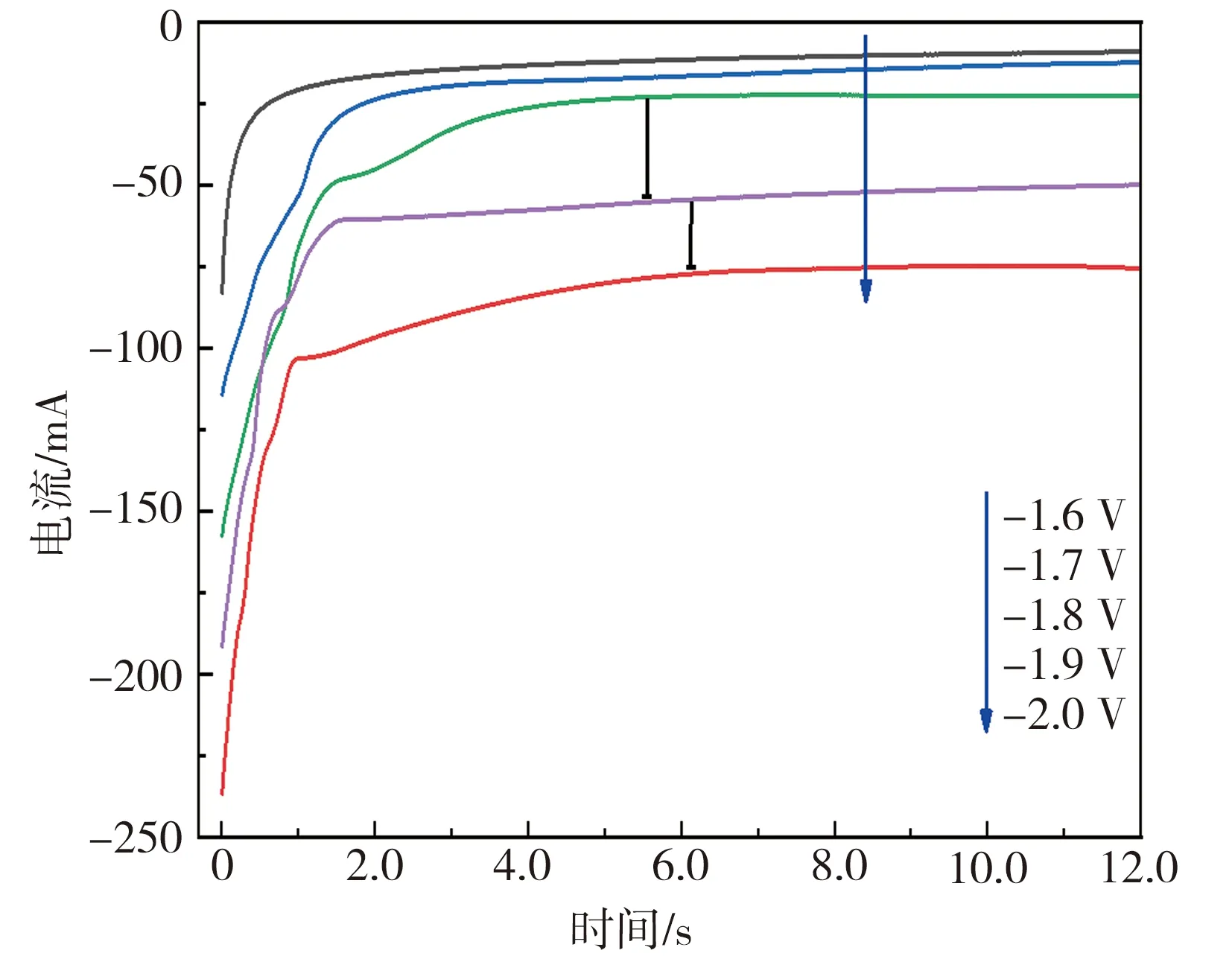
(b) -1.6~-2.0 V
图4为根据-1.5、-1.6 V阶跃电位下熔盐的计时电流数据(图3)所作的I(t)-t-1/2关系曲线,可以看出,当图3(a)中时间t<2.04 s时,对应图4初始阶段,I与t-1/2不呈线性关系,当t超过2.04 s后,I与t-1/2呈线性关系且近似过原点,表明此时间段内Si的沉积是受扩散控制的,可利用Cottrell方程计算Si(IV)的扩散系数[11,13]:
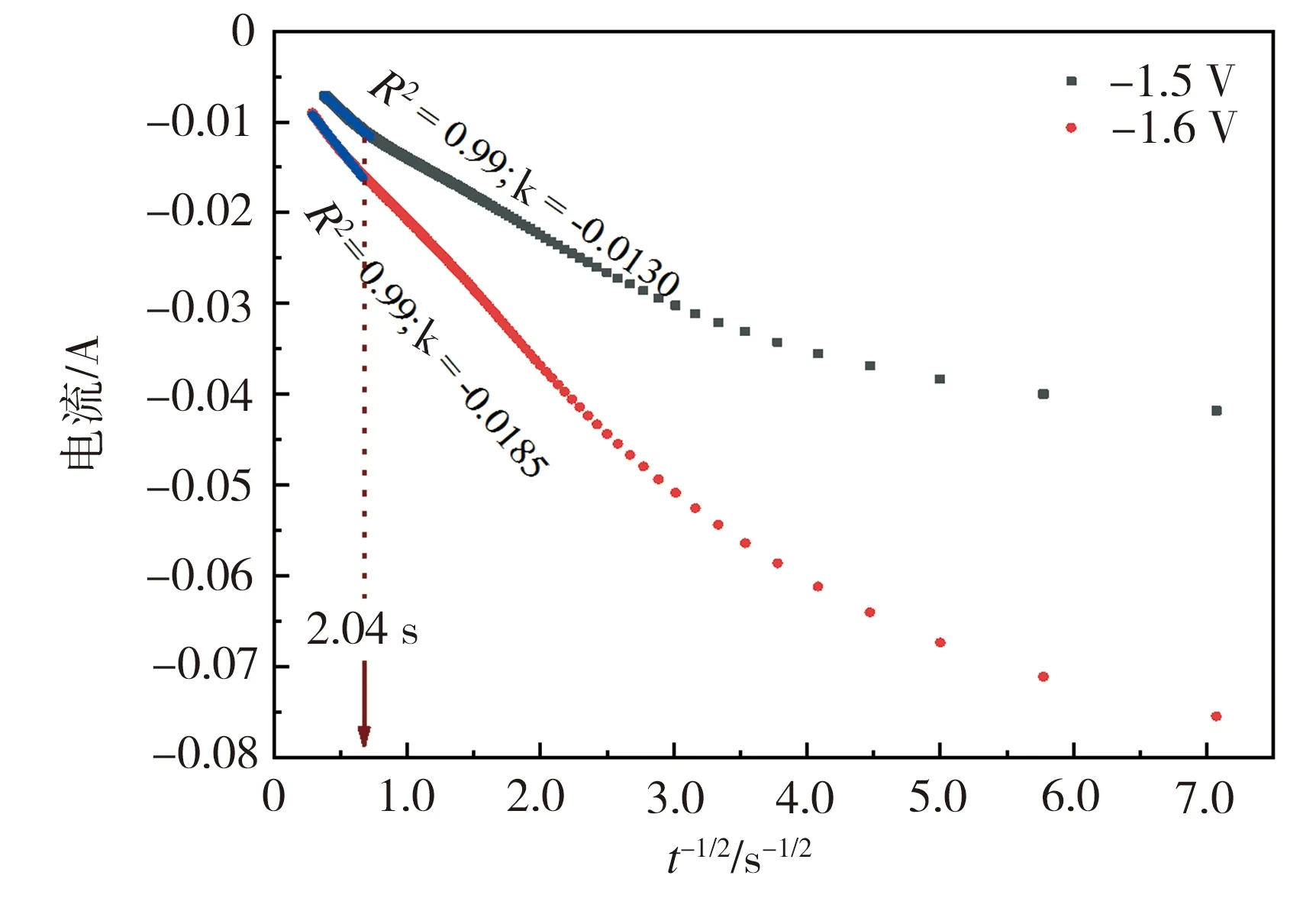
图4 图3中对应-1.5、-1.6 V阶跃电位下I-t-1/2关系
(4)
计算得到-1.5、-1.6 V阶跃电位下,Si(IV)的扩散系数依次为1.0×10-7、2.0×10-7cm2/s,这与前文CV法得到的结果相近。
2.3 讨论
目前,文献中关于熔盐中Si(IV)还原过程的传递系数α值鲜有报道,一般假定α=0.50[3],仅见Cai等[19]在1023 K下利用CV法研究NaCl-KCl-NaF-SiO2熔盐时也得出Si(IV)的还原是不可逆过程,利用式(3)计算得到其电荷传递系数α为0.30,与本研究Na3AlF6-SiO2体系中Si(IV)还原的α值相近。
关于Na3AlF6-SiO2体系下Si(IV)的扩散系数,Sokhanvaran[3]基于CV曲线,采用式(2)计算得到Si(IV)扩散系数D=1.32×10-5cm-2/s(1313 K,5%SiO2),但其认为Si(IV)的还原是分步进行的;Frazer等[5]通过计时电位法,采用Sand公式得到Si(IV)的扩散系数D=6.4×10-5cm2/s(1293 K)。这两个扩散系数均比本文计算值要大得多,分析原因如下:一方面,上述研究往往使用石墨坩埚,易带来副反应,且C溶解于熔盐会增加熔盐的电子导电性,如文献[3]中CV曲线电流过大,甚至达到-2.5 A,从而影响所得电化学曲线的稳定性与准确性,可能会导致所得Si(IV)扩散系数值偏大;另一方面,本文在完全无C环境下采用YSZ管构建新型电化学池,由于Na3AlF6熔体侵蚀性强,可能会有YSZ颗粒溶解或剥落进入到熔体中,导致熔体性质发生变化,包括SiO2浓度可能会降低。
图5为装有Na3AlF6-5%SiO2熔体的YSZ管在1323 K静置30 min熔盐凝固后的SEM照片及相应点位的EDS能谱。由图5可见,固化盐中存在一定量Y、Zr的氧、氟化物颗粒或结晶析出物,这很可能会使熔盐黏度增大,进而导致Si(IV)扩散系数降低。后续研究中,可考虑采取措施降低熔盐对YSZ管的侵蚀(如向熔体中添加YF3,改变熔体成分等[20])。另外,本文熔盐经3 h高温预熔,SiO2也会因化学反应逸出SiF4而遭受损失[21]。依据式(2),忽略SiO2实际浓度下降也会导致Si(IV)扩散系数降低。
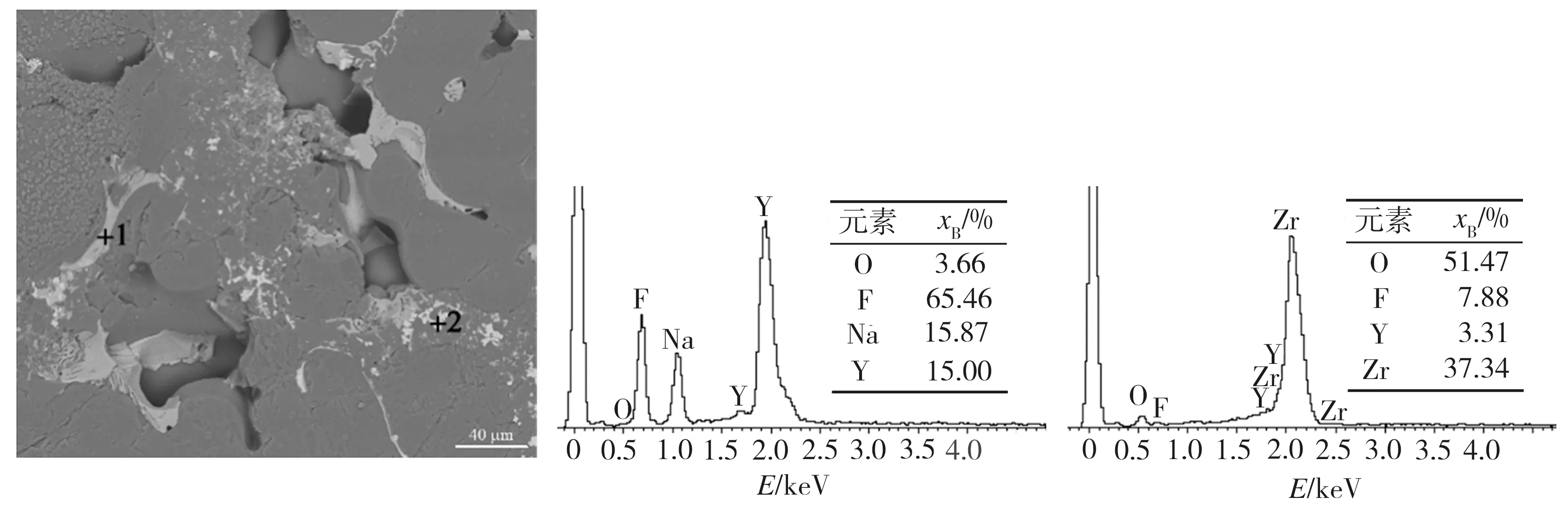
(a)SEM照片 (b)点位1,EDS能谱 (c)点位2,EDS能谱
3 结论
(1)循环伏安法测试结果表明,Na3AlF6-5%SiO2熔盐中Si(IV)的电化学还原是单步骤4电子转移不可逆过程,其电极反应过程受扩散控制,还原产物Si不可溶,电荷传递系数在0.21~0.39范围。
(2)循环伏安法测试结果显示,Si(IV)在Na3AlF6-5%SiO2熔盐中的还原峰电位在-1.6 ~ -1.7 V之间。
(3)通过两种测量方法计算得到,Si(IV)在Na3AlF6-5%SiO2熔盐中扩散系数在10-7cm2/s数量级,两种方法的测试结果接近,但低于文献报道的结果,原因可能是Na3AlF6系熔盐侵蚀性强造成YSZ管剥落进而改变熔体性质,以及SiO2会因化学反应逸出SiF4而导致浓度降低。
(4)相对于传统电化学池,在本文构建的新型电化学池中获得的Na3AlF6-SiO2熔盐的电化学测试曲线更清晰可见,有利于分析Si(IV)电化学还原机理及计算有关电化学参数。后续研究中,应采取措施降低熔盐对YSZ管的侵蚀以及因生成SiF4挥发而造成的SiO2的损失。

