阿达木单抗治疗斑块型银屑病疗效及代谢综合征对疗效的影响
王宥霖 王 睿 赵振凯 孙 杰 张 媛 汤自洁 张 菡 舒 心 李承新
中国人民解放军总医院第一医学中心皮肤科,北京,100853
银屑病(psoriasis)是一种慢性炎症性皮肤病,2008年完成的一项基于我国六省市的流行病学调查显示,银屑病患病率为0.47%[1]。一般认为银屑病是遗传因素与环境因素等多种因素相互作用引起,但发病机制尚不完全清楚。目前公认的发病机制为T细胞介导的免疫相关反应。此病尚无根治的方法,目前多采用药物治疗、物理治疗、生物治疗等方法,以减轻症状和皮损、避免反复、提高患者生活质量为目标,效果差异大,患者满意度低。既往研究提示,伴代谢综合(metabolic syndrome, MS)征的银屑病患者对传统治疗存在抵抗,传统治疗疗效更差[2]。但是伴有代谢综合征的银屑病患者是否对生物制剂如阿达木单抗治疗银屑病的疗效有影响,目前国内外暂无相关报道。因此本研究希望通过分析经阿达木单抗治疗的斑块型银屑病患者,伴代谢综合征与疗效是否存在相关性,从而判断伴代谢综合征银屑病患者是否对阿达木单抗疗效存在抵抗。
1 资料与方法
1.1 对象 收集2020年11月至 2021年3月就诊于我科使用阿达木单抗治疗的斑块型银屑病患者,共19例。纳入标准:年龄≥18岁的斑块型银屑病患者。排除标准:(1)急性点滴型、脓疱型、关节病型、红皮型银屑病;(2)除银屑病外的其他皮肤病;(3)近2周内接受银屑病外用药治疗(维A酸衍生物、维生素D衍生物、糖皮质激素等);(4)近2个月内接受银屑病系统治疗(如免疫抑制剂、维A酸衍生物等)或 NB-UVB治疗;(5)存在活动性感染如病毒、细菌(包括结核杆菌)、真菌感染等;(6)存在心、肝(ALT、AST高于正常上限1.5倍)、肾功能损害(CR高于正常上限1.5倍);(7)存在造血系统异常(血红蛋白低于100 g/L、白细胞低于3.0×109/L、血小板低于100×109/L);(8)妊娠或哺乳期妇女;(9)既往脱髓鞘病变或多发性硬化症病史;(10)恶性肿瘤病史;(11)有生物制剂治疗史;(12)近3个月内参加过其他临床研究者;(13)近半年接受降压药、降糖药治疗等对代谢综合征有治疗效果药物的患者;(14)任何其他研究者认为不宜参加本试验者。所有患者治疗前均行血常规、血生化、肺部CT以及结核、乙肝、艾滋、梅毒等感染指标检测以排除生物制剂禁忌症。治疗前与患者充分沟通治疗期间可能出现的风险与不良反应,并与患者签署知情同意书。
代谢综合征诊断:根据2005年IDF(国际糖尿病联盟)标准[3]:(1)必要条件:腰围(中国男性>90 cm,女性>80 cm)。(2)合并以下四项指标中任两项:1)甘油三酯:>1.7 mmol/L或已接受相应治疗;2)HDL:男<0.9 mmol/L,女<1.3 mmol/L,或已接受相应治疗;3)血压:收缩压≥130 mmHg,或舒张压≥85 mmHg,或此前诊断过高血压病或接受过相应治疗;4)空腹血糖:≥5.6 mmol/L,或已接受相应治疗,或此前诊断为Ⅱ型糖尿病。
1.2 方法 所有符合纳入排除标准的患者自0周起注射阿达木单抗80 mg,此后于第1、3、5、7、9、11周分别注射阿达木单抗40 mg,于第0、4、8、12周观察皮损及改善情况,即记录PASI评分,由两名临床经验丰富的医师同时分别进行,并取均值。
2 结果
2.1 一般资料 入组患者19例,年龄(36.47±10.26)岁,男18例,女1例,银屑病皮损1~25年,0周时PASI评分0.5~31.2,伴MS银屑病患者11例,不伴MS银屑病患者8例。见表1。

表1 人口学基线特征
2.2 治疗4、8、12周后PASI评分变化情况 经阿达木单抗治疗4、8、12周后,19例患者PASI评分自基线时的9.7(2.0,15.6)分别下降到5.2(1.1,6.9)、4.0(0.8,5.4)、3.3(0.4,4.2)。将0、4、8、12周PASI评分纳入重复测量方差分析,发现Mauchly’s球形检验显著性P<0.001,数据呈非对称,采用多变量检验,显著性P=0.001,说明不同时间点之间PASI评分均存在差异性,即19例银屑病患者经阿达木单抗治疗后,0、4、8、12周PASI评分呈持续下降趋势且具有统计学意义。治疗期间患者PASI变化情况见表2,疗效变化见图1。

1a: 0周;1b: 4周;1c: 12周

表2 治疗期间患者PASI变化情况
2.3 伴代谢综合征与疗效之间的相关性 根据是否伴有代谢综合征,将19例患者分为伴有MS和不伴有MS 2组,2组在人口学等基线数据不存在差异(表3)。同样根据患者PASI评分,将19例患者分为PASI 75、PASI 90、疗效差(疗效差指PASI评分改善不足50%)3个等级,3个等级人数分别为4、10、5。根据Spearman相关性得出两组相关性r=-0.679,P<0.01(表4),即伴代谢综合征与疗效间存在重度负相关关系。说明在斑块型银屑病患者中,伴有代谢综合征对阿达木治疗疗效更差。

表3 两组基线数据比较
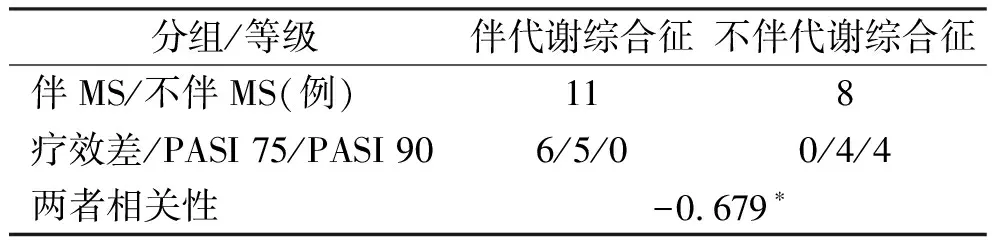
表4 代谢综合征与疗效相关性
2.4 安全性评估 19例患者中,1例因自行保存不当,第8周出现新发皮疹,考虑为药物失活所致银屑病加重。所有患者均无输液反应、局部感染等不良反应。无新发肝肾功能异常。
3 讨论
全人源TNF-α抑制剂阿达木单抗是近年来治疗银屑病使用最广泛的生物制剂之一,其主要药理学作用是与游离的TNF-α结合,阻断与细胞表面TNF-α受体的相互作用,从而调控TNF-α诱导/调节的生物应答[4]。阿达木单抗针对斑块型银屑病疗效显著。一项[5]针对斑块型银屑病的III期临床研究显示,经阿达木单抗治疗12周时,77.8%的患者达到PASI 75;12周时的皮肤病生活质量指数(dermatology life quality index,DLQI)阿达木单抗组下降9.07,远高于安慰剂对照组的4.17。除了针对银屑病疗效显著,不良反应也较少。在心血管事件上,ESPRIT研究发现,使用阿达木单抗 10年随访期间心血管事件的发生率持续保持低水平,低于未接受过生物制剂治疗的银屑病患者发生率。阿达木进行的77项临床试验的安全性数据汇总[6],共纳入29 967例患者,可见常见不良反应如感染、注射部位反应、神经脱髓鞘等。上述发病率处于稳定低值。
有研究表明,代谢综合征常与银屑病共同存在。代谢综合征是一组基于高血压、胰岛素抵抗、超重/肥胖、脂代谢异常、非酒精性脂肪肝等多种表现的综合征,银屑病患者代谢综合征发病率升高[7]。一项研究将银屑病患者按照病情严重程度分为轻、中、重度组,三组患者中代谢综合征的发病率分别为22%、56%、98%[8]。有研究显示伴有代谢综合征的银屑病患者,血清CRP水平明显高于不伴有代谢综合征的银屑病患者[9]。
本研究通过对经阿达木治疗的19例斑块型银屑病患者12周内疗效与伴代谢综合征相关性分析,发现阿达木治疗斑块型银屑病患者疗效明显,73.6%患者经12周治疗后可达到PASI 75;伴代谢综合征与疗效呈重度负相关。由于银屑病与代谢综合征存在共同通路以及相同炎性介质如TNF-α、IL-6、IL-17等[10],有研究显示,伴代谢综合征银屑病患者经治疗后,皮损即使得到清除,但炎性状态仍旧存在[11]。因此可以推测由于代谢综合征加重了银屑病炎症反应从而加重银屑病病情,合并代谢综合征的银屑病患者对于阿达木单抗治疗应答反应以及疗效弱于不合并代谢综合征的银屑病患者。经过相同治疗后,合并代谢综合征的银屑病患者达到不合并代谢综合征患者的相同疗效(如PASI 75),所需时间可能更长。
本研究首次发现,伴代谢综合征银屑病患者使用阿达木单抗疗效差于不伴代谢综合征银屑病患者。但由于样本量小,观察时间短,且只通过皮损改善情况作为疗效指标判定因素,因此接下来需进一步扩大样本量以及观察疗效时间,对于疗效差的患者检测抗药抗体、TNF-α等指标进行评估,同时银屑病患者疗效受到性别、人种、吸烟、体重、银屑病皮损分布部位等多种因素影响[12],需要考虑其他影响因素对银屑病疗效的影响,以便进行综合考量。

