人造肛门括约肌经皮无线供能系统安全性及相容性分析
杨 辰,颜国正,周泽润,华芳芳
(上海交通大学 电子信息与电气工程学院; 医疗机器人研究院,上海 200240)
肛门失禁(FI)是指人体肠道内容物不受生理控制产生自溢出的病症.FI病因有多种,且总会给患者的正常生活带来极大的困扰.相关文献记载,肛门失禁是最令患者心理崩溃和社交恐惧的疾病之一[1].根据Pretlove等[2]的研究,FI发病率与年龄呈正相关.一项在新西兰与澳大利亚的研究表明:老年人中肛门失禁的总发病率约为12%~13%,而因老年护理住院的老者患病率最高达50%[3].
随着我国人口老龄化的加剧,FI患病率提升的严峻形势可被预见.而目前FI的治疗方法效果不佳,无法达到患者的心理预期且常伴有部分后遗症[4-7].而采用经皮无线供能(TET)技术的新型肛门括约肌系统相较传统手动、一次性电池供电或拖线供能括约肌系统具有植入方便、保护患者隐私、能量供给可重复使用等优点.TET系统是一种短距离、跨越皮肤的无线供能系统,通过发射线圈与接收线圈之间的交变磁场来传输电能.目前,TET系统已运用于人造器官的供能.Kaga 等[8]就成功地为心室辅助装置设计了一款工作频率在500 kHz,效率最高为91.82%的TET系统.
然而,TET系统在人造肛门括约肌(AAS)系统中的运用也带来了生物安全性及相容性方面的问题.昝鹏等[9]对TET系统的电磁相容性进行了仿真分析,得出非对称松耦合TET系统的电磁相容性良好的结论.Xiao等[10]针对心脏起搏器的TET系统进行了充电实验与安全性仿真,仿真结果表明低电流、小功率的经皮无线供能系统产生的电磁辐射对于人体大脑的影响几乎可以忽略.Zhou等[11]对人造肛门括约肌的TET系统进行了分析,针对稳压器进行了专门的优化,有效降低了TET工作过程中的升温情况.
以往研究大多局限于TET系统生物安全性的某方面如电磁辐射量或发热量.本文针对TET系统的电磁辐射、温升等进行研究,结合生物相容性对TET系统的植入性能进行一体化分析,为人造肛门括约肌的人体实验奠定基础.
1 TET系统生物电磁安全性研究
1.1 TET系统的构成
人造肛门括约肌系统主要由体内部分和体外部分构成,体内部分主要包括括约肌主体机构及接收线圈,体外部分分为体外控制系统、发射线圈以及体外供能系统,如图1所示.

图1 人造肛门括约肌系统示意图
括约肌主体机构通过调节肛肠角完成控便、排便操作,机构配备压力传感器记录肠道压力数据.体外控制器通过通讯芯片发送控制指令到达机构,同时接收机构记录的压力数据并在压力值到达预设阈值时发出提醒.AAS系统的典型TET系统示意图如图2所示.其主要由发射电源、发射线圈、接收线圈、整流器、稳压器、电源管理模块、锂离子电池及后续的主体机构构成.发射电源为发射线圈提供交变电流,两线圈通过电磁感应传输电能.感应电流经过后续的整流稳压以及电源管理模块为电池充电的同时也为后续系统供能.
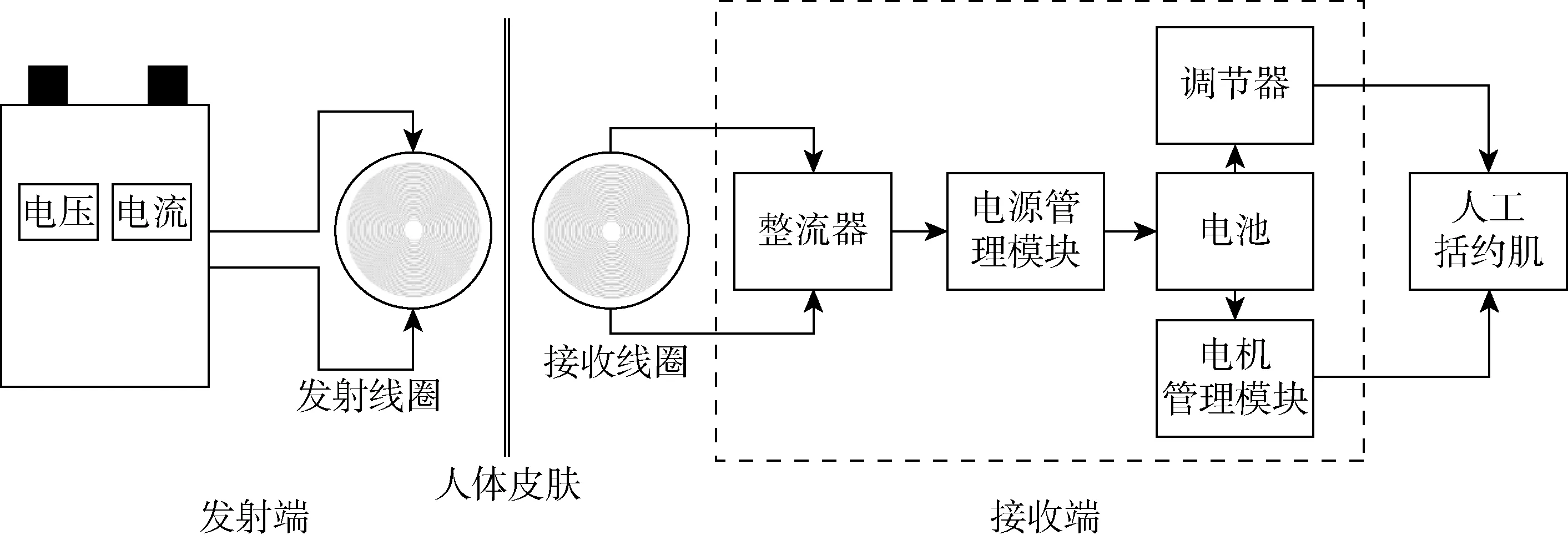
图2 AAS系统的典型TET系统示意图
1.2 比吸收率
电磁辐射对人体的作用机理复杂,常采用比吸收率(SAR)定量分析电磁波与生物体之间的相互作用程度[12].SAR为物体单位质量在单位时间内吸收的电磁能量,计算公式为
(1)
式中:m为受影响组织质量;V为受影响组织体积;W为组织所吸收的电磁辐射能量;E为电场强度;ρ为组织液密度;σ为组织液电导率.基于SAR的定义,常用的生物电磁安全性标准参考量还有SAR1g和SAR10g,分别表示1 g生物体单位时间内吸收的平均能量和10 g生物体单位时间内吸收的平均能量.SAR能表征电磁辐射热效应,无外部热传递时,对典型软组织施加强度为1 W/kg的电磁辐射,其温度升高速率为0.018 ℃/min[13].
1.3 人造肛门括约肌的TET系统电磁安全性仿真研究
1.3.1线圈参数设计 AAS为一种在体长期工作人造器官,充电不可过于频繁,同时为减少患者充电过程中的不便,充电时间应尽量缩短.专业医生建议整个TET系统厚度应控制在8 mm内,否则将给植入手术及患者日常生活带来诸多不便[11].本文根据以上系统需求及目前实际使用的TET系统进行线圈建模,具体参数如表1所示.

表1 线圈参数
仿真中,线圈间传输频率为110 kHz,发射线圈发射功率为10 W,使用阻值为8.2 Ω的电阻等效替代接收线圈的后续负载,测得负载实际接收功率为2.13 W.由于在实际能量传输过程中,发射线圈使用趋肤效应较弱的Litz线绕制成平面螺线圈状,且发射线圈中的电流远大于接收线圈中的电流,发射线圈的电磁场也远大于接收线圈,所以仿真验证主要针对发射线圈.对发射线圈模型进行简化,使用有限密绕螺线管模型来模拟发射线圈,该模型已被证明电磁场强度分布与实际线圈相似[14].
发射线圈安装在锰锌铁氧体材料上,这种线圈结构能够屏蔽非目标方向高频磁场,增强线圈之间的电磁场,提高磁通量密度.为发射线圈配备厚度为0.25 mm,直径为48 mm的圆柱形锰锌铁氧体层,如图3(a)所示.
写作是指学生以文字的形式来描述自己的经历与真情实感。但是在这个过程中,多数学生为了完成老师留下来的任务而应付式的写作。由于缺乏教师针对性的指导,很多学生不重视实际生活中素材积累的意识,在写作的过程中多是以模仿的形式去创作,缺乏自己的真实情感,导致创作出来的文章太过形式化,毫无独特性。还有普遍的虚假作文、“造文”现象非常严重,作为缺少创新,文章缺少灵性。

图3 线圈与人体仿真模型
1.3.2人体结构仿真及结果 为衡量TET系统对人体产生的最大SAR值是否超出安全限制,使用Zhang等[15]完成的中国数字可视化人体图像构建高精度人体电磁计算模型,如图3(b)所示.此人体数据相较于欧美数据更贴近中国人体,构建的模型高度为170 cm,质量为65 kg.在有限元软件HFSS中将模型进行网格划分后,对发射线圈施加10 W正弦激励并分配辐射边界条件.
由于在实际实验过程中,发射线圈放置在正对人体腹部、距离人体5 mm处,所以仿真设计也放置于腹部外5 mm处.通过有限元分析重点研究了发射线圈附近人体组织的电磁能量吸收情况,并通过后处理获得了SAR分布及电场分布图.沿剖面线的SAR1g及SAR10g分布如图4(a)所示.其中:L为该点与剖面线原点的距离.人体模型接收到的SAR1g最大值为13.11 mW/kg,出现在距离皮肤表层4 mm处;SAR10g的走势与SAR1g基本相同,最大值为 4.4 mW/kg,且均随与发射线圈距离的增大而减小.仿真得到的模型全身平均SAR值为49.472 μW/kg,电场强度的最大值为 9.622 1 V/m,电场强度分布如图4(b)所示.
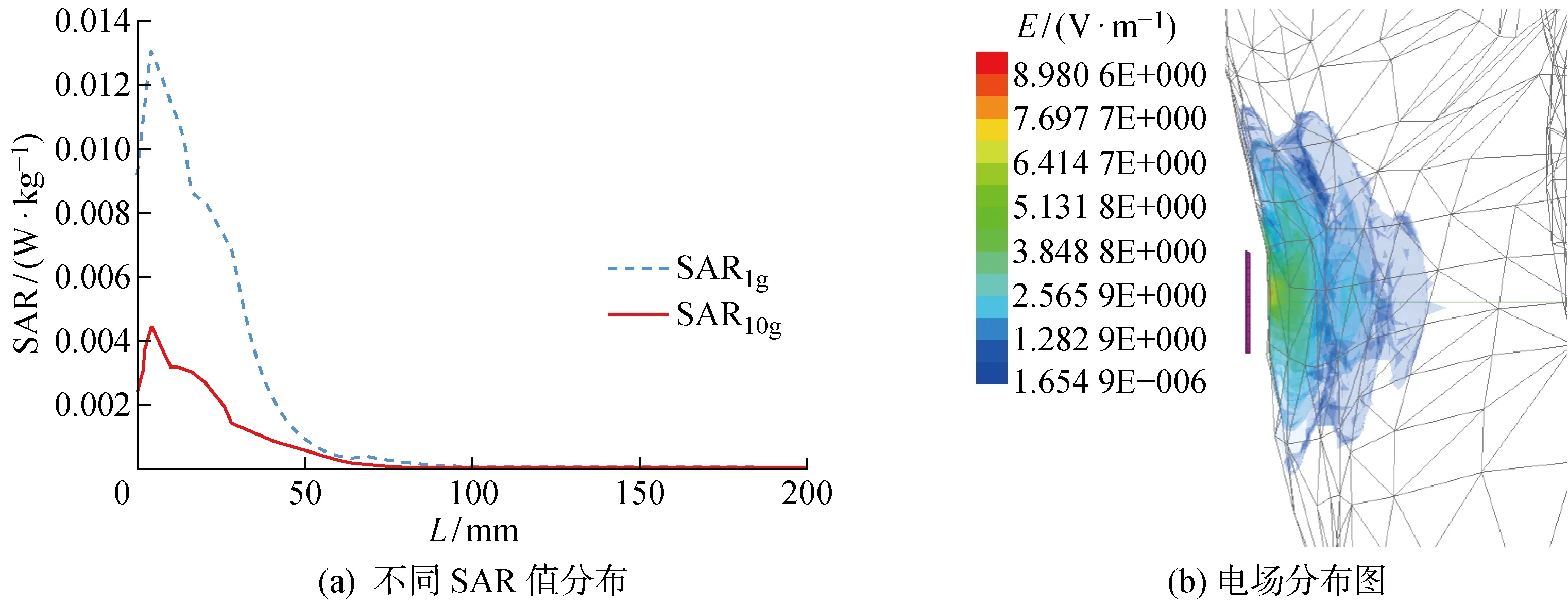
图4 仿真分析结果
1.4 分析与讨论
目前,国际通用的SAR安全标准有国际非电离辐射防护委员会(ICNIRP)制定的IEEE1528SAR-200x标准与美国国家标准学会制定的ANSI/IEEE标准.IEEE1528SAR-200x标准规定在非受控电磁环境下生物组织的SAR10g应低于2 W/kg.ANSI/IEEE标准则规定在任意连续的30 min内,生物组织的SAR1g应不大于1.6 W/kg[16].ICNIRP认为对于普通民众而言,110 kHz下的安全电场强度应不高于11.85 V/m[17].
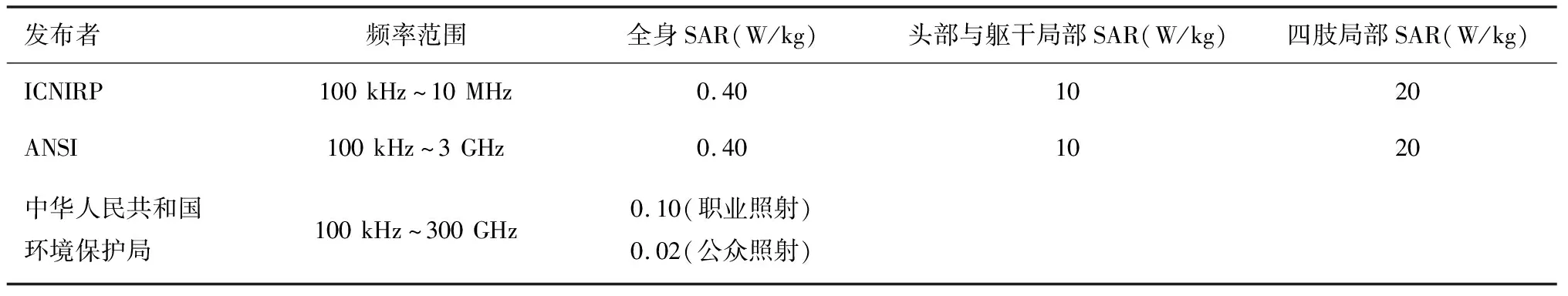
表2 不同标准对于SAR的不同要求
本实验所采用的TET系统最大SAR1g值为13.11 mW/kg,完全符合各项SAR值安全标准,产生的最大电场强度为 9.622 1 V/m,低于ICNIRP规定的安全标准的11.85 V/m.证明在此TET系统形成的电磁场中,人体受到的电磁辐射剂量完全符合国内外电磁辐射安全标准,此系统具有优异的生物电磁安全性.
2 TET系统温控安全性实验
2.1 温控安全性
生物安全性包括生物电磁安全性及温控安全性.过度的升温会改变细胞膜流动性和通透性,导致细胞质被破坏;抑制细胞内DNA、RNA 及蛋白质的合成和修复,导致细胞无法正常工作甚至凋亡.研究认为接收线圈的温度应低于42.5 ℃[18],正常人体腹腔温度接近肛温,为36.5~37.7 ℃,则按照最严格标准,接收线圈升温不得超过4.8 ℃.
2.2 充电实验
温控实验的TET系统与仿真规格一致,充电电池采用标称电压3.7 V,充电终止电压为4.2 V,放电终止电压为3.2 V,容量为 3 420 C的聚合物锂电池.为发射线圈配置耦合电容使谐振频率为110 kHz,调整发射电源的输出功率为10 W,在发射线圈与接收线圈之间垫入厚度为5 mm的猪皮及5 mm的塑料垫片作为中间介质,每隔3 min记录发射线圈下表面温度以及接收线圈上表面温度,同时记录下电池电压,3次充电实验的平均实验结果如图5所示.其中:t为充电时间;U为电池电压;ΔT为平均温度变化量.
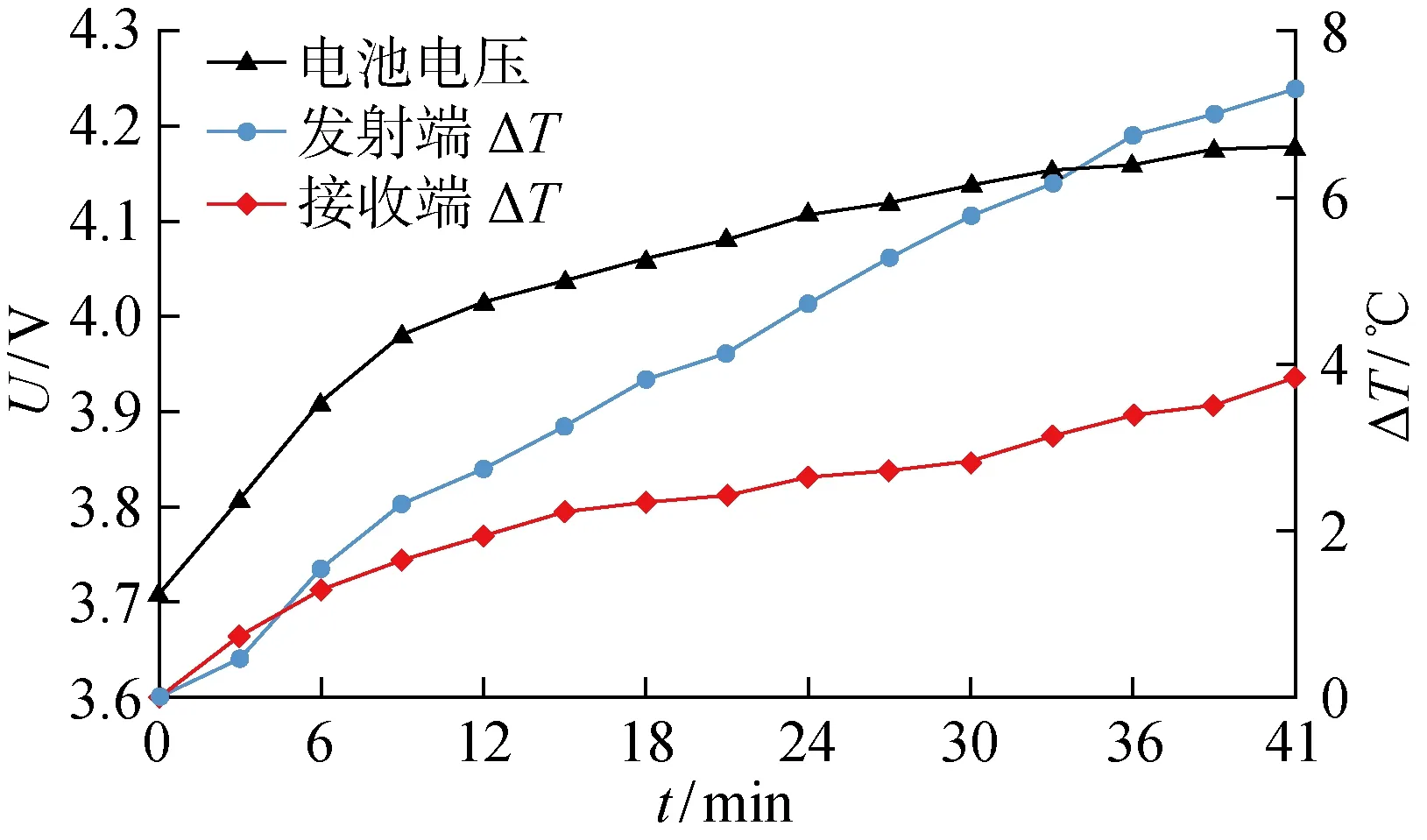
图5 体外充电实验结果
2.3 体外充电实验结果
实际上,接收线圈、电池以及电路芯片均封装在接收线圈外壳内,因此接收线圈表面平均温度变化量正是TET系统实际所造成的温度变化量.实验结果表明,TET系统工作过程中,两线圈温度均不断上升,经过30 min的高速充电,接收线圈表面温升仅2.81 ℃.在41 min后,接收线圈升温3.86 ℃,发射线圈升温7.32 ℃.因此,为保障TET系统在工作过程中的温控安全性,应对充电时长进行限制,且避免发射线圈直接接触人体皮肤.
3 活体实验
3.1 植入手术
对标号为1号与2号的两头健康巴马仔猪进行植入手术,手术由上海市浦东新区人民医院的医生实施.植入过程如图6所示.手术时,仔猪下腹开约8 cm切口,取直肠,将AAS主体机构套装在直肠末端;确认机构正常工作后,埋回直肠与机构;将接收线圈埋入仔猪腹股沟位置皮下近5 mm处,关腹;对仔猪肛门消毒,人为摧毁内外括约肌.两台手术分别耗时51和67 min,手术顺利,无任何并发症.
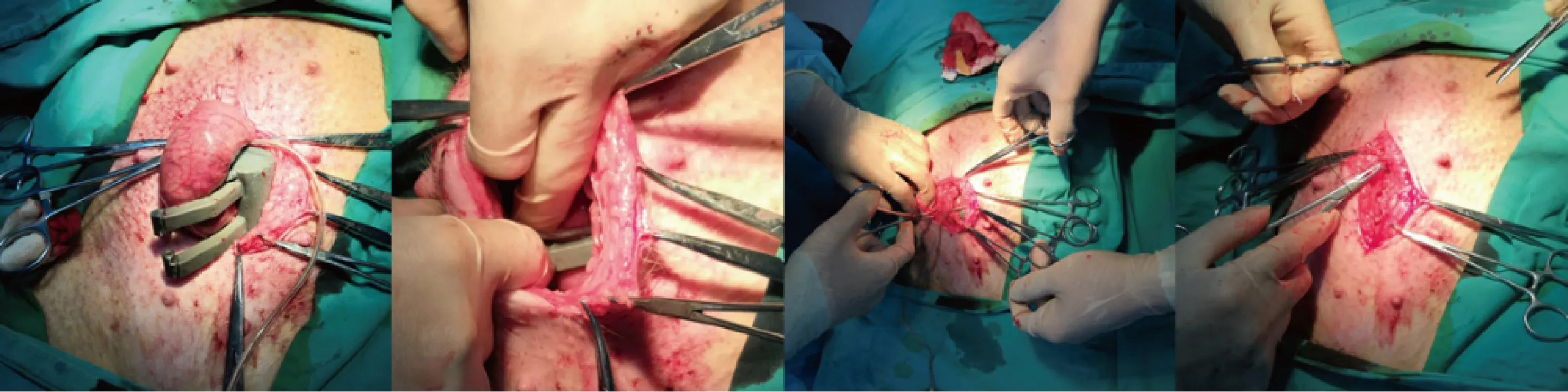
图6 植入过程
3.2 血常规检查
手术后两头仔猪均失去控便的能力,恢复情况均良好.在手术前及2周康复期后,均对两头仔猪的血样进行血常规检查,所测得的各项血液参数如表3所示.
植入后两仔猪的白细胞含量分别下降36%和42.46%,血小板含量分别下降35.5%和21.88%,其余指标与健康巴马仔猪无异.整个实验过程中并未对仔猪进行放射治疗,仔猪白细胞偏低为注射抗生素导致.康复期间为控制仔猪体重,一直严格控制仔猪饮食,导致仔猪存在营养不良、血小板含量偏低的情况.
3.3 活体温控实验
康复期结束后立即进行活体温控实验.当前TET系统供能时需要线圈间距离适中,对心耦合,以达到最佳充电效率.因此对仔猪进行麻醉,四腿固定、腹部朝上、垫上垫片,手动寻找对心位置进行充电实验,并通过接受线圈内置的温度传感器进行温度记录.
实验开始时室温为26.2 ℃,仔猪皮肤表面温度均为40.1 ℃.基于体外温控实验结论,充电时长控制为30 min,每隔3 min记录一次接收线圈温度,实验结果如图7所示.在30 min充电后,1号TET系统接收线圈升温最大值为3.12 ℃;2号TET系统接收线圈升温最大值为2.92 ℃,均低于4.8 ℃,证明TET系统在合理控制充电时长情况下具有良好温控安全性.

图7 活体实验充电数据
3.4 切片染色实验
在AAS系统植入7周以后,对仔猪进行解剖,解剖的过程中没有发现仔猪组织出现热诱导组织学损伤,因此主刀医生做出TET系统温控安全的判断.仔猪增生平均厚度为1.72 mm,相较于前一代尼龙材料的2.84 mm减小了39.44%.切取接收线圈附近的组织进行病理检查,包括苏木精-伊红(HE)染色与Masson三色染色,两种染色结果如图8所示.由图8可以知道,HE染色中组织呈白色坚韧块状,细胞浆难以着色,细胞核可见大量验证细胞浸润;Masson染色可见大量胶原纤维着色,少见弹力纤维着色;说明植入处增生为皮下胶原纤维组织,没有出现感染.与表面为尼龙12材料的接收线圈病理检查结果对比,PEEK材料周围的增生更加细小致密,与正常未植入的组织相似,展现了此系统优异的生物安全性.

图8 巴马仔猪的切片染色实验结果
3.5 活体实验结果
活体实验验证了TET系统的温控安全性与生物相容性.对两头仔猪分别进行30 min快速充电产生的温升分别为3.12 ℃和2.92 ℃,较体外实验稍有增加,但均低于4.8 ℃的安全限制.血常规检查表明,TET系统的植入对仔猪并未造成病理性改变.切片染色实验表明,TET系统表面的增生主要为细小致密的皮下胶原纤维组织,证明此TET系统的生物相容性良好.
4 结语
本文基于人体模型仿真与实验相结合的研究方法,对AAS系统的TET模块的生物安全性与相容性进行相关研究.最终结果证明,AAS系统所使用的TET模块具有良好的生物安全性与相容性,其产生的电磁辐射量远低于国际标准;供能过程温升低于安全阈值;系统植入对周围组织无显著影响.研究验证了TET模块的安全性,为后续AAS系统进行人体实验提供了强有力的理论与实验支撑.此方法不仅能够用于AAS系统的研究,还可用于其他存在电磁辐射的医用植入设备中.
目前系统仍存在一些问题:需控制充电时长、操作依赖人工、受仔猪挣扎影响大等.因此,后续研究将进一步强化TET系统温控方面的能力,提升供能效率,增大供能范围.

