快速心律失常脉冲电场不可逆电穿孔消融治疗研究进展
【作 者】赵志宏,陈永刚,宁忠平,陈新华
1 上海健康医学院附属周浦医院 心血管内科,上海市,201318
2 杭州睿笛生物科技有限公司,杭州市,310003
3 浙江省脉冲电场技术医学转化实验室,杭州市,310003
0 引言
快速心律失常的根治性治疗,为消融损伤阻断心脏内异常电传导通路。消融治疗能量来源包括:射频消融、冷冻消融、微波消融、激光消融、直流电能产生的脉冲电场(pulsed electrical field,PEF)消融方式。现主流是为射频消融,消融导管头端的电极释放低电压高频(30 kHz~1.5 MHz)射频电能,在消融导管头端与局部心肌内膜之间电能转化为热能,达到一定温度(40~60 ℃)后,使特定的局部心肌细胞脱水、变性、坏死,自律性和传导性能均发生改变,从而使心律失常得以根治。微秒脉冲直流电产生高能PEF瞬时释放能量至心肌细胞膜,产生不可逆电穿孔(irreversible electroporation,IRE),细胞内容物泄漏,破坏细胞内环境稳态,导致细胞死亡,减轻炎症反应,脉冲电场作为非致热能量来源[1]。随着材料学领域的进步,PEF作为心律失常消融能量来源的消融方式,IRE消融导管的不同目标设计在快速进行之中,近期在基础研究及临床应用方面取得了很大进展。
1 PEF消融机制
PEF消融通过直流电脉冲发生器释放单相或双相PEF,特点是高电场强度(kV/cm电场强度级别)、快脉冲频率和短脉冲宽度(μs及ns级别),在正、负电极间形成局部高电压差,极短时间内释放高电场的非热能量,选择性作用于心肌区域,即刻实现心肌细胞质膜不可逆电穿孔,造成透壁损伤,细胞内容物泄露,导致心肌细胞死亡,远期纤维疤痕形成和射频消融效果基本相同[2]。通过PEF消融的导管也称为IRE消融导管。快速心律失常消融的IRE消融导管,通过高电压输出,产生单相或双相矩形脉冲波形,将一定数量的电脉冲按序列输出实现消融目的。PEF消融有如下优点:①PEF消融强电场区域内的心肌组织均是有效消融位点,可精准调控,降低对消融电极贴靠压力的要求;②PEF消融为非热能组织消融,在消融过程中不会破坏组织支架结构,不受血流“热沉效应”的影响,不会产生消融局部血栓。具有相对较宽的治疗能量窗口[3];③PEF消融具有组织电阻特异性,心肌细胞的PEF消融损伤阈值400 V/cm,血管、神经、食道等组织器官损伤阈值超过其4倍,且心肌细胞对PEF消融的敏感性远高于其他各种细胞类型;这意味着适宜的PEF消融电压优先损伤心肌,而对血管、神经、食道等邻近组织影响极小且不会损伤。
2 快速心律失常治疗的PEF消融导管及临床应用进展
2.1 心内IRE消融导管
2.1.1 双电极IRE消融导管
直径为5 F(1 F=1/3 mm)的Blazer PEF双电极消融导管,在心内放置位置,如图1所示。一根电极导管放置在冠状窦内,另一根为消融电极放置在心室内拟消融位置同时也作为标测电极记录心室内浦肯野(Purkinje)电位,二个电极距离在3 cm内,PEF消融时两个消融导管电极之间形成高电压电场[4]。NanoKnife消融系统(AngioDynamics,Queensbury,NY)参数中输出电压为750~2 500 V(最小电场强度 250~833 V/cm),频率为1 MHz,释放10个脉冲,每次脉冲时间为90 μs,心电图QRS有效不应期内同步PEF消融。Langendorff离体心脏灌注的体外犬心脏模型,750~1 000 V可有效消融浦肯野电位,2 000~ 2 500 V可有效消融His电位[5]。输出电压1 050~1 125 V下释放10个脉冲,或750 V下释放20或30个脉冲消融,有效消融全麻下猪Purkinje电位,组织学分析确认靶向浦肯野纤维损伤,PEF靶向消融可以在对心肌细胞损伤最小的情况下完成浦肯野纤维消融。
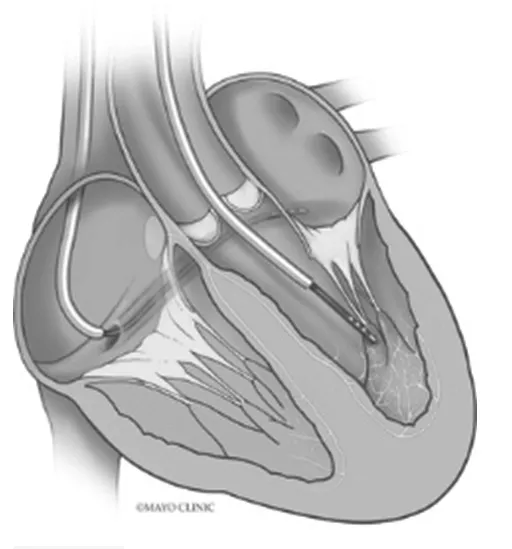
图1 PEF消融导管标测并消融Purkinje电位Fig.1 Location of the ablation catheter used for pulsed electric field delivery
2.1.2 篮状IRE消融导管
直径为12 F的12个电极平均分布于4个独立的半环形结构上的篮状IRE消融导管。消融电极从鞘管内伸出,展开时为电极纵向排列的篮状,头端与心肌组织接触范围最大化,见图2[6]。通过心内超声、透视及三维标测系统在心室内消融导管定位消融。消融电极展开精确定位及保证稳定性,所有电极都可产生IRE消融电场,消融过程通过定制的PEF消融仪2 200 V输出电压放电消融。猪心室消融1个月后组织学分析,平均损伤直径为6.5±1.7 mm,宽度为22.6±4.1 mm,最大深度和宽度为9.4 mm和28.6 mm,在PEF消融部位,纤维组织均匀地替代了肌细胞,纤维组织内及周围保留神经束和血管。损伤周围有狭窄的肌细胞溶解区,没有覆盖的血栓。该IRE消融导管优点是稳定性高,消融范围较大,缺点是一些特殊精细部位不能抵达。图3为改良的FARAFLEX篮状IRE消融导管,并联的每个样条远端增加了一个电极,可行心电标测及起搏标测,称为头端聚焦IRE消融导管(Farapulse Inc,Menlo Park,CA),推送展开前为椭圆形头端,进一步推送展开为最大直径17 mm的半球形,便于心腔内及欧氏脊病灶位置行点状及线性消融[7]。

图2 篮状IRE消融导管Fig.2 Basket pose of the IRE catheter

图3 改良后的头端聚篮状IRE消融导管Fig.3 12-F deflectable focal basket pose of the IRE ablation catheter
2.2 心外膜IRE环状阵列电极消融导管
IRE环状阵列电极消融导管用于心外膜PEF消融。图4为头端8个长度为2 mm、直径为12 mm的环形阵列电极,直径为7 F的IRE消融导管[8]。对猪经剑突下行心包穿刺后通过鞘管送达心包内,冠脉造影定位,消融导管置于冠脉位置之上予以单相除颤器(Lifepak 9;Physio-Control Inc,Redmond,WA)同步200 J放电产生的瞬时高能PEF,持续时间为4~10 ms,在心肌上形成连续的环状损伤。病理结果显示冠状动脉的内膜没有明显增生,冠脉无明显狭窄改变。该电极经皮穿刺送抵心外膜,简单方便,提示经皮心外膜PEF消融的可行性。

图4 直头环状IRE消融导管Fig.4 Circular electroporation ablation catheter
2.3 环肺静脉IRE消融导管
房颤消融治疗目前最有效的主流方法为环肺静脉电隔离。这方面,PEF消融的IRE消融导管设计和应用做了很多开创性的尝试,并有系列相关临床研究,取得优异效果[9]。
2.3.1 环形阵列电极IRE消融导管
环形阵列电极IRE消融导管类似环肺静脉标测电极Lasso电极。图5为7 F头端与连接杆成90o,折角直径为18 mm~20 mm,包含10个长度为2 mm消融电极构成IRE消融导管。单相除颤器200 J放电消融在心肌上形成连续的环状损伤,消融深度足以造成肺静脉电隔离[10]。在全麻猪模型下,该IRE消融导管放置在肺静脉主干内5~10 mm,10个环形阵列电极同步给予200 J放电,NavX 三维标测系统进行术中及术后3个月后评估,经PFA的肺静脉开口未见狭窄,与之对照的经射频消融的肺静脉开口发生狭窄[11]。该消融导管设计参照了Lasso电极,优点是很容易到达肺静脉,缺点是20 mm的直径对肺静脉来说偏小,难以完全贴靠肺静脉。该IRE消融导管未进入临床应用研究。

图5 环状IRE消融导管Fig.5 Circular IRE ablation catheter
2.3.2 9极中空环形阵列电极IRE消融导管
该消融导管初始设计用于射频消融的肺静脉电隔离[12],该消融导管也可当作标测电极用。随后用作双相PEF的IRE消融导管进行研究[13],为9 F头端与连接杆成90o,折角有20°倾角的中空直径25 mm的9个环形阵列电极的IRE消融导管(PVAC GOLD;Medtronic Inc,Minneapolis,MN),其中空结构便于指引导丝抵达肺静脉指导调整消融导管位置,见图6。
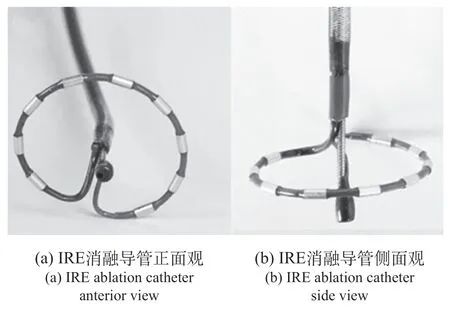
图6 PVAC Gold 相位排列IRE消融导管Fig.6 PVAC Gold array ablation catheter
专利[14]详细叙述了该系统的工作原理、系统构架、参数设置和实验测试结果。奇数1、3、5、7、9电极作为正极,偶数2、4、6、8电极作为负极,心脏同步放电进行PEF消融。模型猪的右上肺静脉及左、右心耳口行双相PEF消融,输出电压为500 V,脉宽100 μs,脉冲间停顿为200 ms,每组60次脉冲,共有5个脉冲组,每个脉冲序列的持续时间为36 ms,R波门控放电时间约为10 s。2周后心肌组织学检查发现PEF消融导致心肌细胞死亡、纤维化,且不会损伤PEF有效消融电场以外的心肌组织;PEF消融纤维化更均匀,心外膜脂肪炎症更轻,病变内血管重塑更少[15]。该IRE消融导管获得美国食品药品监督管理局(Food and Drug Administration,FDA)批准正在进行多中心、前瞻性、非随机对照临床试验——PULSED AF研究(NCT04198701),评估其安全性和有效性。2020年第41届美国心律学会(American Heart Rhythm Society,AHRS)年会发布了该研究14例房颤患者PEF消融结果:研究对象中包括左肺静脉共干和右中肺静脉等复杂病例,所有病例术中均完成肺静脉电隔离,左心房电压标测证实广泛连续肺静脉前庭有效损伤,每支肺静脉消融(7.4±3.5)次;监测食道温度显示术中无改变。30 d内未见手术消融相关的严重不良事件发生,所有病例将随访12个月,观察中远期疗效[9]。
2.3.3 环肺静脉篮状花瓣状IRE消融导管
直径12 F的20个电极均匀分布于5个独立的半环形结构上的篮状花瓣状20个电极IRE Farawave消融导管(Farapulse,Inc,Menlo Park,CA)。消融电极从鞘管内伸出,用抵达肺静脉内的指引导丝指引,控制消融导管展开程度应对不同直径的肺静脉消融,未完全展开时为电极纵向排列的篮状,完全展开时为电极横向排列的花瓣状,最大展开直径分别为30 mm或35 mm[7],见图7。联合头端聚焦IRE消融导管右房房扑三尖瓣峡部消融的25例持续性房颤PersAFOne 临床研究(NCT04170621)中围术期及术后随诊结果表明,该导管安全有效。

图7 篮状花瓣状20电极IRE消融导管Fig.7 Basket-Flower pose of multispline IRE catheter
该消融导管所有电极均能进行PEF消融,最远端的电极可作为起搏和标测电极应用。该IRE消融导管在模型猪上的临床前研究证实:1 800 V双相PEF行肺静脉电隔离不会引起骨骼肌收缩震颤,因此不需要肌松剂;双相PEF消融效果优于单相PEF消融和射频消融[16]。该IRE消融导管优点为消融过程中不需要电极充分接触肺静脉口及前庭壁,也不需要冷盐水灌注,无食管损伤风险[17]。随后采用该IRE消融导管完成15例房颤患者肺静脉电隔离,优势为手术时间短,无急性肺静脉狭窄、肺静脉电位传导恢复、膈神经损伤等并发症,对心肌组织特异性损伤、快速有效肺静脉电隔离,缺点是平均每支肺静脉消融3.26次[18]。随后发表的81例PEF消融病例研究一年内的随诊结果,双相PEF消融时仅予以丙泊酚镇静,双相PEF电压为1 800~2 000 V,放电时间≤3 min,整个手术时间为(92.2±27.4)min。术中双相PEF一次肺静脉电隔离成功率为43%,3次及以上消融达100%,优于单相PEF消融;3个月后重复三维标测证实肺静脉电隔离达到100%成功;无中风、膈神经损伤、肺静脉狭窄和食道损伤等不良事件;1年内维持窦性心律的Kaplan-Meier值为87.4%。该IRE消融导管环肺静脉消融长期安全性良好[19]。该IRE消融导管优点是经皮鞘管内输送到达肺静脉口方便,可根据肺静脉大小而部分或完全展开,缺点是数次消融完成环肺静脉前庭消融。
2.3.4 Lattice-tip导管消融系统
Lattice-tip导管消融系统包括射频消融系统、Sphere-9 IRE消融导管(Affera,Inc,Watertown,MA)、集成标测系统、消融仪和灌注泵。图8为Lattice-tip消融导管,直径7.5 F,经输送鞘管送至左心房后,头端自膨胀展开,形成半径为4.5 mm,材质为具有形状记忆功能的镍钛诺非磁性合金的网格球状消融电极,表面均匀分布着9个直径为0.9 mm的微型电极(含热电偶,也可温控射频消融),球状消融电极内有灌注微孔及中心参考电极[20-21]。射频消融及双相PEF消融可同步转换完成房颤消融过程,也可做为三维标测电极应用,指导消融电极精准定位。Lattice-tip消融导管系统的消融方式为逐点消融,输出电流调到28 A时,环球型电极中心约8 mm半径范围电场强度超过400 V/cm,以此该消融电极非直接接触肺静脉口—前庭部位下即可完成消融[22]。对76例房颤患者按术者经验选择射频消融和PEF消融模式交替应用,行肺静脉电隔离及二、三尖瓣峡部和左心房顶部线性消融,完成房颤标准消融路径,围术期无器械相关并发症,PEF消融组无食道热损伤效应;该研究目标仅限于房颤围术期安全有效性评估,临床疗效需更长随访时间[23]。
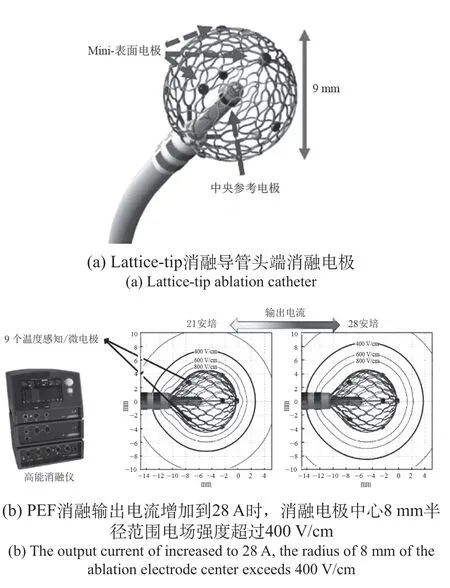
图8 Lattice-tip消融导管及PEF消融Fig.8 Lattice-tip ablation catheter and PEF ablation
2.3.5 球囊电极IRE消融导管
IRE球囊消融导管,球囊表面近端及远端表面喷涂形成条带状电极,作为正负极,同时能进行三维标测和记录局部肺静脉电位[24],见图9。全麻下犬肺静脉PEF消融,造影剂充盈的球囊消融导管抵达左房肺静脉,电极测量局部肺静脉电位,评估电位振幅改变,球囊远、近端二个作为消融电极,输出电压为1 000~2 000 V,脉冲时间为100 μs,按10、100、200个不同脉冲序列消融,实现完全肺静脉电隔离,随访7~44 d,不会导致肺静脉狭窄,也不影响肺、食道、膈神经及左房后壁神经节神经丛。
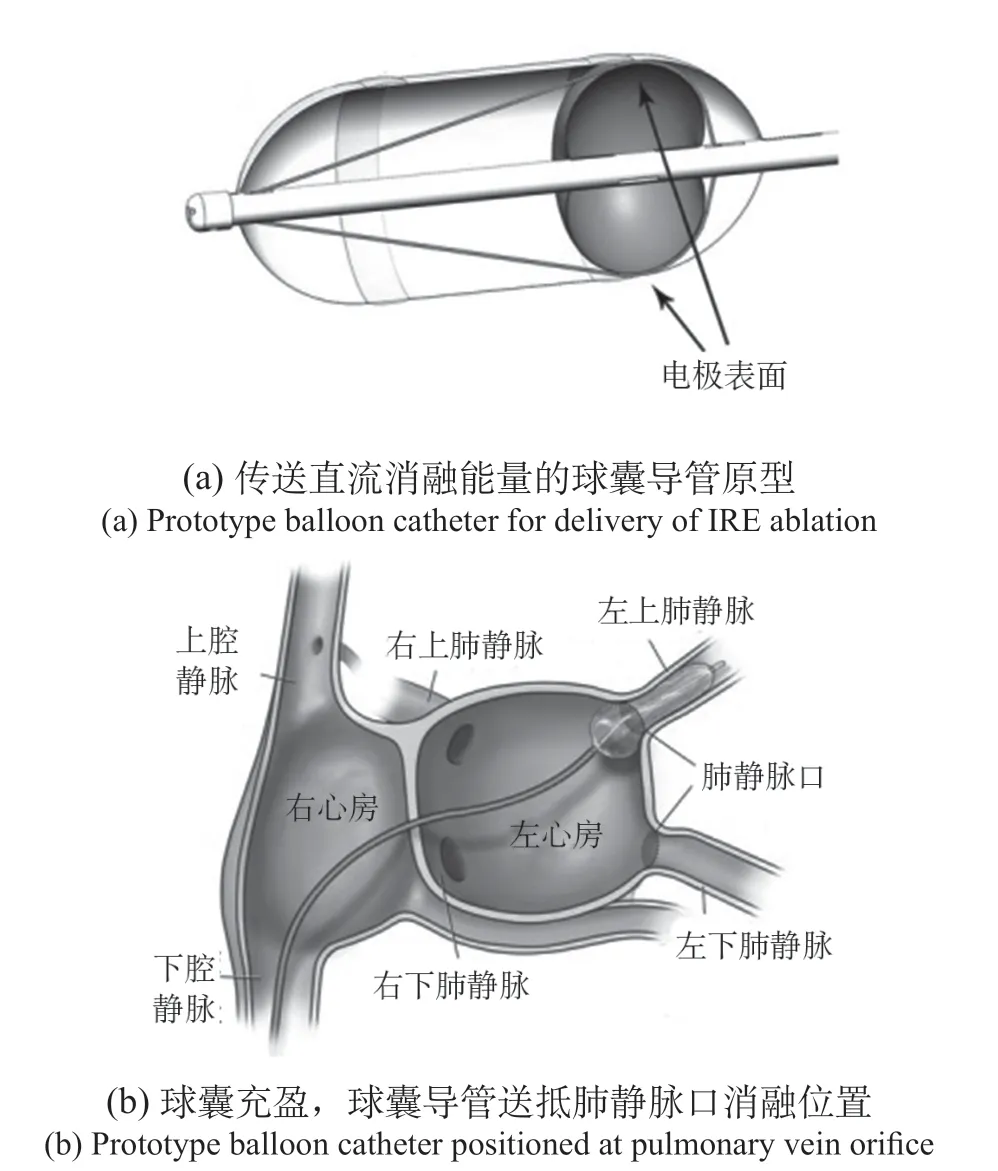
图9 IRE球囊消融导管及肺静脉口消融Fig.9 Prototype balloon catheter and intended ablation location
3 总结
综上,PEF具有高能非热的优势,是极具潜力的临床应用研究方向,推动心律失常消融的技术迭代,消融导管的产品革新,值得进一步深入研究,国内相关研究正在快速推进[25-26],有望进入临床研究。

