常规康复训练及体外冲击波联合治疗脑卒中后上肢痉挛的效果观察
保 婧,蔡 艳,赵智龙,李少敏
脑卒中在我国属常见病、高发病,同时具有高致残率,据统计约有30%以上的患者伴有肢体痉挛障碍,严重影响了患者的运动功能康复[1]。痉挛的持续不缓解加重了肢体的疼痛,从而减弱了自主运动和不随意运动,随即出现关节挛缩畸形,故脑卒中后上肢痉挛严重制约了患者肢体功能的恢复,从而影响了患者日常生活能力(ADL)[2]。当前治疗上肢痉挛,包括应用抗痉挛药物、推拿、物理因子疗法、康复工程技术或手术等方法[3],针对这些方法现仍存有一定的问题,当患者口服抗痉挛药物后会感到全身乏力等不适,康复训练会受到影响,而肉毒素价格高昂且需要反复注射。现已有研究显示,体外冲击波治疗脑卒中后肌肉痉挛有效,而体外冲击波联合常规康复治疗脑卒中后上肢痉挛的临床研究鲜有报道。因此,本文通过针对脑卒中后上肢痉挛患者给予单独常规康复训练以及常规康复训练联合体外冲击波治疗,进一步观察治疗后的疗效,现将结果报告如下。
1 资料与方法
1.1 一般资料:选取2018年1月-2019年12月在银川市第一人民医院接诊,确诊脑卒中后上肢痉挛患者60例,其中男37例,女23例。通过随机数字表法分组,其中观察组30例,男18例,女12例,年龄43~77岁,平均年龄(61±9)岁,脑卒中后上肢痉挛病程11~132 d。对照组30例,男19例,女11例,年龄42~78岁,平均年龄(60±8)岁,脑卒中后上肢痉挛病程12~85 d。2组患者资料比较,差异无统计学意义(P>0.05),具有对比性。
1.2 入选和排除标准:入选标准,即:①第4次全国脑血管病学术会议制定的脑卒中诊断标准;②脑卒中后出现功能障碍且存在上肢痉挛;③病情稳定,能耐受本研究所用治疗方法;④告知病情后患者及其家属均签署知情同意书。排除标准:①病情不稳定且合并严重的心血管疾病;②合并有严重意识障碍及认知功能障碍;③上肢肌肉近期注射过肉毒素。
1.3 治疗方法:2组患者均给予常规康复治疗,包括体位转移训练、主动及被动运动训练,5次/周,治疗1个月为1个周期。观察组患者联合应用体外冲击波治疗仪(MASTEPPLUS MP200)治疗,冲击波探头沿上肢三角肌、冈上肌、冈下肌、肱三头肌、桡侧腕长伸、桡侧腕短伸肌、尺侧腕伸肌、指伸肌、小指伸肌、旋后肌起始点,冲击次数共约2 000次,压力控制1.0~1.2 bar,频率可据患者耐受情况在10~12 Hz间调整。每3 d治疗1次,治疗10次即1个月为1个周期。
1.4 观察指标:在治疗前后1个月,对2组分别进行上肢肢体运动功能的评定,采用改良的Ashworth痉挛量表对肢体痉挛评分[4]依据感受被动活动关节时的阻力,进行分级评估,将痉挛的严重程度从O级表达至Ⅳ级。0级表示肌张力正常,Ⅰ级、Ⅰ+级、Ⅱ级、Ⅲ级肌张力说明痉挛程度逐渐加重,Ⅳ级表示肢体被动活动困难为重度痉挛。采用简式Fugl-Meyer评分法[5]对上肢功能进行评分,66分即为满分,分值大小与上肢运动功能呈正比。

2 结果
2.1 Ashworth上肢肌张力评级:观察组30例中治疗前上肢肌张力Ⅰ级2例、Ⅰ+级7例、Ⅱ级16例、Ⅲ级5例,治疗后0级2例、Ⅰ级7例、Ⅰ+级16例、Ⅱ级5例、Ⅲ级0例;对照组30例中治疗前上肢肌张力:Ⅰ级2例、Ⅰ+级5例、Ⅱ级15例、Ⅲ级8例,治疗后0级1例、Ⅰ级3例、Ⅰ+级13例、Ⅱ级11例、Ⅲ级2例。治疗前2组比较,差异无统计学意义(Z=0.877,P>0.05);治疗1个月后,差异有统计学意义(Z=2.402,P<0.05),见表1。
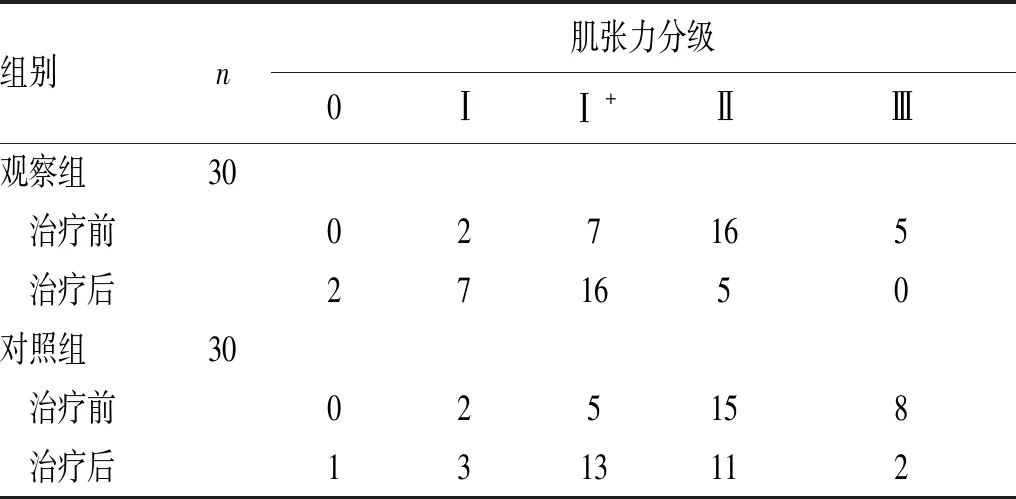
表1 2组患者治疗前后改良Ashworth 痉挛量表评分比较
2.2 Fugl-Meyer运动功能评分:2组患者Fugl-Meyer运动功能评分,观察组由治疗前的31.87分提高到42.47分,治疗前2组比较差异无统计学意义(P>0.05);治疗1个月后,差异有统计学意义(P<0.05),见表2。

表2 2组患者治疗前后运动功能评分比较(分,
3 讨论
脑卒中后出现肌肉痉挛是上运动神经元受损的临床表现之一,上运动神经元受损后,神经元支配的肌肉及肌群原有相互协调、制约受到了破坏,从而使肌张力显著升高,导致脑卒中后患者的偏瘫侧肢体为持续痉挛状态。肌肉持续性痉挛会并发疼痛、关节挛缩,进一步抑制了肌肉的正常运动,对患者肢体功能恢复有着严重影响,增加了康复训练的难度[6]。
据相关报道体外冲击波可改善肌痉挛,体外冲击波疗法有非侵入、安全、有效等特点,几纳秒内形成压力急剧变化产生了冲击波,具备超强的压应力和张应力,可迅速穿透液体和软组织等弹性组织。本研究结果显示,观察组患者进行冲击波联合常规康复治疗脑卒中后上肢痉挛有效率较对照组明显提高。体外冲击波缓解肌痉挛的机制现仍不明确,MARIOTTO等[7]研究认为,体外冲击波是通过诱导一氧化氮(NO)的合成来发挥作用。体外冲击波通过促使血管内皮细胞合成NO,神经肌肉接头的形成有NO参与,体外冲击波增加了神经肌肉接头的形成,故可调节神经传递和突触可塑性,从而促进中枢神经系统的生理功能。CIAMPA[8]等通过研究冲击波针对于小鼠的神经胶质细胞C6,发现冲击波增加了细胞质一氧化氮合成酶的活性,充分表明冲击波能增快神经元NO生成的速度。NO参与了周围神经系统的神经肌肉接头形成,还具有重要的神经传导、记忆和神经突触可塑性的生理功能。
体外冲击波是一种高能机械波,具有机械、空化等作用,其中机械作用能够改善机体组织间的微循环和高密度组织的裂解,松解发生粘连的软组织和结缔组织,从而使肌张力降低,减轻痉挛;即改变脑卒中高渗肌肉的流变特性,改善结缔组织的刚度,促进软组织松解从而减轻了痉挛。冲击波通过对高张力痉挛肌肉的振动刺激,可能促使乙酰胆碱受体快速变性,类似使用神经肌肉传递抑制剂,使脊髓α-运动神经元的兴奋性降低,从而减弱了痉挛肌肉兴奋性。
郭佳宝[12]等对上肢的指屈肌、腕屈肌、肱二头肌进行Meta分析,研究表明体外冲击波对脑卒中后上肢痉挛缓解的即刻及短期效应比对照组更具优势,提示体外冲击波能改善卒中后上肢痉挛,并且治疗结果在短期内可以持续。
体外冲击波治疗脑卒中后上肢痉挛有一定的理论基础,在2019年版中国骨肌疾病体外冲击波疗法指南已明确提出,但是现阶段临床工作中体外冲击波治疗脑卒中后上肢痉挛应用未得到充分的普及。本研究表明,常规康复训练联合体外冲击波可安全有效地改善脑卒中后上肢痉挛,从而改善患者的上肢功能。
但本研究存在一定局限性,患者样本量有限,未明确体外冲击波治疗脑卒中后上肢痉挛的最佳治疗次数、强度及应用部位,还需进一步研究证实。另外,冲击波对脑卒中后上肢痉挛的机制并不明确。总之,冲击波可以作为脑卒中后上肢痉挛治疗的一个有用的替代方案,与现有的治疗方法相比,它具有非侵入性和较少的副作用。本研究结果显示,常规康复训练联合体外冲击波治疗脑卒中后上肢痉挛效果较好,在临床可以推广应用。

