贝伐珠单抗联合化疗在晚期直肠癌治疗中的应用及对患者生存期限的影响研究
马 丹
(项城市第一人民医院 周口 466300)
直肠癌为消化道恶性肿瘤的常见类型,临床上针对晚期直肠癌患者以化疗为主的治疗方案已达成临床共识,但单纯化疗治疗下患者远期生存率仍不理想。近年来,随着肿瘤医学发展进程的不断推进及分子生物学靶向治疗技术的快速研发,分子靶向治疗成为晚期肿瘤患者治疗体系的重要组成部分[1]。贝伐珠单抗为抗肿瘤血管生成的大分子单克隆抗体,本研究以我院收治的90例晚期直肠癌患者为研究对象,探讨贝伐珠单抗的作用机理及临床应用价值。
1 资料与方法
1.1 一般资料
根据本研究方向定向选择我院收治的90例晚期直肠癌为研究对象,病例收集时间2017年1月~2018年12月。病例纳入标准:(1)符合临床诊断者;(2)预计生存周期>3个月者;(3)直肠癌初治者,且自愿签署知情同意书者。病例排除标准:(1)合并其他恶性肿瘤疾病,或已发生肿瘤转移者;(2)对本研究所采用的治疗方案有禁忌症者;(3)有化疗、放疗治疗史者。在予以患者编号、随机分组后,将其分为C组(对照组)和Y组(研究组)各45例,对C组、Y组患者的一般资料进行比较,结果呈一致性(P>0.05),见表1。

表1 C组和Y组患者一般资料分布
1.2 方法
1.2.1C组
C组45例患者实施单纯的化疗治疗。治疗第1d,奥沙利铂静脉滴注(剂量85 mg/m2,时长2h),亚叶酸钙静脉滴注(剂量400 mg/m2,时长2h),氟尿嘧啶静脉推注(剂量400 mg/m2);同时,氟尿嘧啶静脉滴注(剂量2400 mg/m2,时长46~48 h);治疗第2d,氟尿嘧啶静脉滴注(剂量2400 mg/m2,时长46~48 h)。每2周为1个治疗周期,疗程6个周期。
1.2.2Y组
Y组45例患者在C组的基础上联合应用贝伐珠单抗。即于患者每次化疗治疗后将10mg/kg的贝伐珠单抗加入0.9%氯化钠注射液(250ml)中予以患者静脉滴注,每2周为1个治疗周期,疗程6个周期。
1.3 观察指标
1.3.1临床干预效果
于6个周期治疗完成后,根据《肿瘤化疗疗效判定基本标准》分别评价并统计C组和Y组患者CR、PR、SD、PD例数。并计算肿瘤稳定率=(CR+PR+SD)/总例数×100%,肿瘤改善率=(CR+PR)/总例数×100%[2]。
1.3.2生存期限
分别对C组和Y组患者予以两年的随访观察,分别统计肿瘤无进展存期限(PFS)、总生存期(OS),并统计2年内生存率。
1.4 统计学方法
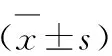
2 结果
2.1 临床干预效果
Y组患者肿瘤干预稳定率为82.22%,高于C组的62.22%(P<0.05);Y组患者肿瘤干预改善率为64.44%,高于C组的44.44%(P<0.05),见表2。

表2 C组和Y组患者肿瘤干预客观效果比较[n(%)]
2.2 生存期限
Y组患者PFS、OS均较C组长(P<0.05),且Y组患者2年内生存率为82.50%,高于C组的56.10%(P<0.05),见表3。

表3 C组和Y组患者生存期限比较
3 讨论
肿瘤血管生成在肿瘤疾病发生、发展病理机制中发挥了重要的参与作用,国内外前沿文献研究报道显示,肿瘤增长过程中若无新生血管形成,肿瘤组织将保持休眠或退化状态[3]。 而临床研究报道证实,血管内皮生长因子(VEGF)的表达水平与肿瘤血管生成密切相关[4]。因此,采用有效的药物下调肿瘤患者VEGF的表达水平,抑制肿瘤血管的生成成为肿瘤疾病靶向治疗的重要靶点。贝伐珠单抗是首个获批用于癌症治疗的抗血管生成药物,其主要作用靶点为VEGF,即通过对VEGF活性的抑制而阻止肿瘤新生血管形成,抑制肿瘤细胞增殖,进而发挥抗肿瘤效果[5~6]。本研究中,C组、Y组患者分别行单纯的化疗治疗、化疗联合贝伐珠单抗治疗,研究结果显示:Y组患者肿瘤干预稳定率为82.22%,高于C组的62.22%(P<0.05);Y组患者肿瘤干预改善率为64.44%,高于C组的44.44%(P<0.05);同时,Y组患者PFS、OS均较C组长(P<0.05),且Y组患者2年内生存率为82.50%,高于C组的56.10%(P<0.05)。即在化疗治疗的基础上联合应用贝伐珠单抗靶向治疗可有效提高晚期直肠癌的治疗效果,延长患者生存期限,值得临床推广应用。

