等离子体催化甲烷干重整实验研究
李嘉卿,徐 彬,王文博,谢建军,*,阴秀丽,吴创之,肖进彬
(1.中国科学院广州能源研究所 中国科学院可再生能源重点实验室 广东省新能源和可再生能源重点实验室,广东 广州 510640;2.中国科学院大学,北京 100049;3.河南省科学院,河南 郑州 450002)
生物质气化技术是前景较好的生物质能利用技术之一[1]。生物质气化可通过改变气化剂种类、调整反应条件获得不同气体组成与热值的气化气用于燃烧或合成化学品[2]。表1 列出了生物质经富氧-水蒸气气化后得到的气体组成。由表1 可知,合成气中含有4%-17% CH4及22%-38% CO2,这两种气体在化工合成过程中无法直接利用。通过CH4干重整过程可将CH4、CO2转化为H2和CO,不但可调变合成气组成,还可提高生物质资源利用效率。

表1 生物质富氧-水蒸气气化的产气组成Table 1 Gas composition of biomass oxygen-steam gasification
甲烷干重整(Dry Reforming of Methane,DRM)是一种发展较为成熟,可满足工业化产氢要求的技术,但其通常在高温及催化剂条件下进行[6]。莫文龙等[7]考察了制备方法(溶液燃烧法、等体积浸渍法、胶体磨循环浸渍法和水热-沉积法)对DRM 反应中Ni/γ-Al2O3催化剂性能的影响。分别使用四种方法制备的催化剂在反应温度为800 ℃,CH4流 量60 mL/min,CO2/CH4物质的量比为1 时进行实验,结果表明,四种催化剂均可达到70%以上的CH4转化率,但随着反应的进行,由于Ni原子烧结,几种催化剂活性呈现不同程度的降低。Akri 等[8]制备Ni 纳米颗粒催化剂和Ni 单原子催化剂,并进行200-800 ℃温度DRM,结果显示,当温度低于450 ℃时,CH4并未进行反应;在750 ℃反应温度下使用两种催化剂时CH4转化率均可达到79%。但此温度下Ni 单原子催化剂容易因烧结和聚集而失活,Ni 纳米颗粒催化剂比Ni 单原子催化剂具有更好的抗烧结性,但反应后发生大量碳沉积现象。方琼等[9]通过共沉淀法制备添加La 助剂的NiMgAl 水滑石催化剂,在750 ℃下进行CH4干重整,考察了La 助剂对重整过程催化剂活性和抗积炭性能的影响,实验发现当La 负载量为1.0%时,在反应温度750 ℃下取得最大CH4和CO2转化率,分别为89.05%和94.53%;反应10 h后,催化剂表面积炭16%,而没有La 负载时催化剂表面积炭21%。以上可知,DRM 反应需要在较高温度下进行,并且反应过程中催化剂易因烧结和积炭而失活;在催化剂中添加助剂La,可以大幅抑制催化剂的积炭现象。
低温等离子体技术具有反应条件温和及抗积炭的优势[10]。结合低温等离子体和催化剂组成的等离子体耦合催化剂反应体系,近年来在DRM 方向得到了广泛研究[11]。Alawi 等[12]在微波反应器中进行放电功率700-1200 W,CO2/CH4物质的量比2.0-5.0,N2和Ar 气氛等不同条件下的DRM 实验,实验表明,Ar 气氛下可获得更高的H2和CO选择性及收率,在放电功率700 W,CO2/CH4物质的量比2.0 时,CH4及CO2转化率分别为79.35%与44.82%的。滑动弧放电由于其紧凑的结构、高能量效率、快速启动和响应等特点[13]而得到广泛应用。Zhu 等[14]利用改进的滑动弧放电装置与Ni/γ-Al2O3催化剂耦合进行CO2/CH4物质的量比为7∶3的DRM 实验,研究了Ni 含量对等离子体甲烷干重整过程性能的影响,发现当Ni 的质量分数为10%时,最大CH4转化率可达58.5%,H2收率为20.7%。表2 中列出了介质阻挡放电(Dielectric Barrier Discharge,DBD)等离子体DRM 相关研究进展。Andersen 等[15]比较了DBD 中不同填充材料对DRM的影响,反应过程中控制放电功率45 W,气体流量25 mL/min,发现使用Pt/Al2O3催化剂时CH4转化率32.5%,H2选择性38%,能量效率0.205 mmol/kJ。等离子体耦合催化剂可以在较低的温度下实现DRM 反应,兼具高CH4转化率和高H2选择性,在DRM 方面具有明显优势。但合成气中除了CH4和CO2,还有H2、CO、N2、H2O 等气体,却鲜有研究报道DRM 过程中这些气体组分对催化剂性能和放电状态的影响。

表2 介质阻挡放电甲烷干重整Table 2 Research progress of dry reforming of methane by dielectric barrier discharge
基于此,本文借助CH4干重整常用的La-Ni/γ-Al2O3催化剂和DBD 进行耦合,构建以La-Ni/γ-Al2O3为床层填充材料的DBD 反应体系,研究了反应温度、CH4/CO2物质的量比、合成气主要气体组成(N2、H2、CO、H2O)等因素对DRM 过程CH4、CO2转化率及产物中H2、CO 选择性的影响。并讨论了等离子体催化DRM 过程的能量效率及重整反应后催化剂表面积炭情况,研究结果可望为生物质气化合成化工品的工艺开发提供基础数据和参考依据。
1 实验部分
1.1 实验装置与方法
实验装置主要由等离子体发生装置、配气系统、DBD 反应器及产物分析系统组成,详见图1。等离子体发生装置由低温等离子体电源(CTP-2000K,南京苏曼)、调压器(TDCG2-1,南京苏曼)与数字示波器(DPO 2024B,Tektronix)组成。配气系统由三个质量流量计(MFC-D07 系列,七星)和水蒸气产生/混合单元组成。
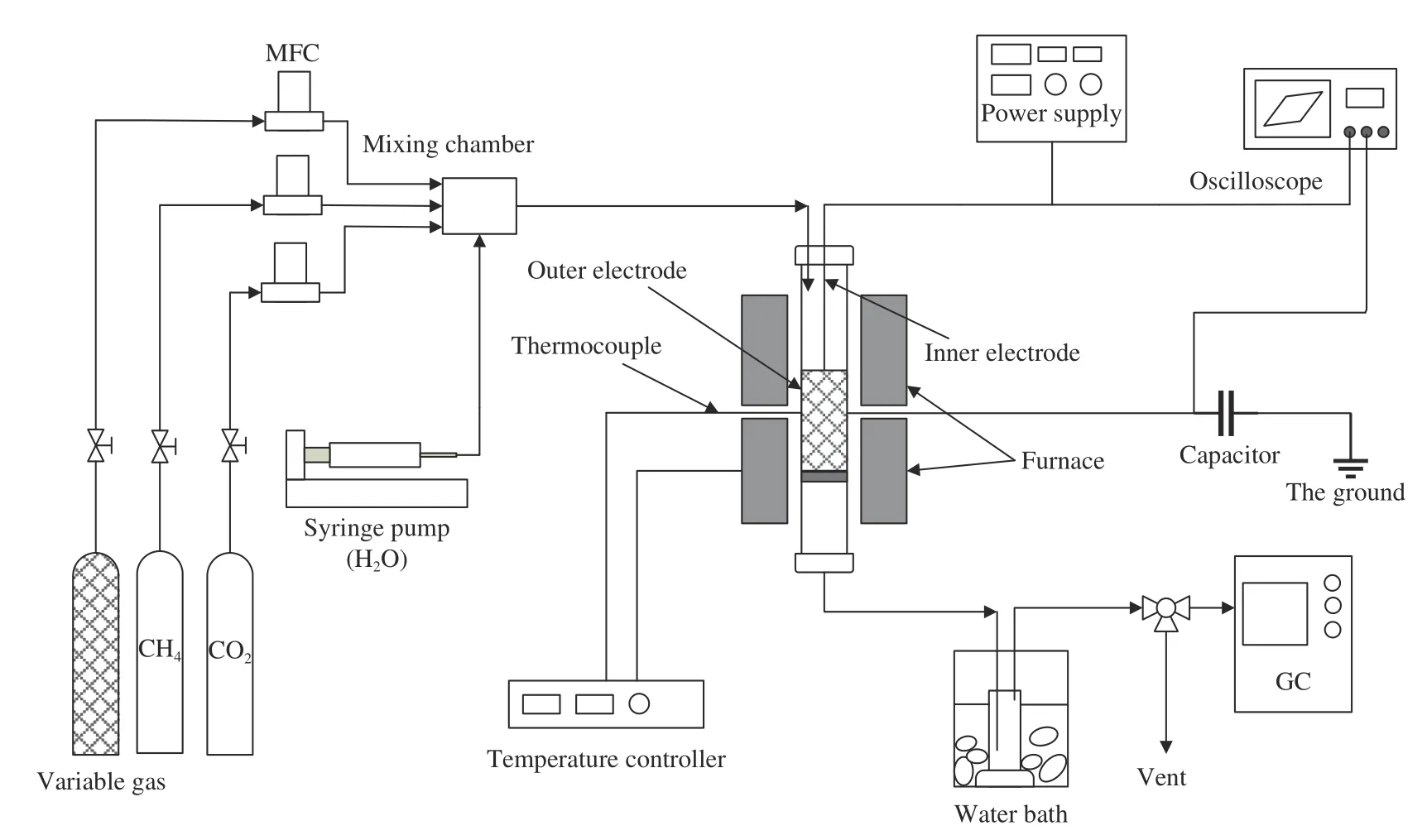
图1 实验装置示意图Figure 1 Schematic diagram of the experimental device
DBD 反应器包含一根外径25 mm,内径20 mm的刚玉管,其轴心处放置一根外径16 mm 的不锈钢棒作为高压电极,在不锈钢棒底部固定一片外径20 mm 的不锈钢网用作反应床支撑,刚玉管外侧包裹一层长100 mm 的不锈钢网作为接地电极,相应放电间隙为2 mm,放电空间为11.3 mL。
实验过程中,CH4、CO2、N2、H2、CO 通过质量流量计控制其流量,H2O 则通过微量注射泵(LSP01-1A,Longer)输送至预热炉,所有气体在进入DBD反应器前通过气体混合单元充分混合。DBD 反应器置于带有程序升温的管式加热炉,反应器高压电极与等离子体发生电源相连,接地电极通过0.1 μF的电容与大地相连。放电电信号通过数字示波器记录,放电功率采用Lissajous 图形法计算。反应尾气使用气体采样袋收集,收集前后分别使用皂膜流量计进行流量测定,取三次测量结果的平均值。收集后由气相色谱仪(490 Micro GC,Agilent)检测CH4、CO2、H2、CO、C2H6、C3H8的浓度。
由于等离子体放电会使反应器局部发热,实验前通过预实验摸索电加热与等离子体放电的温升情况,在实验过程中通过温度控制单元实时监控以保证反应过程中反应器达指定温度。
1.2 催化剂的制备与表征
采用等体积浸渍法分别制备La-Ni/γ-Al2O3和Ni/γ-Al2O3催化剂。将一定质量的Ni(NO3)2·6H2O和La(NO3)2·6H2O 溶于去离子水中,取一定量的γ-Al2O3(160-200 目,500 ℃烘干预处理)加入硝酸盐混合溶液中,使载体被充分浸润。超声震荡30 min,室温静置24 h,然后在105 ℃下烘干。最后将样品置于600 ℃下空气气氛中焙烧4 h。
将制备好的催化剂样品加入一定量的硅溶胶黏结剂、田菁粉、硅铝酸钠和水,混合拌匀后真空练泥、陈腐、挤压成型并切条。自然晾干后再105 ℃烘箱中干燥,最后置于500 ℃马弗炉中焙烧。使用前将催化剂粉碎筛分至20-40 目,将催化剂样品置于H2气流中500 ℃还原2 h 即可得到实验所需的La-Ni/γ-Al2O3和Ni/γ-Al2O3。
分别使用全自动化学吸附仪(Chemstrat,Quantachrome)进行催化剂的程序升温还原(H2-TPR)测试,使用X 射线衍射仪(X’pert Pro MPD,PANalytical)对催化剂的晶体结构进行分析,使用全自动独立多站比表面积和孔隙度分析仪(Quadrasorb SI-MP-10,Quantachrome)进行催化剂比表面积和孔结构测试。
使用波长色散X 射线荧光光谱仪(AXIOS mAX petro,PANalytical V.B.)对成型催化剂中有效成分进行测定,为了保证数据准确性,对两样品进行三次测量并取平均值作为最终数据。使用X 射线光电子能谱仪(ESCALAB 250Xi,Thermo Fisher Scientific)分析La 改性对Ni 电子结构的影响。
为进一步了解等离子体协同催化DRM 过程中H2、CO、N2加入对催化剂积炭的影响,将反应后催化剂的积炭形貌与数量进行了热重(SDT650,Waters)分析、拉曼光谱分析(LabRAM HR800,HORIBA JOBIN YVON)及元素分析(Vario EL cube,Elementa)。
1.3 计算公式
CH4、CO2转化率由下式计算:


式中,P为放电功率,单位W,[CH4]、[CO2]是反应转化的CH4、CO2的摩尔流量,单位是mmol/s。
2 结果与讨论
2.1 催化剂的表征
由于催化剂成型使用了约30%黏结剂,通过XRF 测得成型Ni/γ-Al2O3催化剂中Ni 的实际含量为8.72%,成型La-Ni/γ-Al2O3催化剂中Ni 的实际含量为8.31%,La 的实际含量为1.43%。图2 为Ni/γ-Al2O3、La-Ni/γ-Al2O3催化剂的H2-TPR 谱 图。由图2 可知,两种催化剂的还原峰峰温和峰型存在较大差异。Ni/γ-Al2O3主要有两个还原峰,还原温度为550、780 ℃,分别对应NiO 与镍铝尖晶石NiAl2O4的还原峰。La-Ni/γ-Al2O3具有三个还原峰,400 和550 ℃的还原峰分别归属于自由态和立方态NiO 的还原[20],另外780 ℃镍铝尖晶石NiAl2O4还原峰则与Ni/γ-Al2O3相似。与Ni/γ-Al2O3的TPR谱图相比,La-Ni/γ-Al2O3中NiO还原峰的峰型更为弥散,说明La 的添加削弱了活性组分Ni 与载体γ-Al2O3之间的相互作用,La-Ni/γ-Al2O3上可还原的NiO 物种更多[21]。

图2 不同催化剂的H2-TPR 谱图Figure 2 H2-TPR spectra of different catalysts
图3 给出了Ni/γ-Al2O3和La-Ni/γ-Al2O3催化剂Ni 2p3/2区域的XPS 光谱谱图。两种催化剂在851.4、856.5 和862.4 eV 处出现峰值。851.4 和856.5 eV 处的特征峰分别归因于NiO 和NiAl 尖晶石[22,23],862.4 eV 处峰值归因于851.4 和856.5 eV 处特征峰的卫星峰。La-Ni/γ-Al2O3催化剂较Ni/γ-Al2O3在851.4 eV 处出现约0.4 eV 的偏移。一般认为,单个组分的化学键能通常受其周围化学环境的影响,峰移是可能是La 对Ni 的修饰作用。表3 给出了Ni 2p峰面积定量分析结果。由表3 可知,La-Ni/γ-Al2O3中NiO 的含量(851.4 eV 处特征峰)大于Ni/γ-Al2O3中的含量。这与H2-TPR 分析结果一致。
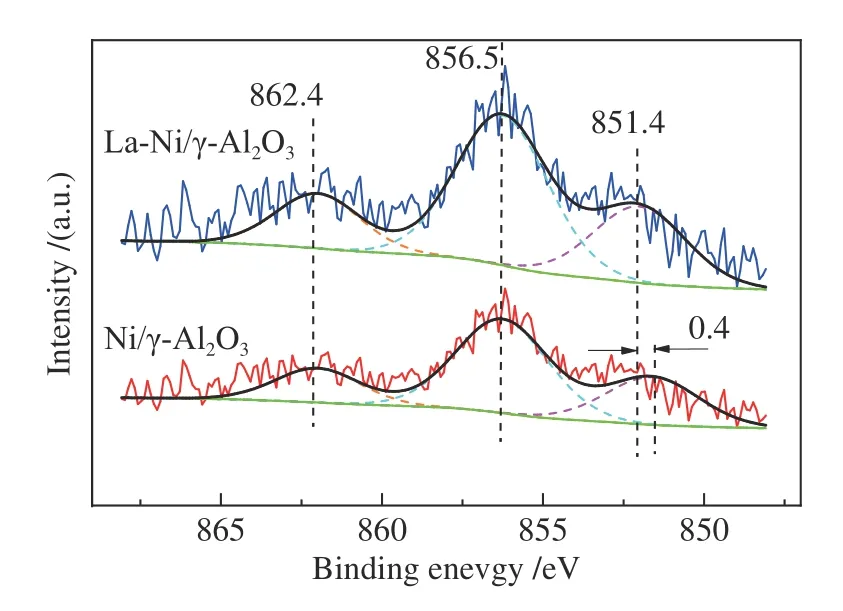
图3 Ni/γ-Al2O3 和La-Ni/γ-Al2O3 催化剂Ni 2p3/2区域的XPS 光谱谱图Figure 3 XPS spectra of Ni 2p3/2 region of the Ni/γ-Al2O3 and La-Ni/γ-Al2O3 catalyst
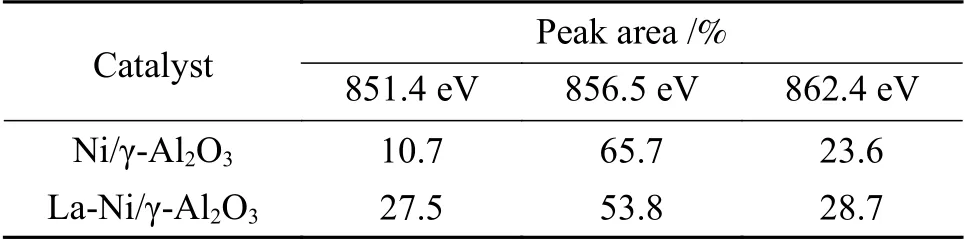
表3 Ni/γ-Al2O3 和La-Ni/γ-Al2O3 催化剂XPS 光谱Ni 2p3/2 区峰面积Table 3 Peak areas of Ni 2p3/2 region in XPS spectra of Ni/γ-Al2O3 and La Ni/γ-Al2O3 catalysts
表4 为本文所用两种催化剂及载体的比表面积和孔容积比较。γ-Al2O3和Ni/γ-Al2O3具有相似的比表面积,但是负载Ni 后孔容积从0.281 cm3/g降低到0.259 cm3/g。负载La、Ni 后催化剂比表面积和孔容积均有较大幅度的降低,分别降低到97.99 cm2/g 和0.243 cm3/g。这可能是La、Ni 颗粒填充在γ-Al2O3孔道中,堵塞了部分孔道,导致比表面积和孔容积的减小。

表4 不同催化剂的比表面积和孔容积Table 4 Specific surface area and pore volume of different catalysts
图4 为γ-Al2O3、还原前后Ni/γ-Al2O3催化剂及还原后La-Ni/γ-Al2O3催化剂的XRD 谱图。图中19.88°、37.46°、39.42°、45.66°和67.16°处的衍射峰属于γ-Al2O3[22]。与γ-Al2O3的XRD 谱图相比,NiO/γ-Al2O3的XRD 谱图中在2θ为37.34°、43.26°和62.96°处可见属于NiO 的衍射峰。催化剂还原后,属于NiO 的衍射峰消失,在44.41°和52.09°处新出现属于金属Ni 的衍射峰。La-Ni/γ-Al2O3的XRD 谱 图与Ni/γ-Al2O3的衍射峰出峰情况一致,并未发现属于La 的衍射峰,这有可能是其在Al2O3表面呈单层分布导致[24]。

图4 γ-Al2O3、Ni/γ-Al2O3 及La-Ni/γ-Al2O3催化剂的XRD 谱图Figure 4 XRD spectra of γ-Al2O3,Ni/γ-Al2O3 and La-Ni/γ-Al2O3 catalysts
2.2 反应床层填充材料的影响
为考察La-Ni/γ-Al2O3与DBD 等离子体协同效果,在DBD 反应床层中填充不同材料进行DRM实 验,量 取5 mL 2%La-10%Ni/γ-Al2O3、10%Ni/γ-Al2O3催化剂,分别与8 mL 石英砂充分混合作为DBD 填充物进行CH4干重整实验,并将其与单独等离子体(填充石英砂)、单独填充催化剂(无等离子体)在相同反应条件下的干重整实验结果进行比较。实验温度为450 ℃,放电功率55 W,进气中仅含CH4与CO2两种气体,物质的量比为1.0,总气体流量为300 mL/min,后续实验若无特别说明,均在此工况下进行,实验结果见图5。
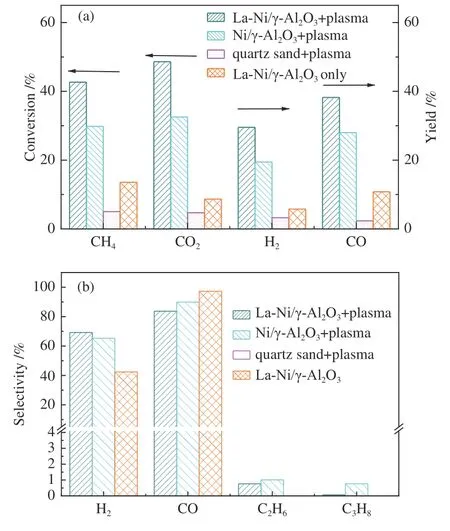
图5 催化剂对CH4 干重整的影响Figure 5 Effect of catalyst on (a) the conversion rate of CH4,CO2 and the yield of H2 and CO (b) the selectivity of H2,CO,C2H6 and C3H8
由图5 可知,当填充Ni/γ-Al2O3催化剂时,CH4转化率达29.75%,H2收率和选择性分别为19.46%和65.29%;填充La-Ni/γ-Al2O3催化剂时,相同条件下CH4转化率提高至44.06%,且副产物C2H6和C3H8选择性也降低到1%以下,仅为0.78%和0.07%。这表明La 元素的添加可促进CH4转化,并提高H2、CO 选择性。
仅填充La-Ni/γ-Al2O3的热催化重整实验中CH4和CO2转化率为14.06%和9.27%。填充石英砂的等离子CH4重整实验中CH4和CO2转化率仅为5.05% 和4.74%,并且副产物C2H6和C3H8的选择性高达17.30% 和3.77%。表明等离子体催化DRM 可有效提高CH4转化率。
文献[11,14,15,25]讨论了催化剂在等离子体DRM中的作用,在等离子体中引入催化剂一方面可能会影响放电类型和加速电子分布,从而影响激发态的反应性等离子体物种的形成[13]。与热催化反应相比,通过等离子体可生成高能电子、激发态分子、自由基和离子,这些物质可活化反应物分子,从而显著提高CH4及CO2转化率。另一方面,等离子体放电过程中产生的高温粒子可使催化剂表面升温,从而影响催化剂表面吸附物种的脱附;另外,等离子体的存在还可能影响催化剂表面的电子分布,CO2在过渡金属表面的化学吸附和解离是由电子控制的,并且过程中需要形成CO2-的阴离子CO2前驱体[14],等离子体通过影响催化剂表面电子分布的方式影响CO2-的形成,进而影响催化剂活性。所以与纯等离子体干重整相比,等离子体和催化剂之间的协同作用较大程度地提高了产物的选择性,有效地抑制了副产物的生成。
2.3 反应温度的影响
本节考察了反应温度对CH4、CO2转化率,H2、CO 收率及能量效率SEC 的影响,实验过程中反应温度为350-550 ℃,实验结果见图6。
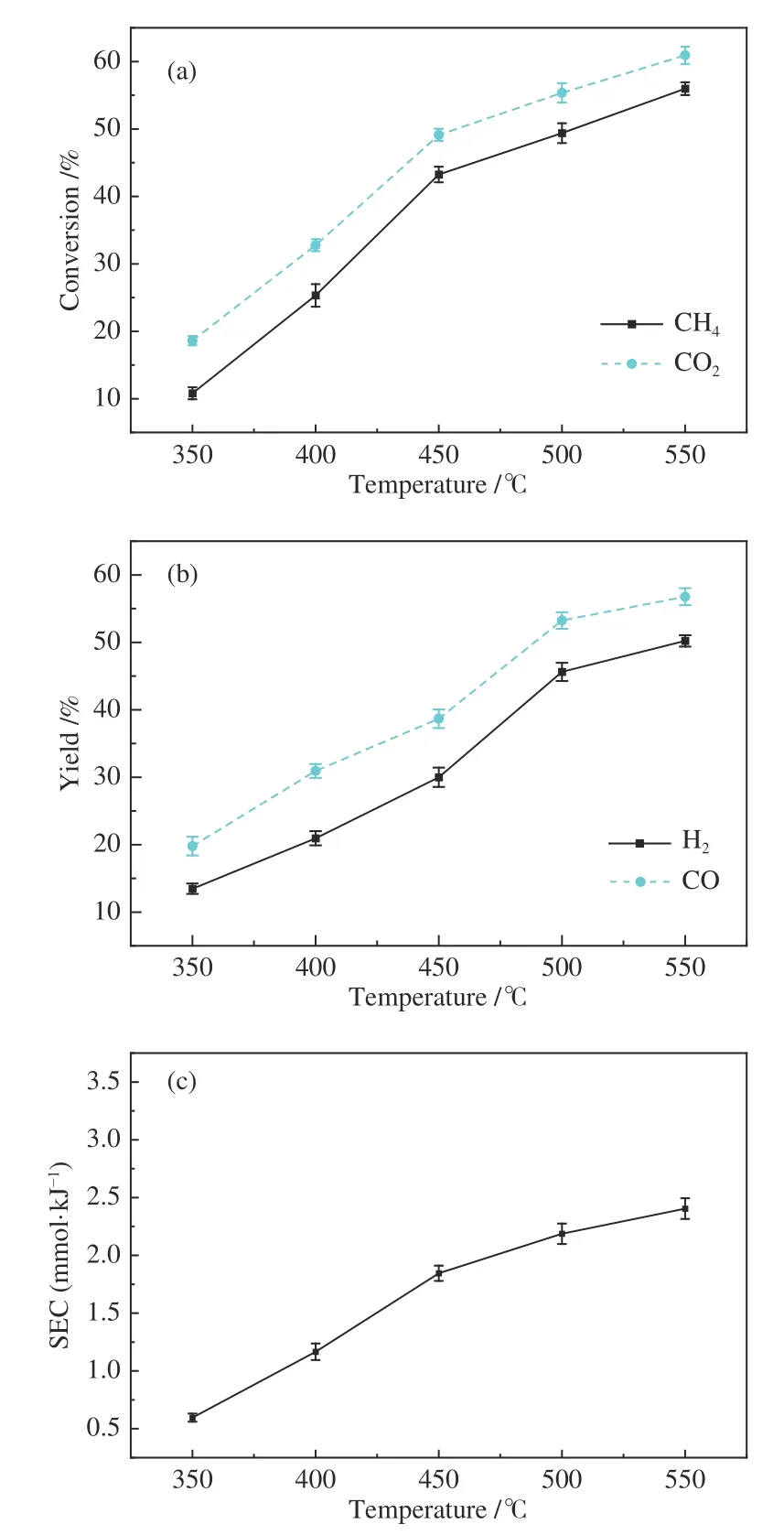
图6 温度对CH4 干重整的影响Figure 6 Influence of temperature on (a) the conversion rate of CH4 and CO2,(b) the yield of H2 and CO,(c) energy efficiency
由图6 可知,CH4、CO2转化率随温度升高而增大,且CO2转化率均高于CH4转化率。当温度从350 ℃升高到550 ℃时,CH4、CO2转化率分别从11.44% 和19.01% 增加到56.63% 和60.82%,同时H2、CO 收率从12.92%和19.79%增加到49.80%和56.64%。CH4转化率随床层温度升高而增加[11,26-28],温度从350 ℃升高到550 ℃过程中,CH4、CO2转化的能量效率从0.62 mmol/kJ 增加到2.34 mmol/kJ,提高反应温度可促进等离子体催化DRM 的能量效率。与热催化DRM[7-9]相比,本研究采用等离子体耦合催化剂方式进行DRM 反应,当温度为450 ℃时,CH4转化率达到43.24%。
DRM 反应是一个吸热反应(式(9)),因此,升高温度有利于反应进行。反应过程中CO2的转化率高于CH4,可能发生了逆水煤气变换反应(式10)。
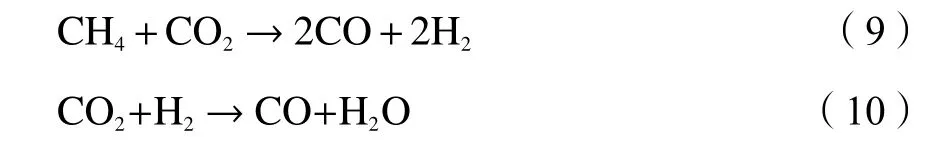
2.4 CO2/CH4 物质的量比的影响
通常合成气中CO2含量比CH4多(表1),为此本节考察了CO2/CH4物质的量比(1-5)对CH4、CO2转化率,H2、CO 及副产物收率和能量效率SEC的影响。实验过程中改变CO2/CH4物质的量比时进料总流量300 mL/min 保持不变,实验结果见图7。
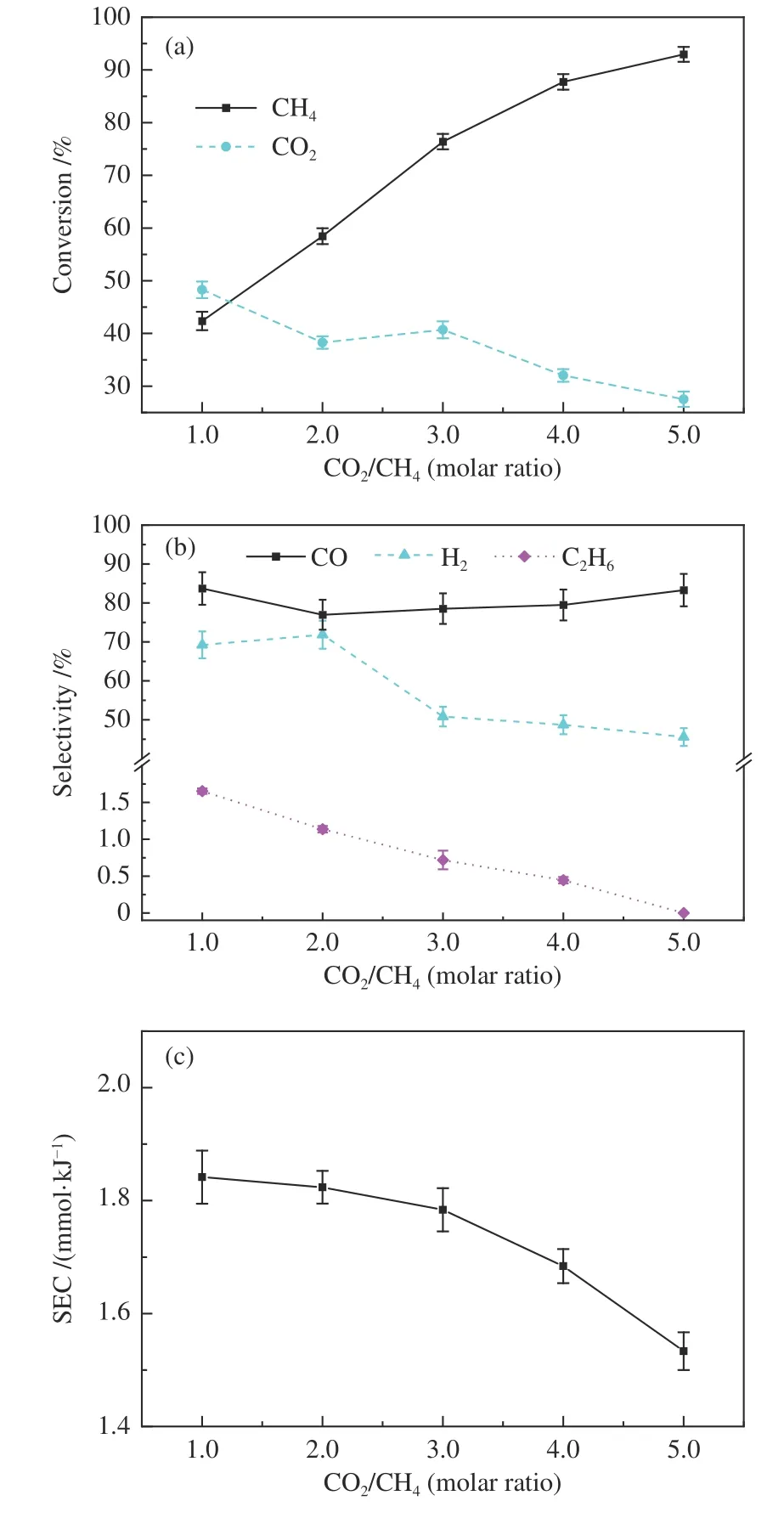
图7 CO2/CH4 物质的量比对CH4 干重整的影响Figure 7 Effect of CO2/CH4 molar ratio on (a) the conversion rate of CH4 and CO2 (b) the selectivity H2,CO and C2H6(c) the energy efficiency
如图7(a)所示,将CO2/CH4物质的量比从1.0提高到5.0,CH4转化率从41.57% 升高到92.82%;CO2转化率则呈下降趋势,当CO2/CH4物质的量比为5.0 时,CO2转化率仅为26.86%。值得注意的是,由于逆水煤气变换反应(式10),H2和CO2反应生成H2O 和CO,所以当CO2/CH4物质的量比为1.0 时,CO2转化率为49.74%,略高于CH4转化率;但CO2含量升高,有利于CH4向H2和CO 转化,CH4转化率迅速提高并且超过CO2转化率。前人文献[12,29,30]也发现,当CO2量超过DRM 反应的化学计量比时,发生CO2的转化率降低而CH4转化率增加的现象。图7(b)为H2、CO 及主要副产物C2H6选择性随CO2/CH4物质的量比变化的趋势。由图7(b)可见,H2的选择性随CO2/CH4的增加而呈现下降趋势,从69.22%下降到45.59%;而CO 选择性受物质的量比影响不大,稳定在80% 附近。实验过程中仅在CO2/CH4物质的量比为1.0 时检测到副产物C3H8(选择性为1.65%),当CO2/CH4物质的量比 ≥ 2.0 时,C3H8选择性为0。等离子体催化DRM 反应的能量效率受CO2/CH4物质的量比影响较明显,当CO2/CH4物质的量比从1.0 提高到5.0 时,能 量效 率SEC 从1.84 mmol/kJ下 降到1.53 mmol/kJ。与Alawi 等[12]在微波反应器进行实验相比,本研究在较低的放电功率下取得了与其相似的效果,尤其是在高CO2/CH4物质的量比时,CH4转化率均达到90% 以上;与Andersen 等[15]在DBD 反应器中进行的DRM 相比,能量效率明显大于其实验结果0.205 mmol/kJ。
在DBD 等离子体反应器中,高能电子与反应物分子的非弹性碰撞有利于激发态物种的形成,相同放电功率与气体流量下,提高CO2/CH4物质的量比有利于CO2产生过量激发态的高能粒子,这些高能粒子通过与CH4分子碰撞、结合促进了CH4的转化。同时由于CH4转化产生大量氢气,CO2产生的高能粒子可能会进一步与H2发生逆水煤气反应[29],表现为当CO2/CH4物质的量比从2.0 变化到3.0 时H2选择性迅速下降。
2.5 N2/H2/CO 添加的影响
本节分别考察了合成气中主要组分N2、H2、CO对CH4、CO2转化率,H2、CO 收率及SEC 的影响,实验过程中CO2/CH4物质的量比保持1.0 不变,并仅添加某一种组分至CO2与CH4的混合气中,N2、H2、CO 的体积分数变化为0-30%。图8为CH4、CO2转化率随N2、H2、CO 体积分数变化的趋势,图9 给出的是H2、CO 选择性及能量效率的变化。由图8 可见,随进气中N2含量增加,CH4、CO2转化率均有不同程度的提高。当N2体积分数从0 增加到30%时,CH4转化率从39.01%增加到45.76%,CO2转化率从39.64% 增加到54.49%。在DBD 反应器中,反应体系中的分子、电子吸收能量转变为激发态分子、原子、离子、自由基等,N2在等离子体体系中会产生激发态N2*[13,31],N ≡N叁键键能(946 kJ/mol)大 于C-H 键键能(414 kJ/mol)和CO2中 C=O双键键能(803 kJ/mol),N2分子结构较稳定,因此,在反应体系中会通过分子间碰撞的方式将能量传递给更容易发生反应的CH4和CO2分子,促进CH4和CO2分子化学键断裂,有利于反应进行。
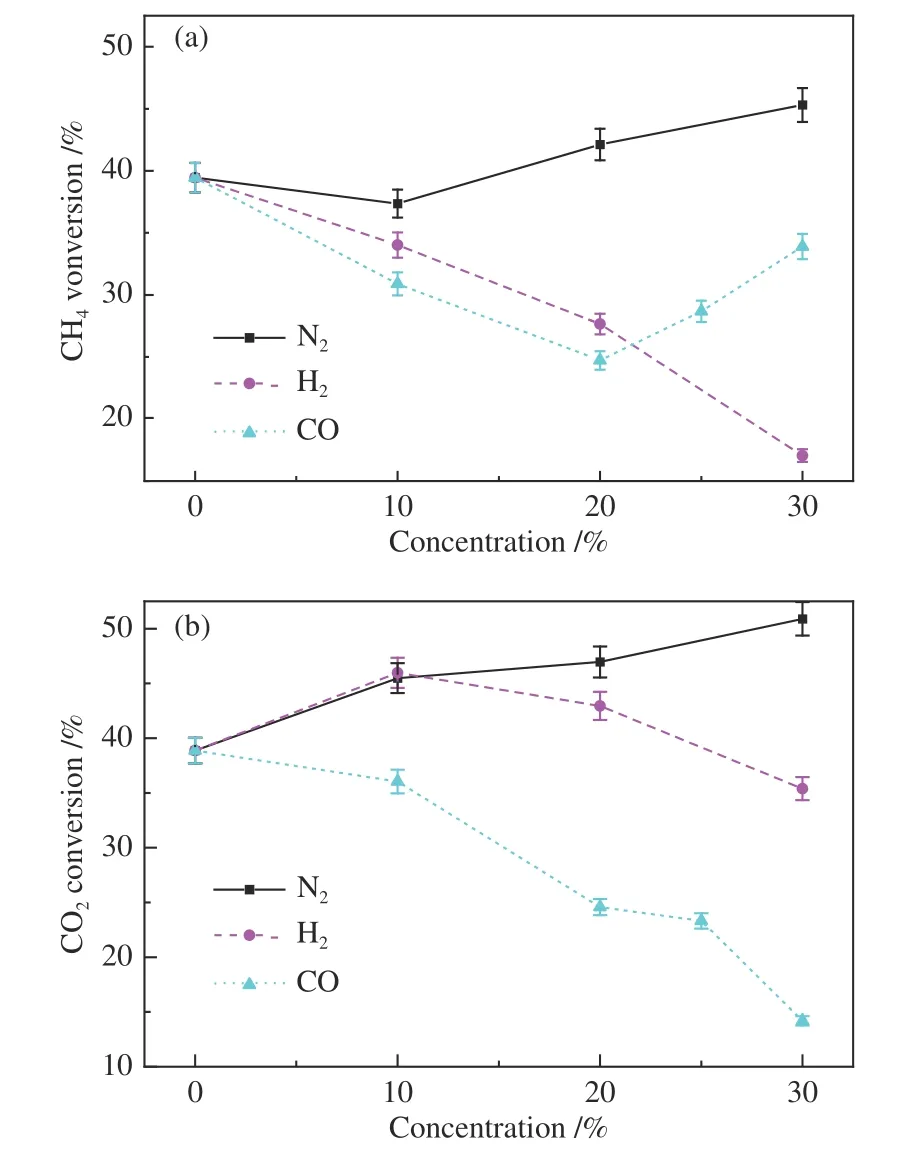
图8 入口气体中N2、H2、CO 体积分数变化对CH4、CO2转化率的影响Figure 8 Influence of the concentration of N2,H2 and CO in the inlet gas on the conversion rate of (a) CH4 (b) CO2

图9 入口气体中N2、H2、CO 体积分数变化对H2、CO 选择性及能量效率的影响Figure 9 Influence of the concentration of N2,H2 and CO in the inlet gas on the selectivity of H2,CO and energy efficiency(a):H2;(b):CO;(c):SEC
与N2相比,在反应进料中添加H2和CO 均会导致CH4、CO2转化率下降(图8)。H2和CO 在反应体系中作为反应产物,提高H2和CO 体积分数会抑制CH4和CO2反应向正向进行,降低CH4和CO2转化率。比较特殊的是当CO 体积分数从20%提高到30%时,CH4转化率从24.72%增加到33.90%。这可能是过量的CO 相互之间发生歧化反应生成了C 和CO2(式(11)),并且CO2体积分数的增加促进了DRM 反应正向移动,提高了CH4转化率。不同CO 添加量工况下反应后催化剂的TG 曲线(图10,将在2.6 节详细讨论)证实了该猜想:当进料中CO 体积分数从20% 增加到30% 时,催化剂积炭含量迅速增加到8.17%。
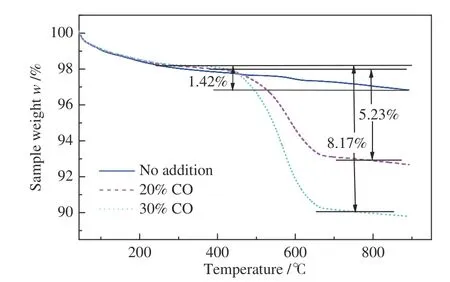
图10 不同CO 添加量工况下反应后催化剂的TG 曲线Figure 10 TG curves of the catalyst after the reaction under different CO addition conditions

由图9 可知,添加H2、CO 对产物收率和能量效率的影响比N2更大。随着N2体积分数从0 增加到30%,H2收率保持在30%左右,CO 的收率保持在40% 左右。将入口气体的H2体积分数从0 提高到30%时,产物中H2的收率从27.78%迅速降低到7.63%;CO 收率变化很小,保持在37%左右,可能原因是在反应体系中H2和CO2发生了逆水煤气变换反应(式10),消耗H2和CO2生成CO 和H2O。CO 体积分数从0 增加到30%时,H2收率从27.38%降低到22.96%,CO 收率从37.25% 降低到12.46%。三种气体对能量效率均有不利影响,如图9(c)所示,比如当向入口气体添加CO 时,SEC 从1.58 mmol/kJ 降到0.68 mmol/kJ(CO 体积分数30%)。
2.6 添加N2/H2/CO 后催化剂的积炭
为了进一步探究不同添加气氛下催化剂的积炭形貌与积炭量,分别进行了元素分析、拉曼表征、热重分析。表5 为不同气氛下反应20 min 后催化剂的积炭量。由表5 可知,添加CO 后催化剂表面的积炭量最大。当反应气氛中含有30%CO 时,催化剂上的积炭量为7.69%;N2气氛中反应后催化剂积炭量也有较大程度的增加。
图10 为不同CO 添加量工况下反应后催化剂的TG 曲线。由图10 可知,催化剂TG 曲线主要有两个失重阶段,分别是温度低于200 ℃时催化剂失去表面吸附水及内部结合水引起的失重[2],和300-700 ℃由于催化剂上积炭氧化造成的失重。在CH4和CO2干重整反应体系中添加CO 导致催化剂更容易发生积炭现象,当CO 体积分数从0 增加到20% 时,催化剂上的积炭量从1.42% 增加到5.23%,CO 体积分数进一步增加到30%时,催化剂表面积炭量达到8.17%,这与元素分析结果基本一致(表5)。
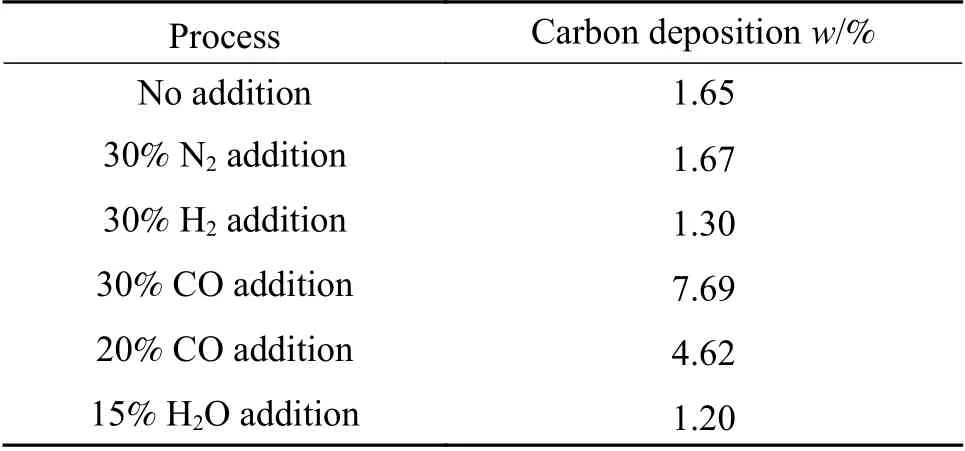
表5 不同气氛下反应20 min 后催化剂的积炭量Table 5 Carbon deposition on catalyst after 20 min reaction under different atmosphere
图11 为N2、H2、CO 三种气氛下催化剂的拉曼光谱谱图。由图11 可知,催化剂上的积炭存在两个比较明显的峰:在1300 cm-1附近的峰(D 峰)属于无定型炭的峰,而1590 cm-1附近的峰可归属于石墨炭的振动峰(G 峰)[2]。两个峰的峰强比值(IG/ID)可用于表征积炭的石墨化程度,IG/ID值越大,说明积炭形态越接近石墨炭的结构。图中所有样品的D 峰均大于G 峰强度,N2、H2、CO 三种气氛下IG/ID值分别为0.62、0.61 和0.56,可见CO气氛中反应后催化剂的积炭形态更接近无定形炭结构。
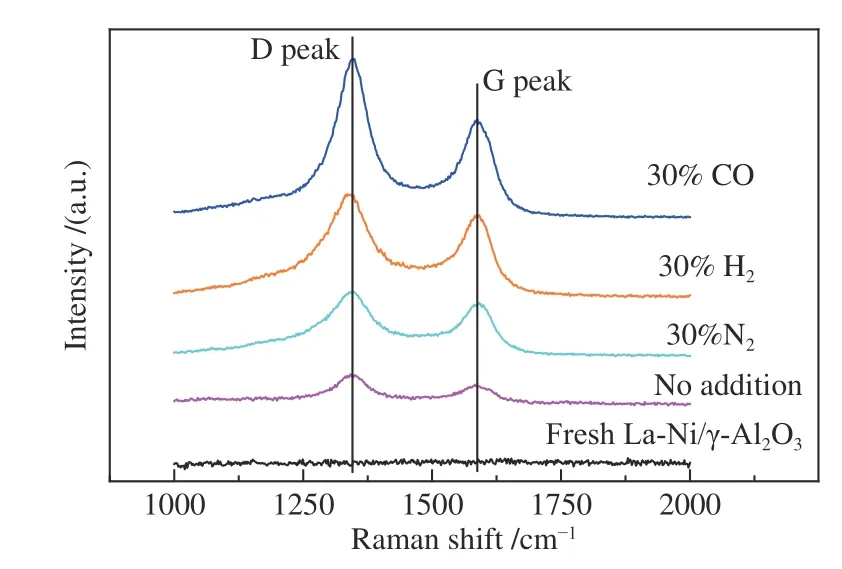
图11 不同气氛条件下催化剂的拉曼光谱谱图Figure 11 Raman spectra of catalysts in different atmosphere conditions
2.7 H2O 的影响
本节考察了生物质合成气中携带的少量水蒸气对CH4干重整反应的影响。实验结果见图12。当进气中水蒸气含量从0 增加到15% 时,CH4转化率从42.43% 增大到49.94%,CO2转化率也从39.64%增大到49.25%。添加H2O 对H2收率和选择性的影响较CO 更为明显(图12(b)),随入口气体中H2O 含量从0 提高到15%,H2的收率从26.45%增大到41.54%,选择性也从68.31%增加到105.64%。研究还发现,随H2O 含量增加,气相副产物C2H6选择性保持在1.12%-1.30%(图12(c))。添加H2O还可导致能量效率SEC 略有降低,当H2O 含量增加到15% 时,对于CH4、CO2的能量效率SEC 从1.65 mmol/kJ 降低到1.39 mmol/kJ(图12(d))。
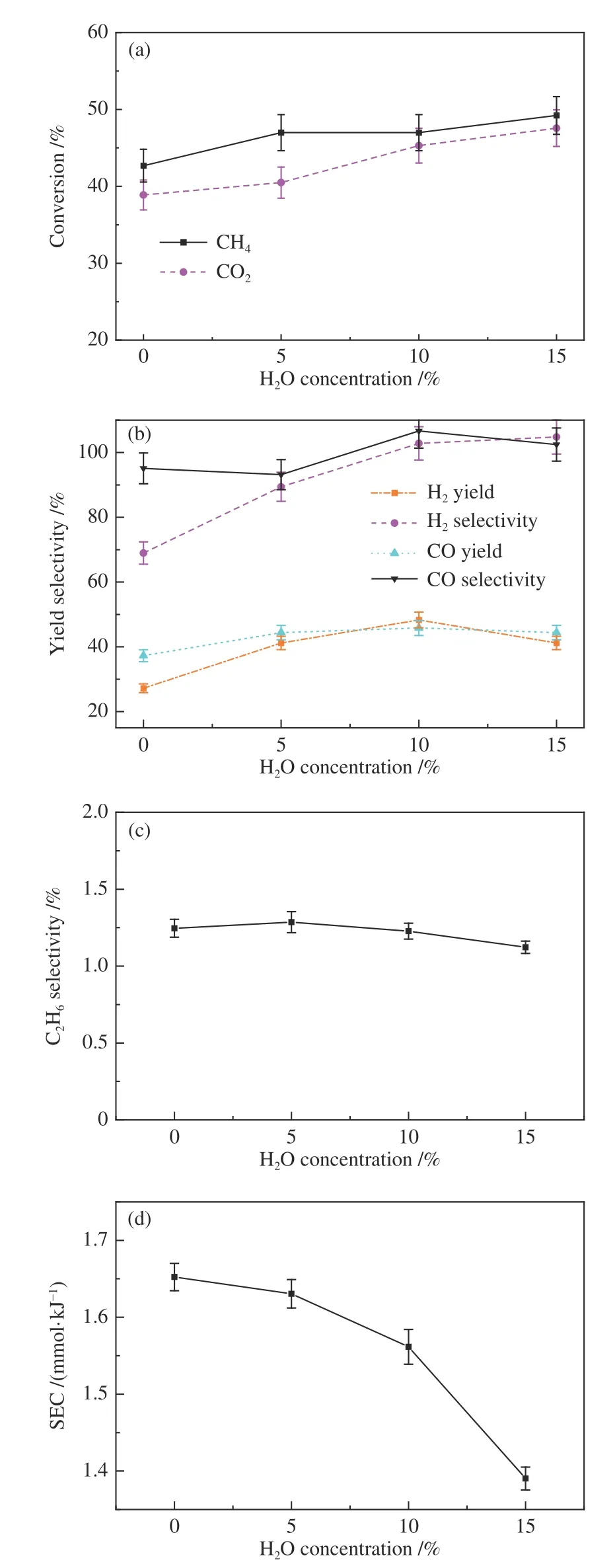
图12 H2O 含量对CH4 干重整的影响Figure 12 Influence of the concentration of H2O in the inlet gas on (a) the conversion rate CH4 and CO2 (b) the yield and selectivity of H2,CO,(c) the selectivity of C2H6,and (d) the energy efficiency
前人有关H2O-CH4重整[32-34]、H2O-CO2-CH4重整[35,36]的实验结果均表明,有H2O 参与的CH4重整反应有利于提高H2的选择性,并提高H2/CO物质的量比。李智等[36]进行了CH4含量为33%,H2O/CO2物质的量比从0 到1.0 变化的等离子体CH4重整实验,其CH4转化率保持在50%左右,但随着进料中H2O/CO2物质的量比增大,H2选择性趋近100%,H2/CO 物质的量比从0.6 增加到3.8。本实验中H2O 添加也呈现出对H2选择性的促进作用,与图8(a)中N2含量对CH4转化率影响结果比较表明,反应体系中含有10% H2O 时CH4转化率(47.50%)略高于10% N2时CH4转化率(39.92%),H2O 在反应体系中将作为反应物参与CH4重整反应。一方面,H2O 直接与CH4发生水蒸气重整反应;另一方面,H2O 可以与反应过程中生成的碳发生消碳反应,生成H2和CO。
3 结 论
等离子体耦合催化CH4干重整的优势主要体现在两方面:一是,通过等离子体放电在催化剂表面形成局部高温,提高催化剂活性;二是,形成高能激发态粒子有利于化学键断裂,降低了干重整反应所需的温度。
温度对DRM 具有明显的促进作用。随温度升高,CH4、CO2转化率,H2、CO 收率以及能量效率均有明显的提升。且由于逆水煤气变换反应的进行,CO2转化率总高于CH4转化率,并且CO 收率高于H2收率。
提高CO2/CH4物质的量比可增加CH4转化率。当CO2/CH4物质的量比为2.0 时,CH4转化率可达58.45%,H2选择性为71.83%,能量效率为1.82 mmol/kJ。当CO2/CH4物质的量比 ≥ 4 时,CH4转化率可达87.73%,但H2选择性降低到45.58%。
N2可以在等离子体反应体系中形成激发态,有利于CH4和CO2化学键的断裂。当CO2/CH4物质的量比为1.0 的混合气中N2体积分数增加到30%时,CH4转化率从39.01% 增加到45.76%,H2和CO 的收率分别达到31.63%和41.74%。与之相比,H2和CO 明显抑制了CH4的转化,添加30% H2和CO,CH4转化率分别降低到33.89% 和17.05%,并且由于CO 发生歧化反应,添加30% CO 使得CH4转化呈现先降后升趋势,反应结束后在催化剂表面产生大量积炭。
添加水蒸气可提高CH4和CO2转化率。当水蒸气含量 ≥ 5% 消炭反应进行得显著,在保持 CH4和CO2转化率不变时提高H2和CO 的选择性。

