粗针穿刺活检在射频消融治疗甲状腺微小乳头状癌中的临床应用
阎 琳,宋 青,肖 静,张 颖,罗渝昆
1中国人民解放军总医院第一医学中心超声诊断科,北京 1008532大连医科大学附属第二医院健康管理中心,辽宁大连 116023
甲状腺癌是最常见的内分泌肿瘤,在过去几十年中,甲状腺癌发病率增长迅速,位于全球恶性肿瘤发病率的第9位[1- 2]。甲状腺癌发病率的增长,50%与甲状腺微小乳头状癌(papillary thyroid microcarcinoma,PTMC)有关,这是一种不考虑是否存在高危特征,最大径小于1.0 cm的乳头状癌[3]。PTMC多为低危亚型,其主要治疗方式手术治疗或积极监测[4- 5]。近年来,射频消融(radiofrequency ablation,RFA)等热消融疗法开始逐渐应用到PTMC的治疗中,并取得了不错的疗效[6- 9]。但是,RFA的应用仍存在一定的争议。有学者认为可能存在不完全消融的可能[10- 12]。RFA术后评价方法主要是依赖超声检查,无法获得肿瘤细胞是否完全清除的病理学信息。目前,尚无粗针穿刺(core-needle biopsy,CNB)应用于RFA术后评价的报道,本研究主要探讨CNB在RFA术后疗效评估中的作用。
对象和方法
对象回顾性分析2016年6月至2018年9月行超声引导下射频消融治疗的甲状腺乳头状癌患者,入选标准:(1)CNB证实为PTMC,非病理学高危亚型(如高细胞、岛状细胞、柱状细胞癌);(2)超声提示为单发病灶,最大径≤1.0 cm;(3)肿瘤未侵犯甲状腺被膜或周围组织(距离>2.0 mm);(4)无影像学发现的颈部淋巴结转移及远处转移;(5)患者不耐受手术或明确拒绝手术治疗;(6)随访时间大于6个月;(7)无甲状腺癌家族史,无青少年或童年时期颈部放射暴露史。排除标准:(1)CNB诊断为病理学高危亚型;(2)病灶最大直径大于1.0 cm;(3)肿瘤贴近被膜或存在被膜侵犯;(4)存在颈部可疑转移性淋巴结或远处转移;(5)严重心、肺疾病,肝、肾功能衰竭;(6)严重出血倾向的凝血机制障碍或正在服用抗凝药物;(7)随访时间小于6个月。本研究经本院伦理委员会审核通过(伦理号S2019- 211- 01号),所有患者术前均知情同意并签署知情同意书。本研究共190例患者入选。其中女性142例、男性48例,年龄20~74岁,平均年龄(42.75±10.01)岁,肿瘤平均最大径(5.43±1.64)mm,平均体积(106.29±96.15)mm3。所有患者消融前均签署知情同意书。
消融前评估所有患者消融前均行超声和超声造影检查(contrast-enhanced ultrasonography,CEUS),使用超声仪器如下:西门子512超声诊断仪,探头中心频率为7 MHz;西门子S2000超声诊断仪,探头中心频率为8 MHz;迈瑞Resona 7超声诊断仪,探头频率为5.6~10 MHz。二维超声测量结节大小并计算体积,体积计算公式为:长(cm)×宽(cm)×高(cm)×0.524。
消融治疗过程使用德国Olympus公司生产的Celon AG 型射频消融系统,双极射频针100-T15,电极裸区长度为15 mm。消融过程中的超声引导仪器为西门子512超声诊断仪。患者取仰卧位,颈部后伸。常规消毒铺巾,1%盐酸利多卡因局部麻醉。如肿瘤与气管、食管、喉返神经等重要结构之间的距离<5 mm时,将生理盐水和1%盐酸利多卡因的混合液注入两者之间以形成至少1 cm的隔离带,防止邻近重要结构受到热损伤。超声引导下将18 G射频针置入结节深部,设定输出功率为3 W,启动射频仪,开始消融。如果5~10 s内射频针尖端未形成瞬时高回声带,则提高输出功率。消融过程使用经峡部入路的移动消融法。为了防止肿瘤的残留或复发,采用扩大消融法,即强回声的覆盖范围超过肿瘤边界至少3 mm[13]。消融后即刻行CEUS检查,如有残留,及时进行补充消融;如消融区无增强范围完全超过原病灶范围终止消融。消融后密切观察1~2 h,无声音嘶哑、局部出血等并发症时方可离开。
随访消融术后1、3、6、12个月及随后每半年行超声和CEUS检查。测量消融灶大小及体积,并计算体积缩小率(volume reduction rate,VRR)(%)=(消融前体积-随访时体积)/消融前体积×100%。随访时对甲状腺及颈部进行重点观察,一旦发现可疑病灶,将行CNB明确诊断。
术后穿刺时间为RFA术后第3或第6个月。由于消融灶可分为中心区、周边区及周围甲状腺实质[14],CNB至少对中心区、周边区进行穿刺。CNB的诊断标准参照细针穿刺的诊断标准[15]。将Bethesda Ⅱ定义为CNB阴性,Bethesda Ⅵ定义为CNB阳性,Bethesda Ⅰ、Ⅲ、Ⅴ定义为无明确结论。CNB阳性者进行补充消融,CNB无明确诊断结果者进行二次穿刺。

结 果
RFA结果所有PTMC均按计划行扩大消融,其中平均功率(4.53±1.11)W,消融耗时(175.13±96.04)s,平均能量(781.16±476.51)J。患者的平均随访时间为(30.04±12.41)个月,体积由(106.29±96.15)mm3缩小至(1.47±8.00)mm3,VRR为(99.08±4.32)%(表1、图1)。
术后穿刺结果RFA术后,145例患者于术后3个月进行穿刺,45例患者于术后6个月进行穿刺。共有146例病灶进行了中心区、周边区和周围甲状腺实质3个区域穿刺,44枚病灶进行了中心区和周边区穿刺。穿刺时的平均体积为(124.04±136.42)mm3。在190枚病灶中,CNB阴性者共188枚,CNB无明确诊断者0枚,CNB阳性者2枚,均为Bethesda Ⅵ出现在周边区。两例CNB阳性患者术前术后体积及体积缩小率变化见表2。随后对这两枚消融灶进行了补充消融,补充消融后3个月行CNB检查,结果均为阴性。
并发症所有患者的手术及穿刺均顺利进行,未出现喉返神经损伤、甲状旁腺功能减退等严重并发症,无血肿、皮肤烧伤等轻微并发症的发生。
讨 论
RFA作为一种局部治疗方法,已经被多个指南推荐为甲状腺良性结节及复发性甲状腺癌的治疗方法[4,16- 17]。近年来,RFA也逐渐应用于低危PTMC的治疗中[6- 9]。然而,有研究显示RFA存在无法完全治疗肿瘤原发灶的情况,引发广泛讨论[11- 12,18- 19]。Ma等[10]报道11例乳头状癌和1例PTMC病灶RFA术后行外科手术,术后组织病理学显示肿瘤残留。虽然RFA并不是低危PTMC的首选治疗方法[4],但其作为一种替代治疗方法,已应用于不耐受手术或拒绝手术患者中[17]。因此,避免不完全治疗和早期发现可能残留的肿瘤细胞是热消融治疗的关键。
目前,低危PTMC疗效评价指标有体积、VRR、完全消失率等,但均无法提供肿瘤细胞是否清除的病理学信息。甲状腺良性结节、微小癌及颈部转移性淋巴结热消融治疗专家共识,建议应考虑在术后通过穿刺病理检查判断RFA疗效的确切性[16]。既往研究多应用FNA在术后1、3和12 个月分别对消融灶进行穿刺[20- 21]。但本研究选择CNB进行术后疗效评价,原因有以下几点。首先,FNA虽然被广泛应用于甲状腺结节的诊断,但是与CNB相比,FNA的诊断准确性较低、假阴性率较高。其次,RFA后肿瘤组织发生凝固性坏死和细胞凋亡,会降低FNA的诊断准确性[14,22]。最后,CNB的并发症发生率较低,尤其在有经验超声医师操作下,其安全性可得到进一步提高[23]。

表1 RFA治疗前后PTMC的体积及体积缩小率变化情况
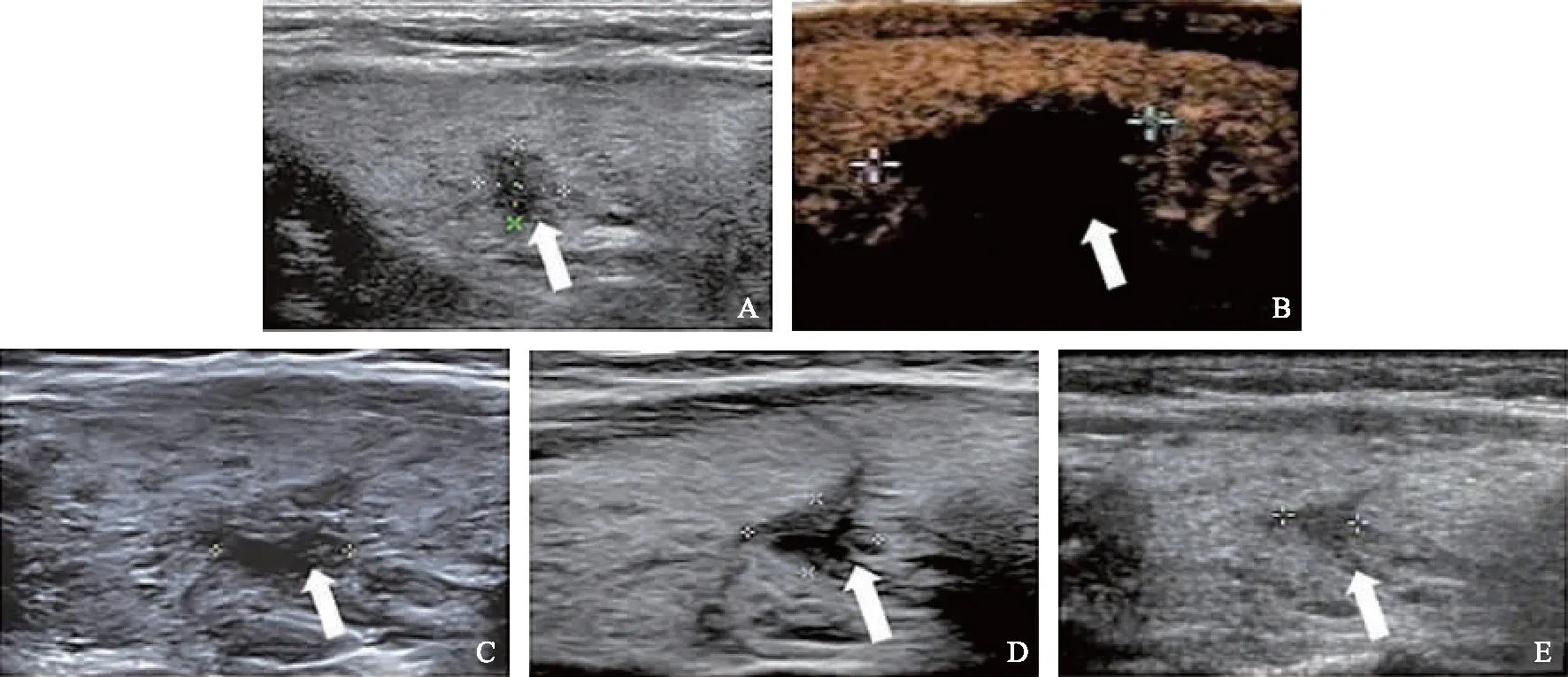
A.超声显示甲状腺右叶低回声结节(箭头);B.消融术后即刻,超声造影显示消融灶呈无增强区(箭头);C~E.消融术后3(C)、6(D)、12(E)个月,消融灶体积逐渐缩小(箭头)

表2 术后粗针穿刺阳性病灶体积及体积缩小率变化情况
本研究共有2枚消融灶术后CNB阳性,且均出现在周边区。原因可能为在消融过程中,肿瘤的中心区在超过60°C的高温下受到直接损伤导致凝固性坏死,然而周边区温度在41°C~45°C,这只会引起间接的可逆性损伤,导致该区域组织发生细胞凋亡或从可逆性损伤中恢复[14]。消融灶CNB阳性,表明一些肿瘤细胞仍然存在,它们可能为受损的肿瘤细胞由可逆性损伤中恢复,或者由于扩大消融不充分导致存在未能完全灭活的肿瘤细胞。甲状腺良性结节热消融治疗术后结节残留首先也出现在消融灶的周边区[24- 26],但与良性结节消融改善症状的治疗目的不同,PTMC需要达到完全治疗。因此,肿瘤周边区是消融治疗的关键区域,对该区域进行充分消融是保证完全治疗的前提。
目前,低危PTMC的RFA术后评价方法主要依赖于超声检查。本研究显示2枚CNB阳性的消融灶,其体积在每次随访中均缩小,表明体积缩小并不意味着肿瘤细胞的完全消失。超声检查无法评价肿瘤细胞是否完全灭活,也无法早期发现存在残留肿瘤细胞的消融灶,因此,PTMC术后仅使用超声检查进行有效性评价是不够的。本研究应用CNB进行低危PTMC术后评估,患者均能耐受穿刺过程,无并发症发生。且对于本研究大部分患者,RFA术后仅进行了1次CNB检查,从而避免了术后多次随访中的多次穿刺检查。
本研究存在以下局限性。第一,本研究为单中心回顾性研究,随访时间较短。第二,由于无法对消融灶进行手术病理学检查,无法评价RFA术后CNB的诊断效能。第三,超声对于中央区淋巴结和隐匿性病灶的敏感性较低。
综上,CNB是一种便捷有效的评价低危PTMC消融有效性的检查方法,可在消融术后早期发现残留肿瘤。

