燃料电池用氢气的制备工艺探讨
聂家波,邓建悦
(1.天津新氢能源股份有限公司,天津 300450;2.天津渤化永利化工股份有限公司,天津 300450)
近年来,地球环境持续恶化,全球气候变暖加剧。2019年全球的二氧化碳排放量达341.7亿t左右,全球的平均气温在14.8℃左右,比工业革命前高出1.1℃,已接近《巴黎协定》的危险线。为给地球“降温”,各国均制定了碳中和目标,我国也力争在2030年前实现碳达峰,2060年前实现碳中和。
氢能的储量丰富,能量密度高,能量转化效率高,转化过程中只产生水,不产生温室气体,是一种清洁的二次能源,可以应用于氢燃料电池车、发电、化工、冶金等行业。在氢燃料电池车的发展中,氢气的来源是整个产业发展的首要问题。目前制氢方法有多种,包括化石资源制氢(煤制氢、天然气制氢、石油制氢等)和可再生资源制氢(水制氢、生物质制氢、太阳能制氢、风能制氢等)等。化石资源制氢是具有经济性、生产可实现规模化、占主导地位的制氢方式;工业副产品制氢几乎无额外的资本投入和化石原料投入,所获氢气在成本和减排等方面有显著优势;电解水制氢消耗电能,只产生氢气和氧气,不产生温室气体,是未来最有前景的制氢方式。在实现碳达峰、碳中和目标的前提下,利用现有资源和副产品,研究开发出切实可行的制氢技术,为氢燃料电池提供充足的燃料来源,具有重要意义。
1 化石原料制氢
全球氢气中约92%来自煤和天然气,约7%来自工业副产气,1%来自电解水。煤制氢、天然气制氢技术的大规模应用,是基于石油替代和经济方面的原因。煤气化制氢和天然气制氢的工艺成熟,规模庞大,成本低,是目前工业制氢的主要途径。
1.1 煤气化制氢
我国的能源结构特点是“多煤贫油少气”,煤气化制氢主要用于石油炼化、甲醇、天然气、氨、柴油等行业。
煤与氧气经高温气化产生合成气(CO+H2),CO和水蒸气经变换转化为H2+CO2,再经酸性气体脱除,可以得到相对纯净的氢气。Shell气化炉在CO2工况下,在经过低温甲醇洗的合成气中,H2含量达到95%以上,含量数据见表1,主要杂质为N2,另有少量CO、CO2、CH4、Ar和微量的CH3OH、硫化物。

表1 低温甲醇洗净化气组分数据
1.2 甲烷制氢
天然气制氢是油气产出国普遍采取的制氢路线,目前的主要方法有甲烷水蒸气重整制氢和甲烷部分氧化制氢。
1.2.1 甲烷水蒸气重整制氢
此过程中会发生甲烷裂解(CH4→C+2H2)和一氧化碳歧化反应(2CO→CO2+C),2个反应都会产生积碳,造成甲烷水蒸气重整反应催化剂的失活[1]。工业上为降低积碳行为,会在提高反应压力的同时提高原料的水碳比。工业生产中,水蒸气和甲烷的摩尔比一般为3~5,生成的H2/CO摩尔比约为3。
CO和H2混合气在变换炉内,CO和水蒸气发生变换反应,将CO转化为CO2和H2,反应方程式如下:
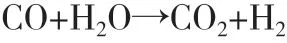
此反应为放热反应,根据热力学平衡,低温有利于水煤气变换反应,从而提高H2的回收率。
1.2.2 甲烷部分氧化制氢
甲烷经过压缩脱硫后,与氧气在850℃以上发生反应,反应方程式如下:
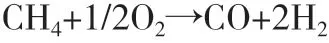
张雨舒认为[2],甲烷部分氧化制氢的反应,受温度和压力的影响较大,副反应可能有11种。甲烷制氢气体中除了H2,还有CO2、CH4、CO、H2O等杂质,其他杂质由天然气品质决定。
1.3 醇氨制氢
1.3.1 氨裂解制氢
氨裂解制氢是合成氨的逆反应,使用Ni或Fe催化剂,在650~800℃的高温下,氨受热分解产生75%氢气和25%氮气的混合气,分解率达到99%以上。反应方程式如下:
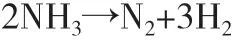
混合气冷却后进入PSA进行氮气和氢气的分离,得到高纯度氢气。该方法的制氢成本较高,主要受液氨和燃料价格的影响,产生的氢气气量较小,会产生惰性气体N2且不易除净。此工艺适合1000Nm3·h-1以内用量的小规模用户和需要氮氢混合气的行业,比如浮法玻璃生产、有色金属行业等[3]。
1.3.2 甲醇直接裂解制氢
甲醇直接裂解制氢是合成甲醇的逆过程。在催化剂作用下,甲醇直接裂解制氢,产生H2和CO,产品分离难度大。将混合气和水蒸气进行变换,可产生CO2和H2,反应方程式如下:
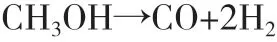
甲醇裂解制氢过程中,使用Cu/ZnO基催化剂,大部分可转化为CO和H2,甲酸甲酯是主要的中间产物[4]。反应方程式如下:
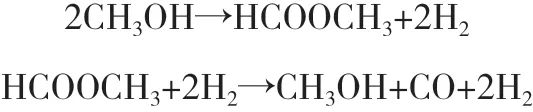
1.3.3 甲醇水蒸气重整制氢
脱盐水与甲醇按一定比例混合后,加热气化并过热,在温度220~280℃、压力0.8~2.5MPa、催化剂存在的条件下,转化为H2和CO2。反应方程式如下:
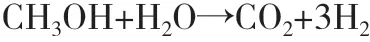
甲醇在水蒸气作用下会产生甲酸甲酯和H2,甲酸甲酯作为中间产物[5],经过其他反应,生成CO2和H2,还可能生成CO和HCHO。副反应的反应方程式如下:

根据相关文献,甲醇直接裂解制氢和甲醇水蒸气重整制氢,中间产物均为甲酸甲酯和H2,副反应为分解逆变换理论,目前还没有公认的关于甲醇水蒸气重整制氢的反应理论。甲醇直接裂解制氢,杂质可能有HCOOCH3、甲醇、CO和CO2;甲醇水蒸气重整制氢,杂质可能有CO2、CO、CH3OH、HCOOCH3、HCHO和HCOOH。
1.4 化工原料制备燃料电池用氢气的局限性
采用不同的化工原料制氢,产生的氢气和杂质存在差异,各制氢工艺对应的氢气和杂质见表2。煤制氢、甲烷制氢和甲醇制氢均会产生大量CO2,直接进行变压吸附提纯,氢气的回收率低,要经酸性气体脱除装置脱除大部分CO2、硫化物后,再经脱硫塔和变压吸附提纯,才能得到燃料电池用氢气。氨裂解制氢会产生大量N2,不产生CO2,碳排放很低,杂质中含有N2和氨,因变压吸附剂对H2和N2的吸附能力接近[6],直接使用变压吸附会导致回收率较低。氢燃料电池的Pt电极对CO、HCHO、HCOOH、NH3、卤素、硫化物等极其敏感,国标GB/T 37244-2018对以上成分的要求均在1×10-6以下。
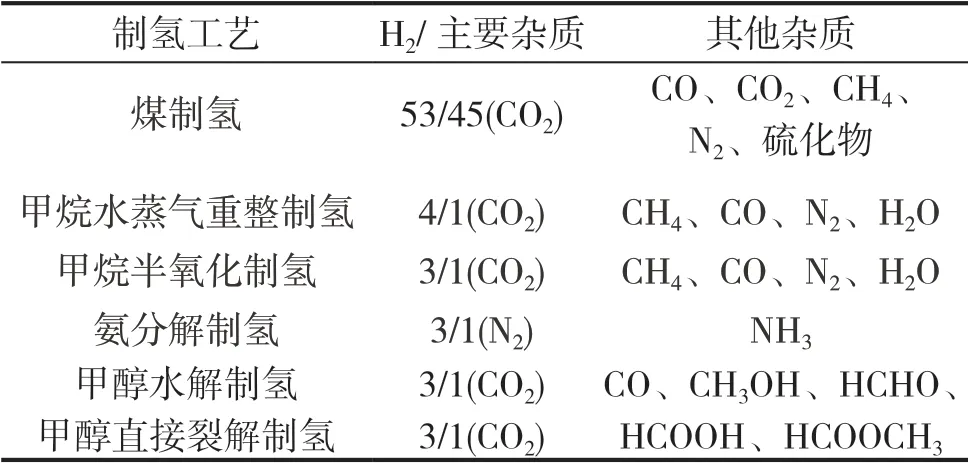
表2 不同化石原料制氢工艺产生的杂质
我国的煤化工产能庞大,具备发展煤制氢的先天资源优势和技术优势。与煤制氢相比,天然气制氢的投资低,CO2排放量较少,耗水量低,氢气产率高,是理想的制氢方式。但天然气的气源供应无法保障,需要依赖进口。随着我国天然气储量的不断增加和开采成本的降低,天然气制氢将更有优势。我国的甲醇产能过剩,甲醇制氢装置的投资低,建设周期短,制氢装置的规模灵活,但在燃料电池用氢气方面,甲醇现场制氢目前仍存在设备成本高、稳定性和可靠性差等缺陷。氨分解制氢与甲醇分解制氢的优点相似,不产生CO2,但是氨具有腐蚀性,存在运输、储存有安全风险等问题,目前在燃料电池用氢气的制备中少有应用。
2 副产气制氢
工业副产氢气主要有氯碱制氢、丙烷脱氢、炼厂气制氢、焦炉煤气制氢和甲醇驰放气制氢等。炼厂气催化产生的氢气主要用于炼油加氢和加氢裂解,焦炉煤气净化后用于副产甲醇和天然气,甲醇驰放气经膜分离后合成甲醇,其他工业过程副产的氢气很少被有效利用。若将这部分气体用于制取燃料电池用氢气,具有很大的应用潜力。
2.1 氯碱制氢
氯碱制氢用离子交换膜电解氯化钠,阳极产生氯气,阴极产生氢气。氢气中含有碱液、O2、N2、CO、CO2、H2O、Cl2、氯离子等,经洗涤、冷却、脱氯、脱氧、干燥等工艺,生产压力为0.8MPa、流量约1000Nm3·h-1的工业氢,纯度为99%,O2、N2含量很高,杂质含量见表3[6]。
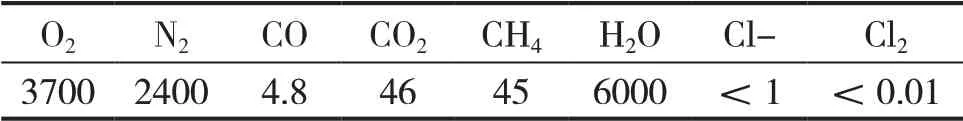
表3 氯碱副产氢气中的杂质含量 /×10-6
2.2 丙烷脱氢(PDH)
丙烷脱氢生产丙烯,在600℃左右、0.05MPa条件下发生反应,产出丙烯和氢气,单程转化率40%~45%。采用铬/铝催化剂,经多个(5~10个)固定床反应器,通过顺控程序实现丙烷脱氢/热空气的再生循环和主物料的连续操作[7]。
在催化剂作用下,丙烷脱氢会发生副反应[8],使得氢气中的杂质有CH4、C2H6、C2H4、C3H8、CO、水、硫化物(由丙烷原料决定)等。丙烷脱氢的主反应方程式如下,此外还会有副反应发生。

2.3 炼厂气制氢
炼厂气是炼油厂副产的尾气,成分复杂,烃类组分多,氢气含量30%~90%,还含有CH4、C2H4、C2H6、C3+、CO、CO2、H2O、硫化物等。张睿[9]介绍了天然气和炼厂气工艺80000m3·h-1制氢装置。天然气和炼厂气预热后进行烯烃加氢饱和,有机硫转化为无机硫,再通过2个脱硫反应器(顶层有脱氯剂)吸收氯,将氯含量降至0.01mg·L-1以下,再经脱硫剂和精脱硫剂深度脱硫后,实现硫含量在0.02mg·L-1以下。预转化气与蒸汽混合后,在催化剂作用下,重质有机化合物裂解为甲烷,部分转化为H2、CO、CO2。混合气升温进入转化管后,轻烃和水蒸气发生进一步的转化反应,转化为H2、CO、CO2和少量甲烷,CO和水蒸气则在变换炉内反应生成CO2和H2。
2.4 焦炉煤气制氢
焦炉煤气是煤焦化后产生的煤气,成分复杂,主要成分为氢气、甲烷、一氧化碳和二氧化碳,含量分别为50%、20%、5%和2%左右,还包括O2、N2、HCN、NH3、有机物(苯、萘、焦油等)、硫化物等。
殷文华[11]提出了焦炉煤气制取燃料电池用氢气的方案。焦炉煤气脱焦油和萘后,压缩至一定压力,经耐硫变换,把有机硫转化成H2S,把CO变换成H2和CO2。变换气进入脱硫装置脱除H2S后,进入PSA脱碳段脱除CO2和部分CH4等组分。脱碳气再进入PSA提氢段,得到半产品氢气。半产品氢气经脱氧和干燥,得到纯度和杂质组分都满足燃料电池要求的氢气产品。
郭武杰[11]提出将焦炉煤气处理后用于制取甲烷,产生的气体通过膜分离工序,分离提纯后得到天然气和富氢尾气。富氢尾气的主要成分是氢气、甲烷和氮气,含量分别为84.5%、14.2%和1.3%。
2.5 甲醇驰放气制氢
甲醇驰放气是甲醇系统排放的高压驰放气,压力7.2/8.3MPa,成分为H2、N2、CO、CO2、CH4等,气体成分数据见表4。氢回收是指驰放气经气体预处理(脱水、升温)和膜分离后,经过膜分离器的3.2MPa渗透气(H2含量大于80%)被送往压缩机,与新鲜气汇合后重新参与反应生成甲醇。
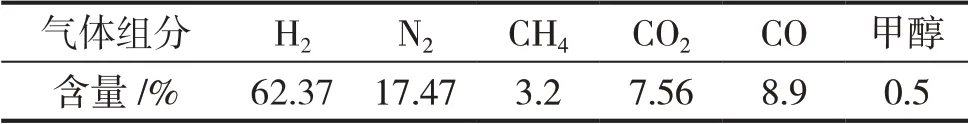
表4 甲醇驰放气的主要成分
韦光建[12]使用4.5MPa压力进行变压吸附,实现了氢气纯度在99%以上,回收率为77%,N2为0.75%,CO+CO2<10mg·L-1。
2.6 工业副产气制备燃料电池用氢气的局限性
不同工业副产气的杂质种类见表5。氯碱制氢直接产生的氢气纯度高,未经提纯已能达到99%,但氯碱制氢用于生产燃料电池用氢,需要对卤化物进行严格管控。丙烷脱氢使用PSA技术精制氢气,纯度可达99.99%[14],但其产物中仍含有有机物。炼厂气的成分复杂,含有大量高分子有机化合物,需要经过预处理和重整反应,将有机物和水蒸气转化成H2和CO2,后续除去酸性气体后再提纯。焦炉煤气的成分复杂,需经预处理除去氰化物、氨、硫化物、大分子有机物(焦油、苯、萘等),后续工艺与炼厂气工艺类似。甲醇驰放气中存在大量N2和CH4、CO、CO2,一般送往压缩机与新鲜气汇合后,重新参与反应生成甲醇,若用来制取燃料电池用氢,需要考虑N2、CO2、CO的提纯技术。
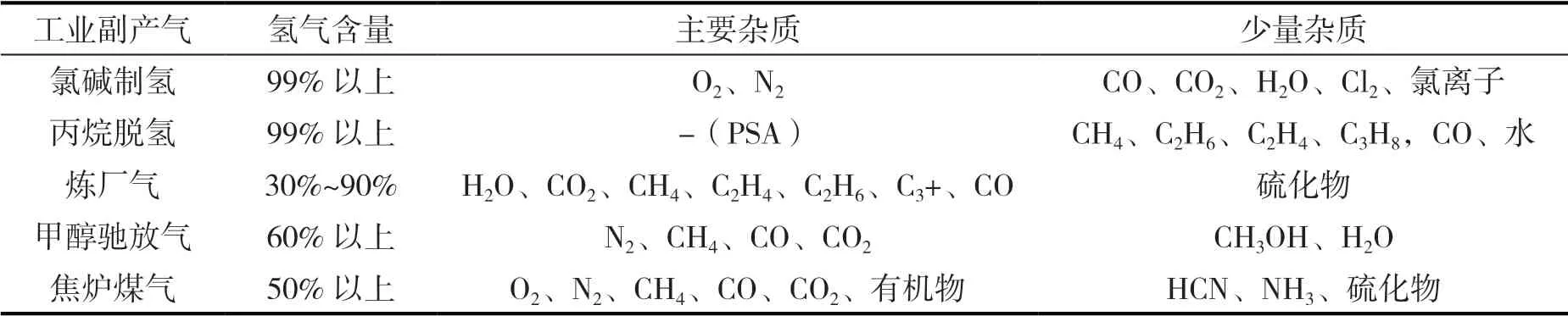
表5 不同工业副产气制氢气的杂质
3 电解水制氢
电解水制氢以水为原料,由电能提供能量制备氢气,是一种将电能转化成化学能和热能的化学反应过程,只产生氢气和氧气,不产生温室气体。根据电解池的不同,可分为碱性电解池、质子交换膜电解池和固体氧化物电解池。
3.1 碱性电解池制氢
在碱性电解质溶液中完成电解水制氢过程,OH-离子经隔膜到达阳极,失去电子产生O2,水在阴极得到电子,产生H2和OH-。

碱性电解池的结构简单,易于实现,成本低廉,技术成熟,只需使用非贵金属电催化剂(Ni、Co、Mn等)就可实现稳定的反应。但该技术存在一些不足:1) 负荷较低时(<40%)氧气产率很低,因此氢气分压会上升,造成氢气与氧气混合而导致爆炸危险;2)电解液的内阻较大,单位时间内传递的离子有限,导致最大工作电流较小;3)阴阳电极两侧的压力差,会随着产气的增加而增加,气体容易扩散,导致气体掺杂,需要特殊的压力平衡设计[14];4)产生的氢气中存在碱液、水蒸气和少量氧气,需要净化除去。
3.2 质子交换膜电解池
在直流电压作用下,水发生电离产生H+和OH-。H+通过质子交换膜达到阳极,得到电子产生H2,阴极的OH-失去电子变为H2O和O2。
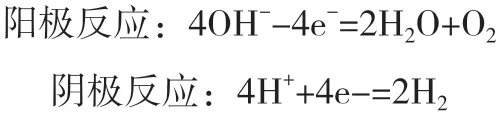
质子交换膜电解池的质子交换膜只有H+能单向通过,产生的气体纯度高,安全性高。电解池内的电极间距小,直喷法技术的电解槽的极间距可以做到200μm以下,使得电解槽的结构紧凑,同等产氢量的占地面积小;电流密度高,无污染,无腐蚀;装置能够快速启停,且运行负荷跨度大(0~100%之间任意智能连续调节氢气产出量)。质子交换膜电解水制氢技术实现产业化的关键,是廉价催化剂的活性与稳定性、膜的渗透性以及膜电极的结构等。
3.3 固体氧化物电解池
在高温状态下,利用电离技术将水蒸气电离,产生氢气和氧气。水分子电离后产生H+和O2-,在阳极,O2-失去电子转化为O2,阴极上,H+得到电子转化为H2,电解效率高。但是高温条件会导致热能损失和水资源的过度使用,且电解池材料比较昂贵,因此固体氧化物电解池无法大规模使用。
3.4 电解水制备燃料电池用氢的优势及局限性
电解水制氢,氢气的纯度高,杂质种类少,仅需过滤、干燥、净化等工序就可以得到燃料电池用氢。碱性电解池制氢技术已实现产业化,技术成熟,但制氢过程中难以快速启动或变载,无法快速调节制氢的速度。质子交换膜电解水技术仍处于研发阶段,其电流密度高,电解槽体积小,运行灵活,利于快速变载,与风电、光伏(发电的波动性和随机性较大)具有良好的匹配性。固体氧化物电解池水电解技术仍处于研发阶段。
4 结论
我国的煤化工、石油化工、氯碱行业、丙烷脱氢等的产能规模大,技术成熟,产生的氢气杂质易于除去,是燃料电池用氢气的优质来源。但是行业和工艺不同,产生氢气的纯度和杂质种类也不同。为了生产出适合燃料电池用的氢气,应对富氢气体进行预净化,将CO、CH4、有机物、硫化物等转化成CO2、H2S,通过酸性气体脱除,并针对性地对特殊杂质进行预处理后,得到纯度更高的氢气,再经变压吸附得到燃料电池用氢气。
氨分解制氢和甲醇驰放气中存在大量N2,无法单独使用PSA进行提纯,需要考虑多种分离工艺联用。炼厂气、焦炉煤气的杂质成分复杂,需要经过预处理后,再经过水蒸气重整转化提纯制氢。质子交换膜用于生产燃料电池用氢气时,等级要求高,在选择分离和提纯工艺时,应对原料氢气有充分了解,有针对性地对特殊的杂质组分进行吸收净化,再进行提纯,从而更好地生产燃料电池用氢气。电解水制氢的技术成熟,氢气纯度高且环境友好,但制氢成本高。我国的碱性电解水制氢技术是目前最成熟的电解水制氢方法,但成本仍然偏高,制氢综合成本至少在1.7元·m3。在国外,质子交换膜电解池制氢技术已进入市场导入阶段,国内仍处于研发阶段。与碱性电解水制氢技术相比,质子交换膜电解池制氢设备的价格高昂,但因具有对负荷变化的响应速度快的特点,更适应可再生能源发电的间歇性、波动性、随机性的特点,因此有望在装备成本降低后,成为未来更具市场前景的电解水制氢技术。

