LC-ESI-MS/MS法测定清开灵注射液中5种有效成分的含量
龙凯,王娟,彭建彪(云南省红河州食品药品检验所,云南 蒙自 661199)
清开灵注射液主要由猪去氧胆酸、胆酸、栀子、黄芩苷、金银花等8 味中药制成,具有清热化痰、醒神开窍的功效,多用于热病、神昏、上呼吸道感染、肺炎证候者。猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸为其主要有效成分,《中国药典》2020年版一部中收载了该品种猪去氧胆酸、胆酸、栀子、黄芩苷含量测定的HPLC 方法[1],但需用两种不同的检测器分别进行测定,主色谱峰出峰时间较长,原质量标准未制订金银花含量测定的项目,没有进行全面质量控制。目前尚无同时测定该剂型5 种成分含量的相关报道[2-4],日常质量检测工作中操作繁琐费时,为简化检测方法,研究采用LC-ESI-MS/MS 法同时测定清开灵注射液中5 种成分的含量。
1 仪器及试药
Thermo UltiMate 3000 高效液相色谱仪(美国Thermo Scientific);AB SCIEX QTRAP4500三重四极杆质谱仪(AB SCIEX 公司);Sartorius BP211D 电子天平(德国赛多利斯)。猪去氧胆酸(批号:100087-201411,含量:99.7%)、胆酸(批号:100078-201415,含量:98.9%)、栀子苷(批号:110749-201919,含量:97.1%)、黄芩苷(批号:110715-201821,含量:95.4%)、绿原酸(批号:110753-202018,含量:96.1%),(对照品中国食品药品检定研究院);清开灵注射液(吉林省集安益盛药业股份有限公司,规格:10 mL/支,批号:20011803、20021901、20041505、20030601、20042801、20061102);甲醇(色谱纯,霍尼韦尔贸易上海有限公司);水为超纯水;其余试剂均为色谱纯。
2 方法与结果
2.1 分析条件
2.1.1 色谱条件 色谱柱:ACE UltraCore 2.5 Super C18(100 mm×2.1 mm,2.5 μm);流动相:甲醇(A)-含0.1%甲酸的5 mmol·L-1甲酸铵溶液(B),梯度洗脱(0~3.0 min,5%A;3.0~4.0 min,5%~100%A;4.0~8.0 min,100%A;8.0~9.0 min,100%~5%A;9.0~10.0 min,5%A);流速:0.4 mL·min-1;进样量:2 μL:柱温:40℃。
2.1.2 质谱条件 离子源:ESI;检测方式:正负离子切换模式;扫描方式:多反应离子监测(MRM);离子化电压:正负离子模式均为4500 V;干燥气(N2)温度:500 ℃;喷雾气(N2)压力:50 psi;5 种成分质谱参数[5-7]见表1。

表1 质谱参数Tab 1 Mass spectrum parameters
2.2 溶液配制
2.2.1 对照品溶液 精密称取猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸对照品适量,置25 mL 量瓶中,用甲醇溶解并定容,制成每1 mL 含猪去氧胆酸372 μg、胆酸361 μg、栀子苷94 μg、黄芩苷563 μg、绿原酸55 μg 的混合对照品溶液(均按纯度折算)。
2.2.2 供试品溶液 精密量取样品1 mL,置100 mL 量瓶中,用甲醇稀释至刻度,用0.22 μm 微孔滤膜过滤,即得。
2.3 方法学考察
2.3.1 专属性考察 分别取对照品溶液、供试品溶液、空白溶液(甲醇),按“2.1” 项下色谱条件进样,记录色谱图,结果见图1,图中可见空白溶液在猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸相应保留时间处无干扰峰。
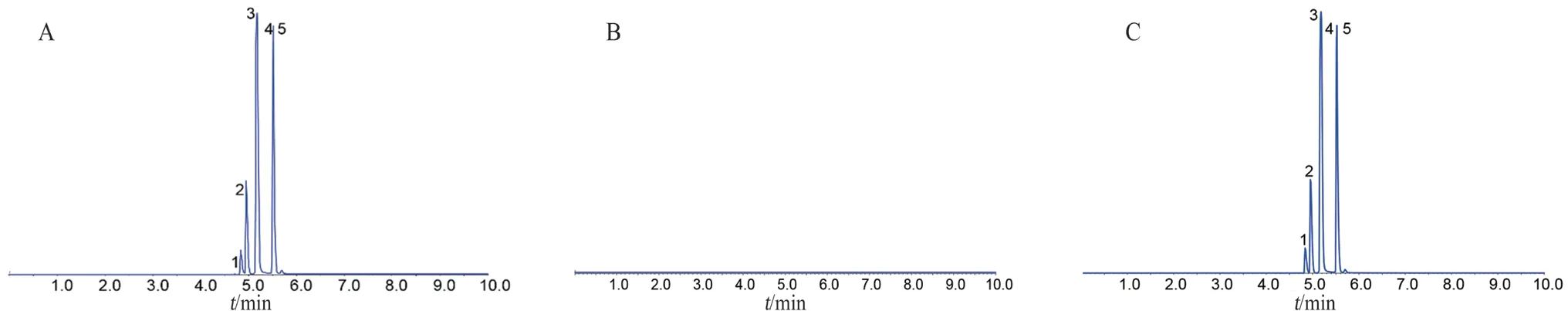
图1 清开灵注射液多反应监测(MRM)色谱图Fig 1 MRM chromatogram of Qingkailing injection
2.3.2 线性关系考察 精密量取“2.2.1”项下混合对照品溶液0.2、0.4、0.6、0.8、1.0、1.2 mL分别置于10 mL 量瓶中,用甲醇稀释至刻度,作为系列混合对照品溶液,各精密吸取2 μL 进行测定,记录峰面积,以对照品溶液质量浓度X(μg·mL-1)为横坐标,以峰面积Y为纵坐标,绘制标准曲线,进行线性回归,结果见表2。
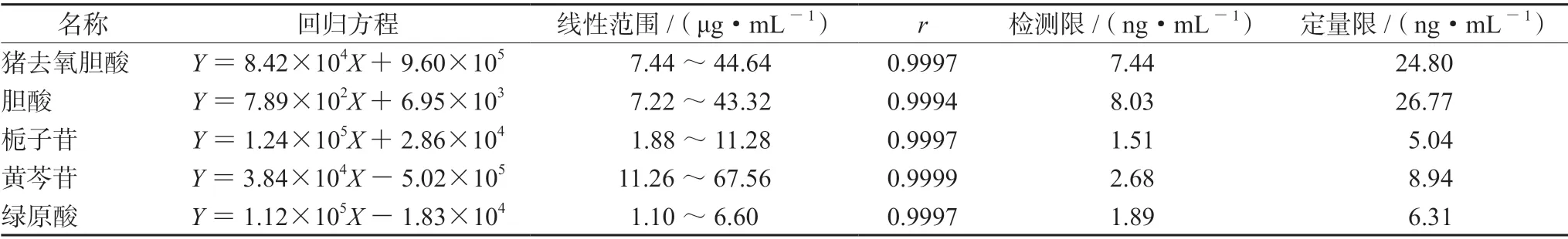
表2 线性关系考察、检测限和定量限Tab 2 Linearity,limit of detection and limit of quantization
2.3.3 精密度试验 精密量取“2.2.1”项下混合对照品溶液1 mL,置10 mL 量瓶中,用甲醇稀释至刻度,按“2.1”项下分析条件连续进样6 次,猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸峰面积RSD分别为0.99%、0.93%、0.83%、0.77%、1.0%(n=6)。间隔24 h 取同一混合对照品溶液在相同分析条件下再连续进样6 次,5 种成分峰面积RSD分别为1.0%、0.99%、0.90%、0.85%、1.1%(n=12)。结果表明仪器精密度良好。
2.3.4 稳定性试验 取“2.2.2”项下供试品溶液,按“2.1”项下分析条件分别于0、1、2、4、8、12、24 h 测定,结果猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸峰面积的RSD分别为1.1%、1.1%、1.2%、1.0%、1.3%(n=7),表明供试品溶液在24 h 内稳定。
2.3.5 重复性试验 取批号20011803 的样品,按“2.2.2”项下方法制备供试品溶液6 份,按“2.1”项下条件测定,计算样品中猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸的平均含量分别为3.11、3.21、0.55、5.25、0.36 mg·mL-1,RSD分别为1.1%、1.1%、1.3%、1.0%、1.3%(n=6),表明方法重复性良好。
2.3.6 检测限和定量限 精密量取“2.2.1”项下混合对照品溶液1 mL,置10 mL 量瓶中,用甲醇稀释至刻度,按“2.1”项下分析条件测定,以信噪比(S/N)约为3 和10 时分别计算猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸的检测限和定量限,结果见表2。
2.3.7 加样回收试验 精密量取已知含量的样品(批号:20011803)1 mL 置10 mL 量瓶中,用甲醇稀释定容,取1 mL 置100 mL 量瓶,共6 份,分别精密加入“2.2.1”项下混合对照品溶液1.0 mL,用甲醇稀释至刻度,进样测定,计算加样回收率,平均加样回收率分别为99.6%、99.4%、98.5%、99.8%、98.7%;RSD分别为1.1%、0.98%、1.5%、0.83%、2.0%(n=6)。
2.4 样品含量测定
取清开灵注射液样品6 批,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件进样测定,计算猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸的含量,结果见表3。
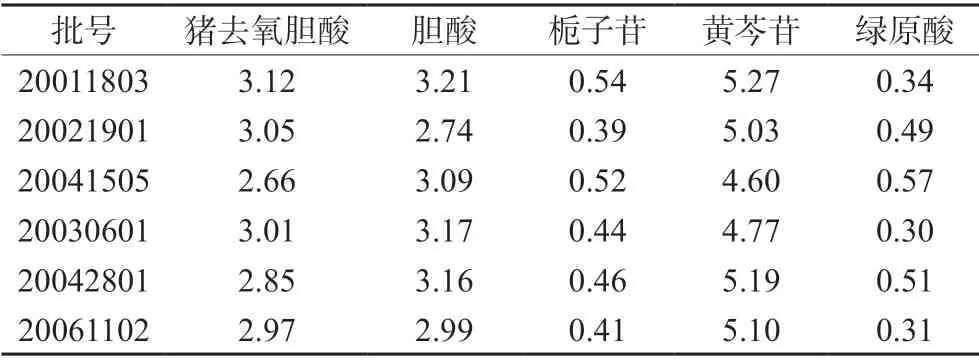
表3 样品含量测定结果(n=2,mg·mL-1)Tab 3 Content determination of samples (n=2,mg·mL-1)
3 讨论
曾用甲醇-0.1%甲酸水溶液作为流动相体系,结果黄芩苷峰形拖尾严重,响应值低。而使用甲醇-含0.1%甲酸的5 mmol·L-1甲酸铵溶液作为流动相时黄芩苷峰形较好,响应值稳定且更高,因此本方法采用甲醇-含0.1%甲酸的5 mmol·L-1甲酸铵溶液作为流动相。
在正、负离子模式同时扫描时,黄芩苷和绿原酸在两种模式下均有明显的响应值,黄芩苷在正离子模式下响应值更高,而绿原酸在负离子模式下响应值更高。猪去氧胆酸分子量为392.6,[M-H]-离子为m/z391.6,使用质谱对其进行扫描,未发现其特征性的子离子碎片,参考文献[8]选择m/z391.6→391.6 作为猪去氧胆酸的检测离子对,并得到了良好的色谱峰和响应值。
批号20041505 与批号20030601 的样品绿原酸含量测定结果相差较大,可能是由于金银花不同产地、不同季节、不同批次所含绿原酸量差异所导致。
本方法可以在较短时间内同时测定猪去氧胆酸、胆酸、栀子苷、黄芩苷、绿原酸的含量,色谱分离效果好,具有高灵敏度、高专属性、准确、稳定的特点,相较高效液相色谱法在定性定量方面更为准确,为清开灵注射液5 种主要成分含量的分析提供了便捷有效的质控方案。

