蒙药益母草对心血管系统和中枢神经系统的影响
张微,李君,胡玉霞,张谦,郭佳庆,张丁元,程明杰,常福厚*(1.内蒙古医科大学新药安全评价研究中心,呼和浩特 010110;2.内蒙古自治区新药筛选工程研究中心,呼和浩特 010110;3.内蒙古医科大学药学院,呼和浩特 010110;.内蒙古医科大学第一临床医学院,呼和浩特 010110)
蒙药益母草(Leonurus japonicusHoutt.)为唇形科(Lamiaceae)益母草属(Leonurus)植物益母草的新鲜或干燥地上部分,被收载于《神农本草经》和 《本草纲目》,其具有活血化瘀、利尿消肿之功效[1],别名益母艾、苦草、坤草等,其味辛、微苦,性微寒,入心包、肝经,具有活血化瘀、利尿消肿之功效。益母草主要含有生物碱类、黄酮类和二萜类成分,被蒙医视为疮疾圣药,是蒙药处方使用的道地药材。益母草目前在我国临床上应用越来越广泛,主要用于月经不调、产后瘀痛、心脑血管疾病、血液病等疾病的治疗,但现代药理毒理研究甚少,其质量标准体系和安全性评价有待深入研究。
目前尚未有研究数据来综合评价益母草对于心血管系统和中枢神经系统的毒性。本项目采用植入式生理信号遥测系统(DSI)观察清醒比格犬灌胃益母草细粉混悬液后对于心血管系统的影响;通过大鼠运动协调试验、小鼠自主活动试验和戊巴比妥钠阈下催眠试验,考察益母草对中枢神经系统的影响[2-6]。一方面,为蒙药益母草的药用安全性提供科学依据;另一方面,为内蒙古医科大学新药安全评价研究中心将要建立的蒙药毒理数据库提供资料。
1 材料
1.1 试药
益母草(安国路路通中药饮片有限公司,批号:20180117,经内蒙古医科大学生药学教授渠弼鉴定为正品);羧甲基纤维素钠(CMC-Na)(天津市光复精细化工研究所,批号:20170810);布洛芬缓释胶囊(中美天津史克制药有限公司,批号:20171208,规格:0.3 g/粒);碘伏(文水大有实业有限公司,批号:20170315);生理盐水(山东华鲁制药有限公司,批号:D16070503)。
1.2 仪器
植入式生理信号遥测系统(美国Data Sciences International 公司);动物麻醉机(美国Matrx公司);YLS-1C 小动物活动记录仪、YLS-31A 大小鼠转棒测试仪、YLS-27A 大小鼠尾部自动标号仪(济南益延科技发展有限公司);DS-Y350 型粉碎机(上海市顶帅工贸有限公司);CIC1P1-150FE-L 电子秤、BSA4202S 分析天平(赛多利斯科学仪器有限公司);灌注器(苏州伟康医疗器械有限公司,批号:170305);胃管(太平洋医材股份有限公司,批号:15025519)。
1.3 实验动物
普通级Beagle 犬6 只,5~6月龄,雌雄各半[北京玛斯生物技术有限公司,实验动物生产许可证号:SCXK(京)2016-0001],动物初次给药体质量:10.45~13.85 kg,饲养于内蒙古医科大学药物安全性评价中心普通设施,实验动物使用许可证号:SYXK(蒙)2014-0003,环境控制(温度:18~26℃,日温差<3℃,湿度:40%~70%,12 h/12 h 明暗交替)。单笼饲养,每笼1 只,饲料为购于北京科奥协力饲料有限公司的犬维持饲料,定时定量投饲(在动物实验前禁食过夜),自由摄取,自由饮水。
SPF 级ICR 小鼠80 只,雌雄各半,5~6 周龄,体质量:18~22 g;SPF 级SD 大鼠40 只,雌雄各半,5~6 周龄,体质量:170~250 g [北京维通利华实验动物有限公司,实验动物生产许可证号:SCXK(京)2012-0001]。大、小鼠饲养于内蒙古医科大学药物安全性评价中心屏障设施,实验动物使用许可证号:SYXK(蒙)2014-0003。环境控制(温度:20~26℃,日温差<3℃,相对湿度:41%~64%,换气次数≥15 次·h-1,12 h/12 h 明暗交替),饲养密度:5 只/笼,饲料为购于北京科奥协力饲料有限公司的60Co 放射灭菌鼠全价颗粒饲料,定时定量投饲(在动物实验前禁食过夜),自由摄取,自由饮水。
2 方法
2.1 手术及护理
在Data Sciences International 公司工程师指导下,参照DSI D70-PCTR 手术指南方法进行植入手术,术前用异氟烷麻醉实验动物,术中维持,麻醉后对实验动物进行充分备皮,主要包括整个胸腹部和腹外侧及前肢内侧,备皮面积要大于手术区域;植入过程主要包括植入子主体植入、压力导管的植入及电极的植入。植入子主体放于实验动物腹部左侧;心电电极采用模拟标准Ⅱ导联放置,实验动物胸右侧2~3 肋间隙与锁骨中线相交处为电极负极,胸左侧12~13 肋骨体与腋中线相交处为电极正极;呼吸电极植入结束后应对基线阻抗进行确认,确保呼吸波幅在(60±10)ohms 范围内;压力导管插入腹股沟腹动脉,为防止压力导管因犬活动拉扯滑出,压力导管植入后应预留O 型回路并用非吸收线缝合固定。手术植入及缝合结束后进入护理周期,术后给予布洛芬缓释胶囊3 d,1 次·d-1,1 粒/次,每日使用碘伏对伤口消毒1 次,连续7 d,恢复期3~4 周,待全部动物恢复后开始给药。
2.2 分组及给药
2.2.1 比格犬分组及给药 6 只比格犬采用拉丁方进行实验组别设计,分为4 组,即溶媒对照组(1% CMC-Na),益母草细粉混悬液低、中、高剂量组(0.24、0.72、2.16 g·kg-1)(约相当于人临床拟用剂量倍数的2、6、18 倍,人体质量按70 kg 计算,益母草人临床拟用量为9 g,即0.12 g·kg-1),设4 个给药周期,各给药周期间隔7 d。实验组别设计详见表1。

表1 益母草细粉混悬液心血管系统安全性药理组别设计Tab 1 Design of cardioprotective pharmacology group for leonuri herba suspension
2.2.2 小鼠及大鼠分组及给药 根据体质量、性别随机分组,实验给药剂量详见表2。

表2 中枢神经系统安全性药理剂量设计Tab 2 Design of central nervous system of leonuri herba suspension
2.3 数据采集
2.3.1 比格犬心电、血压、体温试验 采用植入式生理信号遥测系统采集动物心电、血压及体温指标,心电指标包括心率、PR 间期、QRS 间期、QT 间期、P 波、R 波、ST 段、T 波。记录给药前1~2 h 基础数据及给药后24 h 数据。采集间隔为每10 s 系统自动记录一次。统计时选取给药前0.5 h(给药前基础值)及给药后0.5、1、2、3、4、6、8、12、14、18、24 h,取每个时间点后5 min平均值作为该时间点数据,剔除因动物躁动等因素引起的大幅度漂移数据。
2.3.2 小鼠自主活动影响试验 选用5~6 周龄SPF 级ICR 小鼠40 只,雌雄各半,随机分为4组,即溶酶对照组(1% CMC-Na),益母草细粉混悬液低、中、高剂量组(1.2、2.4、4.8 g·kg-1),每组10 只,各组别分别经口单次灌胃。于给药前30 min 及给药后0.5、1、2、3、4、6、8 h 时间点放入记录仪的活动箱中,测定各组小鼠活动情况,记录10 min 内的自主活动次数。
2.3.3 小鼠戊巴比妥钠阈下剂量催眠影响试验 选用5~6 周龄SPF 级ICR 小鼠40 只,雌雄各半,随机分为4 组,即溶酶对照组(1% CMCNa),益母草细粉混悬液低、中、高剂量组(1.2、2.4、4.8 g·kg-1),每组10 只。于给药后6 h 腹腔注射30 mg·kg-1戊巴比妥钠,注射体积均为10 mL·kg-1(质量浓度为3.0 mg·mL-1),即刻开始观察注射戊巴比妥钠30 min 内每组翻正反射消失达1 min 以上的动物数,凡30 min 内动物翻正反射消失达1 min 以上者,表明发生了睡眠,翻正反射恢复即为动物觉醒,翻正反射消失至恢复这段时间为动物睡眠时间。记录每组发生睡眠的小鼠数和入睡潜伏期、睡眠时间。
2.3.4 大鼠协调运动的影响试验 SD 大鼠置于大小鼠转棒仪滚筒上训练,转速为12 r·min—1。训练结束后,选取能在转棒仪滚筒上维持3 min 以上不掉落的大鼠40 只,雌雄各半,按潜伏期分为4 组,即溶酶对照组(1% CMC-Na),益母草细粉混悬液低、中、高剂量组(0.81、1.62、3.24 g·kg-1),每组10 只。分别经口灌胃给药。分别于给药后0.5、1、2、3、4、6、8 h 将大鼠放在转棒仪滚筒上,记录每只大鼠从转棒仪滚筒上掉落所用时间,若10 min 以上不掉落则以10 min 计。
2.4 数据处理与分析
计量资料采用均数±标准差(±s)表示,采用SPSS 20.0 统计软件进行数据处理分析。用Levene’s test 方法检验方差齐性,若方差齐用单因素方差分析(ANOVA)进行统计分析,两组间用LSD test(参数法)进行比较分析。若方差不齐,用Kruskal-Wallis 检验,两组间用Dunnett’s Test(非参数方法)进行比较分析。
3 结果
3.1 益母草细粉混悬液对清醒比格犬心血管系统的影响
与溶媒对照组同一采集时间点的数值相比,蒙药益母草细粉混悬液高、中、低剂量组清醒比格犬的心率、PR 间期、QRS 间期、QT 间期、P波、T 波、ST 段及R 波均未出现明显改变(P>0.05),结果如图1所示。

图1 益母草细粉混悬液对清醒比格犬各项指标的影响Fig 1 Effect of leonuri herba suspension on indicators of conscious Beagle dogs
3.2 益母草细粉混悬液对清醒比格犬血压的影响
与溶媒对照组同一采集时间点的数值相比,益母草细粉混悬液低、中、高剂量组对清醒Beagle 犬的收缩压、舒张压及平均压均未产生明显影响(P>0.05),结果如图2所示。

图2 益母草细粉混悬液对清醒比格犬收缩压(A)、舒张压(B)和平均压(C)的影响Fig 2 Effect of leonuri herba suspension on systolic blood pressure(A),diastolic pressure(B),and average pressure(C)of conscious Beagle dogs
3.3 益母草细粉混悬液对清醒比格犬体温的影响
与溶媒对照组同一采集时间点的数值相比,益母草细粉混悬液低、中、高剂量组体温未出现明显改变(P>0.05),结果如图3所示。

图3 益母草细粉混悬液对清醒比格犬体温的影响Fig 3 Effect of leonuri herba suspension on temperature of conscious Beagle dogs
3.4 益母草细粉混悬液对小鼠自主活动的影响
与溶媒对照组同一采集时间点的数值相比,益母草细粉混悬液低、中、高剂量组自主活动次数未出现明显改变(P>0.05),结果如图4所示。

图4 益母草细粉混悬液对ICR 小鼠自主活动的影响Fig 4 Effect of leonuri herba suspension on spontaneous activity of ICR mice
3.5 益母草细粉混悬液对小鼠戊巴比妥钠阈下剂量催眠的影响
与溶媒对照组同一采集时间点的数值相比,益母草细粉混悬液低、中、高剂量组睡眠潜伏期及睡眠时间均未出现明显改变(P>0.05),结果如图5所示。
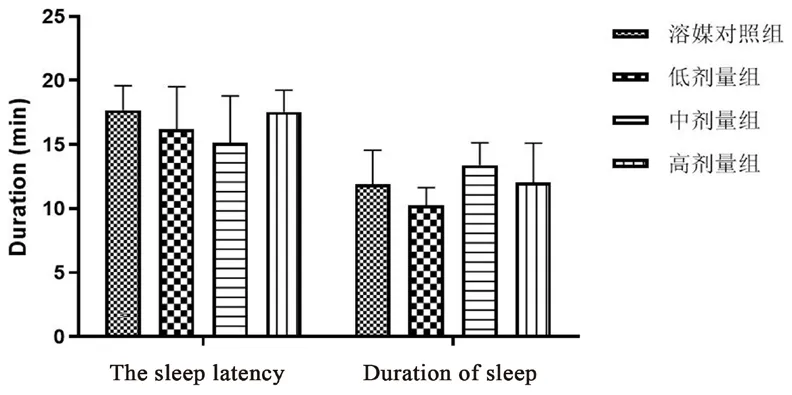
图5 益母草细粉混悬液对ICR 小鼠睡眠潜伏期和睡眠时间的影响Fig 5 Effect of leonuri herba suspension on sleep latency and sleep time of ICR mice
3.6 蒙药益母草细粉混悬液对大鼠协调运动的影响
与溶媒对照组同一采集时间点的数值相比,益母草细粉混悬液低、中、高剂量组大鼠协调运动未出现明显改变(P>0.05),结果如图6所示。

图6 益母草细粉混悬液对SD 大鼠协调运动的影响Fig 6 Effect of leonuri herba suspension on coordinated exercise of SD rats
4 结论与讨论
安全药理学是考察受试药物在治疗范围以内或治疗范围以上剂量时,潜在的不期望出现的对生理功能的不良影响,即观察药物对中枢神经系统、心血管系统和呼吸系统的影响[7-11];目前诸多关于心血管系统安全药理学的研究多采用麻醉或束缚状态下的实验动物,麻醉或束缚状态下所采集的心电、血压及体温等参数可能会对实验产生较大的影响,在研究特殊药物时,可能还会与受试药物产生相互作用;ICH-S7A《人用药物安全药理学研究指导原则》建议采用清醒动物遥测技术进行心血管系统实验,最大限度降低因麻醉剂、人为操作、动物应激等因素对实验产生的干扰[12-14]。结果表明,益母草细粉混悬液在0.24~2.16 g·kg-1剂量范围内对清醒比格犬的心电、血压及体温无明显影响;在1.2~4.8 g·kg-1剂量范围内对ICR 小鼠自主活动、睡眠潜伏期及睡眠时间无明显影响;在0.81~3.24 g·kg-1剂量范围内对SD 大鼠协调运动无明显影响。

