安罗替尼治疗晚期非小细胞肺癌的系统评价
徐 晨, 王 胜, 李春颖
(1.安徽中医药大学研究生院, 安徽 合肥 230000 2.安徽中医药大学第一附属医院老年病中心呼吸内科, 安徽 合肥 230000)
肺癌是世界范围内发病率和死亡率最高的恶性肿瘤之一,占总癌症病例的11.6%,也是癌症死亡的主要原因(占总癌症死亡的18.4%)[1]。其中以非小细胞癌(Non-small cell lung cancer,NSCLC)最为常见,约占85%。由于肺癌起病隐匿,生物学特性复杂,约有2/3患者初次确诊时已是晚期,失去手术机会[2]。根据一项长达14年、涉及全球71个国家的随访跟踪调查项目显示,全球范围内非小细胞肺癌患者的5年生存率为10%~20%[3],而晚期非小细胞肺癌患者的5年生存率仅为6%[4]。近年以来,基于第三代化疗药物包括铂类、紫杉醇、多西他赛、吉西他滨治疗晚期NSCLC的联合化疗方案疗效难以提高并造成包括骨髓抑制、发热、失眠、便秘、食欲减退、恶心呕吐在内的多种不良反应[5],严重影响患者的生活质量。以肺癌分子靶向药物治疗为代表的新型治疗手段对晚期NSCLC的临床实践产生很大影响,分子靶向药物可有效抑制肿瘤血管生成从而起到抑制肿瘤细胞增殖的作用,使得晚期NSCLC患者的治疗效果越来越好,生存期得到延长。安罗替尼(Anlotinib)是我国自主研发的新型多靶点小分子抗血管生成药物,可抑制血管内皮生长因子受体(Vascular endothelial growth factor receptor,VEGFR)、血小板衍生生长因子受体(Platelet derived growth factor receptor,PDGFR)、成纤维细胞生长因子(Fibroblast growth factor receptor,FGFR)、c-Kit、Ret等多个靶点[6]。由于安罗替尼上市时间较短且其价格昂贵,在二三线治疗失败的晚期肿瘤病人中推广范围有限,临床研究样本量较少且国内尚无相关系统评价报道,因此本文将采用Meta分析的方法对其作为晚期非小细胞肺癌治疗药物的有效性和安全性做系统评价,以期提供进一步循证依据。
1 资料与方法
1.1纳入与排除标准
1.1.1研究类型:国内外公开发表的随机对照试验(Randomized Controlled Trials,RCTs),无论是否采用盲法。
1.1.2研究对象:①年龄18~75周岁,无性别限制;②病理学诊断为晚期(ⅢB/Ⅳ期)非小细胞癌;③至少接受过两种系统性化疗方案的三线及以上或无法耐受治疗的NSCLC患者;④EOG PS评分0~1分且预计存活期3个月以上;⑤治疗前无化疗禁忌症,肝肾功、血液学、心电图无明显异常。排除小细胞肺癌(SCLC,包括混合性小细胞肺癌/非小细胞肺癌)、有咯血史、有症状的脑转移或脑转移控制在2个月、鳞状细胞肺癌或非小细胞肺癌中央空洞伴咯血(每天450mL)、以及在前4周或本研究中安排的全身抗肿瘤治疗的患者。
1.1.3干预措施:安罗替尼vs安慰剂或其他化疗药物(安罗替尼vs吉西他滨+顺铂、安罗替尼vs含铂双药化疗、安罗替尼vs白蛋白+紫杉醇、安罗替尼vs培美曲塞+顺铂)或其他最佳支持治疗。
1.1.4结局指标:①有效性:客观有效率[Objective Response Rate,ORR,ORR=(完全缓解+部分缓解)/总例数],疾病控制率[Disease Control Rate,DCR,DCR=(完全缓解+部分缓解+疾病稳定)/总例数],总生存期(Overall Survival,OS),无进展生存期(Progression-Free Survival,PFS);②安全性:指药物不良反应的评估,根据美国国立癌症研究所推荐的不良事件标准(NCI-CTCAE)4.0版进行评估[4]。根据不良反应严重程度分为5级,1级:轻度;无症状或轻微;仅为临床或诊断所见;无需治疗。2级:中度;需要较小、局部或非侵入性治疗;与年龄相当的劳动性日常生活活动受限。3级:严重或医学上有重要意义但不立即危及生命;导致住院或延长住院时间;致残;个人日常生活活动受限。4级:危及生命;需要紧急治疗。5级:与不良事件相关的死亡。
1.1.5排除标准:①重复发表的文献;②非中、英文文献;③数据不全或无法获得数据的文献;④动物实验;⑤研究为评论、会议摘要等。
1.2文献检索策略:计算机检索PubMed、EMbase、Web of Science、Cochrane Library、万方、维普网、中国知网、SinoMed数据库,检索时限为2018年1月至2020年3月。英文检索词为包括:NSCLC、advanced non-small cell lung cancer、advanced non-small cell lung carcinoma、anlotinib、AL3818、Randomized Controlled、Clinical Observation、Clinical Reasearch。中文检索词包括:安罗替尼、晚期非小细胞肺癌、非小细胞肺癌晚期、随机对照试验、临床研究、临床观察。同时对纳入文献的参考文献进行追溯以求数据收集尽量完整。以PubMed为例,检索式为:[(#NSCLC OR #advanced non-small cell lung cancer OR #advanced non-small cell lung carcinoma) AND (#Anlotinib OR #AL3818)]。
1.3文献筛选和资料提取:由2名研究员分别独立阅读文献题目、摘要及全文,筛选符合上述纳入及排除标准的研究并交叉核对,保证数据的准确性可靠性。如遇分歧时则共同讨论结局或咨询第三方解决。
1.4文献质量评价:对纳入文献采用Cochrane干预措施系统评价手册5.1.0进行方法学质量评价,评价内容包括以下6个方面:①随机方法;②分配隐藏;③盲法;④不完全结局数据;⑤选择性结局报告;⑥其他偏倚来源。若完全满足上述六大标准,则存在产生偏倚的风险小;若不完全满足,则存在产生偏倚的风险大。据此将文献评估分为:高风险(high risk)、低风险(low risk)、未知风险(unclear risk)。
1.5资料分析:应用Revman5.3统计软件对文章数据进行提取及分析,PFS、OS属于计量资料,采用风险比(Hazard Risk,HR)为效应指标,当HR<1时,表示试验组风险低于对照组;反之则表示试验组风险高于对照组。有效和无效、不良反应发生率均属于二分类数据,采用相对危险度(Risk Ratio,RR)为效应指标,当RR>1时,表示试验组效应量大于对照组;当RR小于1时,表示试验组效应量小于对照组。各效应量均合并95%置信区间(95%CI)进行评价。采用卡方检验和I2对研究进行异质性检验,若(P<0.05,I2>50%)时,采用随机效应模型,反之则采用固定效应模型,P<0.05时结果有统计学意义。
2 结 果
2.1检索结果:计算机检索相关文献215篇,其中中文文献119篇(万方数据库27篇、维普网22篇、中国知网58篇、SinoMed12篇),英文文献96篇(PubMed7篇,EMbase36篇,web of science14篇,Cochrane library39篇),阅读标题、摘要后,初步筛选40篇符合纳入标准的研究,将文献导入EndNote X9.1后,剔除重复文献、阅读全文后,最终确定文献8篇[7~14],共784例患者。文献检索流程见图1。

图1 文献检索流程图
2.2纳入研究的一般特征:共纳入784例研究病例,其中试验组474例,对照组310例。单个研究最多病例为437例,最少病例为7例。其中4个研究[7,10,13,14]为安罗替尼vs安慰剂,共585例病例;3个研究[8,11,12]为安罗替尼vs含铂类双药化疗(安罗替尼vs吉西他滨+顺铂、安罗替尼vs含铂双药化疗、安罗替尼vs白蛋白+紫杉醇、安罗替尼vs培美曲塞+顺铂)共159例病例;1个研究[9]为安罗替尼vs最佳支持治疗(具体疗法不详),共40例病例。纳入文献的基本特征见表1。
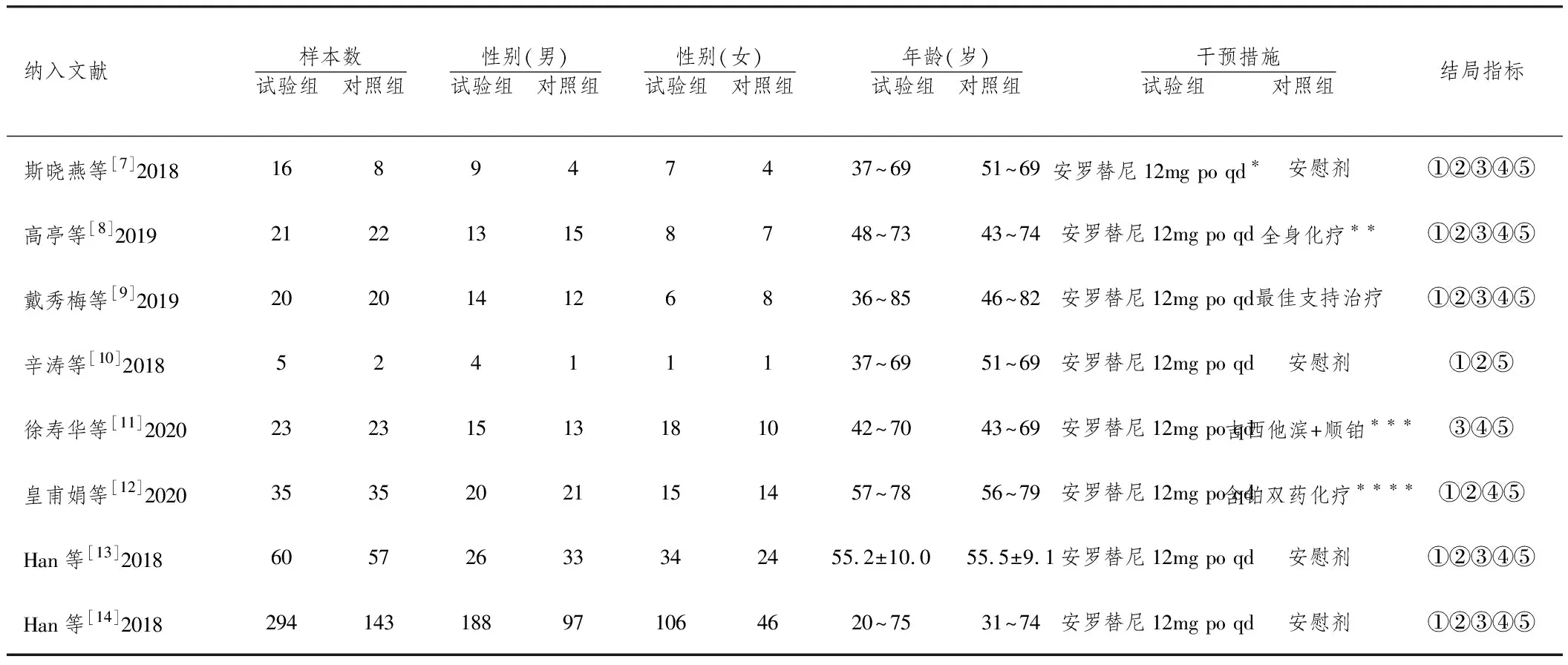
表1 纳入文献的基本特征
2.3纳入研究的方法学质量评价:纳入的8篇文献中,其中2篇为多中心研究[13,14],6篇文献[7,9,10,12~14]提到了采用随机分组的方法,在随机方法上有1篇文献[9]采用随机数字表方法,其余均未提及具体随机方法。4篇文献[7,10,13,14]报告使用了盲法,但未说明具体的施盲对象。6篇研究[7~9]未提及分配隐藏。2篇文献[7,11]各有1例研究对象失访。所有研究结局数据均完整,无选择性报告结局及其他偏倚来源。根据Cochrane评价手册对纳入文献进行评价,具体结果参考图2、3。

图2 偏倚风险总结图
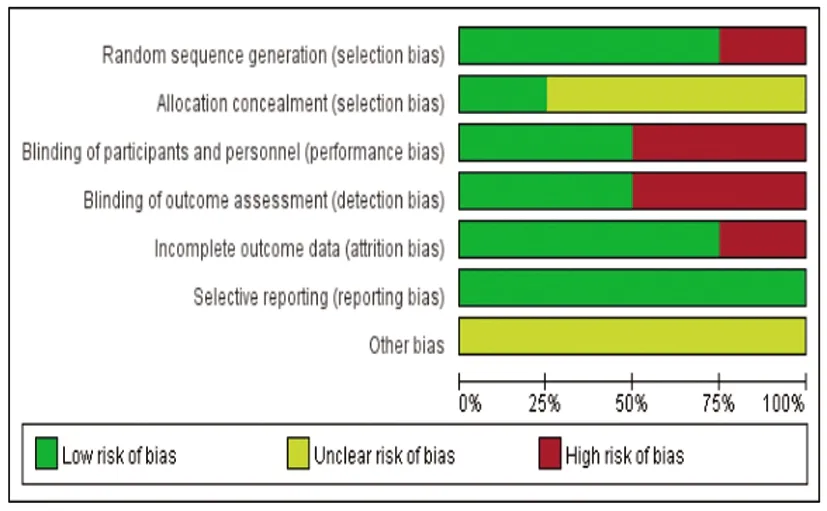
图3 偏倚风险图
2.4Meta分析结果
2.4.1有效性
2.4.1.1PFS:共纳入5个研究[7~9,11,12],随机效应模型Meta分析结果显示,各组间存在轻度异质性(P=0.12,I2=46%)。试验组PFS高于对照组,差异有统计学意义[HR=0.34,95%CI(0.30,0.39),P<0.00001]。见图4。
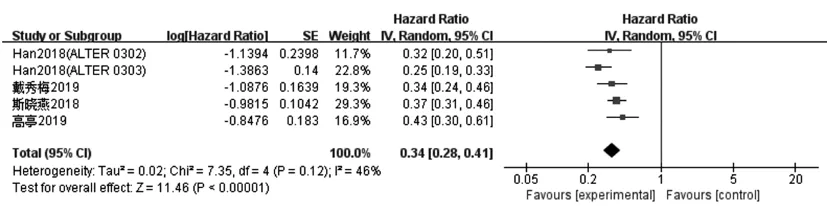
图4 试验组与对照组对比治疗晚期非小细胞肺癌PFS的Meta分析森林图
2.4.1.2OS:共纳入5个研究[7~9,11,12],固定效应模型Meta分析结果显示,各组间无明显统计学异质性(P=0.94,I2=0%)。试验组OS高于对照组,差异有统计学意义[HR=0.73,95%CI(0.63,0.85),P<0.0001]。见图5。
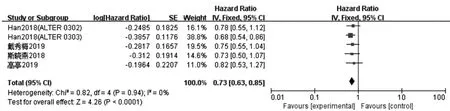
图5 试验组与对照组对比治疗晚期非小细胞肺癌OS的Meta分析森林图
2.4.1.3DCR:共纳入7个研究[7~9,11~14],随机效应模型Meta分析结果显示,各组间存在明显重度异质性(P<0.00001,I2=93%)。试验组效应量大于对照组,差异有统计学意义[RR=1.66,95%CI(1.06,2.58),P=0.03],证明安罗替尼可提高疾病控制率。见图6。
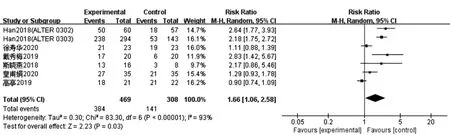
图6 试验组与对照组对比治疗晚期非小细胞肺癌DCR的Meta分析森林图
2.4.1.4ORR:共纳入7个研究[7~9,11~14],随机效应模型Meta分析结果显示,各组间存在中度异质性(P=0.05,I2=53%)。试验组效应量大于对照组,差异有统计学意义[RR=2.03,95%CI(1.06,3.58),P=0.03],证明安罗替尼可提高客观有效率。见图7。
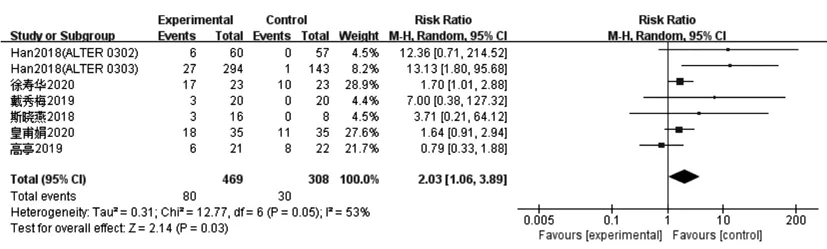
图7 试验组与对照组对比治疗晚期非小细胞肺癌ORR的Meta分析森林图
2.4.2安全性:8个研究均报道了与安罗替尼有关的不良反应,以发生不良反应的种类分组,共纳入4个研究[7,12~14]。结果如表2所示。
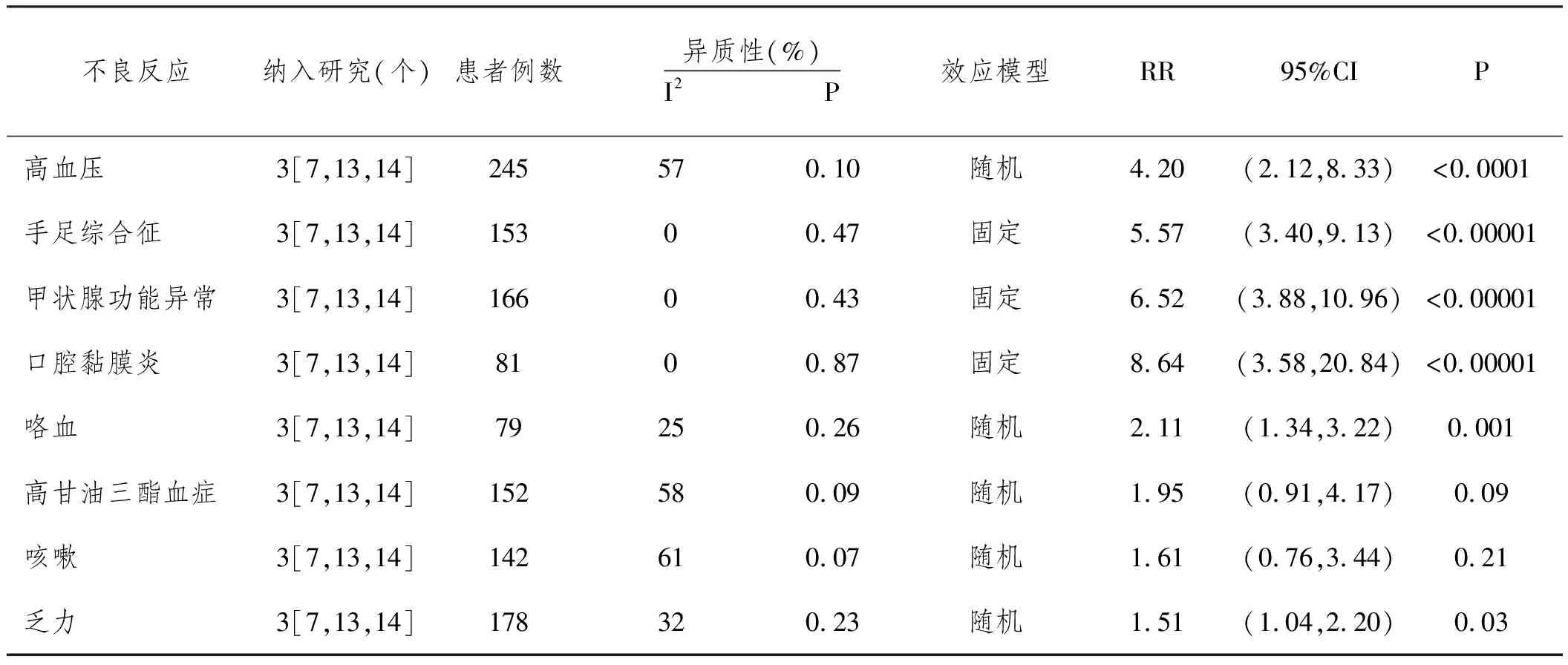
表2 不良反应分析汇总
2.4.3发表偏倚:分别以PFS、OS作为指标绘制漏斗图,结果见图8、9。当漏斗图不对称呈偏态分布时,说明存在发表偏倚。本研究纳入的文献散点较为集中的分散在直线两侧,总体上分布比较均匀,提示纳入研究的发表偏倚较小。

图8 PFS的漏斗图

图9 OS的漏斗图
3 讨 论
3.1研究意义:根据美国NCCN发布的NSCLC2020指南显示,肺癌是美国2019年癌症死亡的首要原因,全年预计新增肺癌和支气管癌病例228150例并预计有142670例肺癌患者死亡[15]。在所有肺癌患者中,5年以上存活率仅18%[16]。根据循证医学证据和国内外多种指南推荐,无论是驱动基因突变阳性还是阴性的NSCLC患者,一线二线治疗方案均已明确,关键在于其三线治疗目前没有充分证据支持三线使用细胞毒药物治疗,且三线治疗仍缺乏标准治疗规范。换言之,目前临床上肺癌的三线治疗主要是根据一些证据级别不高的数据来选择较为可行的治疗方案,并无较强循证医学证据的支撑和指导。最早出现的单抗类或大分子血管靶向药例如恩度、贝伐珠单抗等的单药使用均未在晚期NSCLC的三线治疗中取得令人满意的效果。而安罗替尼作为一种新型多靶点小分子抗血管生成抗肿瘤药物,可同时抑制 VEGFR/PDGFR/ FGFR介导的三条信号通路,并全面阻断肿瘤血管新生[17]。安罗替尼单药治疗多种类型实体肿瘤包括结肠腺癌,非小细胞肺癌,肾透明细胞癌,甲状腺髓样癌,软组织肉瘤的Ⅱ期临床试验已经取得初步疗效。因此,安罗替尼对于晚期NSCLC人群的有效性需进一步证实。
3.2结果及局限性:本研究结果显示,在与安慰剂或全身化疗对比时,安罗替尼可有效提高晚期NSCLC患者的DCR和ORR,并延长患者中位PFS和中位OS。这说明安罗替尼在治疗晚期NSCLC方面有明显的效果,这与斯[7]等及Han[13,14]等的研究结果一致。此外,戴[9]等及辛[10]等还报道了部分出现肿瘤病灶缩小的试验组病例。由于晚期NSCLC病人的整体机能、耐受能力及生活质量均差于正常人,安罗替尼作为一种口服的多靶点小分子抗血管生成抗肿瘤药物,可成为晚期NSCLC患者的重要选择。Xie[18]等研究发现,安罗替尼是一种高效的VEGFR抑制剂,尤其是对于VEGFR-2和VEGFR-3靶点的选择性远大于其他酪氨酸激酶抑制剂如舒尼替尼,其对VEGFR-2/3靶点的抑制作用是舒尼替尼的20倍。由此可看出,安罗替尼与同类药物相比具有更好的抗肿瘤作用。但在安全性方面,试验组不良反应发生率明显高于对照组。其中高血压为最常见的不良反应,共有245例。其次为乏力、甲状腺功能异常、手足综合征等不良反应。由于安罗替尼是一种VEGF通路抑制剂,其引起血压升高的作用机制可能为:①抑制一氧化氮(NO)合成从而使血管收缩;②微血管疏松导致系统性血管阻力增加;③神经内分泌机制产生的激素导致抗血管生成性高血压[19]。而甲状腺功能异常主要指甲状腺功能减退,这与安罗替尼是一种酪氨酸抑制剂(Tyrosine kinase inhibitors,TKI)有关,研究[20]认为,安罗替尼对酪氨酸激酶在血管功能方面造成了影响,使得甲状腺内血流减少从而导致了缺血性甲状腺炎的产生,最终甲状腺遭到逐步破坏形成甲减。8个研究中所提到的不良反应大部分为轻度不良反应,严重不良反应少,并且通过一定的治疗方法可对不良反应进行控制和逆转。因此本研究提示:安罗替尼能有效延长晚期NSCLC患者生存期,提高患者治疗效率,使大多数患者获益,且患者对安罗替尼的总体耐受较好,值得临床推广。
本Meta分析仍存在以下问题:①纳入文献数量较少,且只有2篇文献为多中心研究,6篇文献提到了随机方法,3篇文献提及盲法,6篇文献未采用分配隐藏;②纳入的8篇文献当中,除2篇文献[13,14]样本数超过100例外,其余均为小样本研究;③研究对照组的处理方法不一且纳入研究较少,故未能进行亚组分析,导致研究间具有异质性;④大多数研究未能对性别、是否吸烟及癌症的分期进行亚组分析;⑤未能对研究发表潜在偏倚。以上局限性均对研究结果产生一定影响,仍需样本数量更大、质量更高的临床随机对照试验来对结果进行进一步论证。

