不锈钢酸洗废水蒸发结晶渣中铁镍铬的分离与回收
李衍林 李旻廷 魏 昶 李兴彬 邓志敢
(1.云南驰宏锌锗股份有限公司,云南 曲靖 655011;2.昆明理工大学 冶金与能源工程学院,昆明 650093)
不锈钢因其优良的耐腐蚀性和良好的外观而被广泛应用。酸洗是不锈钢生产加工过程必不可少的环节[1]。一般,首先用硫酸除去表面的氧化铁皮,然后用硝酸和氢氟酸混酸进行酸洗。随着酸洗过程的进行,酸洗液中游离酸越来越少,反应生成硫酸盐越来越多。当酸洗液中金属浓度达到50~60 g/L时,金属盐将从酸洗液中结晶析出,此时就必须清洗或更换酸洗槽[2]。因此,酸洗废水中含有大量Fe2+及游离酸,同时含有少量Cr3+、Ni2+、Mn2+等。该酸性废水是对环境污染严重和对人类危害大的工业废水之一,必须对其进行处理。
目前国内外主要有三类处理方法:1)单纯酸回收技术[3-5],如扩散渗析法、双极膜电渗析法、蒸发法、树脂吸附法等;2)金属离子回收技术[6-9],主要是选择性沉淀法、析晶法;3)酸和金属离子联合回收技术[10-13],如热解法、纳滤—结晶法等。不管采用何种工艺,酸性废水回收再生后均形成两种产物,一种是脱除大部分重金属的处理后液,处理后液或排放或返回循环使用;另一种是重金属的浓缩产物(称为“盐泥”),通常含镍、铬等金属,被认为是危险废物。由于该盐泥中硫酸亚铁产品纯度低、杂质含量高,不能直接作为产品对外销售,盐泥的堆存将对环境造成潜在的威胁;另一方面,作为危废处置时,由于处置费用较高,给企业带来了巨大的经济压力。因此,必须对盐泥进行进一步处理,以实现盐泥的资源化利用或无害化处理。
目前,关于该蒸发结晶渣中铁和镍的分离回收处理鲜有报道。张克宇等[14-15]采用结晶的方法处理钛白副产物—硫酸亚铁,通过多次溶解结晶后,制备得到了符合国标 GB/T664—2011《化学试剂七水合硫酸亚铁》要求的硫酸亚铁产品。但该研究并不涉及其他有价金属(如镍、铬等)的综合回收。马保中等[16]对不锈钢酸洗废水有价组分进行梯级分离、钙以硫酸钙晶须形式回收。结果表明,铁、镍和铬的选择性沉淀率均超过99.9%,再生硝酸浓度超过143 g/L,硝酸再生率超过95%。
本研究对象蒸发结晶渣是不锈钢硫酸酸洗废水采用减压蒸发的方法处理后得到的一种含铁、镍、铬、锰等硫酸盐的混合结晶物。针对该结晶渣中含有大量的铁和游离酸以及一定量镍的特点,将结晶渣溶解以配制接近饱和的硫酸亚铁溶液,利用同离子效应(结晶渣中含有大量的硫酸)进行冷却结晶,制备硫酸亚铁初级产品;然后再通过产品纯化,制备得到符合国标GB/T 10531—2016 Ⅱ类要求的水处理剂硫酸亚铁产品。上述处理实现了大部分铁与镍铬等的分离,为后续镍的回收创造了较好条件,得到的结晶母液用于后续镍的回收。本文重点研究硫酸亚铁产品的制备,考察结晶温度、时间、初始铁浓度和结晶方式对硫酸亚铁结晶效率和纯度的影响。
1 实验
1.1 实验原料及试剂
实验原料为某钢铁企业的硫酸酸洗废水通过减压蒸发后得到的结晶渣,其主要成分见表1。从表1可知,结晶渣含铁23.27%、镍0.5%、锰2.31%、游离硫酸含量达到8.65%,结晶渣中的铁和镍具有一定的回收价值。结晶渣中的铁主要以FeSO4·2H2O形式存在。

表1 实验原料的主要化学成分
实验试剂包括去离子水、NaOH、硫酸、盐酸、磷酸、重铬酸钾、氯化汞、氯化亚锡、二苯磺酸钾,试剂均为分析纯。
1.2 实验原理
KOBYLIN等[17]研究了硫酸亚铁在不同温度下的结晶物相及溶解度,对硫酸亚铁的冷却结晶而言,当温度低于56.6 ℃时,对应的平衡固相主要为FeSO4·7H2O;而当温度高于56.6 ℃时,对应的平衡固相主要为FeSO4·H2O。同时,当温度为64 ℃时,此时对应的硫酸亚铁溶解度最大。因此,本文结晶渣溶解实验温度恒定在64 ℃。
为实现铁与镍铬的分离,在结晶过程中,期望硫酸亚铁尽可能多地结晶析出,而镍铬等组分尽可能留在结晶母液中。为实现上述目标,必须了解不同金属硫酸盐在不同温度下的溶解度。铁、镍、铬、锰等金属硫酸盐的溶解度见表2。
由表2可知,铁、镍、铬、锰等硫酸盐的溶解度存在一定差异。在温度低于60 ℃时,硫酸亚铁溶解度随温度升高而增加;当温度大于60 ℃时,其溶解度逐步增加。而硫酸镍溶解度随温度升高而增加。硫酸锰溶解度随温度先增加后降低,在20~30 ℃时达到最大。常温下,硫酸铬(Ⅲ)溶解度较大,这对抑制铬进入硫酸亚铁晶体是有利的。实验原理就是利用不同温度下各金属硫酸盐的溶解度差,差值越大,越有利于控制硫酸亚铁中镍、铬、锰等杂质含量。
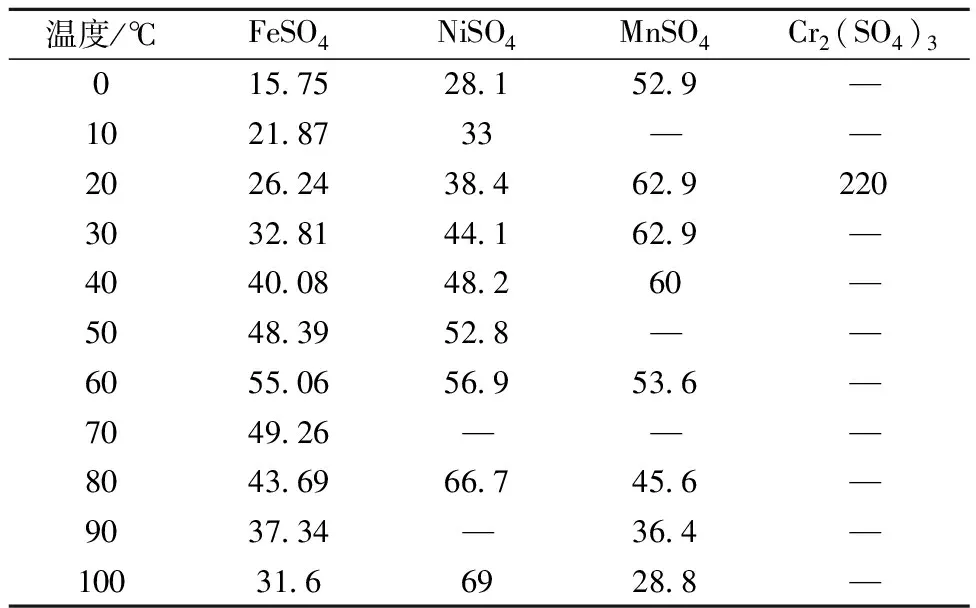
表2 几种金属硫酸盐的溶解度
采用溶解—结晶的方法来分离结晶渣中铁和镍铬等,主要分为溶质的溶解过程和结晶析出过程。溶解过程是在一定条件下将结晶渣中的可溶物质溶解在水中,并结晶或达到饱和。冷却结晶过程依据溶质在不同温度溶剂中溶解度的不同,通过控制温度,使溶质结晶析出,从而达到分离结晶渣中铁和镍铬的目的[14]。
1.3 实验方法
1.3.1 硫酸亚铁初级产品制备
1)结晶渣溶解
采用溶解平衡法配制接近饱和的硫酸亚铁溶液。在2 L烧杯中用一定量的水溶解结晶渣,然后升高溶液温度至64 ℃,此后,每间隔1 h,取样分析溶液中的铁。当铁浓度接近平衡时,则溶液接近饱和,确定此时溶解过程的液固比。
2)硫酸亚铁初级产品制备
结晶过程的设备为低温恒温反应浴(DFY-5/40,上海保玲仪器设备有限公司)。将已制备好的接近饱和的硫酸亚铁溶液冷却至30 ℃,恒温1 h,为Ⅰ段结晶,液固分离后得到30 ℃时的硫酸亚铁结晶;Ⅰ段结晶母液继续冷却到5 ℃,恒温1 h,即为Ⅱ段结晶,液固分离后得到5 ℃时的硫酸亚铁结晶及结晶母液。30、5 ℃的产物均为硫酸亚铁初级产品。对实验所得的液体样和固体样进行成分分析,计算硫酸亚铁纯度、杂质含量及结晶率。
在硫酸亚铁初级产品制备过程中,考察初始铁浓度的影响时,控制不同的溶解液固比,以制备得到不同Fe浓度的溶液,供后续实验使用。
1.3.2 硫酸亚铁初级产品纯化
将硫酸亚铁初级产品进行纯化实验,纯化过程采用溶解再结晶工艺,结晶过程分为Ⅰ段和Ⅱ段,其结晶温度分别控制在30 ℃和5 ℃、结晶时间均为1 h。纯化后的产物即为七水硫酸亚铁。
1.3.3 镍铬锰回收
将结晶母液蒸发浓缩到体积减少50%,然后在-20 ℃下冷冻结晶1 h,冷冻后液用NaOH溶液中和至pH值为10.5,过滤后得到中和渣和中和后液;中和渣洗涤后得到的洗渣即为含镍沉淀物。将洗水和中和后液混合后进行除氟,加入石灰乳进行除氟,液固分离后得到除氟渣和除氟后液。对除氟后液进行蒸发后可得到硫酸钠产品。工艺流程如图1所示。
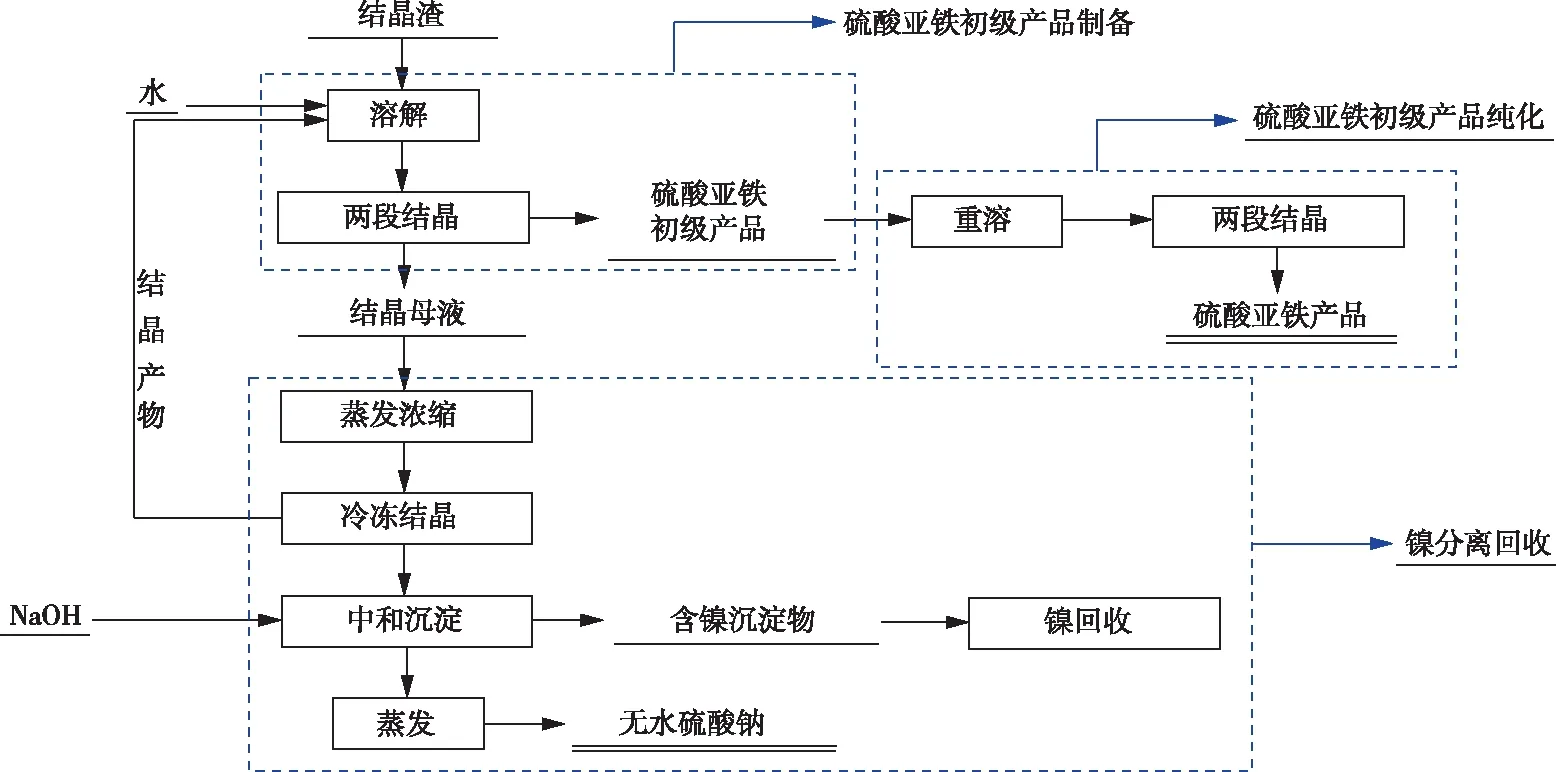
图1 结晶渣处理工艺流程
1.4 分析方法
实验过程液样中元素的浓度采用火焰原子吸收光谱(AAS)(WFX-320型火焰原子吸收光谱仪,北京瑞利分析仪器公司)进行分析。硫酸亚铁产品的分析采用国标GB/T 10531—2016方法。原料XRD采用X射线衍射仪(TTR18kW 铜靶X射线衍射仪,日本理学公司)进行分析。
2 结果与讨论
2.1 硫酸亚铁初级产品制备研究
2.1.1 结晶渣溶解
在一定的体系中,硫酸亚铁的溶解度是一定的。为实现溶解后液中铁的高效结晶,必须配制接近饱和的硫酸亚铁溶液。硫酸亚铁在64 ℃时的溶解度最大。因此,在64 ℃的条件下研究了结晶渣的溶解行为。实验结果如图2所示。

图2 实验原料溶解后液中铁浓度与时间的关系
从图2可知,溶解1 h后,铁浓度为110 g/L,此后继续延长溶解时间,铁浓度变化并不明显,表明溶液中铁浓度接近饱和。因此,后续实验中盐泥溶解后的铁浓度控制110 g/L左右。在此条件下制备了50 L溶解后液作为后续实验料液,主要成分(g/L):TFe 114.2、Ni 2.59、Cr 2.88、Mn 7.57、H2SO449.20。
2.1.2 结晶温度的影响
温度是影响硫酸亚铁结晶过程最重要的因素之一,决定着硫酸亚铁结晶效率,同时对硫酸亚铁结晶中杂质含量也有重要的影响。因此,在初始铁浓度114.2 g/L、时间60 min、搅拌转速300 r/min的条件下,考察了结晶温度对结晶后液中金属浓度的影响,结果如图3所示。
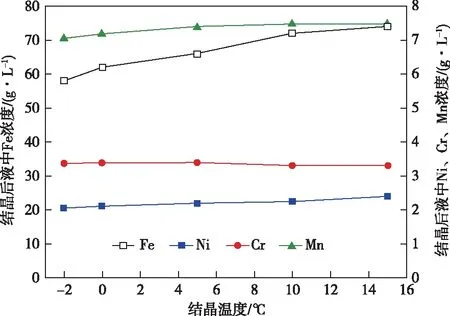
图3 结晶温度对结晶后液中金属浓度的影响
图3表明,结晶温度对溶液中离子浓度影响较大,结晶后液中铁浓度从—2 ℃时的58 g/L提高至15 ℃时的74 g/L。表明,随着结晶温度的升高,结晶后液中铁浓度升高,铁结晶效率降低。与结晶前相比,结晶后液中镍和锰的浓度降低,表明结晶过程中,镍和锰会结晶析出(或者机械夹带);而结晶后液中铬浓度增加,表明铬的结晶量较少,即铬在结晶后液中有富集趋势,这对控制硫酸亚铁晶体中铬含量是有利的。因此,对硫酸亚铁的结晶析出过程而言,要尽可能控制较低的结晶温度,以提高结晶效率;但结晶温度越低,杂质金属,如镍、铬、锰等进入硫酸亚铁的量将会增加。为此,需要对结晶效率与产品杂质含量进行综合考虑,以确定结晶温度。从表3可知,当结晶温度在-2~15 ℃时,铁结晶效率从57.52%逐渐降低至45.74%,结晶所得硫酸亚铁晶体的纯度从91.34%逐步升高至93.58%。基于结晶效率和纯度两方面考虑,结晶温度控制在5 ℃较为适宜。
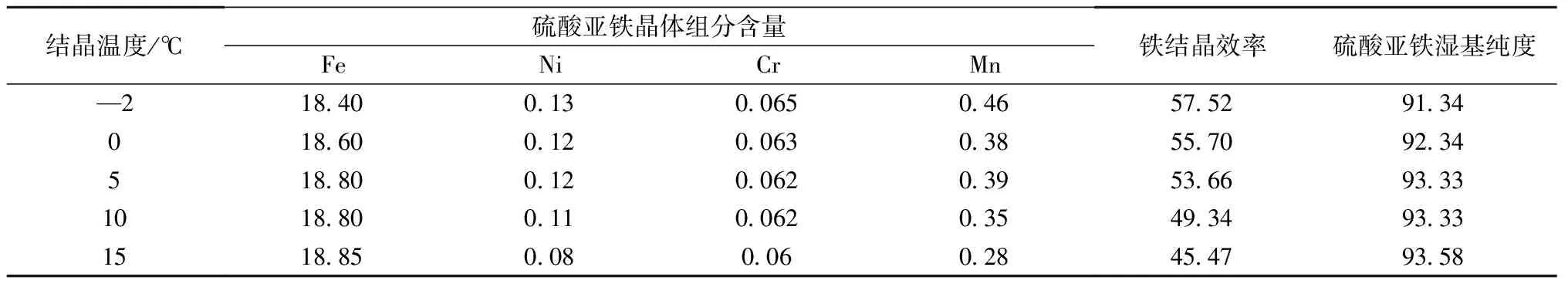
表3 结晶温度对硫酸亚铁中杂质含量及纯度的影响
2.1.3 结晶时间的影响
在结晶温度5 ℃、初始铁浓度114.2 g/L、搅拌转速300 r/min的条件下,考察了结晶时间对结晶后液中金属浓度的影响,结果如图4所示。从图4可知,结晶时间对硫酸亚铁的结晶效率影响不大。当结晶时间超过10 min后,结晶后液中Fe、Ni、Cr、Mn浓度变化并不明显,铁浓度从1 min时的67.6 g/L降低至120 min时的65.8 g/L。故此,为保证铁的结晶效率,后续实验中时间控制在30 min。在晶体的生长过程中,待结晶物质从液体本体中心向晶体表面扩散,并在晶粒表面吸附、沉积。晶核生长速率的快慢直接影响到杂质离子在晶粒表面沉积的快慢,进而影响提纯的效果。而当稳定晶核形成后,其生长速率主要由温度和溶液过饱和度控制,一方面饱和度越大晶核生长速率越快;另一方面随温度升高晶核生长速率亦随之增大[18]。
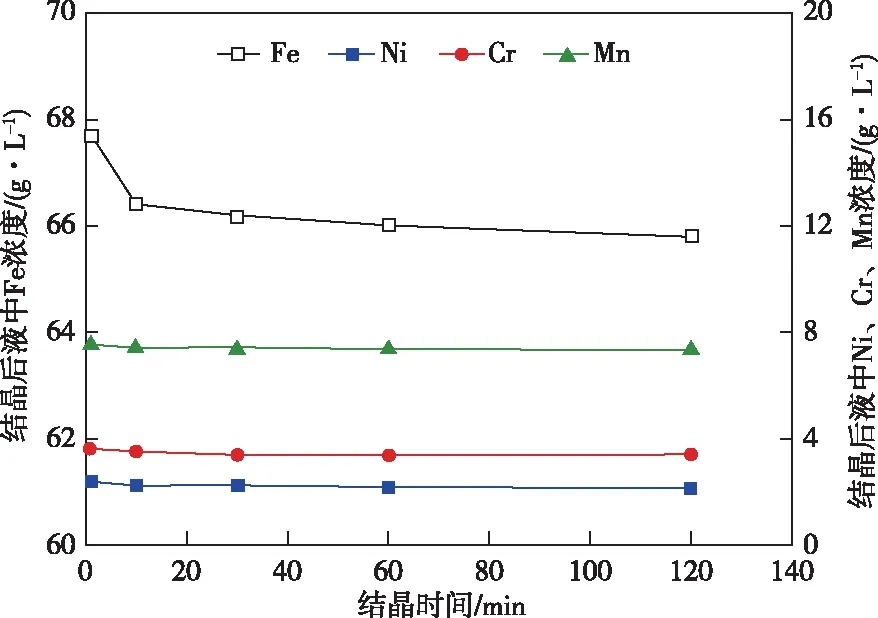
图4 结晶时间对结晶后液中金属浓度的影响
结晶时间对硫酸亚铁结晶效率和纯度的影响见表4。由表4可知,随着结晶时间的延长,硫酸亚铁结晶效率和湿基纯度均略有增加,但增加幅度并不明显。

表4 结晶时间对硫酸亚铁结晶效率及纯度的影响
2.1.4 初始铁浓度的影响
初始铁浓度是影响硫酸亚铁结晶效率的另一个重要因素,也对硫酸亚铁结晶纯度有一定的影响。因此,在初始铁浓度分别为100、109、123、134 g/L、恒温时间30 min、控制搅拌转速为300 r/min的条件下,考察了初始铁浓度对硫酸亚铁结晶效率及纯度的影响,实验结果如图5和表5所示。

图5 初始铁浓度对结晶后液铁浓度和硫酸亚铁纯度的影响

表5 初始铁浓度对硫酸亚铁结晶效率和湿基纯度的影响
图5和表5数据表明,初始铁浓度对结晶滤液铁浓度、结晶效率、硫酸亚铁纯度影响较大。随着初始铁浓度的增加,结晶后液中铁浓度呈逐渐降低的趋势,结晶效率呈逐渐升高的趋势,说明初始浓度越高,结晶过程中析出的硫酸亚铁晶体越多。在123 g/L时总结晶率达到71.5%,之后增长速率下降,在134 g/L达到76%。硫酸亚铁产品的纯度随着初始浓度略有降低的趋势。综合硫酸亚铁纯度、结晶效率、杂质含量等因素,初始铁浓度确定为120 g/L左右。
2.1.5 结晶段数的影响
在初始铁浓度121.5 g/L、时间30 min、搅拌转速300 r/min的条件下,考察了结晶段数对硫酸亚铁结晶效率、结晶后液中金属浓度、硫酸亚铁湿基纯度的影响,实验条件和结果见表6和表7。由表7可知,当Ⅰ段结晶温度为35 ℃时,硫酸亚铁结晶效率为18%左右,而当结晶温度降低至30 ℃时,硫酸亚铁结晶效率提高至27%,此时两段总的结晶效率为66.39%,相比一段结晶时54%(表3)的结晶效率而言,提高了12个百分点。这表明,采用两段结晶,有利于提高铁的结晶效率,有利于铁与镍铬的分离。

表6 结晶段数过程的实验条件
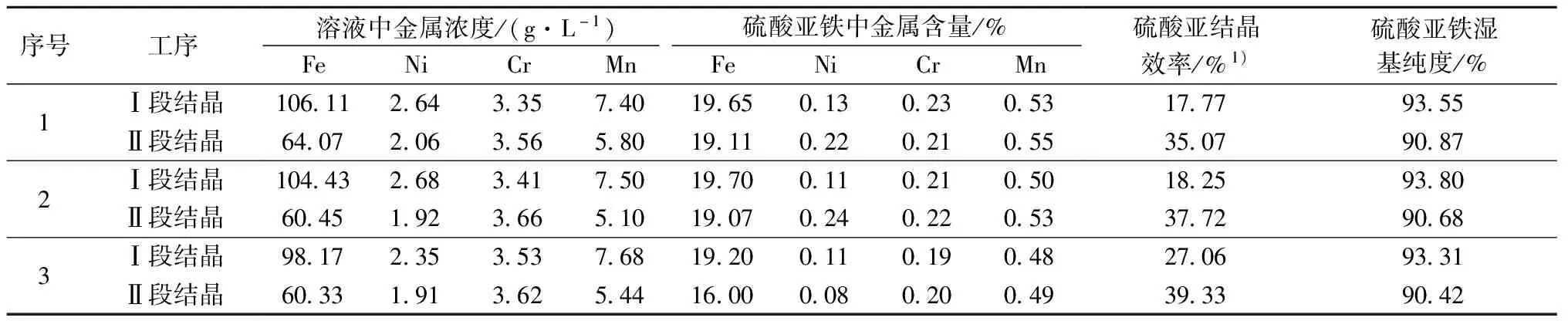
表7 结晶段数实验结果
2.2 硫酸盐亚铁初级产品纯化研究
上述研究虽然实现了结晶渣中大部分铁与镍铬锰的分离,并制备得到了硫酸亚铁初级产品,其湿基纯度可达93%以上,但该产品中杂质含量较高,尤其是Cr含量高,不能直接作为产品对外销售。针对这一问题,开展了产品纯化实验研究,目的是获得满足GB/T 10531—2016要求的产品。实验结果如表8和表9。

表8 纯化(重溶—结晶)实验结果
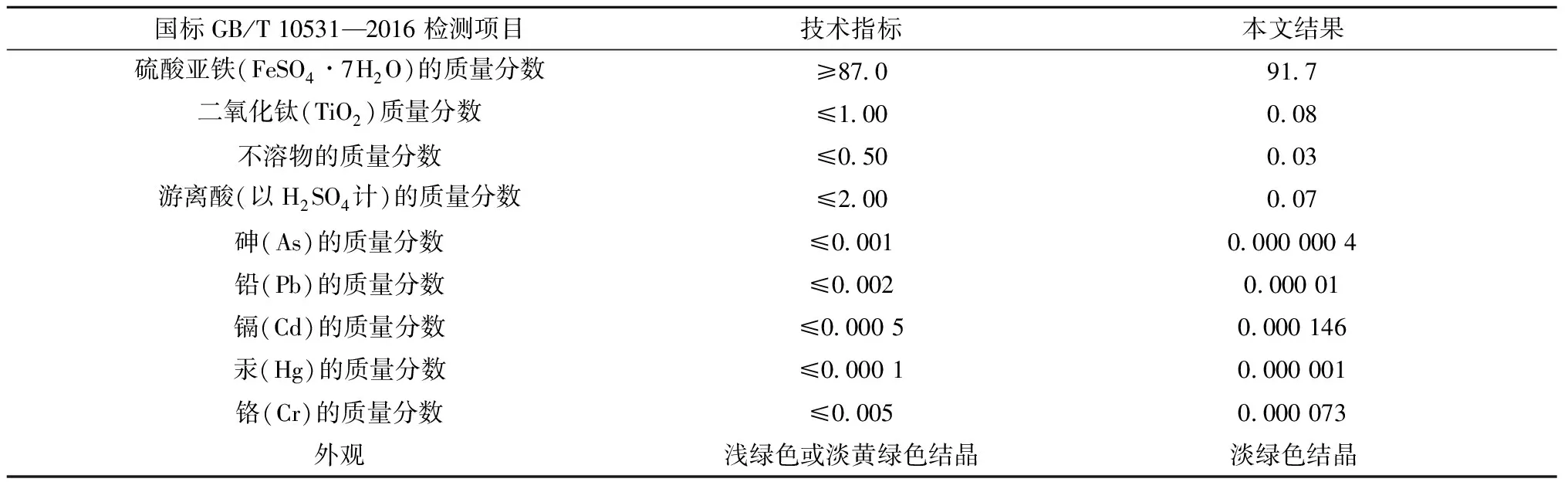
表9 纯化后Ⅱ段结晶物产品质量检测结果
从表8和表9可知,硫酸亚铁初级产品通过重溶—两段结晶的纯化处理后,不管是Ⅰ段还是Ⅱ段结晶产物中,Cr含量大幅度降低。其原因在于,Cr2(SO4)3在30 ℃和5 ℃时的溶解度远高于硫酸亚铁,但在这两个温度下Cr2(SO4)3并不结晶析出,仅有少量夹带进入硫酸亚铁晶体中。因此,通过重溶—两段结晶的纯化处理后,硫酸亚铁产品质量可以达到GB/T 10531—2016 Ⅱ类产品要求。与此类似,张克宇等[14-15]采用结晶法处理钛白副产硫酸亚铁,采用多次结晶处理,获得了符合国标GB/T 664—2011《化学试剂七水合硫酸亚铁》的产品。
2.3 镍、铬的回收研究
通过溶解—结晶—纯化处理实现了大部分铁与镍、铬的分离,但结晶母液中铁浓度较高(68 g/L,表8),镍的回收困难,必须进一步对母液进行处理。采用蒸发浓缩—冷冻结晶的方法对其进行处理,实验结果见表10。
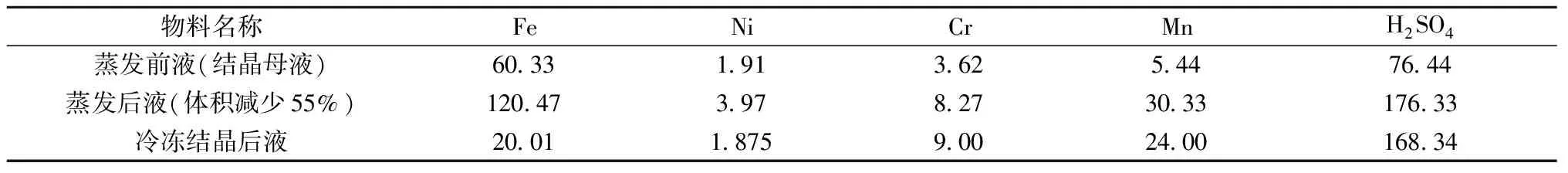
表10 结晶母液蒸发浓缩—冷冻结晶实验结果
对冷冻后液进行了中和沉淀—蒸发制备硫酸钠的实验,得到了含镍4%左右的沉淀物,该沉淀物可作为镍回收的原料,其主要成分(%):Fe 6.67、Ni 4.13、Cr 9.98、Mn 10.79、F 5.04、S 3.85。可以看出,中和沉淀物中,镍含量达到4.13%,与实验原料中镍含量0.5%相比,富集倍数为8倍,镍回收率为53%,其余的镍分散损失在硫酸亚铁产品中。该中和沉淀物可作为硫化镍精矿造锍过程的配料使用。中和沉淀后液通过除氟后,进行蒸发结晶,制备得到无水硫酸钠产品,产品指标如表11。
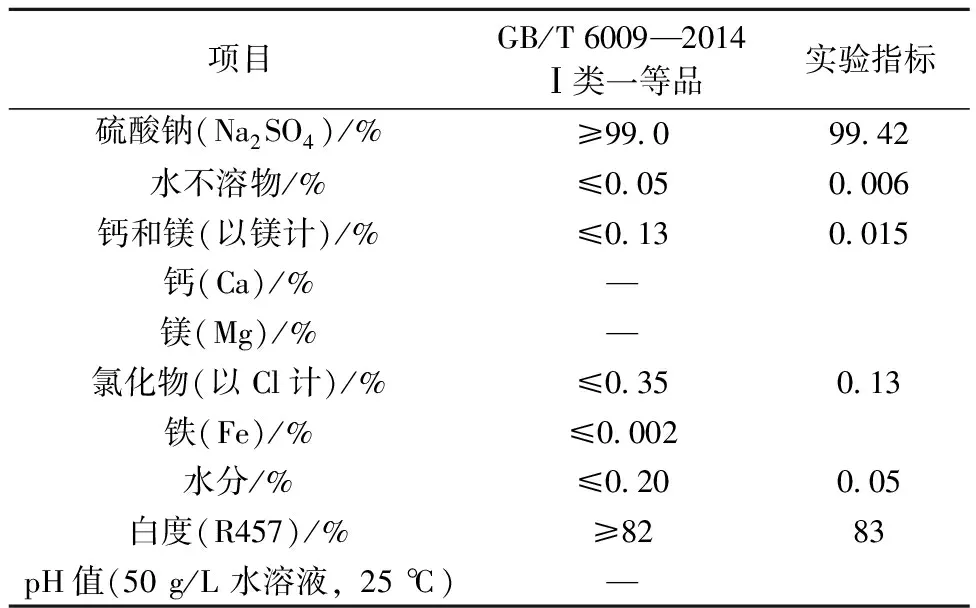
表11 硫酸钠产品质量
3 结论
1)采用溶解—结晶—纯化工艺流程,能够实现不锈钢酸洗废水蒸发结晶渣中铁与镍、铬的分离,制备得到符合GB/T 10531—2016 Ⅱ类产品要求的硫酸亚铁。
2)硫酸亚铁的结晶效率随着结晶温度的降低和初始铁浓度的增加而升高,但其纯度呈现相反的规律。在溶解温度64 ℃、Ⅰ段和Ⅱ段结晶温度分别为30、5 ℃、Ⅰ和Ⅱ段结晶时间均为30 min、搅拌转速300 r/min的条件下,硫酸亚铁结晶效率可达66.39%,其湿基纯度为93%。
3)结晶母液通过蒸发浓缩—冷冻结晶—中和沉淀—蒸发制备硫酸钠,可获得含镍4%的提镍原料,以及GB/T 6009—2014 Ⅰ类一等品的无水硫酸钠产品。

