超声评估不同钙化程度对甲状腺结节良恶性鉴别的影响
沈 艳
(涟水县人民医院超声科 江苏 涟水 223400)
甲状腺结节属于临床常见疾病之一,指的是甲状腺体内出现结构异常、局部硬化组织,严重影响患者的日常生活与健康。女性患病率略高于男性,且随着年龄的增长,甲状腺结节患病率同比升高[1]。甲状腺结节多数为良性结节,仅5%~15%患者为恶性结节,但近几年研究发现,甲状腺结节恶变率升高,及时鉴别诊断甲状腺结节良恶性对疾病治疗及患者预后均有重要价值。随着医疗水平的提高,超声技术逐渐发展并完善,广泛用于疾病的鉴别诊断中。长时间研究发现,通过超声评估甲状腺结节患者不同钙化程度,可初步鉴别良恶性,具有较高的准确性,倍受认可[2]。本文针对2018年4月—2021年2月我院门诊接诊的64例甲状腺结节患者为例,分析甲状腺结节不同钙化程度患者良恶性情况,内容具体如下。
1 资料与方法
1.1 一般资料
选取2018年4月—2021年2月我院门诊接诊治疗的甲状腺结节病患64例观察分析,所有患者均接受超声诊断,其中30例患者表现为微钙化程度,包括男性病患9例,女性病患21例,年龄20~74岁,平均年龄(45.4±1.4)岁,病程4~21个月,平均病程(13.8±1.1)个月;19例患者表现为环状钙化程度,包括男性病患7例,女性病患12例,年龄21~75岁,平均年龄(45.5±1.6)岁,病程3~22个月,平均病程(13.9±1.2)个月;15例患者表现为粗钙化程度,包括男性病患4例,女性病患11例,年龄20~75岁,平均年龄(45.7±1.5)岁,病程4个月~23个月,平均病程(14.0±1.3)个月。
1.2 方法
所有患者均接受超声诊断,使用彩色多普勒超声诊断仪(ACVSON X600),调整患者体位至仰卧位,叮嘱患者头略向后,保证颈部充分暴露,使用高频探头平扫,设定参数为7.5 MHz~12.0 MHz,记录患者结节大小、位置、形态、边界及内部钙化程度。
1.3 观察指标
根据临床诊断判断患者结节良恶性,并对比超声评估钙化结果,分析不同钙化程度患者恶性结节检出率。
1.4 统计学分析
通过SPSS 26.0完成统计学处理分析,计数资料采取率(%)表示,计量资料采取()表示,分别利用卡方、t值检验,P<0.05反映差异存在明显统计学意义。
2 结果
30例微钙化程度甲状腺结节患者确诊恶性患者28例,19例环状钙化程度甲状腺结节患者确诊恶性患者14例,15例粗钙化程度甲状腺结节患者确诊恶性患者9例,微钙化甲状腺结节患者恶性率显著高于其他钙化程度患者(P<0.05),见表1。
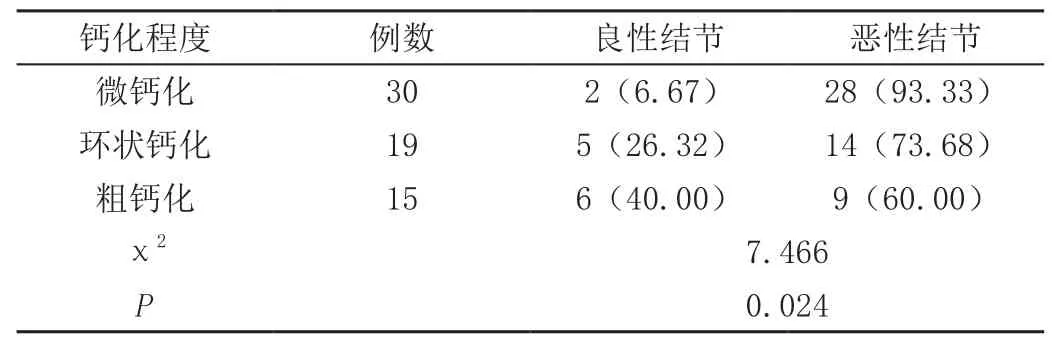
表1 不同钙化程度良恶性结节概率[n(%)]
3 讨论
甲状腺结节属于甲状腺组织发病率较高的病变之一,其即为局部组织结构异常,使其硬度明显高于周围其他组织。根据临床大数据调查显示,我国甲状腺结节患者群体中女性多于男性,且随着年龄的增加,甲状腺结节的发病率也会明显提升[3]。患者中超过85%者为良性病变,而恶性甲状腺结节发病率仅为5%~15%,如确诊为恶性甲状腺结节,则需采取外科切除手术方式进行治疗,而良性病变通常不推荐手术。因此,为了有效降低不必要的手术操作,也为了控制术后并发症概率,就需要准确判断甲状腺结节的性质,并根据实际情况制定合理的、针对性的治疗方案。但实际情况下,恶性甲状腺肿瘤具有较高的隐匿性,且自身生物学特征也具有变化性,其中部分特征和良性病变也存在交叉的情况,因而导致现有的诊断技术均存在一定程度上的误诊概率[4]。
临床评估甲状腺结节性质时主要选择超声影像学技术和细针活检,其中细针活检是利用细针穿刺的方式进入甲状腺,再对甲状腺病灶组织进行多点采集,而后通过细胞学检验方式确定病灶所属状态,该诊断方式的准确率最高,也被认定为肿瘤类疾病诊断的“金标准”,但由于其属于有创诊断技术,加之甲状腺距离头部过近,使得大多数患者从心理层面抵触这种检查方式[5]。超声影像学技术则属于无创性诊断方式,临床常用方式包括B超、CT、磁共振、核素扫描等,其中CT、核素扫描等方式虽然成像更加清晰,但拥有较高的辐射量,因此存在禁忌人群,而辐射较低的磁共振、PET成像技术则医疗成本较高。超声属于最早应用在临床诊断工作中的技术之一,其在实际应用时完全没有辐射问题,且临床研究证明对甲状腺结节病灶具有较高的敏感性,近似100%,对直径在1~2 mm的病灶也可探查,而对于直径超过2 mm的病灶敏感性超过CT、磁共振等技术,加之该诊断手段医疗成本相对较低,因此将其作为评估甲状腺结节病变的首选技术[6]。
随着超声技术的不断发展,将其应用在临床时可发现直径在1 mm左右的微小型病灶,并可用于评估结节、肿瘤等病灶内的钙化情况、血流情况等。病灶钙化主要是由发生病变的组织内、细胞内的钙盐沉积所产生的,因病变组织的生理功能发生障碍,因此导致细胞内、细胞间液当中所含有的钙盐无法正常代谢,继而发生沉积情况。在超声影响下可见,良性结节的病灶内无钙化征象,或仅具有微钙化情况,征象为点状,这种微钙化灶的本质为胶质结晶体。需要注意的是,超声影像对于胶质结晶体的表现存在一定的差异,其中大部分表现为点状的强回声,而如病灶内具有囊性成分,则会发现彗星拖尾的征象[7];如病灶为囊室性,则其边缘的清晰度相对较低,或偏实性结构,因而鉴别难度进一步提升。根据临床大数据统计指出,胶质结晶体沉淀通常在多发型甲状腺结节中出现,而单发型病灶内较为罕见,且需进一步注意海绵样结节当中可能存在的微小型囊肿回声。利用超声技术还可对细针活检操作进行引导,从而更加准确地寻找到甲状腺结节的病灶位置。恶性结节病灶内出现钙化的原因和癌细胞异常增生有着密切联系,癌细胞不断增殖就导致组织出现过度增生的情况,挤压细胞导致细胞破裂,使内部的钙盐物质大量流入组织内,同时病灶本身也可分泌一定的钙化物质,包括糖蛋白等,可捕捉钙盐,从而加剧钙化的进程。
现代临床研究发现,良性结节和恶性结节内的钙化机制具有差别,其中恶性结节的增殖速度更快,因此钙化征象出现的相对较早;良性结节由于增殖速度缓慢,因而钙化病灶通常会在发病后较长时间后方可检查出,因此甲状腺结节内钙化程度和病灶性质具有一定联系,可用于评估良恶性。但需要注意的是,临床并未形成统一的标注,用以衡量病灶钙化程度和良恶性[8]。超声检查下如钙化病灶直径低于1 mm,则将其归为微钙化,而含有微钙化灶的恶性结节的检出率要高于环状钙化灶,而环状钙化灶和粗钙化灶恶性检出率间无明显差异,因此可将微钙化灶作为判断病灶是否恶化的可靠指标。但需要注意的是,如病灶内存在环状钙化灶、粗钙化灶,也不能立即判定为良性结节,需将其归为疑似恶性病变内,并开展进一步的准确检查,以确保控制误诊和漏诊的概率。由此可见,甲状腺病灶内钙化情况可作为判断其良恶性的重要指标,尤其是微钙化灶的准确率相对较高,而其他分型则不能作为特异性指标,但可用于诊断的临床参考。同时需要注意的是,为最大程度提升临床检查的准确率,在未发现微钙化灶时需综合多方面指标共同参考,不能单纯以钙化情况作为最终诊断标准。

