穿戴式动态心电图记录仪在心房颤动筛查中的应用
傅文霞,陈力秀,乐佳玮,李若谷,2
1.上海市胸科医院/上海交通大学附属胸科医院心功能室,上海 200030;2.上海市胸科医院/上海交通大学附属胸科医院心内科,上海200030
心房颤动(atrial fibrillation,AF)是最常见的心律失常,目前已成为全球重大的公共卫生问题之一[1]。2014年Circulation公布的2010年全球疾病负担数据显示,全球AF患病率为0.5%[2]。国内首个大型AF流行病学调查结果显示,中国AF总患病率为0.77%,阵发性AF患病率为0.26%[3]。中国AF患者超过800万,且发病率随年龄增长而明显上升[4]。由于AF患者的检出率和知晓率均较低,很多患者在经历卒中等不良事件后才意识到自己患有AF,启动抗凝治疗,造成了医疗卫生资源的更多消耗,产生了巨大的社会经济负担[5]。因此,早期筛查、识别隐匿性AF显得尤为重要。本研究为单中心前瞻性注册自身对照研究,拟比较国产穿戴式动态心电图(electrocardiogram,ECG)记录仪与12导联ECG的性能,以及在不同体位及运动后验证穿戴式动态ECG记录仪对于检测AF的有效性及安全性,为院外AF筛查及管理提供可靠的无创筛查手段。
1 对象与方法
1.1 研究对象
纳入自2020年6月24日至7月24日就诊于上海市胸科医院门诊并同时行ECG检查的受试者116例。入选标准:年龄>18岁;经评估后可配合试验。排除标准:不能配合检查;身体状况不能满足本临床研究的要求;存在严重的上肢动脉闭塞或者缺血;体内植入心脏起搏器、除颤器或其他电子设备;已经登记入选其他可能影响本研究的临床研究。最终入选114例(其中2例中途撤回知情同意书)。记录受试者人口学特征、既往史及用药史等基本信息。本研究是一项前瞻性注册自身对照研究(NCT04462653),经上海市胸科医院伦理委员会批准(审批号:LS2035)。受试者均签署知情同意书。
1.2 图像采集
图像采集设备由腕带、心电记录仪、嵌入式软件(安装在心电记录仪上)、手机应用(Amazfit CardiDoc程序)、充电线组成。受试者平静呼吸,体位采用仰卧位,通过12导联ECG记录,根据12导联ECG结果判定是否为AF。为了保证研究结果的一致性,统一将穿戴式动态ECG记录仪的腕带佩戴在左手腕(在手机程序中进行预置)。受试者分别采取仰卧位、站立位佩戴穿戴式动态ECG记录仪1 min,爬3层楼后佩戴穿戴式动态ECG记录仪站立1 min,最后采用12导联ECG重新记录受试者心电图。受试者将右手示指放在穿戴式动态ECG记录仪的触摸按钮上,并以足够的力度按下,以确保在整个记录过程中电极传感器与左手腕皮肤接触。这个过程模拟肢体导联Ⅰ导联。穿戴式动态ECG记录仪的ECG被实时传输到Amazfit CardiDoc应用程序和云服务器,并使用互联网服务器上的人工智能(artificial intelligence,AI)算法进行评估。AI采用深度卷积神经网络(SEResNet),训练21 618个标记心电图(4 734个为AF病例)和8 518个标记心电数据源(241个为AF病例)的测试集,开发出RealBeats人工智能生物数据引擎(Huami Technology)。测试集的灵敏度和特异度分别为93.36%和99.75%。
1.3 图像分析
将12导联ECG结果作为金标准。12导联ECG的结果由2位有3年以上工作经验的心电图医师诊断为“非AF”“AF”或“无法判断”。通过穿戴式动态ECG记录仪记录完成后,软件自动保存心电数据,同时通过AI算法给出的诊断为“非AF”“AF”或“无法判断”(信号质量不佳,或者不能满足做出判断的要求,则输出“无法判断”)。如果与电极接触并采集信号的过程中断开,记录停止,则需要重新启动。
1.4 临床评价标准
1.4.1 有效性评价标准
(1)主要终点 完成检测后,分别统计AF、非AF或无法判断的病例数,然后对结果进行一致性评价;如果95%CI下限高于临床可接受的最低一致率(80%),则认为产品可靠性可以接受。
(2)次要终点 根据有效的临床研究结果,进行灵敏度、特异度、阳性预测值和阴性预测值的计算。
1.4.2 安全性评价标准
(1)不良事件 记录临床研究过程中发生的不良事件和严重不良事件,并判定不良事件和严重不良事件是否与测试器械有关。不良事件与测试用器械的关系,分为“无关”“可能无关”“肯定有关”“可能有关”“无法判定”。
(2)器械缺陷 记录临床研究过程中测试用器械出现的问题,如不能佩戴、无结果输出、信号干扰等,评价测试用器械使用的可靠性和稳定性。
1.5 统计学分析
按照《医疗器械临床试验质量管理规范》(食品药品监督管理总局2018年第6号文)的相关要求,经临床研究机构和申办方共同讨论,采用配对试验设计。根据公式
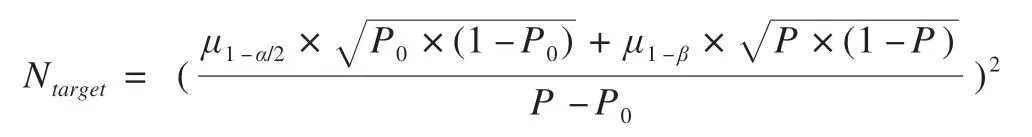
计算样本量。其中双侧采用α=0.05、1-β=0.8、P=90%,P0为临床能够接受的一致率,此处取80%,代入公式,共选合格受试者108例才具有统计学意义。按照5%的脱落率计算,最终需要入选受试者114例。根据《北京市第二类体外诊断试剂临床试验指导原则(2016年版征求意见稿)》中“定性测试的产品,阳性样本比例应不低于30%”,最终选择阳性AF样本54例、非AF样本60例。定量资料和定性资料分别用xˉ±s和例数(百分比)表示。定量资料根据数据分布,采用两独立样本t检验或非参数检验;定性资料采用χ2检验或Fisher精确概率法。根据AF和非AF的诊断结果,建立四格表。统计是否为AF和非AF的真阳性(true positive,TP)、真阴性(true negative,TN)、假阳性(false positive,FP)和假阴性(false negative,FN)的例数。无法分类的结果定义为“TPTN”或者“FPFN”。计算穿戴式动态ECG记录仪的AI算法判断结果与人工判断结果的匹配率,用来评价阳性结果一致性[6]。计算敏感度[TP/(TP+FN)]、特异度[TN/(TN+FP)]、阳性预测值[TP/(TP+FP)]、阴性预测值[TN/(FN+TN)]和一致性[(TP+TN)/(TP+TN+FP+FN)]。采用Wald方法确定95%CI。数据分析采用SPSS 22.0软件。P值为双侧,P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料
最终入选114例受试者(AF组53例,对照组61例)。AF组受试者年龄显著大于非AF组(P=0.000),CHA2DS2-VASc评分高于非AF组(P=0.001),合并冠状动脉粥样硬化性心脏病的比例高于非AF组(P=0.014)。2组服用口服抗凝药、抗血小板药、钙通道阻滞剂(calcium channel blocker,CCB)、利尿剂、地高辛、β-受体阻滞剂的比例差异均有统计学意义(均P<0.05),详见表1。
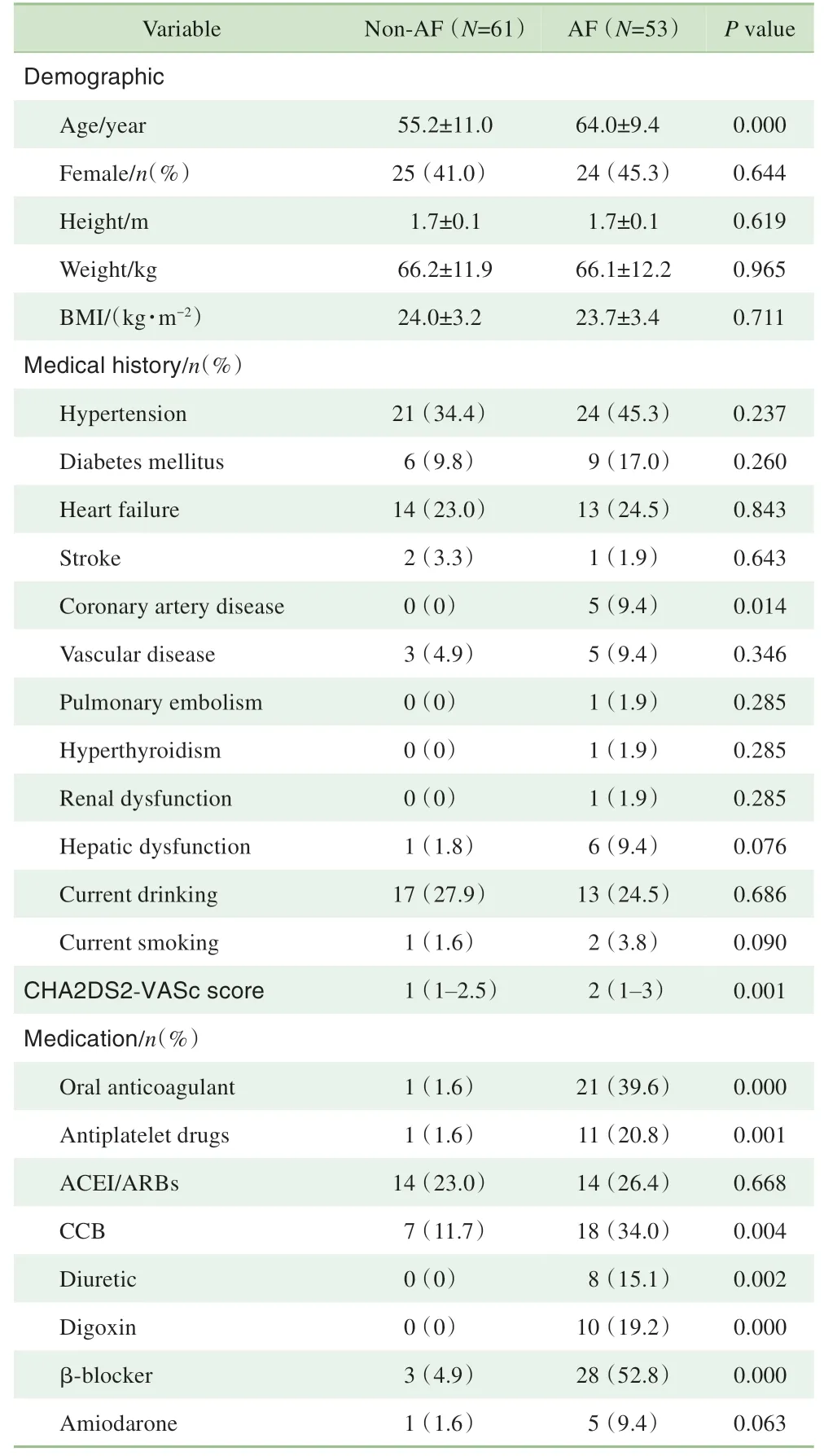
表1 2组受试者临床特点比较Tab 1 Baseline information of participants
2.2 有效性评价
2.2.1 仰卧位检测AF的有效性 根据12导联ECG采集的ECG波形确定AF 53例、非AF 61例。受试者取仰卧位,佩戴穿戴式动态ECG记录仪60 s,ECG检测由AI算法自动判定AF 47例、非AF 65例、无法判断2例。与12导联ECG比较(无法判断为TPTN),穿戴式动态ECG记录仪诊断AF的一致性为96.49%(95%CI91.03%~98.92%),灵敏度为92.45%(95%CI81.64%~97.52%),特异度为100%(95%CI92.91%~100%),阳性预测值为100%(95%CI91.32%~100%),阴性预测值为93.85%(95%CI84.78%~98.02%)。与12导联ECG比较(无法判断为FPFN),穿戴式动态ECG记录仪诊断AF的一致性为94.74%(95%CI88.76%~97.80%),灵敏度为88.68%(95%CI77.06%~95.07%),特异度为100%(95%CI92.91%~100%),阳性预测值为100%(95%CI90.98%~100%),阴性预测值为91.04%(95%CI81.48%~96.16%)。
2.2.2 站立位及运动后检测AF的有效性 受试者取站立位,佩戴穿戴式动态ECG记录仪的60 s,ECG检测由AI算法自动判定AF 50例、非AF 61例、无法判断1例。受试者走3层楼梯后,佩戴穿戴式动态ECG记录仪60 s,ECG检测由AI算法自动判定的结果与站立位完全相同。与12导联ECG比较(无法判断为TPTN),穿戴式动态ECG记录仪诊断AF的一致性为98.25%(95%CI93.43%~99.91%),灵敏度为96.23%(95%CI86.51%~99.69%),特异度为100%(95%CI92.91%~100%),阳性预测值为100%(95%CI91.63%~100%),阴性预测值为96.83%(95%CI88.50%~99.77%)。与12导联ECG比较(无法判断为FPFN),穿戴式动态ECG记录仪诊断AF的一致性为97.37%(95%CI92.21%~99.44%),灵敏度为94.34%(95%CI84.03%~98.65%),特异度为100%(95%CI92.91%~100%),阳性预测值为100%(95%CI91.48%~100%),阴性预测值为95.31%(95%CI86.57%~98.92%)。
2.3 安全性
穿戴式动态ECG使用的医疗器械属于风险管理级别较低的二类医疗器械,研究过程中未发生不良事件,亦无明显的器械缺陷。
3 讨论
近年来,国内外针对AF的治疗指南不断更新,AF的诊治水平得到明显提高,诊疗过程进一步规范。虽然部分AF患者无明显不适,但卒中、心功能不全等风险依然高于一般人群。AF可导致卒中、心力衰竭等一系列不良临床后果,具有很高的致残率和致死率[7]。卒中可能为其首发表现,若及时诊断AF并给予干预,可明显减少此类事件的发生。无症状AF多为阵发性AF,具有突发突止的特点,并且受到筛查方法的限制。因此,加强对隐匿性AF的筛查,提高检出率显得尤为重要。
目前,传统的筛查AF的方法有12导联ECG、动态ECG、脉搏触诊、植入式心电监测等方法。常规ECG可用于阵发性AF的确诊,但对于持续时间短的阵发性AF,当到达医院行ECG检查时,可能AF发作已经停止,导致未能及时发现并留下临床证据。因此,常规ECG容易受到检测空间和时间的限制,只能在医院进行检查。动态ECG延长心电监测的时程,弥补了常规ECG的不足。虽然与常规ECG相比,动态ECG提高了阵发性AF的检出率,但长时程监测影响患者的日常生活,部分患者皮肤不能耐受[8];加之受到医疗费用等经济学相关因素的影响,无法进行大规模人群筛查。在患者感觉不适时,立即进行脉搏触诊,发现异常后立即就诊,完善ECG检查,理论上可提高阵发性AF的检出率。但对普通人群来说,未经过专业培训,发现脉搏不规律较为困难。植入式心电监测设备诊断AF的敏感度和特异度均较高,但费用较高、有创伤,推广困难,严重限制了其大规模使用的可能性。因此,使用低成本可穿戴电子设备在大量健康人群中进行长期筛查和监测,具有巨大的推广潜力。
近年来多种安全、无创的AF筛查新方法应运而生,这为AF的院外筛查提供了新思路。AF治疗结合AF筛查可能会使更多患者获益。既往研究[9-15]表明,智能设备(智能手机、手持设备、手环、手表)可用于AF检测。一项家庭环境下佩戴穿戴式连续ECG贴片监测未确诊AF效果的随机临床试验(mSToPS研究)[10]结果显示,立即监测组在4个月时的AF新诊断率高于延期监测组(3.9%vs0.9%)。随访1年时,心电监测贴片组较未佩戴组新诊断AF的比例更高(6.7%vs2.6%)。该试验评价了家用可穿戴心电监测贴片对AF高危人群早期诊断的应用效果。虽然采用这类监测工具后AF检出率提高,但长期佩戴心电监测贴片的安全性及佩戴者的舒适度未提及。2019年Apple Heart研究[11]发表数据,智能手表使用光电容积描记法(photoplethysmographic,PPG)能够及时有效地发现佩戴者是否存在AF,在AF筛查中起到积极作用。但是,智能手表在老龄化加剧的中国普及性不高,且阳性预测值仅为71.3%。国内也进行了AF筛查的研究[12],该研究是基于PPG技术进行AF筛查,阳性预测值为91.6%。但是,此项研究无法提供与基于PPG的智能设备同步的实时12导联ECG数据,因为数据是在仰卧位收集的,而仰卧位并不能反映家庭筛查的实际情况,运动对PPG信号的影响较大。实际上,单导联ECG与PPG技术需要避免运动造成的干扰,以提高准确性。本研究分别采用仰卧位、站立位及运动后模拟佩戴者的日常体位和姿势,更加反映其真实状态。测试结果证实了该设备在不同状态下诊断AF结果的可靠性。
基于以上研究的优缺点,为了便于日后开展大规模AF无创性筛查,本研究采用前瞻性设计,纳入门诊受试者,而不是在复律前后进行比较[16]。本研究应用的检查仪器是国内首批将单导联ECG应用于手环的器械,穿戴方便,易于操作;且利用AI算法处理心电信号,不同体位及运动后穿戴式动态ECG记录仪能准确发现AF,特异度及阳性预测值达到100%。本研究的可穿戴式动态ECG记录仪不需要与智能手机频繁通信,从而减少了功耗,增加了持续记录数据的时间,最长可待机7 d。佩戴时不影响日常活动,而且防水,安全可靠。当应用程序检测到AF时,向佩戴者及相关亲属发送短信,及时告知其AF发作。亲属也可以及时告知老年佩戴者,促使佩戴者及时就诊,这为AF发作起到很好的预警作用。
本研究尚存在一些局限性。首先,ECG监测纳入没有症状的受试者,而不是在有症状的受试者中进行。其次,该设备仅用于鉴别AF和窦性心律,无法检测其他心律失常。在未来的研究中,我们将继续使用新的算法来识别并区分窦性心律失常和其他形式的心律失常。最后,本研究样本量较少,需要进一步在多中心大规模人群中进行AF筛查。
总之,穿戴式动态ECG记录仪具有较高的特异度及阳性预测值,且在监测到AF后可及时告知佩戴者,起到预警作用。该方法具有操作简便、准确、安全等优点,克服了传统筛查AF方法在时间、空间上的局限性,能广泛应用于社区、家庭;不仅提高了阵发性AF的检出率,也改变了既往对AF筛查的认知及AF患者的管理模式,为AF的院外筛查和管理提供了新的研究思路。
参·考·文·献
[1] Staerk L,Sherer JA,Ko D,et al.Atrial fibrillation:epidemiology,pathophysiology,and clinical outcomes[J].Circ Res,2017,120(9):1501-1517.
[2] Chugh SS,Havmoeller R,Narayanan K,et al.Worldwide epidemiology of atrial fibrillation:a Global Burden of Disease 2010 Study[J].Circulation,2014,129(8):837-847.
[3] 周自强,胡大一,陈捷,等.中国心房颤动现状的流行病学研究[J].中华内科杂志,2004,43(7):491-494.
[4] Ugowe FE,Jackson LR,Thomas KL.Racial and ethnic differences in the prevalence,management,and outcomes in patients with atrial fibrillation:a systematic review[J].Heart Rhythm,2018,15(9):1337-1345.
[5] Ball J,Carrington MJ,McMurray JJ,et al.Atrial fibrillation:profile and burden of an evolving epidemic in the 21st century[J].Int J Cardiol,2013,167(5):1807-1824.
[6] Chen E,Jiang J,Su R,et al.A new smart wristband equipped with an artificial intelligence algorithm to detect atrial fibrillation[J].Heart Rhythm,2020,17(5 pt b):847-853.
[7] Benjamin EJ,Levy D,Vaziri SM,et al.Independent risk factors for atrial fibrillation in a population-based cohort.The Framingham Heart Study[J].JAMA,1994,271(11):840-844.
[8] Tu HT,Spence S,Kalman JM,et al.Twenty-eight day Holter monitoring is poorly tolerated and insensitive for paroxysmal atrial fibrillation detection in cryptogenic stroke[J].Intern Med J,2014,44(5):505-508.
[9] Svennberg E,Engdahl J,Al-Khalili F,et al.Mass screening for untreated atrial fibrillation:the STROKESTOP study[J].Circulation,2015,131(25):2176-2184.
[10] Steinhubl SR,Waalen J,Edwards AM,et al.Effect of a home-based wearable continuous ECG monitoring patch on detection of undiagnosed atrial fibrillation:the mSToPS randomized clinical trial[J].JAMA,2018,320(2):146-155.
[11] Turakhia MP,Desai M,Hedlin H,et al.Rationale and design of a largescale,app-based study to identify cardiac arrhythmias using a smartwatch:the Apple Heart Study[J].Am Heart J,2019,207:66-75.
[12] Zhang H,Zhang J,Li HB,et al.Validation of single centre pre-mobile atrial fibrillation apps for continuous monitoring of atrial fibrillation in a realworld setting:pilot cohort study[J].J Med Internet Res,2019,21(12):e14909.
[13] Tang SC,Huang PW,Hung CS,et al.Identification of atrial fibrillation by quantitative analyses of fingertip photoplethysmogram[J].Sci Rep,2017,7:45644.
[14] Halcox JPJ,Wareham K,Cardew A,et al.Assessment of remote heart rhythm sampling using the AliveCor heart monitor to screen for atrial fibrillation:the REHEARSE-AF study[J].Circulation,2017,136(19):1784-1794.
[15] Bumgarner JM,Lambert CT,Hussein AA,et al.Smartwatch algorithm for automated detection of atrial fibrillation[J].J Am Coll Cardiol,2018,71(21):2381-2388.
[16] McManus DD,Lee J,Maitas O,et al.A novel application for the detection of an irregular pulse using an iPhone 4Sin patients with atrial fibrillation[J].Heart Rhythm,2013,10(3):315-319.

