食管癌微创McKeown术后胸腔胃和纵隔胃的形成对心肺并发症的影响*
叶飞 李源奇 张静 张国庆 侯志超 李强明 罗文卿 李向楠
作者单位:①郑州大学第一附属医院胸外科(郑州市450052);②中南大学湘雅公共卫生学院;③郑州大学第一附属医院手术部
尽管目前外科技术和癌症治疗方案不断发展,食管癌仍然是威胁人们生命的恶性疾病[1]。食管切除加淋巴结清扫是食管癌治疗的主要方式,而食管癌微创手术因兼顾肿瘤根治与微创原则,其在保护肺功能、降低肺部并发症方面的优点获得广泛共识[2-3],其中微创McKeown 术式因食管切除长度和喉返神经旁淋巴结清扫方面的优势,是目前外科治疗食管癌的主流术式之一[4]。食管切除会导致消化道的中断,因此寻找合适的食管替代物行消化道重建在食管癌手术中十分关键。胃是最常见的食管替代物[5-6],而切除胃小弯侧制成的管状胃代食管的近远期效果优于全胃,因此国内管状胃的建立在临床上已广泛开展[6-9]。消化道重建可以经皮下、前纵隔或后纵隔,因后纵隔重建途径可使心肺并发症发生率及手术死亡率显著降低[10],故后纵隔是目前最常见的消化道重建途径[11]。但在实际工作中通过复查胸部CT 发现,在行微创McKeown手术时,即使术中所有患者均经后纵隔食管床将管状胃上提至颈部行胃食管吻合,部分患者的管状胃却不在后纵隔食管床内,而是位于胸腔内。关于其形成机制及对术后并发症的影响目前鲜见报道。本研究对经微创McKeown 术后两种不同位置管状胃的形成机制及其对患者术后心肺并发症的影响进行探讨。
1 材料与方法
1.1 病例资料
本研究纳入2017年12月至2020年9月于郑州大学第一附属医院经食管癌微创McKeown 手术的患者。纳入标准:1)经胃镜活检确诊为食管癌;2)肿瘤位于胸段食管;3)顺利完成微创McKeown 手术;4)实现R0 切除。排除标准:1)颈段食管癌或贲门癌;2)保留全胃或者全胃切除;3)术前经新辅助放疗;4)同时患有其他部位肿瘤;5)术后院内死亡;6)行开放、纵隔镜、达芬奇机器人等非McKeown 手术;7)临床资料不全。根据上述标准,最终纳入697 例患者,其中胸腔胃组422 例,纵隔胃组275 例。患者及家属均签署知情同意书。
1.2 方法
所有患者行微创McKeown 食管癌根治术联合系统性淋巴结清扫。患者左侧卧位,右侧腋中线第7 肋间建立观察孔,腋前线第4 肋间、腋后线第9 肋间及腋后线第5 肋间建立操作孔。钝锐性结合游离出胸段食管,清扫淋巴结,充分止血后关胸。换平卧位,于脐左1 cm 处建立观孔,上腹壁建立操作孔。游离出胃大弯和胃小弯侧,清扫淋巴结并以超声刀切断腹腔肠黏连,游离出贲门周围并打开食管裂孔。于左颈部沿胸锁乳突肌前缘切口,向上游离食管至左颈部后切除食管肿块。剑突下腹部正中切口,切除胃小弯侧将胃缩成管状并间断缝合胃壁浆肌层包埋。将管状胃沿后纵隔食管床上提至左颈部后以管状吻合器与食管行机械吻合。腹部充分止血后逐层关腹。
1.3 观察指标与评价标准
观察指标:1)管状胃位置;2)住院期间心肺各项并发症的发病率。在本研究中,肺部并发症包括肺不张、气胸、胸腔积液、肺炎、脓胸、皮下积气、呼吸衰竭;心血管并发症及心律失常,主要包括房颤和房室传导阻滞;3)一般临床特征,包括年龄、性别、BMI、胸腔宽度、肿瘤位置、病理类型、T 分期和N 分期、肿瘤分化程度、是否新辅助化疗、心血管疾病史、术前FEV1;4)术中相关变量,包括手术时间、手术失血量、切除食管长度、切除胃组织面积、管状胃宽度、胃胸比、淋巴结清扫数目和术中输血情况。
评价标准:患者术后常规胃肠减压,经肠内营养支持,根据患者术后恢复情况,个性化选择经口进食时间,常规第7 天试饮水,同时行上消化道造影检查,如无异常逐步过渡至正常饮食。胸胃的扩张可能会影响管胃位置的判断,所以常规早期行胃肠减压,用以避免管胃扩张。以术后第3 天复查胸部CT 时管状胃的位置作为分组依据,管状胃部分或全部位于胸腔内,定义为胸腔胃组;管状胃位于后纵隔食管床内,定义为纵隔胃组(图1)。病理学T 分期和N 分期、肿瘤分化程度根据第8 版UICC/AJCC-TNM 食管癌分期标准。根据本院病理科测量胃组织长度和宽度的报告,计算切除胃面积。于隆突水平测量胸椎前缘正中距一侧胸壁的距离为胸腔宽度,同一水平测量管状胃宽度,定义管状胃宽度和胸腔宽度的比值为胃胸比。

图1 胸腔胃和纵隔胃的胸部CT
1.4 统计学分析
采用SPSS 25.0 软件进行统计学分析,定性资料采用χ2检验,定量资料用±s表示,正态性检验及方差齐性检验进行均值比较,方差齐性的数据用t检验,方差不齐的数据用秩和检验。以P<0.05 为差异具有统计学意义。
2 结果
2.1 一般临床特征
两组患者的年龄、性别、BMI、胸腔宽度、肿瘤位置、病理类型、T 分期和N 分期、肿瘤分化程度、是否行新辅助化疗、心血管疾病史、术前FEV1 比较差异均无统计学意义(P>0.05,表1)。
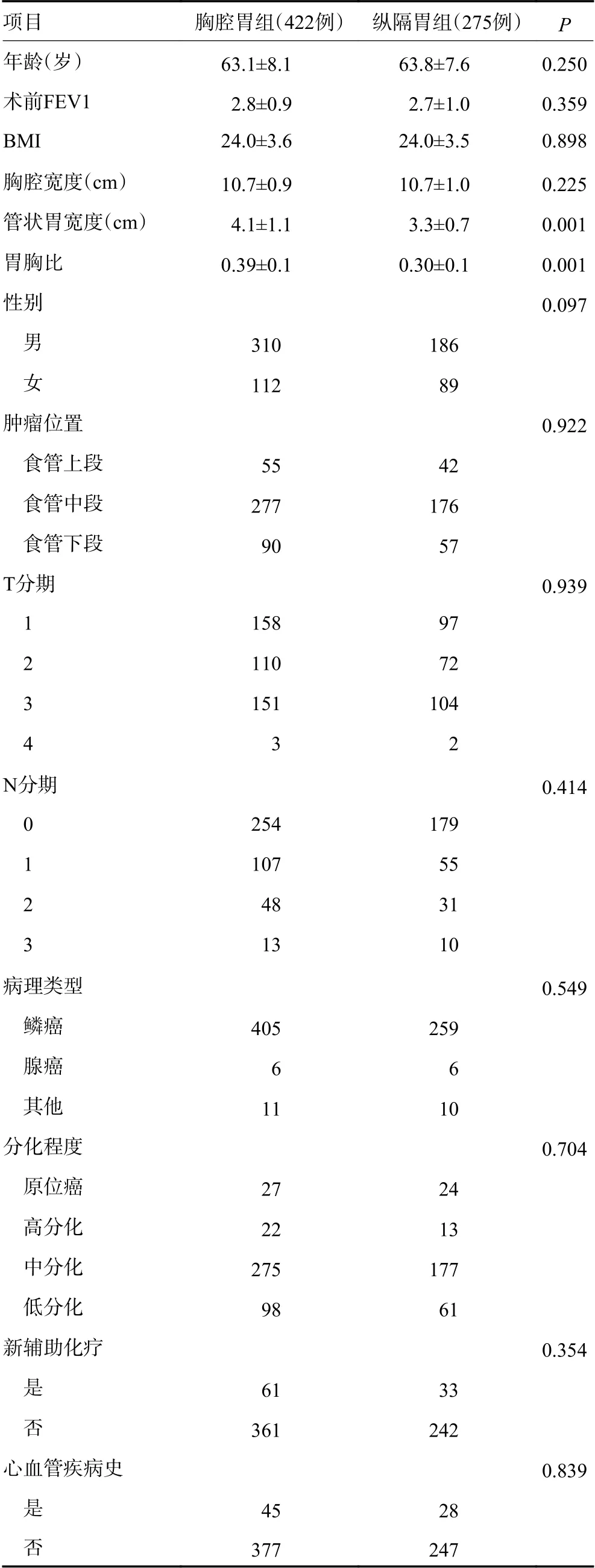
表1 胸腔胃组和纵隔胃组患者一般临床特征的比较
2.2 手术相关变量
对比纵隔胃组,胸腔胃组的胃组织切除面积更小[(55.0±31.7)cm2vs.(65.7±38.2)cm2,P<0.001]、管状胃更宽[(4.1±1.1)cmvs.(3.3±0.7)cm,P<0.001]、胃胸比更大[(0.39±0.1)vs.(0.30±0.1),P<0.001],其他手术变量包括手术时间、手术失血量、是否输血、切除食管长度、淋巴结清扫数目差异无统计学意义(P>0.05,表2)。
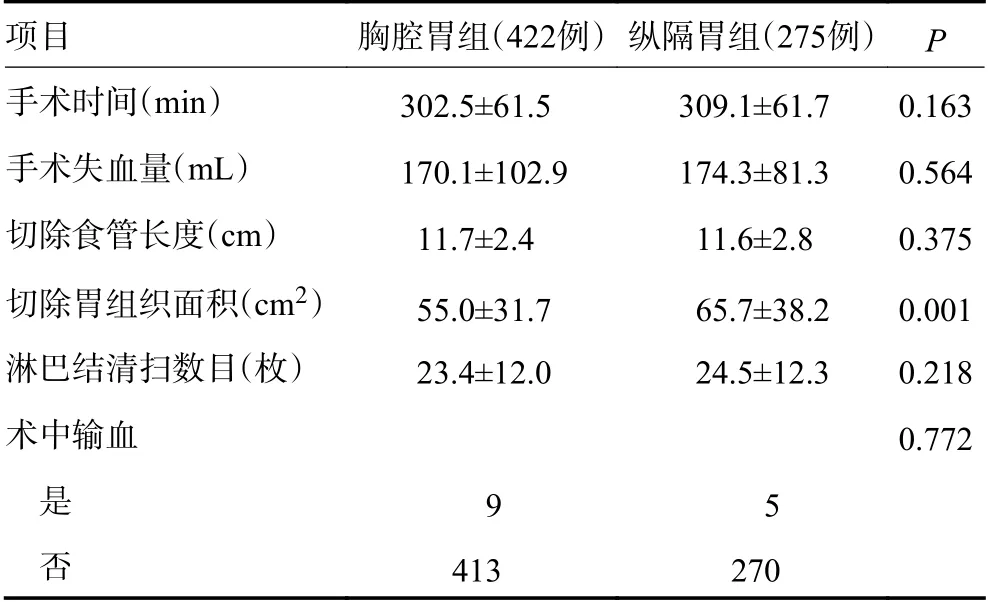
表2 手术相关变量的比较
2.3 术后并发症
纵隔胃组肺不张(36.0%vs.54.2%,P<0.001)、胸腔积液(40.7%vs.53.8%,P=0.001)和心血管并发症(16.0%vs.22.3%,P=0.042)的发生率较胸腔胃组低,而气胸、脓胸、皮下积气、呼吸衰竭、吻合口瘘及吻合口狭窄的发生率两组差异无统计学意义(P>0.05,表3)。
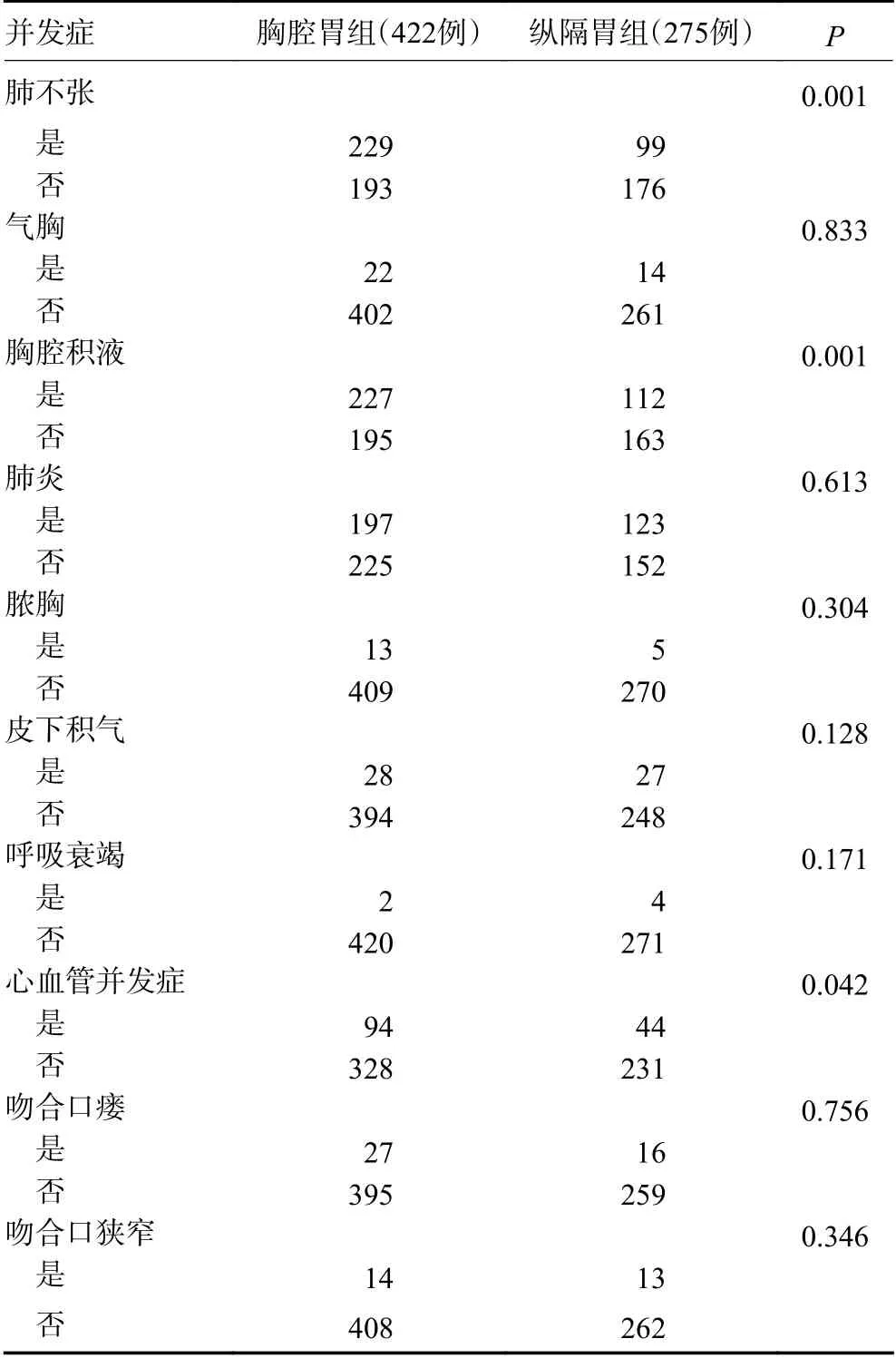
表3 胸腔胃组和纵隔胃组术后并发症的比较
按照胃胸比将胸腔胃组和纵隔胃组各分为3 组进行分层分析,结果显示各组心肺并发症的发病率的差异无统计学意义(P>0.05,图2,3)。
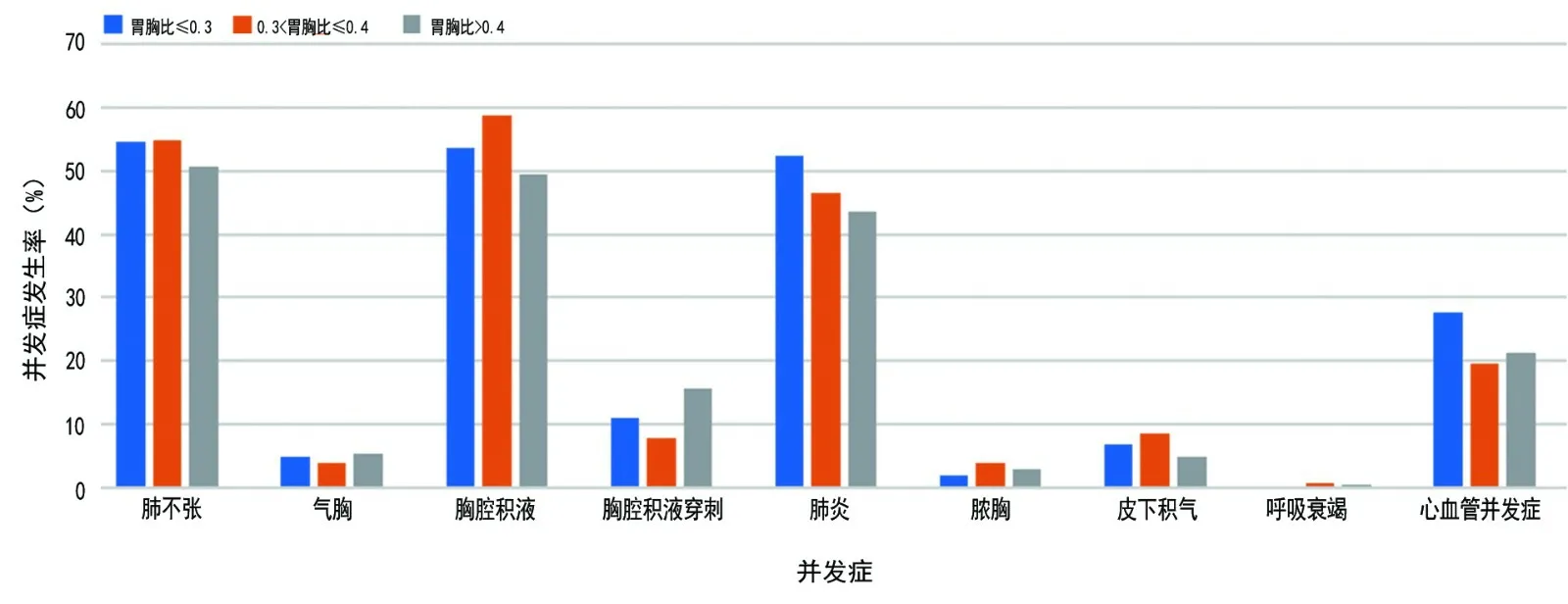
图2 胸腔胃组胃胸比与心肺并发症的关系
3 讨论
中国是食管癌的高发国家,每年约22 万例新发食管癌患者[12]。食管癌的治疗以外科手术为主,虽然可以延长患者的生存,但其术后并发症发生率高达45%~80%[13-16]。并发症的发生不仅降低食管癌术后患者的生存质量,更有研究指出肺部并发症直接影响其近期及远期预后[17-19]。Bartels 等[10]研究指出经后纵隔较胸骨后行消化道重建可以减少心肺并发症的发生。本研究旨在探讨经后纵隔消化道重建后不同管状胃位置的形成机制及其对患者术后心肺并发症的影响。
关于管状胃位置对术后肺部并发症的影响,本研究显示纵隔胃组肺不张(36.0%vs.54.2%,P<0.001)、胸腔积液(40.7%vs.53.8%,P=0.001)的发病率均低于胸腔胃组。胸腔胃可使肺组织膨胀受限,从而造成压迫性肺不张,由于肺组织膨胀不全,液体不易经引流管排出而造成积存,故胸腔积液更为常见。而纵隔胃能减轻对肺组织的压迫,更符合人体的生理。另外纵隔胃通过填塞后纵隔不仅保护气管和支气管树,还可压迫手术创面,减少胸水的渗出[10,20-21]。本研究通过术后复查胸部CT 发现胸腔胃组管状胃的扩张主要以上段居多(隆突水平以上),而纵隔胃组管状胃无明显扩张处,由于胸腔管状胃扩张的存在可能会对气道造成肿块效应,并影响肺的复张,导致胸腔胃组肺不张发病率升高[22]。对于发生肺部并发症的患者,除鼓励患者咳嗽、咳痰、加强呼吸道管理等基础支持治疗外,必要时还需针对不同并发症采取不同的治疗措施。肺不张、气胸、胸腔积液可采取彩超引导下穿刺或放置引流管,促使肺复张;肺炎、脓胸静脉应用广谱抗生素、雾化吸入化痰药物,减轻感染、促进排痰。
对比两组心血管并发症,本研究发现纵隔胃组的发病率(16.0%vs.22.3%,P=0.042)较胸腔胃组低。心律失常的影响因素众多,由于麻醉与手术创伤对心肺功能的影响较大,尤其是术后胸腔或肺部感染、疼痛、水电解质失衡,均可引起心律失常的发生[23-25]。由于肺不张和胸腔积液可导致心律失常的发生[26],另有相关报道阐述了心脏受压与心律失常之间的关系[25,27-28],胸腔胃在压迫肺的同时,也压迫心脏,心脏受到管状胃的刺激,易导致心律失常的发生。上述原因共同导致两组患者心血管并发症的差异。食管癌术后心律失常的治疗措施应该是综合性的,不仅包括发作时治疗,还需要根据患者个体情况控制基础疾病,必要时需应用抗心律失常药物,以改善长期预后,预防心脏性猝死。
食管癌颈部吻合口瘘与吻合口狭窄的发生不仅影响患者术后的生存质量,严重时更可导致患者死亡。相对于胸内吻合,颈部吻合口瘘和吻合口狭窄发生率更高,但死亡率极低,也使得一些医生热衷于食管癌切除后作颈部吻合。既往研究表明吻合口部血运术前COPD、病变位置及术后并发肺部感染均可增加吻合口瘘发生的风险[29],而吻合口狭窄的发生与手术方式、吻合方式和吻合部位等因素相关[30-32]。本研究显示管胃的位置并不影响吻合口瘘(6.4%vs.5.8%,P=0.756)和吻合口狭窄(3.3%vs.4.7%,P=0.346)的发生率。吻合口瘘是食管癌术后较为严重的并发症,一般采取保守治疗,包括禁食、胸腔闭式引流、充分引流(局部换药治疗),静脉应用广谱抗生素控制感染,有效的营养支持(静脉高营养或空肠造瘘)及纠正水电解质紊乱,还可每日定时采取生理盐水持续胸腔内灌洗及三管法治疗[33]。吻合口狭窄可导致患者进食哽噎,通常需采取扩张治疗,且一般需扩张2~3 次后患者进食哽噎才有明显好转。
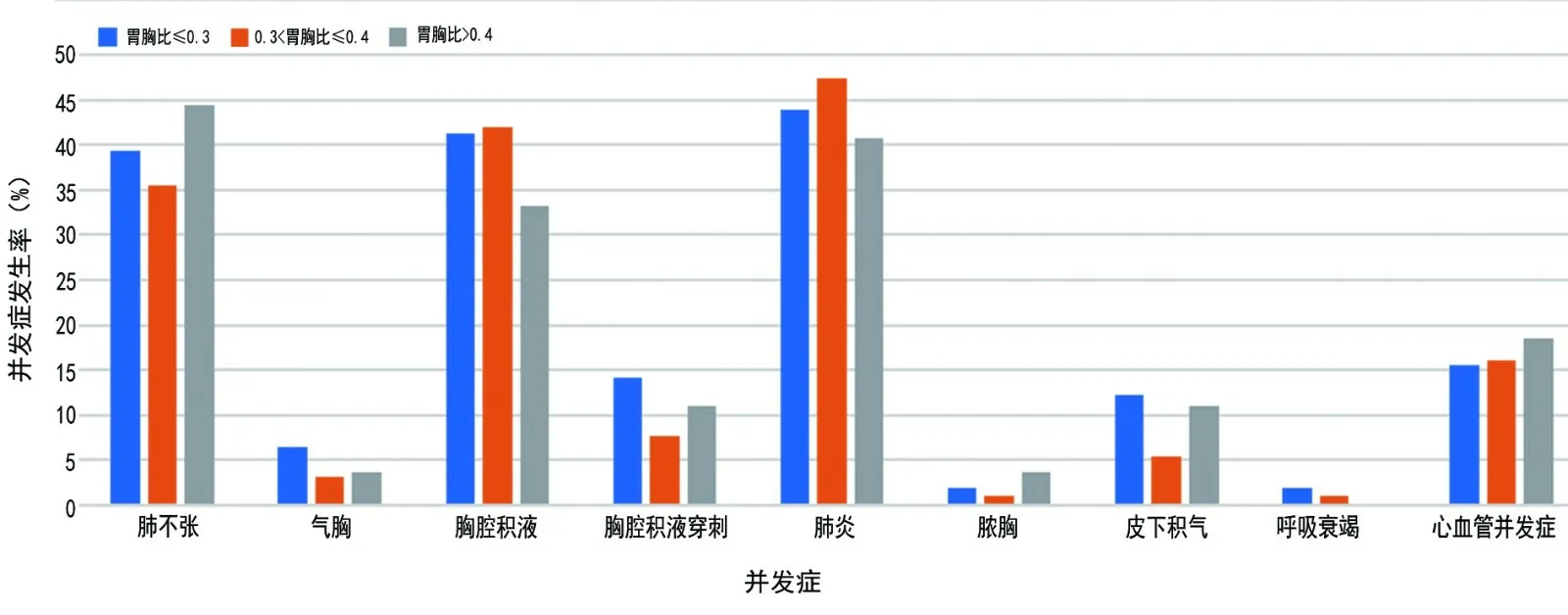
图3 纵隔胃组胃胸比与心肺并发症的关系
本研究中两组管状胃患者一般临床资料的差异无统计学意义。而手术相关变量方面显示,更大的胃切除面积可能与纵隔胃的形成有关,目前鲜见相关报道。分析原因可能是由于胃切除面积越大时,形成的管状胃更窄,使管状胃更易留在后纵隔食管床内,相反粗管状胃则容易滑出食管床而进入胸腔内,这与研究中实际测量的胸腔胃较纵隔胃更宽相符。
管状胃宽度对食管术后并发症的影响仍争议不断,尽管有研究称当管胃较细时,更有益于降低患者术后并发症的发生[34-35]。但本研究发现不同胃胸比组间心肺并发症的差异无统计学意义,说明心肺并发症的发生与管胃宽度并无直接联系,这与何晓峰等[36]的研究结果相符。值得一提的是,目前众多研究关于粗细管状胃的划分多是根据管胃的直径,但由于不同患者的身高、体质量不同,按照管胃宽度所占胸腔宽度的比值,即胃胸比划分粗细管胃应更为合理。
本研究尚有不足之处,首先考虑到术后各种因素可能导致管胃扩张,经胸部CT 影像测得的管状胃宽度可能无法完全体现手术制作的管状胃宽度[36]。除此之外,本研究认为管状胃的位置还可能与手术操作相关,如胸腔胃的形成还可能与在游离食管过程中,后纵隔未能充分打开以及在行管状胃上提至颈部吻合时未将管状胃完全放入食管床有关,但临床资料并不能完全体现。
综上所述,在行食管癌微创McKeown 手术时,纵隔胃的形成可降低肺不张、胸腔积液和心血管并发症的发病率,胃切除面积与两种管状胃的形成有关,当胃切除面积较大时更易形成纵隔胃。

