基于FAERS挖掘阿法替尼相关不良反应信号*
郑冬妮,周后凤△,任常谕,钟 科,吴逢波
(1.四川省成都市第五人民医院,四川 成都 611130; 2.四川大学华西医院,四川 成都 610041)
非小细胞肺癌(NSCLC)的传统疗法主要是以铂类为主的联合化学治疗(简称化疗),选择性较差,对肿瘤以外的组织毒性较大,效果有限。随着医疗技术的发展,表皮生长因子受体(EGFR)的发现改变了NSCLC的治疗模式[1]。EGFR作为原癌基因的表达产物,能将重要的生长信号分子从细胞外转导到细胞内,调控细胞生长、分化及癌细胞的增殖、转移,是NSCLC最常见的驱动基因。阿法替尼与受体酪氨酸激酶域的ATP位点相结合,通过阻断信号转导通路来促进细胞的增殖及凋亡[2-3]。表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)被广泛应用于EGFR突变阳性NSCLC的治疗。作为二代不可逆的EGFR-TKI,阿法替尼能对EGFR与底物ATP的结合产生持久抑制作用,对于一代耐药的EGFR敏感突变的NSCLC仍具较高的抗肿瘤活性,是中国临床肿瘤协会(CSCO)在《原发性肺癌诊疗指南》中推荐的Ⅳ期EGFR突变阳性NSCLC一线治疗药物。阿法替尼于2013年7月12日被美国食品和药物管理局(FDA)批准用于存在EGFR敏感突变的晚期NSCLC的一线治疗[4]。2017年,原国家食品药品监督管理总局批准其在国内上市,并于次年纳入医保。自阿法替尼上市以来,FDA多次在其药品说明书的不良反应(ADR)项中增加内容,包括可致恶心、呕吐、胰腺炎、中毒性表皮坏死松解症、Stevens-Johnson综合征、甲病等,提示需继续对阿法替尼的安全性进行调查[5]。本研究中运用数据挖掘方法检测阿法替尼的ADR信号,对其上市后的安全性做初步评价,为临床合理应用提供参考。现报道如下。
1 数据来源与方法
1.1 数据来源
数据来源于美国FDA不良事件报告系统(FAERS)[6],本研究中检索2013年第3季度至2019年第3季度(共25个季度)的数据。
1.2 数据处理
排除无关、信息不确定及重复报告后,得到总的药品不良事件(ADE)报告数。限定药品名称为“Afatinib”“Gilotrif”进行检索,得到首要怀疑(PS)药品为阿法替尼的ADR报告数[7]。按国际医学用语词典(MedDRA)术语对其报告中的首选语(PT)进行主系统器官分类(SOC),排除无法判读、不符合逻辑关系的报告,最终得到总的ADR报告数及PS药品为阿法替尼的报告数。对照MedDRA标准写法,归纳、整理PT含义相同的报告。
1.3 信号挖掘
采用比例失衡法[7]中频率法[8-10],包括报告比值比(ROR)法和比例报告比值(PRR)法[11-12]进行信号挖掘。
首先根据数据处理结果,筛选出报告数≥3的PT,得到a值,并分别计算所有筛选出来的PT的b,c,d值,以生成信号。信号生成条件为:a≥3,双侧检验95%CI下限≥1。并设定ROR法和PRR法的信号强弱标准,1<ROR(PRR)-1.96SE<50时信号较弱;50≤ROR(PRR)-1.96SE<1 000时信号中等;ROR(PRR)-1.96SE≥1 000时信号较强。由于所用方法灵敏性很强,较易出现假阳性信号[13],且信号检测能力受a值影响[14],本研究中对ROR法和PRR法同时有信号的PT作为研究对象进行二次筛选。筛选方法为目标药物的目标ADR报告数(a)>5,所有药物的目标ADR报告数(a+c)≥100[15],提高阈值,避免假阳性导致资源浪费。
2 结果
2.1 累及系统/器官
经过数据处理,得到ADR报告25 007 035份,以阿法替尼为PS药品的ADR报告1 971份,阿法替尼ADR信号325个。将结果进行二次筛选,得到完全重合的信号219个,去除癌症进展、肿瘤转移等可能与疾病转归相关的无效信号29个,共挖掘出ADR信号190个,按MedDRA术语对其报告中的PT进行主系统器官分类,ADR信号主要集中在胃肠道系统(47个信号),皮肤及皮下组织(41个信号),呼吸系统、胸及纵隔系统(22个信号),感染及侵染类疾病(19个信号)等;其中,新的ADR信号113个,主要集中在胃肠道系统(37个),皮肤及皮下组织(17个),呼吸系统、胸及纵隔系统(13个),感染及侵染类疾病(7个),详见表1。提示在上述系统中要重点关注新的ADR。值得注意的是,结果中显示血液系统ADR信号占比较低,累计ADR数较少,证实了阿法替尼作为小分子靶向药的主要优势,如选择性高,副作用小,可避免传统化疗引起的广泛细胞毒作用(尤其是针对骨髓等增殖较活跃的组织)。

表1 阿法替尼ADR信号系统/器官分类及临床表现Tab.1 SOC and clinical manifestation of ADR signals of afatinib
2.2 ADR信号强度
将ROR法、PRR法检测出的结果经过二次筛选,并去除考虑本身肿瘤治疗无效引起的重叠信号的阿法替尼ADR信号后按发生次数(a值)和信号强度(95%CI下限)进行分组,并按信号强度排序,前50位的ADR信号见表2。
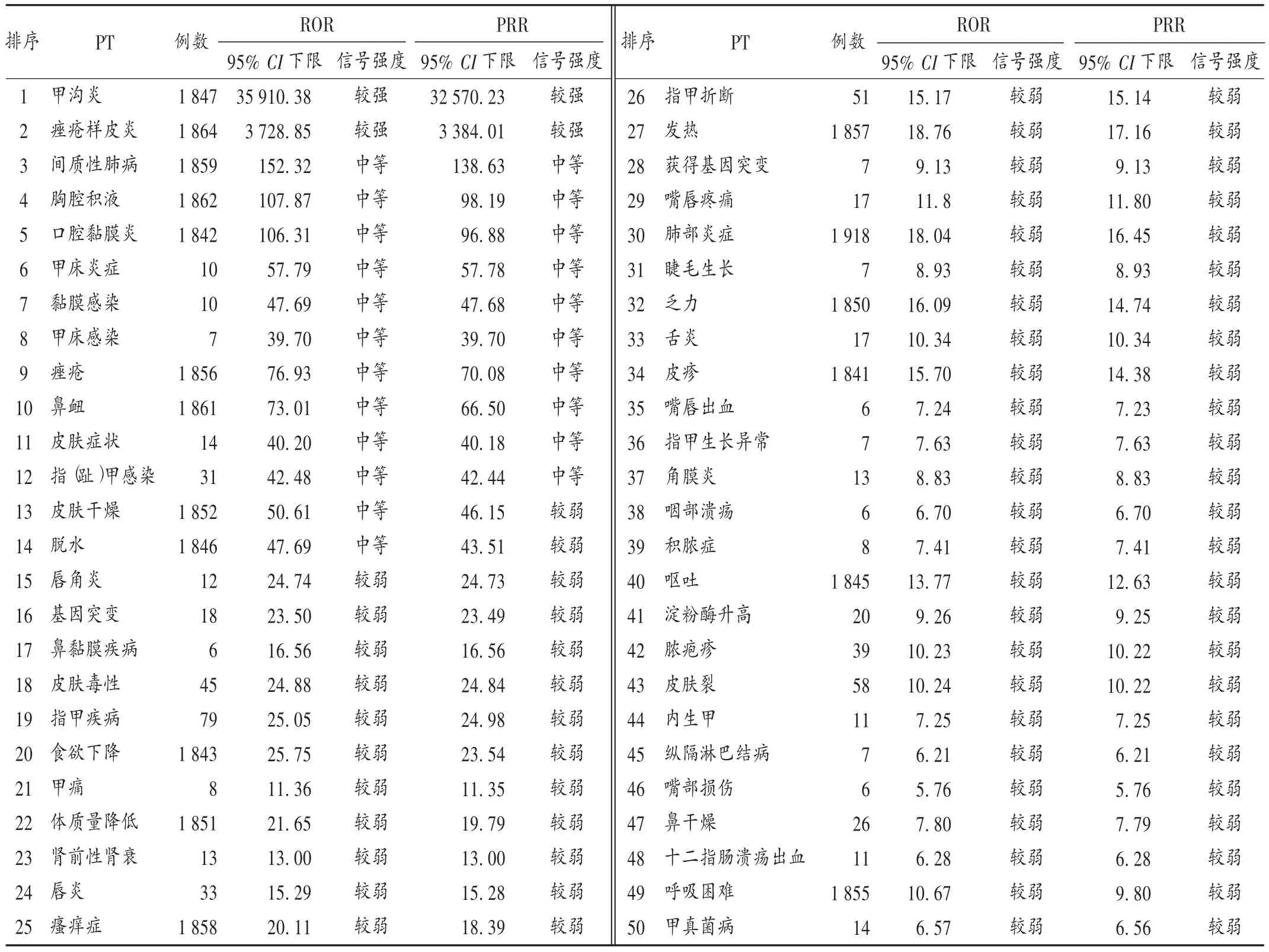
表2 阿法替尼ADR信号强度排名前50的ADRTab.2 Top 50 ADR signals of afatinib in descending order of signal strength
3 讨论
3.1 ADR累及主要系统/器官
本研究中,阿法替尼的ADR信号涉及19个系统,其中排名前5的分别为胃肠道系统,皮肤及皮下组织,呼吸道系统、胸及纵隔,感染及侵染类和代谢及营养类,临床表现包括恶心、呕吐、腹泻、口腔黏膜炎、痤疮样皮疹、甲沟炎、间质性肺炎等,与药品说明书和文献[15]报道基本一致,可证实ROR法和PRR法对于ADE信号挖掘的可信度。
本研究中挖掘出ADR信号个数最多的为胃肠道系统,其次为皮肤及皮下组织。胃肠道系统的ADR与肿瘤患者免疫力低下、胃肠道功能紊乱有一定相关性。EGFR-TKIⅢ期试验表明,阿法替尼易导致腹泻,而EGFR-TKI引起腹泻的机制目前尚不明确,有研究提示可能与氯离子的过度分泌有关[16]。另外,由于EGFR对皮肤生理学有多种作用,包括刺激表皮生长、抑制分化、加快伤口愈合等。抑制EGFR的活性可引起多种皮肤ADR,如皮疹、皮肤干燥、瘙痒等[17]。故建议在临床使用中应重视阿法替尼对胃肠道及皮肤的损害。若患者发生严重腹泻,需警惕有无伴肾功能损害的脱水,而当该药引起剥脱性皮肤疾病、Stevens-Johnson综合征等严重皮肤损伤时,应及时停药。另外,本研究中还挖掘出了药品说明书中与停药相关的ADR,如严重肝损害、角膜炎、左心室功能异常等,建议在用药期间密切监测。
挖掘出新的信号共113个,占总信号的59.47%。ROR法检测出的较强和中等信号中,除胸腔积液外,其余均为药品说明书中已有的ADR。NSCLC患者随疾病进展极可能出现包括胸腔积液、呼吸困难等呼吸系统相关症状[18]。提示临床使用阿法替尼时,应仔细甄别上述症状是否为阿法替尼的ADR。
3.2 频次和强度较高的ADR
按信号强度排序,列前3的分别为甲沟炎、痤疮样皮炎、间质性肺病,分别对应感染及侵染类疾病,皮肤及皮下组织类,以及呼吸系统、胸及纵隔系统。有研究认为,阿法替尼引起间质性肺疾病的原因可能为,抑制气管上皮细胞生长和损伤的修复,从而加重肺损害,同时引起肺泡和支气管上皮损伤及慢性炎症,从而逐渐导致肺纤维化[19]。除上述系统外,需关注阿法替尼引起的代谢及营养类ADR,除药品说明书中已提及的脱水、食欲下降、体质量下降、低钾血症,还出现了新的信号如低血容量、低白蛋白血症、高尿酸血症等,在使用过程中可通过临床监测指标发现并及时对症治疗,预防出现严重的休克等。另值得注意的是,在强度排名前50的ADR信号中,提到了肾脏及泌尿系统的肾前性肾衰,提示在临床使用中,尤其对肾功能不全或老年患者,需监测肾功能。
由于自发报告系统的局限性,存在漏报、患者基本信息缺失、无法估算ADR发生率等情况,且未考虑疾病本身及联合用药对ADR的影响,可能影响挖掘结果。此外,阿法替尼在临床应用愈发广泛,故其安全性需做进一步监测和评价。

