二代线性探针技术在结核病诊断及耐药检测中的应用研究
张耀辉,刘 元
陕西省西安市胸科医院:1.医务科;2.检验科,陕西西安 710100
结核病是一种严重危害人类健康的疾病,在全球范围内每年新增结核病患者达数百万。同时,结核病也是导致死亡的十大原因之一。2018年,全球估计有1 000万人新感染结核,中国约有88.9万人新感染结核,在全球结核病患者中估计有48.4万人为新发耐利福平结核病,中国约占14%[1]。因此,找到一种快速检测结核分枝杆菌感染及耐药水平的方法,对结核病防治起着至关重要的作用。二代线性探针技术(MTBDR plus V2.0)是一种快速检测结核分枝杆菌及其耐药基因的方法,在结核病诊断及耐药检测方面优势巨大。本文通过对比MTBDR plus V2.0、MGIT 960液体培养及药敏试验在检测结核分枝杆菌耐药性中的差异,探讨MTBDR plus V2.0在临床的应用前景。
1 资料与方法
1.1一般资料 选取2018年6月至2019年6月在本院就诊的疑似肺结核患者作为研究对象,肺结核诊断参考《肺结核诊断标准:WS288-2017》[2]。本研究共纳入研究对象1 322例,其中男898例、女424例,平均年龄(42.05±18.30)岁。纳入标准:(1)年龄10~80岁;(2)疑似肺结核(有肺结核临床症状,咳嗽、咳痰≥2周,持续发热、盗汗、体质量下降等);(3)普通X线摄片或CT扫描提示肺结核可能;(4)人类免疫缺陷病毒阳性不予排除,可纳入本研究。排除标准:针对目前病情已进行抗结核治疗超过3周(不包括既往患结核病有治疗史者)。
1.2仪器与试剂 BACTEC MGIT 960液体培养系统购自美国BD公司;GT-blot 48杂交仪购自法国生物梅里埃公司;MGIT液体培养管及分枝杆菌药物敏感性检测试剂盒购自美国BD公司;MPT64快速抗原检测试剂购自杭州创新生物检控技术有限公司;Geno Type MTBDR plus V2.0试剂盒购自法国生物梅里埃公司。
1.3方法
1.3.1痰涂片 挑取标本中干酪样、脓样或可疑处涂片,于玻片正面右侧2/3处均匀涂抹形成1 cm×2 cm椭圆形痰膜,于生物安全柜内静置干燥后进行抗酸染色。按照萋尼氏染色镜检分级报告标准报告结果。
1.3.2MGIT 960液体培养 把报阳当天算作第0天,如果是第1~2天直接进行药敏试验接种,第3~5天则先用灭菌生理盐水按照1∶4稀释(1 mL菌悬液,4 mL生理盐水)。接种时,取0.5 mL结核分枝杆菌阳性菌液接种到含药培养基上(利福平药物浓度1 μg/mL,异烟肼药物浓度0.1 μg/mL),对照管内则加入0.5 mL的1∶100倍稀释菌悬液(0.1 mL菌悬液,10 mL灭菌生理盐水),盖紧螺旋盖并混匀,放入MGIT 960培养系统培养。当生长对照管中生长单位(GU)指数达到400时(4~13 d内),评估含药培养管的GU值;含药培养管的GU值<100为敏感,含药培养管的GU值≥100为耐药。
1.3.3MGIT 960药敏试验 取结核分枝杆菌阳性产物0.5 mL接种到含药培养基上(利福平药物浓度1 μg/mL,异烟肼药物浓度0.1 μg/mL)。另取0.2 mL阳性产物用磷酸盐缓冲液稀释100倍后,取0.5 mL接种到生长对照管中,放入MGIT 960培养系统培养。当生长对照管中GU指数达到400时(4~13 d内),评估含药培养管的GU值;含药培养管的GU值<100为敏感,含药培养管的GU值≥100为耐药。
1.3.4MTBDR plus V2.0检测 MTBDR plus V2.0检测利福平耐药性的原理是通过8条分子探针覆盖利福平耐药相关基因rpoB核心突变区(RRDR),并能检测其常见突变[D516V(rpoB MUT1)、H526Y(rpoB MUT2A)、H526D(rpoB MUT2B)、S531L(rpoB MUT3)],当检测区域有突变时,可导致相应的野生型条带缺失或突变型条带显色。检测异烟肼耐药性的原理是检测katG315位点和inhA启动子区基因及其常见突变,2个基因有1个突变即认为异烟肼耐药。
操作步骤:取0.5 mL前处理后的痰标本以10 000×g离心15 min,弃上清,加入100 μL裂解液(A-LYS),95 ℃水浴5 min,短暂离心,加入100 uL中和缓冲液(A-NB),10 000×g离心5 min,上清即为提取的核酸DNA。取5 μL提取后的DNA加入含有35 μL AM-B和10 μL AM-A的扩增体系中,按照说明书的扩增程序进行扩增。扩增完成后取20 μL扩增产物进行杂交,杂交过程包括化学变性、杂交孵育、洗涤、偶联和显色等。根据显色结果进行耐药情况的判读。判读标准:野生条带均显色且突变条带无显色时为敏感,野生条带有缺失或突变条带显色为耐药。
1.4统计学处理 采用SPSS17.0统计软件对数据进行处理和分析。药敏试验结果比较及检测方法效能比较采用Kappa检验。Kappa值>0.75为一致性好;Kappa值<0.45为一致性差。计数资料以例数和百分率表示,对检测方法阳性率的比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1MTBDR plus V2.0和痰涂片方法检测结核分枝杆菌效能 以MGIT 960液体培养结果为标准,痰涂片检测方法的灵敏度为46.74%,特异度为98.73%,阳性预测值为96.17%,阴性预测值为73.04%,Kappa值为0.45。MTBDR plus V2.0检测方法的灵敏度为87.15%,特异度为92.74%,阳性预测值为89.14%,阴性预测值为91.34%,Kappa值为0.80。见表1。
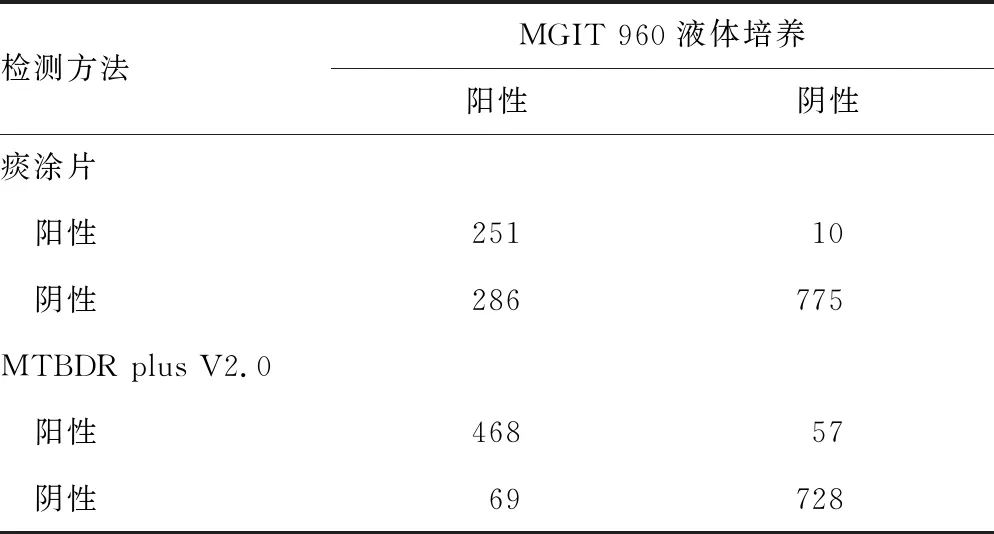
表1 各种方法对痰标本中结核分枝杆菌检测效能比较(n)
2.2涂片阴性肺结核患者中MTBDR plus V2.0与MGIT 960液体培养检测效能比较 1 322例研究对象中,痰涂片阴性者1 061例,其中痰涂片阴性肺结核患者838例,经MTBDR plus V2.0检测结核分枝杆菌阳性250例,阳性检出率为29.83%(250/838);MGIT 960液体培养检测阳性255例,阳性检出率为30.43%(255/838)。MTBDR plus V2.0和MGIT 960液体培养对痰涂片阴性肺结核患者的阳性检出率比较,差异无统计学意义(χ2=0.071,P=0.790)。
2.3MTBDR plus V2.0对利福平和异烟肼耐药性的检测效能 对437例同时进行MGIT 960药敏试验和MTBDR plus V2.0耐药基因检测,以MGIT 960药敏试验检测结果为标准,MTBDR plus V2.0检测利福平耐药性的灵敏度、特异度和Kappa值分别为88.75%、95.52%和0.84,Kappa检验结果显示,MTBDR plus V2.0检测利福平耐药性与MGIT960药敏试验具有较好的一致性。MTBDR plus V2.0检测异烟肼耐药性的灵敏度、特异度和Kappa值分别为71.43%、97.37%和0.69,Kappa检验结果显示,MTBDR plus V2.0检测异烟肼耐药性与MGIT 960药敏试验一致性一般。见表2。
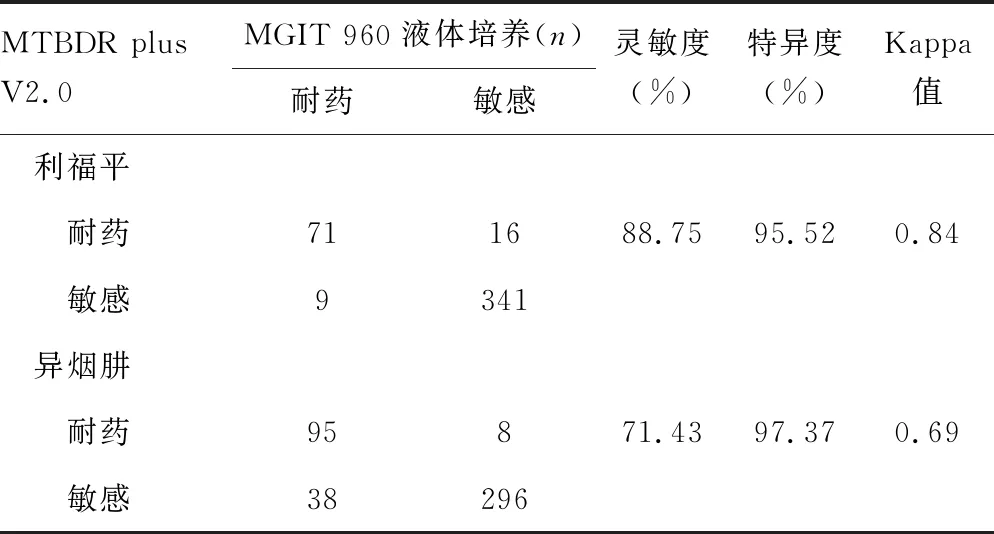
表2 MTBDR plus V2.0对MTB利福平和异烟肼耐药性检测效能
3 讨 论
耐药和耐多药结核病增多是我国结核病疫情控制不佳的主要原因。耐药和耐多药结核病不但病死率高,对健康人群也威胁极大。目前诊断结核病及检测结核分枝杆菌利福平和异烟肼耐药性的“金标准”仍然是结核菌培养和表型药敏检测方法,然而培养和得到药敏结果往往需要1~2个月时间,已不能满足现阶段临床需要。GeneXpert是一种能够在2 h内从患者临床标本中检测出结核分枝杆菌及利福平耐药性的分子检测方法[3],但GeneXpert只能检测利福平耐药性,无法对异烟肼耐药性进行检测,而现阶段异烟肼的耐药形势同样不容忽视,据研究报道,初治结核异烟肼耐药率为%,复治患者约为7.9%[4-5],目前迫切需要一种能快速从疑似肺结核患者临床标本中检测出利福平和异烟肼耐药性的方法。
MTBDR plus V2.0 是一种能够快速从肺结核患者标本中检测出结核分枝杆菌及利福平、异烟肼耐药性的分子检测方法。MTBDR plus V2.0在其第一代技术基础上,优化了DNA提取方法及PCR扩增体系[6],与第一代技术相比提高了检测的灵敏度,MTBDR plus V2.0最大的优点是能对痰涂片阴性肺结核患者标本进行直接检测。在6 h内检测出标本中的结核分枝杆菌及其对利福平和异烟肼的耐药性[7],弥补了表型药敏方法和GeneXpert这2种方法的不足。
本研究中,以MGIT 960液体培养为标准,MTBDR plus V2.0检测痰标本中结核分枝杆菌的灵敏度为87.15%,特异度为92.74%,Kappa值为0.80,与MGIT 960液体培养检验结果具有较好一致性,这与相关研究报道一致[8-9],表明在诊断结核病方面,MTBDR plus V2.0具有较好的诊断能力;同时,与痰涂片进行比较,其诊断灵敏度明显高于痰涂片的46.74%。另外,本研究注意到MGIT 960液体培养阳性的537例标本中经鉴定有12例为非结核分枝杆菌,这12例标本经MTBDR plus V2.0检测均为阴性,表明在临床标本的检测中MTBDR plus V2.0可以避免非结核分枝杆菌对结果的影响,这与说明书上特异度分析结果相符合。
对痰涂片阴性肺结核患者进行检测,MGIT 960液体培养检出率为30.43%(255/838),MTBDR plus V2.0阳性检出率为29.83%(250/838),这2种方法对痰涂片阴性肺结核患者检测灵敏度无差异,略微高于李强等[10]的报道,由此可以认为,MTBDR plus V2.0对于痰涂片阴性肺结核患者具有较好的应用前景。
以MGIT 960药敏试验结果为参考标准,MTBDR plus V2.0检测痰标本利福平耐药性的灵敏度为88.75%,特异度为95.52%,Kappa值为0.84。检测异烟肼耐药性的灵敏度为71.43%,特异度为97.37%,Kappa值为0.69。这与相关研究检测结果基本一致[8-9]。MTBDR plus V2.0与MGIT 960药敏试验检测利福平耐药性有25例不同,其中16例为MTBDR plus V2.0检测耐药而MGIT 960药敏试验检测敏感,分析原因可能为:rpoB基因耐药突变区发生了沉默突变或这些突变株发生了低水平的耐药,MGIT 960药敏试验对这种低水平的耐药检测不出[11-13]。另有9例MTBDR plus V2.0检测敏感而MGIT 960药敏试验检测耐药,原因可能是存在rpoB核心突变区以外的其他耐药突变位点;或者存在其他利福平的耐药机制,比如MTB外排泵基因的过表达[14]。
MTBDR plus V2.0与MGIT 960药敏试验检测异烟肼耐药性共有46例不同,其中38例为MTBDR plus V2.0检测敏感而MGIT 960药敏试验检测耐药,对这38例菌株进行了测序(katG基因和inhA基因),发现有37例未发生katG基因和inhA基因突变,与MTBDR plus V2.0检测一致,分析这一部分表型检测耐药的原因可能为发生了katG和inhA基因以外的突变,比如kasA、ahpC、ndh等其他基因突变,研究报道这一比例约占异烟肼耐药的20%[15]。有1例经测序发生了katG315位点的突变,与MTBDR plus V2.0检测不一致,这一例可能是由于操作误差导致的。另外8例为MTBDR plus V2.0检测耐药而MGIT 960药敏试验检测敏感,经测序发现这8例有3例发生了katG315位点的突变,5例发生了inhA基因突变,与MTBDR plus V2.0检测结果完全一致,分析其可能原因是发生了低水平耐药,MGIT 960药敏试验未检测出来,这种现象在相关研究中均有报道[8,16]。
综上所述,MTBDR plus V2.0能够快速检测MTB,特异度高,具有与MGIT 960相似的灵敏度,对痰涂片阴性肺结核诊断具有较好的诊断能力。同时,可以准确检测利福平和异烟肼耐药性,在结核病诊治及防控中具有广阔的应用前景。

