体验式饮食管理在糖调节受损患者中的应用效果
李芹芹
糖调节受损(impaired glucose regulation,IGR)包括空腹血糖受损(impaired fasting glucose,IFG)和(或)糖耐量异常(impaired glucose tolerance,IGT),是人体处于糖代谢紊乱的早期阶段,可进展为糖尿病[1],是糖尿病发生发展的重要阶段。糖调节受损患者是2型糖尿病的潜在高危人群,并且流行病学研究[2-3]发现,糖尿病的相关并发症从糖尿病前期便已开始。此外有研究[4-5]表明,IGR与心血管疾病关系密切,可增加心血管事件发生的风险。有研究报道[6],2008年全球有IGR患者约3.14亿人,预计到2025年可达到4.18亿人。处于IGR阶段的患者,通过合理的干预病情是可逆的,而饮食控制是预防和治疗的基础。在我国,糖尿病患者以及糖尿病前期的患者,饮食控制现状均不容乐观。张诚霖等[7]的调查研究发现,2型糖尿病患者饮食认知水平不一,建议教育者需根据患者的情况采取有针对性的饮食和行为干预。葛果等[8]对糖调节受损患者的自我管理现状调查提到,糖调节受损患者的自我管理水平受到多种因素影响,医护人员应根据患者的自身特点进行个体化教育。本研究打破以往的知识灌输式饮食教育,将护士对患者单向饮食教育转变为护患双方参与的双向饮食管理,取得较好的研究效果。现报道如下。
1 对象和方法
1.1 研究对象
选取2018年1-6月笔者所在医院糖尿病门诊的120例患者。纳入标准:(1)年龄≥18岁;(2)小学及以上文化程度;(3)首次因血糖异常就诊,既往未接受过饮食治疗;(4)符合中国2型糖尿病防治指南(2017版)中空腹血糖受损(空腹血糖6.1~7.0 mmol/L,且餐后2 h血糖<11.1 mmol/L)或糖耐量异常(餐后2 h血糖7.8~11.1 mmol/L且空腹血糖<7.0 mmol/L)诊断标准;(5)患者意识清楚,认知及沟通能力正常;(6)自愿参加本研究,并签署知情同意书。排除标准:(1)合并高血压、冠心病、脑梗死等慢性疾病;(2)合并严重感染或外伤等应激状态。采用随机数字表法将所有患者分为对照组和观察组,各60例。观察组有1例患者因为工作原因中途退出研究。该研究通过医院伦理委员会批准。2组患者的一般资料比较,差异无统计学意义,具有可比性。见表1。
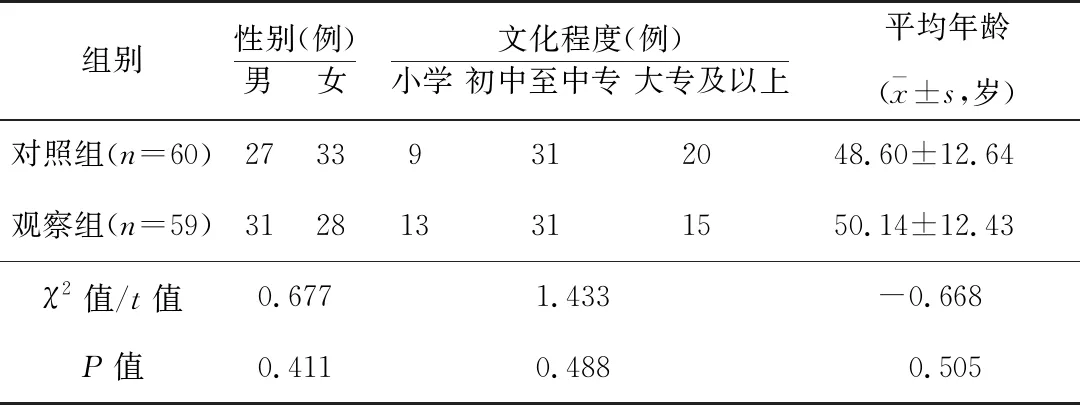
表1 2组患者一般资料比较
1.2 方法
对照组采用传统方式的饮食教育。入组后,由责任护士向患者发放饮食指导手册,为患者进行个体化饮食指导;第1个月进行集体授课,每周1次(每周一15∶00开始),授课时间40~60 min,共4次,内容包括食物总热量的算法,糖尿病饮食种类、搭配、营养素等,由患者自行进行饮食控制。第2个月和第3个月进行电话随访,随访期间继续采用电话沟通的方式进行饮食教育。干预3个月后患者返回门诊复查,观察组在对照组基础上实施体验式饮食管理,具体方法如下。
1.2.1 成立体验式饮食管理团队
由5名糖尿病专科护士和1名营养师组成体验式饮食管理小组,营养师进行患者的营养评估、分析和诊断,糖尿病专科护士负责个体化饮食处方制定和体验式饮食计划的实施。科室布置糖尿病健康教育宣教室,面积有110平米,同时配备食物模型、电子秤、多媒体教学仪器。
1.2.2 实施体验式饮食教育
(1)第1个月进行集中体验式饮食教育,每周六或周日15∶00,在内分泌科糖尿病健康教育宣教室进行体验式饮食教育,体验教育时间为90 min,共4次。将入组患者分为10小组,每组6例患者。(2)饮食教育体验。教育护士根据患者身高、体质量、血脂、活动量及血糖情况,为每例患者制定个体化的饮食处方,包括每日主食、水果、蔬菜、油等的量,在此基础上由患者根据饮食习惯进行三餐搭配。营养师采用多媒体向患者讲解食物血糖生成指数与餐后血糖的关系[9-10]。指导患者进食低血糖生成指数食物。同时,向患者发放食物血糖生成指数表,由患者对照该表进行饮食搭配。糖尿病健康教育宣教室内备有仿真食物模型,护士指导患者进行观察,用手触摸,感受食物的重量、体积、厚度等,并利用已经讲授的知识进行现场仿真食物搭配,使饮食教育更直观,便于患者理解和实践。饮食教育过程中,患者可随时提出疑问,教育护士给予解答,同时教育护士反向提问患者知识掌握情况,指出患者在食物搭配上的问题,指导改进。第2个月和第3个月进行电话随访,评估患者饮食计划执行情况,鼓励患者坚持并帮助解决存在问题。随访期间继续采用电话沟通的方式进行饮食教育。第3个月患者返院至糖尿病护理门诊进行复查。
1.3 评价指标
1.3.1 代谢指标
干预前及干预3个月后,比较2组患者空腹血糖(FBG)、餐后2 h血糖(2 hPG)、糖化血红蛋白(HbA1c)、三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)。实验室指标监测全部于患者入院时及出院3个月复诊时在医院检验科完成。
1.3.2 糖尿病前期自我管理量表
干预前及干预3个月后,根据葛果等[11]研制的糖尿病前期自我管理量表中的饮食管理相关条目,对2组患者进行调查。该量表饮食管理包括5个条目,每个条目采用Likert 5级评分法,5个选项由“从不”到“总是”分别计1~5分,量表总分为5~25分,得分越高,表明患者自我管理能力越高。该量表总的Cronbach′s α系数为0.892,重测信度为0.916,内容效度为0.937,具有良好的信度和效度[12]。
1.4 统计学方法

2 结果
2.1 2组血糖代谢指标比较
干预前,2组FBG、2hPG、HbA1c比较,差异均无统计学意义。干预3个月后,观察组FBG、2hPG、HbA1c均明显低于对照组。见表2。
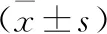
表2 2组患者血糖代谢指标比较
2.2 2组血脂代谢指标比较
干预前,2组TG、TC、LDL-C、HDL-C比较,差异均无统计学意义。干预3个月后,观察组TG明显低于对照组。2组TC、LDL-C、HDL-C比较,差异均无统计学意义。见表3。
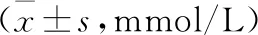
表3 2组患者血脂代谢指标比较
2.3 2组糖尿病前期自我管理量表得分比较
干预前,2组糖尿病前期自我管理量表得分比较,差异无统计学意义;干预3个月后,观察组糖尿病前期自我管理量表得分明显高于对照组。见表4。
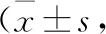
表4 2组糖尿病前期自我管理量表得分比较分 )
3 讨论
本研究结果发现,干预后观察组空腹血糖、餐后2 h血糖、糖化血红蛋白和三酰甘油改善均优于对照组,说明与传统饮食教育相比,饮食体验式饮食管理可有效控制IGR患者的空腹血糖、餐后2 h血糖、糖化血红蛋白和三酰甘油。可能原因如下,(1)体验式饮食管理注重患者参与,采用互动的教育形式,提高了患者参与饮食管理的热情,通过患者的亲自体验,可直观感受糖尿病饮食教育相关内容,使饮食教育更加直观具体,患者容易理解和实践;(2)营养师向患者讲解食物的营养与升糖指数的关系,帮助患者选择低血糖生成指数饮食。摄入低血糖生成指数的食物可减缓葡萄糖的吸收速度, 减少餐后肠道激素和胰岛素升高,延长糖类吸收时间,并可持续抑制血液游离脂肪酸水平和拮抗激素的反应,从而降低血糖[10]。(3)饮食教育的过程中,教育者不断评估患者的实际可操作性和执行情况,提高了患者的饮食依从性;(4)体验式饮食管理更加注重人性化和个体化,患者在知晓每日主食、水果、蔬菜、油等的量的基础上,可根据个人饮食喜好在医护人员的指导下自由搭配食物,制定更加适合自己的饮食处方,有利于患者对饮食方案的长期坚持。
本研究结果发现,干预后观察组糖尿病前期自我管理量表得分高于对照组。观察组患者的代谢指标改善优于对照组,可能与低血糖生成指数饮食有利于血糖相关指标的降低有关,与郑萍萍等[13-14]研究结果相似。该饮食方式可降低糖调节受损患者的代谢指标水平,营养师指导患者避免食用高热量、高脂肪、高蛋白的食物。可能与糖尿病专科护士组建团队的较高执行力和健康教育能力有关,专科护士能够很好的执行体验式饮食管理的每个步骤,通过专业的知识为患者解答疑问,提高患者对疾病的认知,提高患者参与的积极性。有研究[15-16]表明,专科护士主导的健康管理模式可改善患者的代谢指标水平和自我管理能力。
但是本研究中同时监测的胆固醇,低密度脂蛋白胆固醇,高密度脂蛋白胆固醇下降不明显,该指标可能需要长期的饮食控制并加上合理的运动指导[17]进行干预,必要时需要使用药物进行控制。
综上所述,通过体验式饮食管理可有效控制IGR患者的血糖水平,同时可改善部分血脂指标水平,强化患者饮食管理意识,提高患者的饮食依从性,值得临床推广。另外关于糖调节受损患者的转归情况,还有待进一步的随访和追踪。

