微创内镜保胆取息肉术对胆囊息肉患者胆囊收缩功能的影响
王东君
黑龙江省佳木斯市中心医院普外一科 154002
胆囊息肉(Gallbladder polyps)是指胆囊壁向腔内呈息肉样突起的一类病变,包括良性息肉和恶性息肉,以良性息肉更为多见。良性胆囊息肉又包括了胆固醇性息肉、炎症性息肉、腺瘤性息肉、腺肌增生和组织异位性息肉等。其中胆囊腺瘤性息肉是潜在的癌前病变,与胆囊癌的发生有关[1]。胆囊息肉是外科胆道系统的常见病,手术是治疗胆囊息肉的主要方式,以往的手术治疗中,大多应用腹腔镜技术对患者胆囊予以切除[2]。但该法容易引发一定的术后并发症,且需要切除患者胆囊,会对患者的消化系统产生一定的不良影响。近年来,随着内镜技术的不断发展,临床开始尝试对胆囊息肉患者实施保胆取息肉治疗。本文探讨微创内镜保胆取息肉术对胆囊息肉患者胆囊收缩功能的影响。
1 资料与方法
1.1 一般资料 收集我院2016年10月—2019年10月收治的100例胆囊息肉患者,按照住院号排序,以随机数字表法分为对照组与研究组,每组50例。研究组:男25例,女25例,年龄24~63 岁,平均年龄(48.37±1.39)岁,病程0.5~3年,平均病程(2.34±0.54)年;对照组:男27例,女23例,年龄23~65 岁,平均年龄(48.63±3.42)岁,病程0.5~3.5年,平均病程(2.41±0.73)年。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 纳入与排除标准 (1)纳入标准:①均经临床综合诊断,确诊为胆囊息肉患者;②一般情况良好,可耐受手术;③依从性好,可配合完成本次研究者;④本实验方案经本院伦理协会审核批准,入组患者知情并同意参与研究。(2)排除标准:①合并出血性疾病的患者;②合并严重心、肝、肾疾病的患者;③存在凝血机制障碍的患者。
1.3 手术方法 研究组患者均接受微创内镜保胆取息肉术治疗,术前指导患者常规禁食、禁水6h。手术当日对患者实施全身麻醉,麻醉起效后,于患者脐下做切口,切口大小为10mm。建立人工气腹,压力维持在12~14mmHg(1mmHg=0.133kPa),并置入10mm 30°腹腔镜。医生经腹腔镜镜头于直视状态下下降10mm套管针,在患者右肋缘、右锁骨中线部位依次放置5mm套管针,经患者腋前线穿刺孔部位置入腹腔镜抓钳。对患者胆囊底部予以妥善固定,使用电凝钩将胆囊底部切开。经右肋缘下套管针置入纤维胆道镜,将胆汁彻底抽取干净后,注入适量0.9%氯化钠溶液,获得良好的手术视野。医生对患者息肉情况予以仔细观察,明确胆囊息肉大小和数量、位置后,利用超声刀对息肉予以完整切除。切除完毕仔细检查,确认无息肉残留后实施止血。观察患者胆道情况,确认畅通后用使用可吸收线对胆囊予以缝合。缝合完毕进行适度挤压,确认无胆瘘后关腹,妥善缝合切口,完成手术[3]。对照组患者均接受常规腹腔镜下胆囊切除术治疗,于术前30~60min对患者实施阿托品肌内注射。帮助患者调整体位,保持仰卧状态。对患者行气管插管,实施全身麻醉。待麻醉起效后,利用Veress 针穿刺腹部留第一个孔,建立二氧化碳人工气腹,腹内压维持在1.5~2.0kPa。之后在患者腹内置入腹腔镜,借助腹腔镜作用开第二孔、第三孔,并在患者腹内置入手术所需器械。调整患者体位,将患者身体保持适度左侧,倾斜角度为30°左右,并保持脚低头高状态,将胆囊三角区域充分暴露。之后,医生利用2~3个生物夹将胆囊管、胆囊动脉夹住,应用电凝刀实施切断,对胆囊予以分离、切除。切除完毕将胆囊取出体位,并对术野进行检查。确认无异常后将患者腹腔内的二氧化碳排出,拔出套管,对伤口予以缝合[4]。
1.4 观察指标 观察对比两组患者的手术与术后恢复相关指标,包括术中出血量与手术时长、术后首次肛门排气时间与术后住院天数。并对患者治疗前后的胆囊收缩功能进行评估,分析其变化情况。观察比较两组并发症发生情况,包括伤口感染、出血、胆漏、胆道损伤、疼痛。胆囊收缩功能评估:分别在患者空腹与进食脂肪餐1h后对其进行B 超检测,记录患者胆囊壁厚度、胆囊最大前长径、前后径、横径数值,并计算出相应的胆囊容积。胆囊收缩率=[(餐前容积-餐后容积)/餐前容积]×100%[5]。
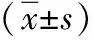
2 结果
2.1 两组患者术中出血量、手术时间、首次肛门排气时间、住院时间比较 研究组的术中出血量、手术时间、首次肛门排气时间、住院时间均小于/短于对照组,差异具有统计学意义(P<0.05),见表1。
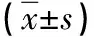
表1 两组患者术中出血量、手术时间、首次肛门排气时间、住院时间比较
2.2 两组治疗前后胆囊壁厚度变化情况比较 治疗前两组胆囊壁厚度、胆囊收缩功能比较差异无统计学意义(P>0.05);治疗后两组胆囊壁厚度、胆囊收缩功能均改善,且研究组优于对照组(P<0.05),见表2。
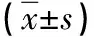
表2 两组治疗前后胆囊壁厚度变化情况比较
2.3 两组并发症发生情况比较 两组并发症发生率比较差异无统计学意义(P>0.05),见表3。

表3 两组并发症发生情况比较
3 讨论
手术是治疗胆囊息肉的主要方式,以往手术治疗中,大多采用腹腔镜胆囊切除术对胆囊息肉患者进行治疗[6]。但腹腔镜胆囊切除术容易引发胆瘘、胆道损伤、腹腔粘连等多种术后并发症出现。同时,人体的胆囊具有极为复杂和重要的功能,是不可缺少和替代的重要消化免疫器官。腹腔镜胆囊切除术需切除患者的胆囊,会对患者的消化系统产生明显影响,导致术后消化系统功能紊乱等问题的出现,严重影响到患者的术后生活[7-8]。为此,积极寻找更为安全、有效的措施,以提高治疗效果至关重要。近年来,随着微创内镜技术的不断发展与广泛应用,临床开始积极的应用微创内镜保胆取息肉方式对胆囊息肉患者进行治疗[9]。
本文结果显示,研究组平均术中出血量、手术时长、首次肛门排气时间与术后住院天数均明显短于/少于对照组。说明微创内镜保胆取息肉术对患者的创伤小,术后恢复快。这是由于微创方式建立手术通道,切口较小,医生可以在直视状态下借助腹腔镜、胆道镜对患者的胆囊息肉情况进行较为直观、细致的观察,并予以彻底清除。手术操作中视野清晰、宽广,便于医生明确不同患者的病灶情况以及息肉大小等,进而可精确切除,避免息肉残留[10]。整个手术操作对患者的器官和组织的影响较小,具有创伤小、手术简单、术后恢复快、住院时间短等优点,对减少组织损伤,促进患者的术后尽快恢复意义重大。本文结果还显示,治疗后两组胆囊壁厚度和胆囊收缩功能均改善,且研究组优于对照组。说明微创内镜保胆取息肉术对患者胆囊功能的影响较小。胆囊息肉会导致胆囊壁的增厚,影响到胆囊的收缩功能。微创内镜保胆取息肉不需要切除胆囊,且具有微创的特点,手术操作对患者胆囊壁的损伤较小。术中清除息肉后,有效改善了胆囊壁的厚度,并保留了有功能的胆囊,因此可以很好地改善患者的胆囊收缩功能。另外,也妥善维持了患者完整的生理功能,避免对患者的消化系统产生较大影响。本文中两组患者的并发症发生情况比较无统计学差异,这可能与本次纳入病例数较少有关。
综上所述,与腹腔镜胆囊切除术治疗相比较,微创内镜保胆取息肉术治疗胆囊息肉具有出血量少、患者术后恢复速度快等特点,且能够更好地改善患者的胆囊收缩功能,是一种理想的治疗方案。

