齐墩果酸C-28位四氮唑衍生物的合成及体外抗肿瘤活性
孙可微,徐阳荣,宋 佳,王洪波,赵风兰,孟庆国
(1.烟台大学药学院,新型制剂与生物技术药物研究山东省高校协同创新中心、分子药理和药物评价教育部重点实验室(烟台大学),山东烟台264005; 2.军事科学院军事医学研究院,毒物药物研究所,北京 100850)
齐墩果酸(Oleanolic acid,OA,图1),又名庆四素、土当归酸,是一种广泛存在于各种水果和可食用植物中的五环三萜类化合物[1],大多以糖苷或游离形式存在于女贞子、青龙衣、夏枯草、白花蛇舌草等植物中[2]。齐墩果酸具有多种药理学作用,如保肝、抗炎、降血糖、抗氧化、抗HIV、预防和治疗心脑血管疾病以及抗肿瘤等[3-8],目前临床上主要用于治疗急慢性肝炎或者作为抗癌辅助药物[9]。近年来合成了许多齐墩衍生物,如糖苷化衍生物[10]、苄基酯衍生物[11]等,以提高其活性、稳定性和生物利用度。

图1 齐墩果酸的结构
五元氮唑类药效团在新药研究中备受关注,它们与其他取代基相缀合或并合所得的衍生物常表现出较强的抑制肿瘤细胞增殖,阻断细胞周期,诱导细胞凋亡和分化等生物活性,提高衍生物与嘌呤、嘧啶等碱基结构片段形成氢键的能力[12]。此前本课题组已设计合成了一系列齐墩果酸氮唑衍生物,并确证其活性与齐墩果酸相比有所提高[13],本研究在此基础上进一步设计合成了一系列在齐墩果酸C-28位骈缀四氮唑结构片段的新化合物,并采用MTT法对新化合物的体外抗肿瘤活性进行评价。
1 实验部分
1.1 试剂与仪器
WRS-1B型数字熔点仪,上海仪电物理光学仪器有限公司;Bruker VANCE-400型核磁共振波谱仪,瑞士布鲁克公司;LCQ Fleet型质谱仪,赛默飞世尔科技有限公司;D8 Venture型X射线单晶衍射仪,德国布鲁克公司;异丙醇,医药级,天津市四友化学品有限公司;其余所用试剂为分析纯。
1.2 化合物的合成路线
以已知天然产物齐墩果酸为原料,在DMF中与氯乙腈反应得到中间体化合物2。化合物2再与叠氮钠在异丙醇/水中经Click反应得到一组互为同分异构体的中间体3a和3b。中间体3a和3b在DMF中与11种取代溴苄反应后得到11组同分异构体,经硅胶柱层析分离纯化后得到化合物A1—A15,合成路线见图2。

图2 目标化合物A1—A15的合成路线
1.2.1 中间体化合物2和3a、3b的合成 中间体齐墩果烷-12-烯-28-酸乙腈酯(2)的合成:反应瓶中加入DMF 50.00 mL,再加入齐墩果酸(5.00 g, 11.00 mmol)、氯乙腈(1.05 mL, 16.50 mmol)和K2CO3(2.20 g, 16.50 mmol),室温搅拌4 h。将混合物倾入碎冰中,抽滤,干燥。硅胶柱层析得到5.01 g化合物2,白色粉末,收率92.0%。
中间体齐墩果烷-12-烯-28-酸-1H-四唑和齐墩果酸-2H-四唑-5(3a和3b)的合成:将化合物2(10.00 g, 20.20 mmol)、叠氮钠(4.00 g, 60.60 mmol)和ZnCl2(5.00 g, 1.82 mmol)加入至90 mL异丙醇和30 mL水中,回流反应8 h。冷却至室温,将混合物倾入碎冰中,抽滤,干燥。硅胶柱层析,得到3a和3b的混合物9.36 g,白色粉末,收率86.1%。
1.2.2 齐墩果烷-12-烯-28-酸-(2-取代四氮唑-5)甲酯(A1—A4)和齐墩果烷-12-烯-28-酸-(1-取代四氮唑-5)甲酯(A5—A15)的合成 齐墩果烷-12-烯-28-酸-(2-邻硝基苄基四唑-5)甲酯(A1)的合成:反应瓶中加入DMF 50.00 mL,再加入混合物中间体3a和3b(0.50 g, 0.93 mmol)、2-硝基溴苄(0.30 g, 1.40 mmol)和碳酸钾(1.92 g, 13.95 mmol),室温反应4 h。将混合物倾入碎冰中,抽滤,干燥。硅胶柱层析得到A10.31g,收率49.8%;A120.19g,收率30.1%。
A1:黄棕色粉末,总收率32.0%,mp: 64.8~68.4 ℃;1H NMR (400 MHz, CDCl3):δ8.22~8.20 (d,J=8.0 Hz, 1H), 7.61~7.55 (m, 2H), 6.89~6.87 (d,J=8.0 Hz, 1H), 6.25 (s, 2H), 5.37~5.22 (m, 3H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HRMS:计算值为C39H54O4N5[M-OH]+656.414 72, 实际值656.417 03.
参照A1的合成方法,合成A2—A15。A2—A15外观、总收率、熔点、1H-NMR, HRMS和13C NMR数据如下。
A2:白色粉末,总收率35.2%,mp:81.6~84.2 ℃;13C NMR (100 MHz, CDCl3)δ: 176.43, 162.45, 142.79, 133.89, 132.26, 131.47, 129.51, 122.10, 117.39, 112.92, 78.46, 55.60, 55.23, 54.65, 47.03, 46.34, 45.24, 41.13, 40.77, 38.75, 38.22, 37.91, 36.47, 33.26, 32.54, 32.17, 31.64, 31.42, 30.15, 29.19, 28.86, 27.58, 27.11, 26.65, 25.31, 23.09, 22.86, 22.45, 22.19, 17.81, 16.27, 15.09, 14.84, 13.63;HRMS:计算值为 C40H54O2N5[M-OH]+636.427 20, 实际值636.425 09.
A3:白色粉末,总收率31.6%,mp:78.3~81.0 ℃; HRMS:计算值为C39H55O2N4[M-OH]+611.429 86, 实际值611.431 95.
A4:白色粉末,总收率33.2%,mp: 74.0~75.5 ℃;1H NMR (400 MHz, CDCl3):δ7.30~7.18 (m, 4H), 7.23~7.21 (m, 2H), 5.75 (s, 2H), 5.33~5.33 (m, 3H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HR-MS:计算值为C40H57O2N4[M-OH]+625.445 54, 实际值625.447 60.
A5:白色粉末,总收率30.3%,mp: 174.8~177.4 ℃;1H NMR (400 MHz, CDCl3):δ7.37~7.32 (m,1H), 7.08~7.04 (dt,J=8.0, 2.0 Hz, 1H), 7.01~6.99 (d,J=8.0 Hz, 1H), 6.96~6.92 (m, 1H), 5.70(s, 2H), 5.35~5.18 (m, 3H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.00~1.92 (dt,J=16.0, 4.0 Hz, 1H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.89 (s, 3H), 0.88 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.63 (s, 3H); HRMS:计算值为C39H56O3N4F [M+H]+647.430 50, 实际值647.433 10.
A6:白色粉末,总收率28.9%,mp: 156.4~158.2 ℃;1H NMR (400 MHz, CDCl3):δ7.27~7.23 (m,1H), 7.09~7.04 (t,J=8.0 Hz, 2H), 5.66 (s, 2H), 5.30~5.18 (m, 3H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.86~2.81 (dd,J=12.0, 4.0 Hz, 1H), 2.00~1.92 (dt,J=16.0, 4.0 Hz, 1H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.89 (s, 3H), 0.88 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.63 (s, 3H); HRMS:计算值为C39H56O3N4F [M+H]+647.430 69, 实际值647.433 10.
A7:白色粉末,总收率31.8%,mp: 159.4~162.7 ℃;1H NMR (400 MHz, CDCl3):δ7.40~7.34 (m, 1H), 7.24~7.22 (d,J=8.0 Hz, 1H), 7.18~7.09 (m, 2H), 5.76~5.67(m, 2H), 5.35~5.20 (m, 3H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H);13C NMR (100 MHz, CDCl3)δ: 176.52, 161.04, 158.57, 150.12, 142.64, 130.81, 130.72, 129.68, 129.65, 124.52, 124.49, 122.38, 120.18, 120.04, 115.56, 115.35, 78.45, 54.56, 52.76, 52.73, 46.97, 46.52, 45.16, 44.68, 44.64, 41.15, 40.81, 38.64, 38.22, 37.89, 36.46, 33.15, 32.47, 32.09, 31.67, 30.10, 29.18, 27.98, 27.03, 26.63, 25.33, 23.04, 22.81, 22.48, 17.76, 16.08, 15.05, 14.76;HRMS:计算值为C39H56O3N4F [M+H]+647.430 55, 实际值647.433 10.
A8:白色粉末,总收率30.1%,mp: 167.5~169.5 ℃;1H NMR (400 MHz, CDCl3):δ7.36~7.34 (d,J=8.0 Hz, 2H), 7.20~7.17 (d,J=12.0 Hz, 2H), 5.66 (s, 2H), 5.27~5.25 (t,J=4.0 Hz, 1H), 5.18 (s, 1H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HRMS:计算值为C39H56O3N4Cl [M+H]+663.401 06,实际值663.403 55.
A9:白色粉末,总收率29.3%,mp: 165.5~168.2 ℃;1H NMR (400 MHz, CDCl3):δ7.45~7.42 (d,J=12.0 Hz, 1H), 7.35~7.25 (m, 2H), 7.07~7.00 (d,J=8.0 Hz, 1H), 5.77~5.76 (d,J=4.0 Hz, 2H), 5.31~5.29 (d,J=8.0 Hz, 2H), 5.26~5.23 (m, 1H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HRMS:计算值为C39H56O3N4Cl [M+H]+663.400 59, 实际值663.403 55.
A10:白色粉末,总收率28.2%,mp: 168.4~169.3 ℃;1H NMR (400 MHz, CDCl3):δ7.51~7.49 (d,J=8.0 Hz, 1H), 7.39 (s, 1H), 7.25~7.23 (d,J=8.0 Hz, 1H), 7.17~7.15 (d,J=8.0 Hz, 1H), 5.67 (s, 2H), 5.27~5.25 (t,J=4.0 Hz, 1H),5.17 (s, 1H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HRMS:计算值为C39H54O2N4Br [M-OH]+689.339 72,实际值689.342 47.
A11:白色粉末,总收率32.2%,mp:179.6~182.2 ℃;1H NMR (400 MHz, CDCl3):δ7.63~7.61 (d, J=8.0 Hz, 1H), 7.33~7.22 (m, 2H), 6.93~6.92 (d,J=8.0 Hz, 1H), 5.74 (s, 1H), 5.35~5.24 (m, 3H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H); HRMS:计算值为C39H56O3N4Br [M+H]+707.350 62, 实际值707.353 03.
A12:黄棕色粉末,总收率28.5%,mp: 147.6~150.6 ℃;1H NMR (400 MHz, CDCl3):δ8.26~7.24 (d,J=8.0, 1H), 7.71~7.57 (m, 2H), 6.98~6.96 (d,J=8.0, 1H), 6.05~6.04 (d,J=4.0, 2H), 5.37~5.36 (d,J=4.0, 2H), 5.27~5.23 (t,J=4.0 Hz, 1H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H);13C NMR (100 MHz, CDCl3)δ: 176.41, 150.85, 146.65, 142.48, 134.11, 129.99, 129.47, 128.79, 125.37, 122.42, 78.45, 54.65, 53.04, 48.43, 46.94, 46.48, 45.08, 41.11, 40.74, 38.62, 38.21, 37.88, 36.45, 33.08, 32.43, 32.06, 31.60, 30.06, 29.18, 27.57, 27.02, 26.62, 25.28, 23.01, 22.79, 22.39, 17.73, 16.15, 15.05, 14.77; HRMS:计算值为C39H56O5N5[M+H]+674.424 71, 实际值674.427 60.
A13:白色粉末,总收率31.4%,mp: 96.6~98.0 ℃; HRMS:计算值为C40H56O3N5[M+H]+654.435 08, 实际值654.437 77.
A14:白色粉末,总收率30.7%,mp: 143.4~145.2 ℃;1H NMR (400 MHz, CDCl3):δ7.38~7.34 (m,3H), 7.24~7.18 (m, 2H), 5.70 (s, 2H), 5.27~5.25 (t,J=4.0 Hz, 1H), 5.17 (s, 2H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H);13C NMR (100 MHz, CDCl3)δ: 176.55, 150.08, 142.60, 132.80, 128.81, 128.58, 127.03, 122.40, 78.44, 54.66, 52.61, 50.80, 46.96, 46.54, 41.15, 40.84, 38.65, 38.22, 37.89, 36.46, 33.14, 32.46, 32.10, 31.72, 30.10, 29.18, 27.58, 27.05, 26.64, 25.32, 23.07, 22.82, 22.47, 17.76, 16.11, 15.06, 14.79; HRMS:计算值为C39H57O3N4[M+H]+629.440 20, 实际值629.442 52.
A15:白色粉末,总收率31.8%,mp: 156.8~159.5 ℃;1H NMR (400 MHz, CDCl3):δ7.29~7.15 (m,3H), 6.90~6.88 (d,J=8.0 Hz, 1H), 5.68 (s, 1H), 5.27~5.25 (t,J=4.0 Hz, 1H), 5.17(s, 2H), 3.22~3.18 (dd,J=8.0, 4.0 Hz, 1H), 2.83~2.79 (dd,J=12.0, 4.0 Hz, 1H), 2.02~1.94 (dt,J=16.0, 4.0 Hz, 2H), 1.85~1.81 (dd,J=8.8, 3.2 Hz, 2H), 1.25 (s, 3H), 1.10 (s, 3H), 0.98 (s, 3H), 0.90 (s, 3H), 0.89 (s, 3H), 0.87 (s, 3H), 0.77 (s, 3H), 0.48 (s, 3H);13C NMR (100 MHz, CDCl3)δ: 176.48, 150.38, 142.58, 135.75, 130.97, 130.66, 128.67, 127.28, 126.22, 122.38, 78.45, 54.65, 52.76, 49.10, 46.96, 46.49, 45.14, 40.82, 38.22, 37.89, 36.46, 33.13, 32.47, 27.58, 27.04, 26.63, 25.32, 23.06, 22.82, 22.45, 22.19, 18.74, 17.75, 16.11, 15.06, 14.79, 13.63; HRMS:计算值为C40H59O3N4[M+H]+643.455 65, 实际值643.458 17.
2 体外抗肿瘤活性评价
将对数生长期的三种肿瘤细胞(人胃癌细胞MKN-45,人乳腺癌细胞MCF-7和大鼠胶质瘤C6细胞)用0.25%的胰酶消化后,配制成一定浓度的单细胞悬液,按4000个/孔接种于96孔板,每孔加入细胞悬液100 μL。24 h后加入浓度为10 μmol/L的化合物和顺铂及相应溶剂对照的完全培养基。每孔加100 μL(DMSO终浓度<0.1%),每组设3个平行孔,于37 ℃继续培养72 h后,弃上清。每孔加入100 μL含0.5 mg/mL MTT的完全培养基,继续培养4 h,弃上清后,每孔加入150 μL DMSO溶解MTT甲瓒沉淀,微型振荡器振荡混匀后,酶标仪在参考波长450 nm,检测波长570 nm条件下测定吸光度A,以溶剂对照处理的肿瘤细胞为对照组,用以下公式计算每种化合物作用下不同肿瘤细胞的抑制率。
细胞抑制率=(1-给药组平均A/对照组平均A)×100%。
3 结果与讨论
3.1 目标物的合成
以齐墩果酸为原料,在室温条件下,以DMF为溶剂,与氯乙腈经亲核取代反应合成齐墩果烷-12-烯-28酸乙腈酯(2),再与叠氮化钠在异丙醇/水中经Click反应,合成齐墩果烷-12-烯-28-酸-1H-四唑和齐墩果酸-2H-四唑-5的混合物(3a和3b),然后与不同结构的溴苄发生取代反应,最终通过硅胶柱层析分离纯化得到15个目标化合物(A1—A15)。
在产物中存在多组同分异构体,从HRMS、1H-NMR和质谱无法辨别其结构,但可通过X射线晶体衍射辨别化合物具体结构。由于化合物A1—A15无法培养单晶,所以将其衍生化后再培养。将化合物A2的3位羟基氧化后得到化合物B1并成功培养出晶体(图3和4),该晶体CCDC编号为1850645。通过晶体结构确证,齐墩果酸四氮唑目标物中A1—A4(2,5取代四氮唑衍生物)为同分异构体中极性较小者;A5—A15(1,5取代四氮唑衍生物)为同分异构体中极性较大者。
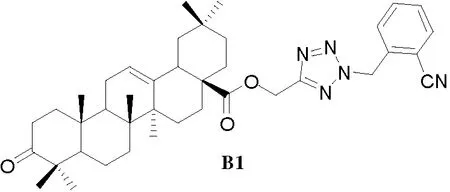
图3 化合物B1的结构
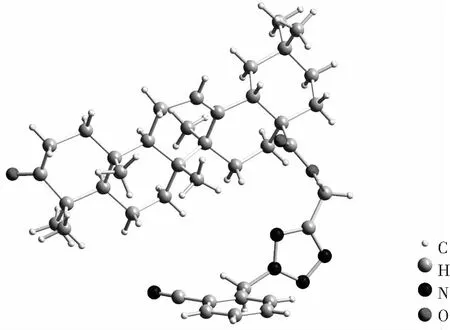
图4 B1的晶体结构
中间体3a和3b的合成中使用了危险化学品叠氮化钠,叠氮化钠在受热、接触明火、或受到摩擦、震动、撞击时会发生爆炸,使用时应格外注意。首先,不能用金属勺或刮刀进行取样称量等操作,应用牛角勺称量取样。其次,本次反应的后处理是将反应液倾入碎冰中再抽滤,滤液中有过量的叠氮化钠,也须小心处理。先加入500倍于过量叠氮化钠的水进行稀释,之后按照多余1 g的叠氮化钠约需10 mL饱和次氯酸钠溶液的比例,在不断搅拌下,滴入饱和次氯酸钠水溶液。此外,叠氮化钠含有剧毒,所有接触过叠氮化钠的器具都要用饱和次氯酸钠水溶液消毒。
3.2 体外抗肿瘤活性评价
本研究采用MTT法,初步评价目标化合物A1—A15的体外抗肿瘤活性,结果见表1。

表1 A1—A15对MKN-45、MCF-7和C6细胞的体外抗肿瘤活性
体外抗肿瘤活性结果表明,浓度为10 μmol/L时,齐墩果酸对三种肿瘤细胞的抑制作用很弱,修饰后的目标化合物抗肿瘤活性较齐墩果酸得到普遍提高,化合物A12对MKN-45肿瘤细胞的抑制率较齐墩果酸提高了3倍以上;化合物A5、A6、A8和A14对MCF-7肿瘤细胞的抑制率较齐墩果酸提高了7倍以上;化合物A1、A2、A5、A6、A7、A12、A14和A15对C6细胞的抑制率较齐墩果酸提高了6倍以上。
4 结 论
本研究采用亲核取代反应和Click反应,在齐墩果酸的C-28位羧基引入四唑,合成了15个齐墩果酸新化合物,并采用HRMS、1H-NMR和X-ray单晶衍射确证结构。以顺铂为阳性对照药,选择人胃癌细胞MKN-45、人乳腺癌细胞MCF-7和大鼠胶质瘤C6细胞等细胞作为试验瘤株,采用MTT法测定了目标物的体外抗肿瘤活性,结果表明,当浓度为10 μmol/L 时,目标物体外抗肿瘤活性较齐墩果酸得到一定提高,即在齐墩果酸的C-28位缀合各种苄基取代的四唑,有利于提高齐墩果酸的体外抗肿瘤活性,证实了齐墩果酸的C-28位衍生物具有进一步研究的价值。

