人参皂苷Rg1对CUMS+LPS致小鼠抑郁行为的改善作用及其机制
王艳芳,朱茂晶,李敏敏,应天昊,黄亚楠,卢永颖,杜 源,张雷明
(烟台大学药学院,分子药理和药物评价教育部重点实验室(烟台大学),山东 烟台 264005)
抑郁症是一种以显著而持久的情绪低沉、心境低落等为临床特征的情感性精神障碍疾病[1-2]。抑郁症的发病机理尚不明确,经典理论包括单胺能假说、神经营养假说、神经可塑性假说、神经内分泌假说及神经免疫假说等。近年来,越来越多的研究表明下丘脑-垂体-肾上腺轴(hypothalamic-pituitary-adrenocortical axis, HPA) 过度激活、炎症反应与抑郁症的发生密切相关[3-5],HPA轴是机体内与应激反应密切相关的神经内分泌系统[6],机体处于应激状态时会激活下丘脑室旁核神经元引发轴兴奋,经过一系列传递使糖皮质激素分泌增多,导致HPA轴过度激活,促进促肾上腺皮质激素(Adrenocorticotropic hormone ACTH)、皮质酮(corticosterone,CORT) 等持续性升高,造成海马等脑区结构功能损伤;此外,应激可导致肠屏障功能破坏,肠黏膜通透性改变,肠道微生物及内毒素(脂多糖Lipopolysaccharide,LPS)等泄漏入血,引起外周及中枢炎症,过度产生的炎症因子能抑制GR表达、核转位以及结合活性,从而进一步加剧了HPA轴过度激活和糖皮质激素(GCs)抵抗,产生更多的GCs,进一步损害海马等脑区神经元,促进抑郁发生[7]。
人参皂苷Rg1是人参的主要成分[8],现代研究显示Rg1能够拮抗应激导致的小鼠焦虑和抑郁样行为[9],还能逆转LPS诱导急性炎症导致的RAW264.7 巨噬细胞 GR 表达下降[10],进而抑制NF-κB激活,从而发挥其抗炎特性[11]。因此,本研究采用经典慢性不可预知温和性刺激(Chronic unpredictable mild stress,CUMS)联合LPS制备抑郁动物模型,从调节HPA轴过度激活、抑制炎症反应角度研究Rg1抗抑郁的作用机制,为其临床应用提供实验依据。
1 材料与方法
1.1实验动物雄性C57BL/6J小鼠,体重19 ~ 21 g,购于济南朋悦动物繁育有限公司,合格证SCXK(鲁)2014-0007。适应性饲养3 d,23~25 ℃,相对湿度40%~60%,自由饮水摄食。动物实验方案已获得烟台大学动物伦理委员会的批准。
1.2实验药品与试剂人参皂苷Rg1(批号:GR-133-160526,纯度≥98%):南京广润生物制品有限公司提供;脂多糖(L2630):sigma公司提供;P65(sc-71675)、GR(sc-56851)抗体:美国Santa Cruz公司提供;小鼠TNF-α ELISA试剂盒(SEKM-0034):北京索莱宝科技有限公司提供;BCA 蛋白浓度测定试剂盒(P0010):上海碧云天生物技术有限公司提供。
1.3实验仪器与设备液相色谱-质谱联用仪(美国Thermo Fisher公司);高速台式离心机(德国Eppendorf公司);酶标仪(美国Molecular Devices公司);Western blot 电泳仪、转膜系统(Bio-Rad公司);凝胶成像系统(日本GE生物科技公司)。
1.4 实验方法
1.4.1 小鼠抑郁模型的制备 将小鼠单笼饲养,并接受11d CUMS,每天随机给予1~2种刺激,刺激不连续出现。刺激结束后,腹腔注射LPS 200 μg/kg,制备小鼠抑郁模型[12]。
1.4.2 实验分组及给药 将动物随机分为对照组、模型组、米诺环素20 mg/kg组、Rg1 5 mg/kg、10 mg/kg及20 mg/kg组,每组10只。除对照组外,其余各组动物给予CUMS,各给药组同时灌胃给药,每日1次,连续11 d,末次给药1 h后腹腔注射LPS 200 μg/kg。
1.4.3 行为学实验 (1)悬尾实验。采用小鼠专用悬尾箱(30cm×30 cm×40 cm,内有固定吊环),距尾尖2 cm处用医用胶布固定于吊环上,使其头部距离地面15 cm。各组悬尾6 min,小鼠首先适应1 min,从第2 min开始记录后续5 min内小鼠的不动时间的总和。
(2)强迫游泳实验。首先将动物适应环境至少1 h,然后将小鼠放入强迫游泳实验装置,使小鼠在水中前爪攀附于缸壁并且不能以后爪支撑身体为标准,保持水温 25±2 ℃。观察6 min,记录后5 min内的累计不动时间。
(3)旷场实验。采用周壁和地面为白色的敞箱,用黑线将白色地面划分为面积相等的16块,将一只100 W的灯泡悬挂在敞箱中央上方。将单只小鼠置于清洁敞箱中央,记录小鼠的水平运动得分(小鼠穿过地面的方块数)和垂直运动得分(小鼠前两爪离地站立次数)。每只小鼠观察5 min。
1.4.4 不同脑区单胺神经递质DA和NE水平检测 给予LPS 24 h后,每组随机取6只小鼠处死,用生理盐水进行心脏灌注,取脑,分离海马、前额叶皮质,称重,与5倍体积的0.1%甲酸水匀浆,与4倍体积的0.1%甲酸乙腈沉淀蛋白,于4 ℃,离心10 min(13 000 r/min),取上清,用液相色谱-质谱联用仪进行检测分析。
1.4.5 前额叶皮质和血清TNF-α及血清ACTH、CORT水平检测 小鼠麻醉取血,室温自然凝固10 min,离心20 min(3500 r/min),收集上清,-20 ℃保存备用。分离前额叶皮质,用超声破碎仪将标本匀浆充分,离心20 min(3500 r/min)。收集上清,分装后-20 ℃保存备用。按照 ELISA 试剂盒说明书操作步骤进行测定。
1.4.6 Western blot检测小鼠海马组织核NF-κB P65、FKBP51、GR蛋白表达 小鼠麻醉处死,取脑组织,于冰上迅速剥离海马组织,称取20 mg海马组织加入250 μL RIPA裂解液于冰上匀浆,4 ℃下12 000 r/min 离心5 min,收集上清液,测定蛋白浓度。将上清液加入5倍体积上样缓冲液,煮沸10 min。10% SDS-PAGE凝胶电泳后进行转膜,随即5%脱脂奶粉溶液封闭2 h,TBST 缓冲液洗膜3次;加入一抗(1∶1000稀释),4 ℃ 孵育过夜,洗膜,加入二抗孵育1 h,洗膜,加入ECL 发光色液,放入凝胶成像系统,曝光拍照。用ImageQuant LAS 4000软件计算条带灰度值。
1.5 统计学方法

2 实验结果
2.1 Rg1对CUMS+LPS致抑郁小鼠行为学的影响
2.1.1 Rg1对CUMS+LPS致抑郁小鼠悬尾不动时间的影响 结果显示,模型组小鼠悬尾不动时间显著延长;米诺环素组小鼠悬尾不动时间显著缩短;Rg1 5 mg/kg组小鼠悬尾不动时间有所缩短,但不具有统计学意义,Rg1 10 mg/kg、20 mg/kg组小鼠悬尾不动时间显著缩短(图1)。

与对照组比较,##P<0.01;与模型组比较,
2.1.2 Rg1对CUMS+LPS致抑郁小鼠游泳不动时间的影响 结果显示,模型组小鼠游泳不动时间显著延长,米诺环素组小鼠游泳不动时间显著缩短;Rg1 5 mg/kg及Rg1 10 mg/kg组小鼠游泳不动时间显著缩短(图2)。

与对照组比较,##P<0.01;与模型组比较,
2.1.3 Rg1对CUMS+LPS致抑郁小鼠旷场实验水平运动及垂直运动得分的影响 结果显示,与对照组比较,模型组小鼠旷场实验水平得分无明显变化;与模型组比较,米诺环素组小鼠旷场实验水平得分无明显变化;Rg1各剂量组小鼠旷场实验水平得分无明显变化(图3(a))。
与对照组比较,模型组小鼠旷场实验垂直得分无明显变化;与模型组比较,米诺环素组小鼠旷场实验垂直得分无明显变化;Rg1各剂量组小鼠旷场实验垂直得分无明显变化(图3(b))。

图3 Rg1对CUMS+LPS致抑郁小鼠旷场实验水平得分、垂直得分的影响
2.2 Rg1对CUMS+LPS致抑郁小鼠不同脑区DA和NE水平的影响
结果显示,模型组小鼠海马DA、前额叶皮质NE水平显著降低,与模型组比较,米诺环素组小鼠海马DA小鼠前额叶皮质NE水平显著升高;Rg1 5 mg/kg组海马DA水平有所增加,但无统计学意义,Rg1 10 mg/kg、20 mg/kg组海马DA水平显著升高(图4(a));Rg1各剂量组小鼠前额叶皮质NE水平显著升高(图4(b))。

与对照组比较,#P<0.05;与模型组比较,
2.3 Rg1对CUMS+LPS致抑郁小鼠中枢炎症的影响
2.3.1 Rg1对CUMS+LPS致抑郁小鼠前额叶皮质及血清TNF-α水平的影响 结果表明,模型组小鼠前额叶皮质及血清TNF-α水平显著升高;米诺环素组小鼠前额叶皮质和血清TNF-α水平显著降低,在小鼠前额叶皮质中,Rg1 5 mg/kg、10 mg/kg组TNF-α水平变化无统计学意义,Rg1 20 mg/kg组TNF-α水平显著降低(图5(a));Rg1 5 mg/kg组血清TNF-α水平变化无统计学意义,Rg1 10 mg/kg、20 mg/kg组血清TNF-α水平显著降低(图5(b))。
2.3.2 Rg1对CUMS+LPS致抑郁小鼠海马组织核NF-κB p65表达的影响 结果显示,模型组小鼠海马核NF-κB p65表达显著升高,米诺环素组小鼠海马核NF-κB p65表达显著降低;Rg1各剂量组小鼠海马核NF-κB p65表达均显著降低(图6)。

与对照组比较,##P < 0.01;与模型组比较,

与对照组比较,##P < 0.01;与模型组比较,
2.4 Rg1对CUMS+LPS致抑郁小鼠HPA轴及海马FKBP51、GR蛋白表达的影响
2.4.1 Rg1对CUMS+LPS致抑郁小鼠血清ACTH、CORT水平的影响 结果显示,模型组小鼠ACTH、CORT水平显著升高,米诺环素组小鼠ACTH、CORT水平显著降低;Rg1 5 mg/kg组小鼠ACTH水平变化无统计学意义,Rg1 10 mg/kg、20 mg/kg组小鼠ACTH水平显著降低(图7(a));Rg1 5 mg/kg、10 mg/kg组小鼠CORT水平变化无统计学意义,Rg1 20 mg/kg组小鼠CORT水平显著降低(图7(b))。
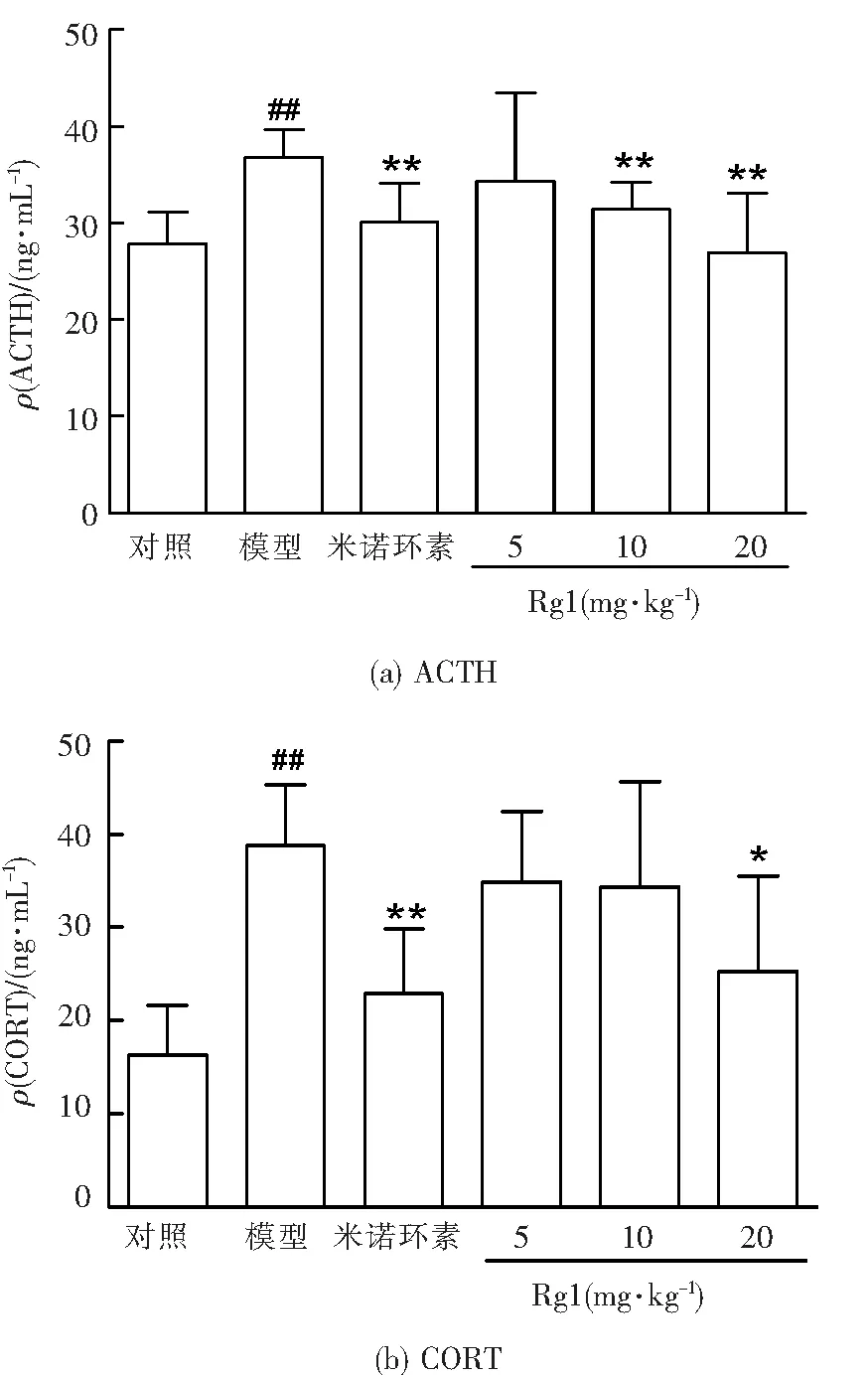
与对照组比较,##P < 0.01;与模型组比较,
2.4.2 Rg1对CUMS+LPS致抑郁小鼠海马组织FKBP51蛋白表达的影响 结果显示,模型组小鼠海马FKBP51表达显著升高,米诺环素组小鼠海马FKBP51表达显著降低,Rg1各剂量组小鼠海马FKBP51表达均显著降低(图8)。

与对照组比较,##P < 0.01;与模型组比较,
2.4.3 Rg1对CUMS+LPS致抑郁小鼠海马组织GR蛋白表达的影响 结果显示,模型组小鼠海马GR表达显著降低,米诺环素组小鼠海马GR表达显著升高,Rg1各剂量组小鼠海马GR表达均显著升高(图9)。
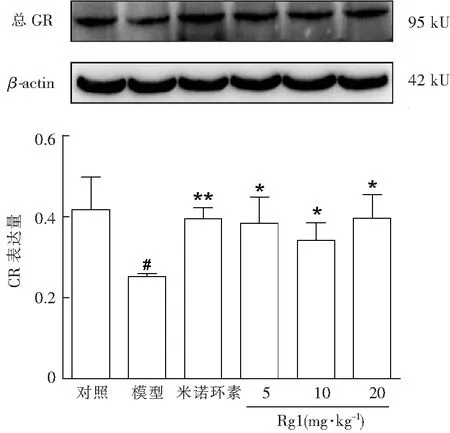
与对照组比较,#P < 0.05;与模型组比较,
3 讨 论
研究表明,应激导致的HPA 轴过度激活以及炎症反应在抑郁症发生中起重要作用,且二者能相互促进,加剧抑郁症发生、发展[13-15]。动物接受CUMS后给予低剂量LPS,可增强慢性轻度刺激动物的抑郁症状,抑郁样不动时间延长,且海马和前额叶皮质炎症增加,5-HT及其受体5-HT2A表达减少[16]。米诺环素是一种四环素类抗生素,脂溶性高,易于穿过血脑屏障,具有良好的中枢神经系统渗透性,可以影响与情绪障碍病理生理学有关的多种相互作用。有研究表明,米诺环素可减轻与LPS诱导的神经炎症有关的疾病症状,防止抑郁样不动,同时海马和皮质中TNF-α以及吲哚胺2,3-双加氧酶(IDO)mRNA表达减少[17]。本实验室前期在CUMS刺激小鼠11 d 的基础上,叠加LPS刺激,成功制备了CUMS+LPS抑郁模型[12]。因此,本研究以米诺环素做阳性对照药物,采用CUMS联合 LPS 制备小鼠抑郁模型,从HPA轴过度激活,炎症反应的角度深入研究Rg1的抗抑郁机制。
本研究结果显示,动物接受CUMS后给予低剂量LPS,模型组小鼠悬尾不动时间和游泳不动时间均延长,Rg1可缩短抑郁小鼠悬尾不动时间与游泳不动时间;在抑郁行为学研究中,旷场实验用于评价抑郁行为同时也用于评价药物对自主活动的影响[18]。由于某些可增加动物活动性的药物会使实验出现假阳性结果, 为了排除Rg1提高动物自发活动性而使小鼠强迫游泳和悬尾不动时间缩短这一可能,实验中采用旷场实验测试了小鼠的自主活动性,结果显示小鼠旷场实验的水平得分和垂直得分均无显著性变化,提示Rg1不影响小鼠的自主活动。
单胺类神经递质学说认为抑郁症的发病与脑内多巴胺(Dopamine, DA)和去甲肾上腺素(noradrenaline, NE)水平低下有关[19],本研究结果显示,模型组抑郁小鼠海马DA和前额叶皮质NE水平下降,Rg1能显著逆转抑郁小鼠海马DA和前额叶皮质NE水平下降。结果提示,Rg1能够通过改善小鼠抑郁样不动行为,提高脑内DA和NE水平而发挥抗抑郁作用。
前期研究显示,炎症在抑郁症的病理生理中起重要作用[20-21]。压力能够激活NLRP3/caspase 1炎症信号通路,释放IL-1β和IL-18。此外,外部压力破坏肠道通透性,导致细菌和细菌产物(例如LPS)从肠道泄漏出来,然后激活了NF-κB等炎症信号通路[22]。NF-κB激活后能够促进TNF-α、IL-6等促炎细胞因子的释放,脑内过量的炎症因子能够激活IDO、iNOS从而减少单胺合成,增加单胺再摄取并增强谷氨酸兴奋性毒性[23]。本研究结果显示,模型组小鼠前额叶皮质和血清中TNF-α水平增高,Rg1各组能够降低前额叶皮质和血清中TNF-α水平;CUMS联合LPS使抑郁小鼠海马组织与炎症密切相关的NF-κB p65蛋白入核明显增加,Rg1各组均可显著下调核内NF-κB p65蛋白表达,提示Rg1对抑郁样行为的影响与其抗炎作用有关。
动物受到CUMS刺激后HPA轴可过度激活,促进垂体ACTH从促肾上腺皮质细胞释放到全身循环,ACTH刺激肾上腺皮质合成分泌大量CORT从而影响GR功能导致HPA轴的负反馈调节失调[24]。同时,有研究表明,GR的功能还与FKBP51有关[25],FKBP51是GR功能的强抑制剂,可通过抑制GR与GC的结合、核转位来影响GR功能,引起糖皮质激素抵抗,最终导致与情感有关的脑区如前额叶皮质和海马神经元受损、结构和功能发生改变,产生抑郁[26]。本研究结果显示,模型组小鼠血清中ACTH、CORT水平升高,Rg1能够显著降低抑郁小鼠的ACTH、CORT水平。此外,CUMS联合LPS能够显著提高海马FKBP51蛋白表达,抑制海马GR表达。Rg1能够逆转海马FKBP51、GR蛋白水平。提示Rg1可能通过调节FKBP51/GR表达抑制HPA轴的过度激活发挥抗抑郁作用。
综上,Rg1的抗抑郁作用机制与其抑制HPA轴过度激活、调节GR功能和抑制炎症反应有关。

