新型冠状病毒肺炎患者的抗血栓治疗研究进展
李健超,李树仁,赵文静,3,郝潇,张飞飞,张倩辉,苑可心,郝清卿
本文创新点:
(1)本文从新型冠状病毒肺炎(COVID-19)与血栓形成关系的角度阐明了COVID-19患者容易患血栓性疾病,且死亡率高,进一步说明该类患者抗血栓治疗的必要性,为临床治疗提供了一定的参考价值。(2)本文从COVID-19患者抗凝和抗血小板治疗两个方面进行论述,指出在选择抗血栓药物前需进行静脉血栓栓塞症(VTE)风险评估,对于高危或中高危VTE患者,抗凝是其主要的治疗手段;对于低危VTE的重型、危重型COVID-19患者,也应进行抗凝预防,在选择合适的抗血栓药物时需考虑合并症及药物间相互作用。
新型冠状病毒肺炎(COVID-19)是由急性呼吸系统综合征冠状病毒2(SARS-CoV-2)感染引起的一种传染病,SARS-CoV-2可通过S蛋白与血管紧张素转换酶2(ACE2)受体结合进入细胞而致使细胞损伤,而后引起一系列的病理生理改变,包括内皮细胞功能障碍、大量炎性因子释放、肾素-血管紧张素系统(RAS系统)激活、血小板激活、凝血功能障碍等,最终导致血栓形成,患者以发热、干咳、乏力为主要临床表现,严重者可出现急性呼吸窘迫综合征(ARDS)、凝血功能障碍、脓毒血症、休克等严重疾病[1]。RAPKIEWICZ等[2]进行的COVID-19尸检报告发现,无论抗凝效果如何,患者肺、肝、肾和心脏的微血管中存在富含血小板的血栓,可见血栓形成是导致COVID-19患者多器官功能衰竭、严重缺氧和死亡的重要因素。ACKERMANN等[3]研究表明,COVID-19患者的肺血管内存在广泛血栓形成并伴微血管病变。综上,笔者推测COVID-19患者容易在静脉和动脉循环中患血栓性疾病。
肺栓塞是最常见的血栓并发症,多来源于下肢深静脉血栓,但也有研究发现COVID-19患者肺组织内有原位微血栓形成[4]。有研究表明,在未进行血栓预防的ICU患者中,静脉血栓栓塞症(VTE)发生率为25%,死亡率为40%[5]。另外,REY等[6]研究显示,COVID-19合并动脉血栓形成的患者病死率达44.7%以上,且预后较差。目前,临床对于COVID-19患者的抗血栓治疗已有一定的理论基础。《新型冠状病毒肺炎诊疗方案(试行第八版)》[1]指出,对于无抗凝禁忌证且D-二聚体水平明显增高的COVID-19患者建议预防性使用抗凝药物。美国国立卫生研究院(NIH)发布的《新型冠状病毒肺炎治疗指南》指出,对于住院患者(非妊娠期成年人)应给予预防性剂量的抗凝药物治疗[7]。本文就COVID-19患者血栓形成的发病机制及抗血栓治疗进行综述,以期为COVID-19患者的抗血栓治疗提供理论指导。
1 COVID-19与血栓形成的关系研究
SARS-CoV-2表面存在多个S蛋白,其是由两个亚基(S1亚基和S2亚基)组成,其中S1亚基可与靶细胞表面特异的ACE2受体结合而造成细胞损伤[8-9]。ACE2受体在人体所有组织中均有表达,而在肺、心、肾、肠等器官中呈高表达,但S蛋白与ACE2受体结合时可导致其表达下降,从而激活RAS系统[8],进而促进血小板黏附和聚集,增加了血栓形成风险。当机体受到严重感染后,免疫系统会对抗病原体,刺激并释放大量炎性因子如白介素(IL)、干扰素、肿瘤坏死因子、集落刺激因子、趋化因子和生长因子等,尤其是IL家族在炎症中起重要作用[10],其可直接作用于血浆分子、红细胞和血小板。此外,活化的血小板会促进中性粒细胞滚动、黏附和聚集;激活的血小板会与中性粒细胞相互作用,促进细胞外基质降解及凝血酶生成。可见,炎症与凝血之间存在相互作用,一方面炎症促进高凝状态,另一方面,血栓中的物质会增加炎性因子活性。因此,SARS-CoV-2引起的血管内皮细胞损伤进一步导致了内皮细胞功能障碍,从而引起凝血级联反应。与凝血、血小板活化和炎症相关的生物学标志物被认为是与COVID-19相关的凝血功能障碍性疾病患者的诊断、预后标志物。有研究表明,以1.5 μg/ml作为D-二聚体预测VTE的临界值,其灵敏度为85.0%、特异度为88.5%[5]。另有研究表明,COVID-19患者患血栓性疾病的风险较高,故建议对COVID-19患者采取药物疗法来预防血栓形成[11]。
2 COVID-19患者的抗血栓形成
2.1 抗凝治疗 COVID-19患者容易患血栓性疾病,尤其是重型及危重型患者。有研究发现,COVID-19患者较易出现凝血功能障碍,其D-二聚体水平明显升高,纤维蛋白降解产物明显增多,多数死亡患者可能存在弥散性血管内凝血(DIC)[12-13]。长期卧床休息和接受激素治疗也会增加重型COVID-19患者VTE发生风险。《上海市2019冠状病毒病综合救治专家共识》[14]中提出,重型COVID-19患者积极应用抗凝药物(如肝素)的有效性仍有待进一步验证。TANG等[15]研究显示,针对脓毒症伴凝血功能障碍或D-二聚体水平明显升高的重型COVID-19患者,使用肝素者28 d死亡率低于未使用肝素者。一项回顾性研究表明,与未接受低分子肝素治疗的COVID-19患者相比,接受低分子肝素治疗者死亡率明显降低[16]。但RUSSO等[17]研究表明,抗血小板、抗凝治疗均不能降低COVID-19患者ARDS或死亡风险。FLAM等[18]研究发现,口服抗凝剂并未降低重型COVID-19患者的死亡风险。MEIZLISH等[19]研究表明,中等剂量抗凝药物治疗可有效降低COVID-19患者住院死亡率。
有研究指出,鼓励轻型、普通型COVID-19患者积极活动,多饮水[20];对于Padua量表或Caprini血栓风险评估量表评估为VTE高危或中高危及低出血风险的COVID-19患者,建议首选低分子肝素治疗[20-21];对于高出血风险患者,建议使用间歇充气加压泵预防治疗[22];对于合并严重肾衰竭者(肌酐清除率<30 ml/min),建议使用普通肝素治疗;对于血小板减少或应用肝素期间出现肝素诱导性血小板减少症的患者,推荐应用阿加曲班、比卢伐定、利伐沙班等抗凝药物治疗。美国NIH发布的《新型冠状病毒肺炎治疗指南》中虽建议住院患者(非妊娠期成年人)采用预防性剂量的抗凝药物治疗,但不建议住院患者使用溶栓剂或高于预防性剂量的抗凝药物来预防VTE[7];如果患者正在应用抗凝或抗血小板药物,若无禁忌证可继续使用。目前越来越多的证据表明了抗凝药物可能会改善重型COVID-19患者预后。对此,笔者认为,在对COVID-19患者进行治疗前需进行VTE风险评估,对于高危或中高危VTE患者,主要采用抗凝药物进行治疗;对于低危VTE的重型、危重型COVID-19患者,需予以抗凝药物进行预防性治疗,还需综合考虑合并症(如肾功能降低、血小板减少)选择合适的药物进行治疗,见图1。GODINO等[9]提出了COVID-19患者抗血栓治疗管理方法,见图2,并指出在任何情况下均应对患者的基线特征、出血和血栓形成风险进行分析、评估。
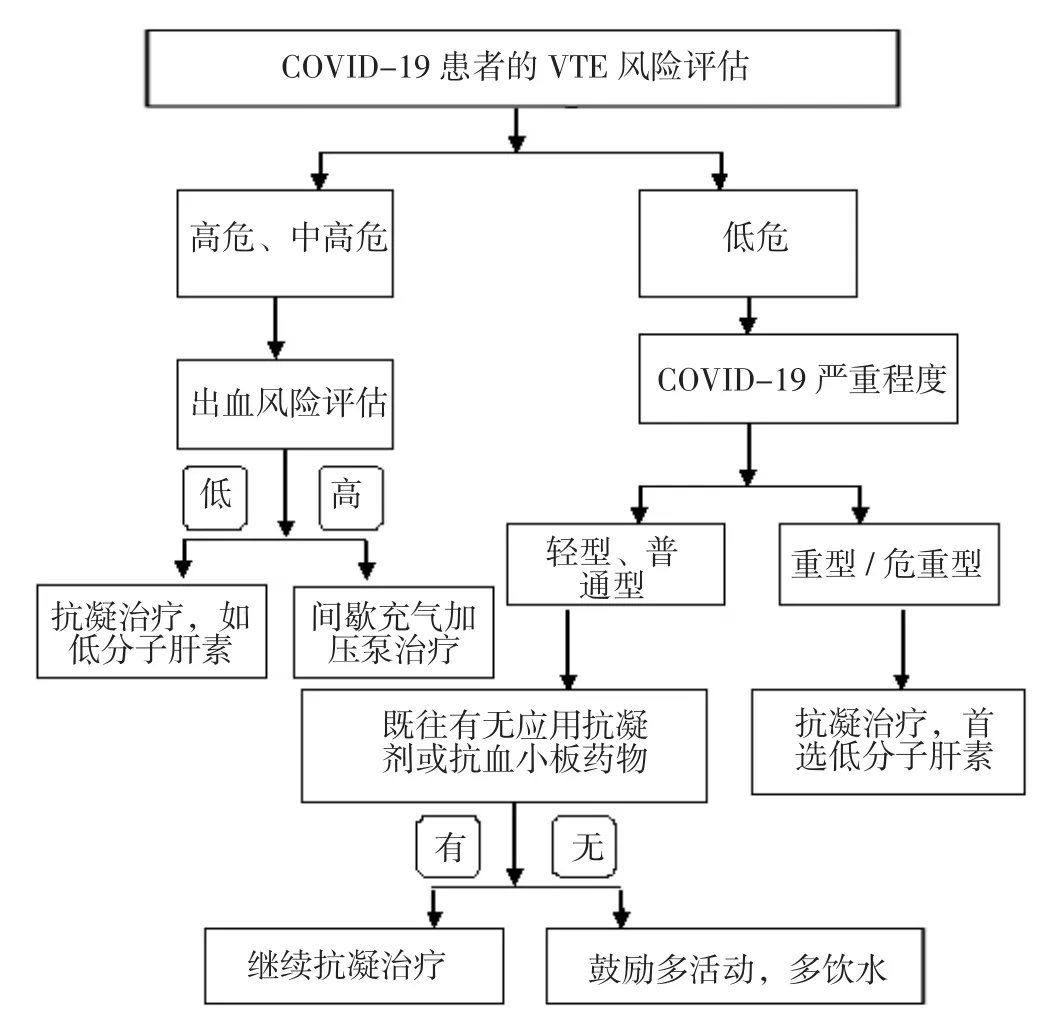
图1 COVID-19患者VTE风险评估及其治疗措施Figure 1 VTE risk assessment and treatment of COVID-19 patients
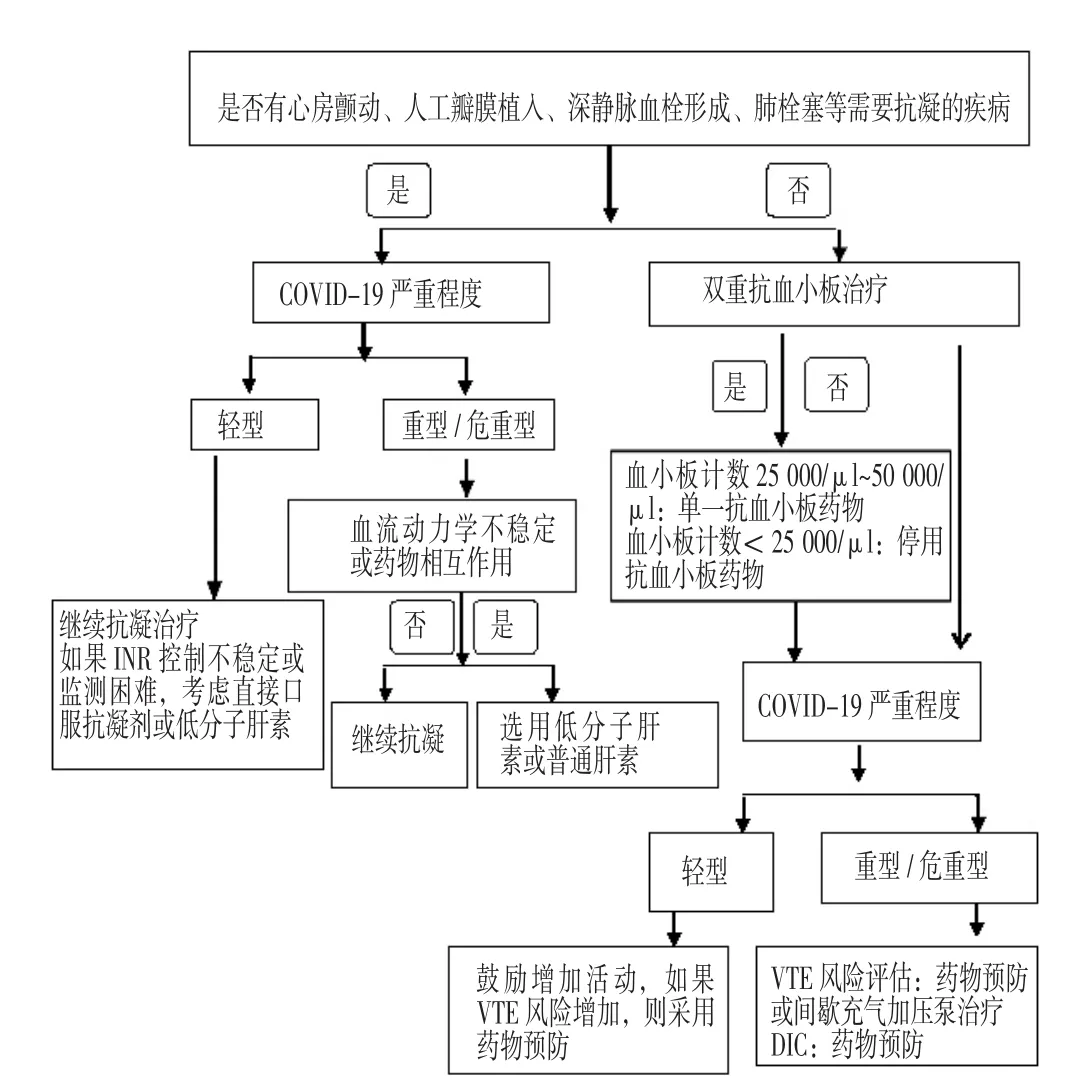
图2 COVID-19患者抗血栓治疗管理方法Figure 2 Management of antithrombotic therapy for COVID-19 patients
2.2 抗血小板治疗 SARS-CoV-2可导致血小板黏附和聚集,最终导致血栓形成。因此,早期应用抗血小板药物可有效抑制血小板黏附、聚集和激活,进而降低主要器官功能障碍发生风险,但其针对不同疾病的有效性仍存在争议。
RUSSO等[17]发现,入院前使用抗血小板药物并未降低COVID-19患者ARDS发生率和住院死亡率。双嘧达莫除具有抗血小板作用外,还具有广谱抗病毒、抗炎和抗纤维化的作用,其可通过抑制SARS-CoV-2复制而达到抗病毒的作用,可抑制炎症,促进黏膜愈合,还可有效预防脏器急性损伤和进行性纤维化发生。LIU等[23]研究表明,双嘧达莫可明显降低COVID-19患者D-二聚体水平,升高血小板计数和白细胞计数,提高重型COVID-19患者临床治愈率和缓解率,可作为辅助治疗。YUAN等[24]研究表明,服用小剂量阿司匹林与未服用阿司匹林的COVID-19患者全因死亡率无统计学差异。但一项回顾性研究显示,COVID-19患者在入院前1周内或入院后24 h内服用阿司匹林,可有效降低住院死亡率[25]。HAQUE等[26]研究表明,阿司匹林可有效预防COVID-19患者血栓性炎症、肺栓塞和血栓形成,并建议SARS-CoV-2感染患者尽早服用阿司匹林进行预防性治疗。最新研究发现,与未接受抗血小板治疗的患者相比,服用阿司匹林的COVID-19患者累积死亡率明显降低[19]。目前,关于COVID-19患者阿司匹林的使用还没有达成共识。
有研究指出,合并冠心病的COVID-19患者应继续服用抗血小板药物[27-28]。对于3个月前接受经皮冠状动脉介入治疗(PCI)的患者,应继续使用P2Y12抑制剂进行治疗;对于在3个月内接受PCI的患者应继续进行双重抗血小板治疗[27-29]。专 家 建 议, 如 果 血 小 板 计 数 为 25 000/μl~50 000/μl,则改用单一抗血小板药物,如果血小板计数<25 000/μl,则暂停治疗[30]。合并心房颤动、人工瓣膜等心脏疾病的COVID-19患者在采用双重抗血小板治疗期间,需始终考虑缺血风险与出血风险,见图2。
2.3 药物相互作用 在COVID-19患者治疗期间,口服抗凝剂与抗病毒药物存在相互作用,如细胞色素P4503A4酶(CYP3A4)对阿哌沙班、利伐沙班代谢具有重要作用,但对达比加群酯、艾多沙班的代谢无明显影响,而P糖蛋白(P-gp)是阿哌沙班、达比加群酯和利伐沙班的重要调节因子。因此,FDA建议COVID-19患者避免同时使用P-gp或CYP3A4诱导剂与阿哌沙班、利伐沙班[31]。此外,COVID-19患者口服抗凝剂与抗血小板药物间也存在潜在的药物相互作用,如洛匹那韦/利托那韦是一种蛋白酶抑制剂,可抑制CYP3A4代谢,但会导致氯吡格雷的有效剂量减少[32],也可能会增强替格瑞洛的作用,同时增加出血风险。因此,应谨慎联合应用氯吡格雷、替格瑞洛与洛匹那韦/利托那韦。替格瑞洛还有一个额外的抑制靶点,即平衡核苷转运体1(ENT1),其可抑制细胞腺苷摄取,从而增强抗炎作用。DE MATOS SOEIRO等[27]指出,氯吡格雷或替格瑞洛在与洛匹那韦/利托那韦同时使用时,需监测血小板活性,在没有禁忌证的情况下可以选择普拉格雷,若存在普拉格雷禁忌证,则可使用氯吡格雷。
基于此,笔者建议长期服用阿司匹林进行心血管预防的COVID-19患者可继续应用阿司匹林;对于合并其他并发症的患者,在应用抗血小板药物期间应注意出血风险及药物相互作用。目前COVID-19患者的抗血小板治疗还需要更多的临床研究来证实其临床获益。
3 小结与展望
COVID-19合并血栓并发症患者具有高的死亡率。因此,对COVID-19患者应该采取合理的抗血栓治疗,而抗血栓治疗(使用抗凝剂/抗血小板药物)的作用还需要在大型观察性研究和随机临床试验的背景下进一步评估。此外,随着公众对COVID-19患者血栓形成机制了解的增多,除了抗凝和抗血小板治疗,还需要探索其他有效的抗血栓治疗方法。
作者贡献:李树仁进行文章的构思与设计,负责文章的质量控制及审校,对文章整体负责、监督管理;李健超、赵文静负责文献/资料收集、整理、分析,撰写论文;郝潇、苑可心、郝清卿进行结果分析与解释;张飞飞、张倩辉进行论文的修订。
本文无利益冲突。

