脑小血管病患者认知障碍危险因素的Meta分析
郭文娟,李蕊萍,张綦慧
本Meta分析的优势与不足:
优势:本Meta分析纳入的文献数量较多、样本量较大,统计因素较全面,结果较稳定,无明显发表偏倚,具有一定代表性。
不足:(1)由于检索语言的限制,本Meta分析仅纳入公开发表的文献,未检索灰色文献,可能造成一定发表偏倚,影响Meta分析结果;(2)纳入研究大部分为我国境内某地区的病例对照研究,受研究类型及患者选择限制,无法避免实施、测量偏倚;(3)除本次Meta分析得出的危险因素外,尚存在其他影响脑小血管病(CSVD)患者认知障碍的危险因素,但由于相关文献数量较少而未进行合并分析。
脑小血管病(cerebral small vessel disease,CSVD)是一种常见的与年龄相关的脑部小动脉、小静脉和毛细血管等微血管病变,其发病与组织损伤缓慢积累有关,其主要表现为静态局灶性脑血管疾病,如静态局灶性腔隙性脑梗死、脑微出血、局部脑白质疏松、进行性认知障碍等[1],是导致认知障碍和血管性痴呆(vascular dementia,VD)的主要原因之一[2]。既往研究表明,CSVD发病率与年龄呈正相关,其中50岁人群CSVD发病率约为5%,90岁以上人群CSVD发病率几乎达到100%[3]。据统计数据显示,CSVD所致认知障碍占所有血管性认知障碍(vascular cognitive impairment,VCI)患者总数的50%~70%,是VCI的第一位病因[4]。根据流行病学调查数据推测,2050年痴呆患者总数将增至1.31亿[5]。虽然痴呆是不可逆转的疾病,但目前公认认知障碍是可以延缓或稳定的[6]。因此,探讨认知障碍的危险因素并尽早防治或可降低人群痴呆发生风险。本研究采用Meta分析方法分析CSVD患者认知障碍的危险因素,以期能早发现、早预防VCI。
1 资料与方法
1.1 文献纳入与排除标准
1.1.1 文献纳入标准 (1)研究类型:国内外公开发表的探讨CSVD进展为认知障碍影响因素的病例对照研究或队列研究。(2)研究对象:有明确的CSVD诊断标准,其中病例对照研究是以伴有认知障碍的CSVD患者为观察组,未伴有认知障碍的CSVD患者为对照组。队列研究是以随访期内发生认知障碍的CSVD患者为观察组,未发生认知障碍的CSVD患者为对照组。(3)危险因素:年龄、性别、受教育程度、吸烟、饮酒、体质指数(body mass index,BMI)、高血压、收缩压、舒张压、高脂血症、高胆固醇血症、糖尿病、动脉粥样硬化、卒中史、同型半胱氨酸(homocysteine,Hcy)、超敏C反应蛋白(high sensitivity C-reactive protein,hs-CRP)、胱抑素C(cystatin C,Cys C)、S100β蛋白、血尿酸(serum uric acid,SUA)、纤维蛋白原(fibrinogen,FIB)、基质金属蛋白酶9(matrix metalloproteinases 9,MMP-9)、碱性磷酸酶(alkaline phosphatase,ALP)、CSVD核磁总负荷评分、脑白质高信号(white matter hyperintensity,WMH)评分、脑室周围脑白质高信号(periventricular white matter hyperintensity,PVH)、深部脑白质高信号(deep white matter hyperintensity,DWMH)、腔隙性脑梗死(lacunar infarction,LI)病灶计数、脑微出血(cerebral microbleeds,CMBs)计数、扩大的血管周围间隙(enlarged perivascular spaces,ePVS)分级、脂蛋白相关磷脂酶A2(lipoprotein-associated phospholipase A2,Lp-PLA2)、过氧化物歧化酶(superoxide dismutase,SOD)、心房颤动、缺血性心脏病史、肌酐清除率、左心室射血分数(left ventricular ejection fraction,LVEF)、踝臂指数、臂-踝脉搏波速度(brachial-ankle pulse wave velocity,ba-PWV)、叶酸、维生素B12、觉醒次数及N3期睡眠比例。
1.1.2 文献排除标准 (1)重复发表的文献;(2)非中、英文文献;(3)无法提取危险因素的文献;(4)低质量文献;(5)综述;(6)基础实验、动物实验。
1.2 检索策略 计算机检索PubMed、Embase、Web of Science、Cochrane Library、中国知网、万方数据知识服务平台、维普网、中国生物医学文献数据库,检索时限为建库至2021-02-28。采用主题词与自由词结合的检索方式,中文检索词:脑血管病认知障碍、脑小血管病认知障碍、脑血管病认知损害、脑小血管病认知损害、脑血管病痴呆、脑小血管病痴呆、危险因素、影响因素、病因、相关因素、病例对照研究、病例对照、队列研究。英文检索词:CSVD、cerebral small vessel disease、cerebral microvascular disease、cognitive impairment、cognitive deficit、cognitive disorder、risk factor、related factors。
1.3 资料提取与方法学质量评价 由两名研究员独立提取资料并交叉核对,包括第一作者、发表时间、研究类型、国家、样本量及危险因素。由两名研究员按照纽卡斯尔-渥太华量表(Newcastle-Ottawa Scale,NOS)[7]独立评估纳入研究的方法学质量,共8个条目,总分9分,以NOS评分≥6分定义为高质量文献,反之定义为低质量文献。评价过程中如遇分歧,则通过协商或寻求第三方意见解决。
1.4 统计学方法 采用Stata 13.1和RevMan 5.3软件进行Meta分析。以OR及其95%CI作为效应量,以I2≤50%、P≥0.10为各研究间无统计学异质性,采用固定效应模型进行Meta分析;以I2>50%和/或P<0.10为各研究间存在统计学异质性,采用随机效应模型进行Meta分析。采用敏感性分析检验结果的稳定性;采用Begg's检验和Egger's检验评估文献的发表偏倚。双侧检验水准α=0.05。
2 结果
2.1 文献筛选流程及结果 初步检索到2 551篇文献,去除重复文献、数据无法提取的文献及综述、动物实验等不符合纳入标准的文献后剩余80篇,通过阅读全文最终纳入47篇文献[8-54],其中中文文献 33 篇[8,10,12-13,16-18,21-46]、英文文献 14 篇[9,11,14-15,19-20,47-54];病例对照研究 41 篇[8-48],队列研究6篇[49-54]。总样本量8 218例,其中观察组4 115例、对照组4 103例。文献筛选流程及结果见图1,病例对照研究及队列研究的基本特征及方法学质量评价结果见表1~2。
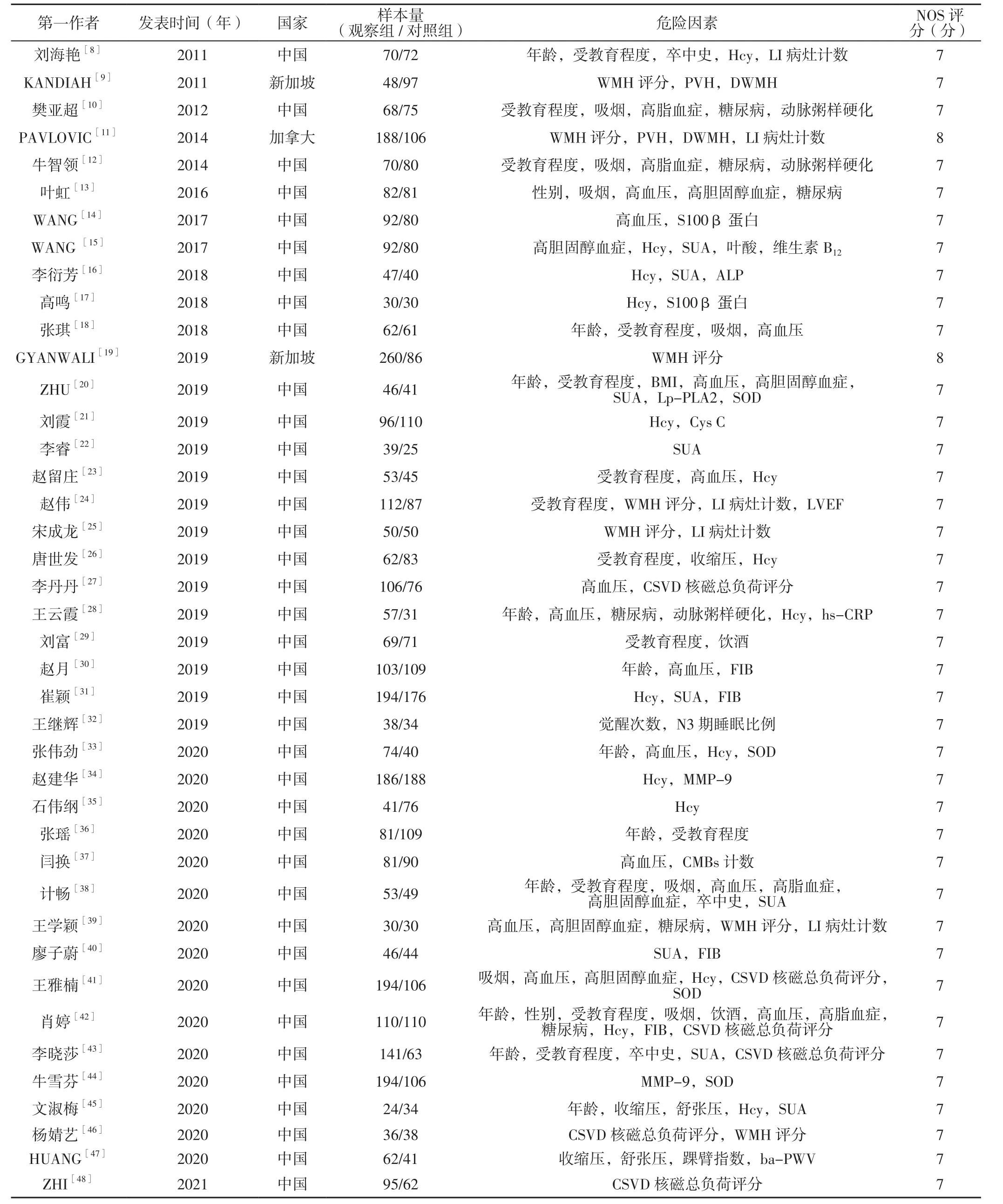
表1 病例对照研究的基本特征及方法学质量评价结果Table 1 Basic characteristics and methodological quality assessment results of included case control studies
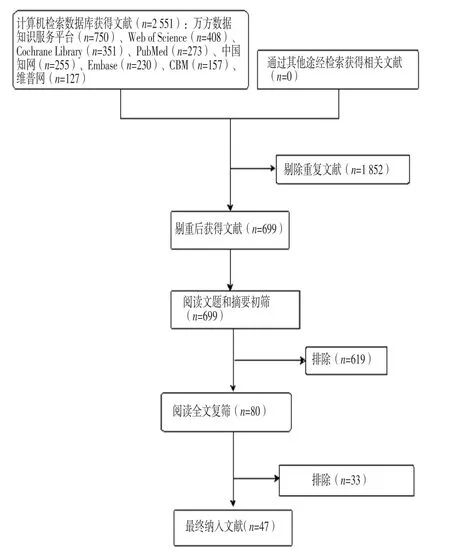
图1 文献筛选流程及结果Figure 1 Literature screening process and results
2.2 Meta分析结果 本Meta分析仅合并纳入文献数≥5条的危险因素,结果显示,受教育程度、吸烟、高血压、高脂血症、Hcy、CSVD核磁总负荷评分、WMH评分、LI病灶计数为CSVD患者认知障碍的危险因素(P<0.05),见表3。
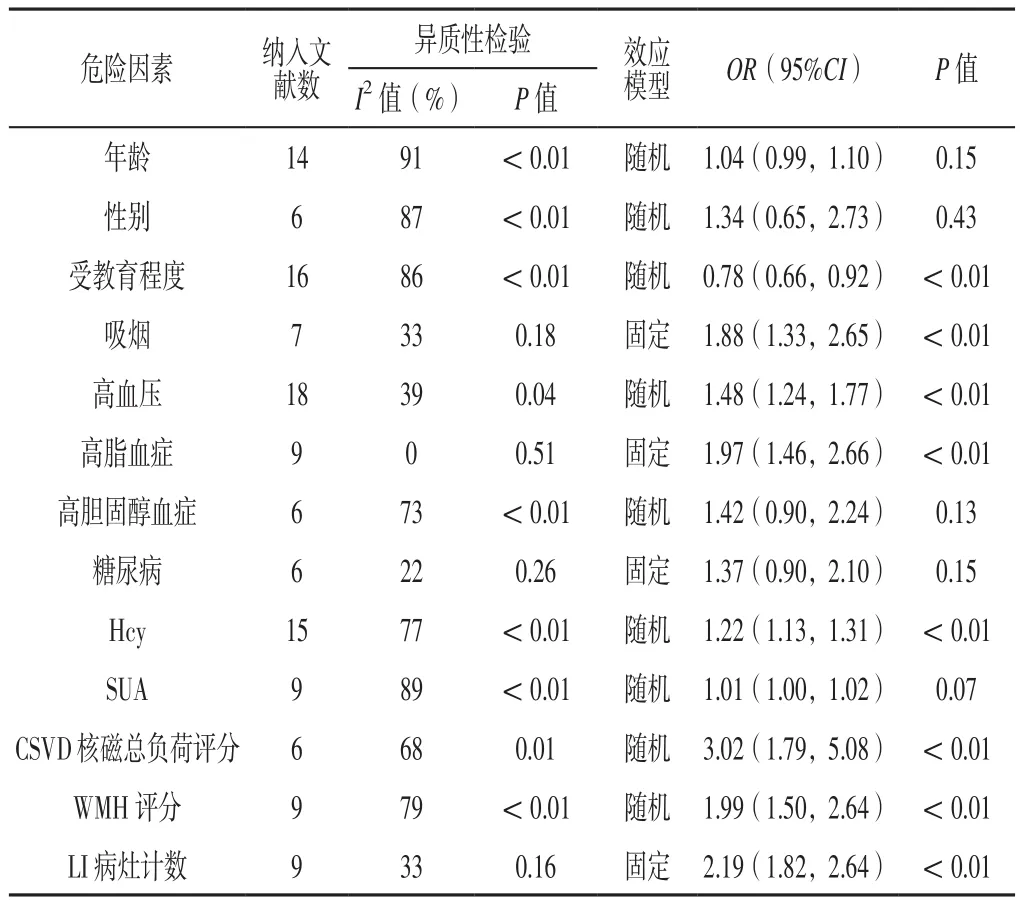
表3 CSVD患者认知障碍危险因素的Meta分析Table 3 Meta-analysis of risk factors for cognitive impairment in patients with CSVD
2.3 敏感性分析 敏感性分析结果显示,除性别外,其他危险因素的Meta分析结果均稳定。
2.4 发表偏倚 Begg's检验结果显示,报道年龄、性别、受教育程度、吸烟、高血压、高脂血症、高胆固醇血症、糖尿病、Hcy、SUA、CSVD核磁总负荷评分、WMH评分、LI病灶计数的文献无明显发表偏倚;Egger's检验结果显示,除Hcy和WMH评分外,报道其他指标的文献无明显发表偏倚,见表4。
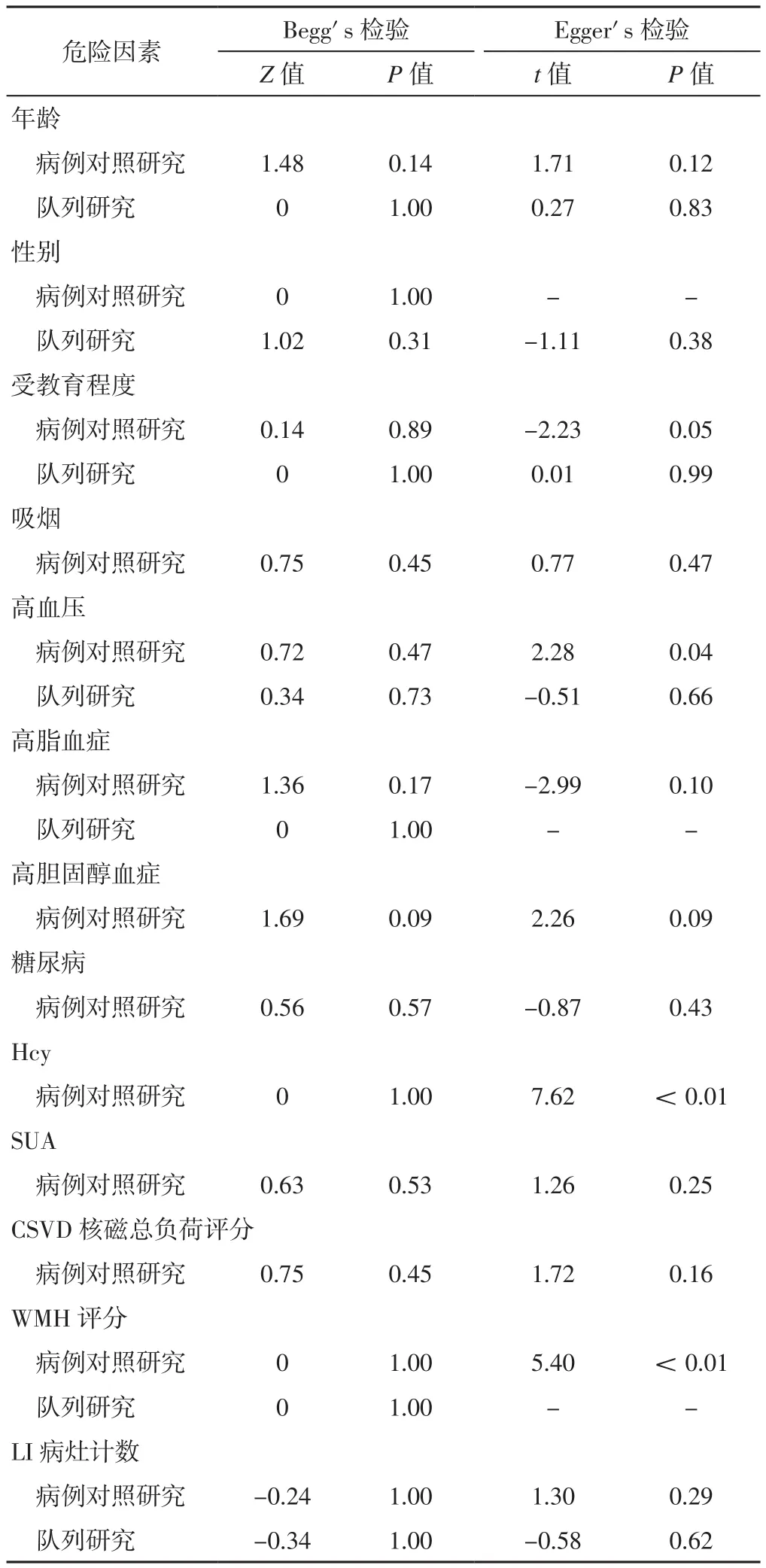
表4 报道CSVD患者认知障碍危险因素文献的发表偏倚Table 4 Publication bias of literatures reporting risk factors for cognitive impairment in patients with CSVD
3 讨论
目前,CSVD致认知障碍和痴呆的潜在机制尚不完全清楚,可能包括动脉僵硬和微血管功能障碍[55]。动脉僵硬导致动脉压力和血流搏动过大,向远端传播并损伤大脑微循环。大脑微血管调节包括脑灌注、神经发生、神经血管耦合、血-脑脊液屏障通透性和大脑自动调节,上述过程的损伤均可能导致神经元功能障碍和缺血,最终导致认知功能下降[56]。
本Meta分析结果显示,受教育程度、吸烟、高血压、高脂血症、Hcy、CSVD核磁总负荷评分、WMH评分、LI病灶计数是CSVD患者认知障碍的危险因素,其中CSVD核磁总负荷评分与CSVD患者认知障碍的关联最强,其次为LI病灶计数、高脂血症和WMH评分,分析其机制可能如下:研究表明,教育程度低与任何年龄的痴呆发病率较高有关[57]。既往研究表明,微血管损伤主要继发于血管危险因素,如高血压、糖尿病、高脂血症、肥胖、吸烟、遗传性血管疾病等[58],上述血管危险因素同时也是认知障碍的重要危险因素,可导致脑缺血或神经纤维变性,加重动脉粥样硬化,引起小动脉壁玻璃样变性[59-60]。有研究指出,动脉僵硬度与认知功能呈负相关[61];动态收缩压、脉压增大及血压下降均是CSVD患者认知障碍的危险因素[62],收缩压每升高10 mm Hg(1 mm Hg=0.133 kPa),认知功能下降风险就增加7%[63],其机制可能为收缩压的高负荷状态导致脉压增大,而脉压增大又导致血压昼夜节律减弱,加重小血管内皮功能损伤,增加血-脑脊液屏障通透性,进而导致血管内物质外渗,血管及其周围组织损伤,进一步导致血管炎症、神经元脱髓鞘、血管壁变厚、血管管腔狭窄,最终导致血管自我调节能力下降,引起慢性、进行性局部甚至弥漫性缺血、闭塞[62]。高同型半胱氨酸血症是VD和阿尔茨海默病的重要危险因素。研究表明,Hcy可干扰与神经元死亡和认知功能衰退相关的通路,其水平升高与认知功能下降、白质损伤、脑萎缩、神经纤维缠结和痴呆有关[64];Hcy水平与整体认知和注意力下降呈负相关,即浓度越高整体认知和注意力下降越明显[65]。研究表明,MRI上WMH的存在和严重程度对CSVD患者认知功能损伤具有重要负面影响[66-67],其机制主要为MRI上WMH与意识反应速度、执行控制和整体认知功能的恶化相关[68];此外,皮质下白质损伤还与CSVD患者血清神经酰胺水平升高和手部灵巧度降低有关[69]。LI患者大多表现为轻微或无身体缺损症状,因此LI导致的认知障碍在临床中常被忽视[70],但一项病例对照研究发现,与WMH的基线负荷相比,LI的基线数量是认知能力下降更强的预测因子,其可使认知功能缺损风险增加3倍[11]。CSVD核磁总负荷评分指MRI上的LI、WMH、CMBs和ePVS评分的总和,其较单独MRI特征能更好地反映CSVD对大脑的整体影响,CSVD核磁总负荷评分越高则患者认知功能越差[71]。但笔者发现,除WMH评分和LI病灶计数外,CSVD核磁其他指标(如皮质下微梗死、CMBs、ePVS和脑萎缩)及其他因素(如LVEF、踝臂指数、SUA等)均与CSVD患者认知障碍存在不同程度的联系,但由于目前缺乏充足证据,故在本Meta分析中未得到证实。
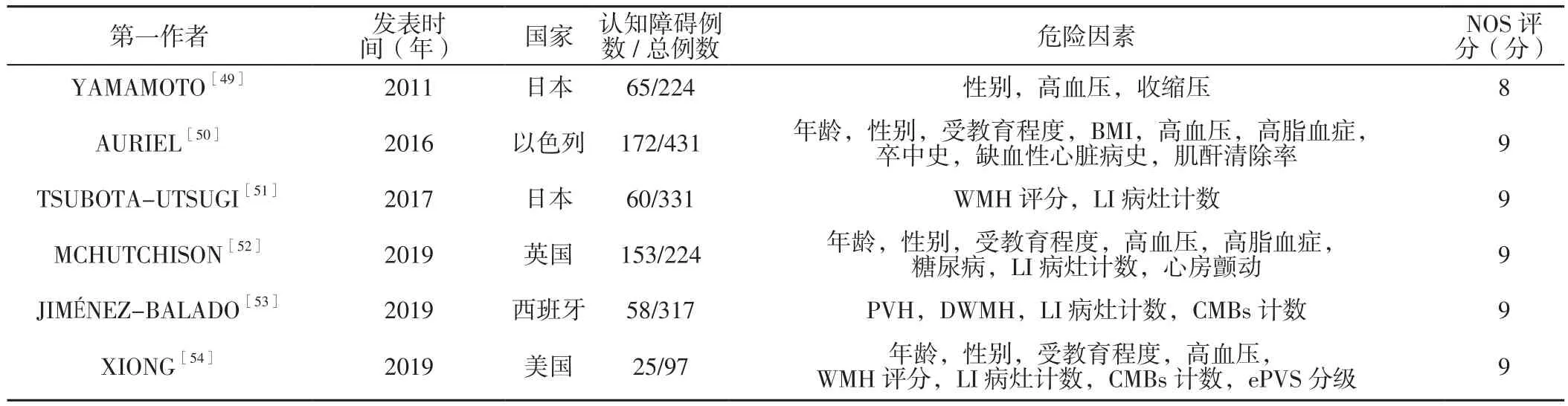
表2 纳入队列研究的基本特征及方法学质量评价结果Table 2 Basic characteristics and methodological quality assessment results of included cohort study
综上所述,现有证据表明,受教育程度低、吸烟、高血压、高脂血症、Hcy、CSVD核磁总负荷评分、WMH评分、LI病灶计数是识别和预测CSVD患者认知障碍首要考虑的危险因素,临床上针对伴有上述危险因素的CSVD患者应加强管理,以降低CSVD进展为认知障碍的风险。
作者贡献:郭文娟、李蕊萍、张綦慧进行文章的构思与设计;郭文娟、李蕊萍进行文献收集、数据整理和分析;郭文娟撰写论文;李蕊萍进行论文的修订;张綦慧对文章整体负责、监督管理。
本文无利益冲突。

