基于二氰基异佛尔酮的荧光探针在检测苯硫酚中的应用
张改清 阴彩霞
(1吕梁学院化学化工系,吕梁 033000)
(2山西大学分子科学研究所,化学生物学与分子工程教育部重点实验室,太原 030006)
硫醇主要包括脂肪硫醇和苯硫醇。半胱氨酸(cysteine,Cys)、同型半胱氨酸(homocysteine,Hcy)、谷胱甘肽(glutathione,GSH)等脂肪硫醇在生理过程中起着非常重要的作用[1-7]。作为硫醇的一种,苯硫酚被广泛用于农药生产、化学合成、制药工程和工业生产中的重要中间体,其使用不可避免地面临高毒性和高污染的重要问题[8-9]。苯硫酚及其衍生物具有高毒性,苯硫酚对鱼类的半致死剂量(LC50)范围为0.01~0.4 mmol·L-1[10],对小鼠的LC50 为2.15~46.2 mg·kg-1[11]。生物体长期接触硫酚会严重损害中枢神经和其他神经系统,导致呼吸急促、肌肉无力、后肢麻痹、昏迷甚至死亡[12-13]。因此,考虑到苯硫酚对生物和环境的不良影响,开发检测苯硫酚的简单、灵敏和具有选择性的方法是非常重要的。
由于具有成本低、灵敏度高以及生物相容性好等优点,荧光方法已在检测和标记中得到广泛应用,是一种非常有前景的工具[14]。由于异佛尔酮衍生物类荧光染料具有给体-π-受体(D-π-A)结构,其超快的分子内转移电荷(ICT)引起大的斯托克斯位移[15],该类染料已经开始应用于各类荧光探针的设计[16-17]。
到目前为止,许多苯硫酚荧光探针已经被设计、合成出来[18-20],但是大多数荧光探针仍是短波长发射。我们用2,4-硝基苯氟苯修饰了二氰基异佛尔酮衍生物,用作荧光开关,以获得用于检测苯硫酚的探针YC1。由于2,4-二硝基苯强的吸电子能力导致的部分的光致电子转移(PET)过程,探针YC1基本上具有较弱的荧光。苯硫酚通过芳香族亲核取代反应机理与探针YC1 发生反应,2,4-二硝基苯作为离去基团离去,随后释放荧光化合物2(发射峰主要在594 nm处),荧光响应信号增强(turn-on),计算得到相应的检出限为0.65 μmol·L-1。此外,探针被成功应用于HeLa细胞内4-甲基苯硫酚的成像。
1 实验部分
1.1 仪器和试剂
1.1.1 仪 器
所用仪器有ME204E 电子天平、FE20-FIve Easy PlusTM酸度计、Bruker AVANCE-600 MHz 核磁共振仪、LTQ-MS(Thermo)电喷雾质谱、U-3900 紫外-可见分光光度计、F-7000 荧光分光光度计、TCS SP5 激光扫描共聚焦显微镜。
1.1.2 试 剂
异佛尔酮、丙二腈、哌啶、冰醋酸、4-羟基-3-甲氧基苯甲醛(香草醛)、2,4-二硝基氟苯和4-甲基苯硫酚等均为分析纯,购自上海阿拉丁试剂有限公司。4-甲基苯硫酚以及探针YC1 的储备溶液用二甲亚砜(DMSO)溶液作为溶剂配制得到。
1.2 探针YC1的制备
探针YC1 的合成路线及响应机理如Scheme 1所示,探针YC1通过3步反应即可得到。
化合物1 和化合物2 根据文献报道的方法合成[21]。
探针YC1 的合成:向化合物2(640 mg,2.0 mmol)与N,N-二甲基甲酰胺(DMF,10 mL)的混合溶液中加入1-氟-2,4-二硝基苯(391 mg,2.1 mmol)和K2CO3(548 mg,4 mmol),室温搅拌2 h。反应过程通过TLC 监测。待反应完成后,除去溶剂。所得粗产品通过硅胶柱色谱法(乙酸乙酯/石油醚,1∶3,V/V)纯化,得到深黄色固体YC1(613 mg,产率为63%)。
结构表征:1H NMR(600 MHz,DMSO-d6):δ8.90(d,J=13.2 Hz,1H),8.41(d,J=9.2 Hz,1H),7.67(d,J=21.9 Hz,1H),7.59~7.47(m,1H),7.45~7.30(m,3H),7.03(d,J=9.3 Hz,1H),6.93(s,1H),3.83(d,J=19.3 Hz,3H),2.63(d,J=18.8 Hz,2H),2.57(s,2H),1.04(s,6H)。13C NMR(151 MHz,DMSO-d6):δ170.8,156.1,155.4,151.4,142.2,141.6,138.8,137.0,136.4,130.8,130.0,123.6,123.1,122.5,122.3,118.1,114.3,113.5,112.6,77.2,56.6,42.8,38.7,32.2,27.9。ESI-MSm/z:[YC1-H]-即[C26H22N4O6-H]-计算值485.146 1;实测值485.147 0。元素分析按C26H22N4O6的计算值(%):C 64.19,H 4.56,N 11.52。实测值(%):C 64.15,H 4.57,N 11.54。
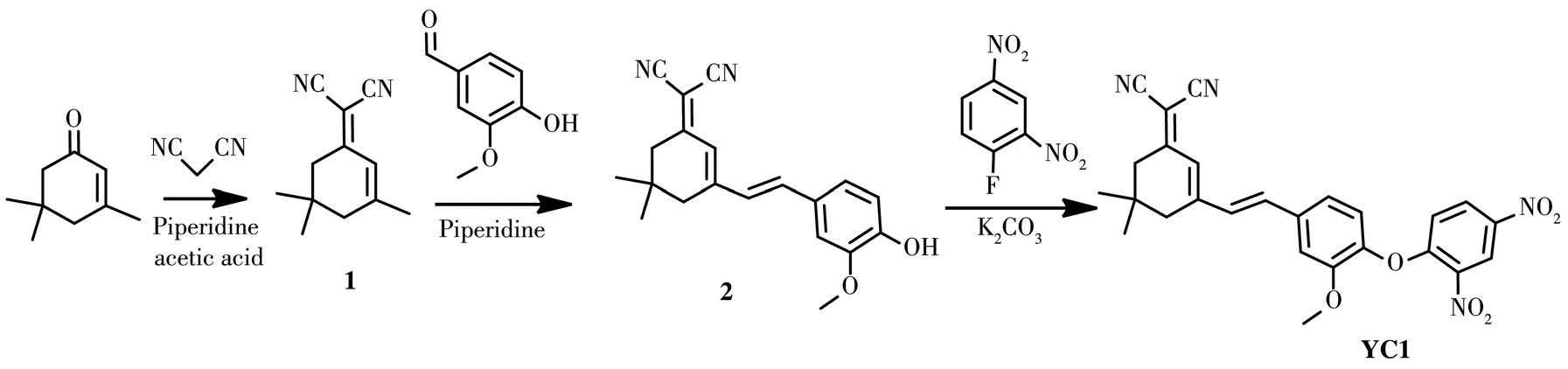
Scheme 1 Synthetic route of probe YC1
1.3 细胞成像
将HeLa细胞接种在激光共聚焦培养皿中,并将细胞于37 ℃、CO2体积分数5%的孵育箱中继续培养24 h以进行荧光成像实验。荧光成像通过共聚焦激光扫描显微镜进行。在种有HeLa 细胞的激光共聚焦培养皿中用探针YC1(5 μmol·L-1)预处理20 min。外源性4-甲基苯硫酚成像:再孵入20 μmol·L-14-甲基苯硫酚孵育30 min,用458 nm 激发获得在红色通道中的活细胞激光共聚焦成像。
2 结果与讨论
2.1 探针YC1的设计以及响应机制
考虑到二氰基异佛尔酮作为荧光母体是一种典型的基于ICT 的荧光团,具有长波长荧光发射、大的斯托克斯位移和良好的光稳定性等优势,我们选择二氰基异佛尔酮作为设计探针的荧光团,通过一个醚键,将二氰基异佛尔酮荧光母体与2,4-二硝基苯基作为识别位点的两部分连接成一体。由于2,4-二硝基苯强的吸电子能力导致的部分的PET 过程,探针YC1 基本上是较弱的荧光。苯硫酚中的羟基具有强的亲核性,通过芳香族亲核取代反应机理与探针YC1 发生反应,2,4-二硝基苯作为离去基团离去,随后释放荧光化合物2(主要是酚形式,发射峰主要在594 nm 处),荧光响应信号增强(turn-on)。Scheme 2 显示了YC1 探针对4-甲基苯硫酚的检测机理。通过质谱法验证了该机理。在图S4(Supporting information)的核磁氢谱中,我们找到了反应后荧光母体上活泼氢的化学位移δ=9.60。核磁结果支持了Scheme 2 中的反应机理。此外,由质谱(图S5)结果发现,[YC1+4-methylthiophenol-H]-(即[C26H22N4O6+C7H8S-H]-)的m/z计算值319.145 2,与实测值(319.1450 7)吻合,这也支持了Scheme 2 中的反应机理。
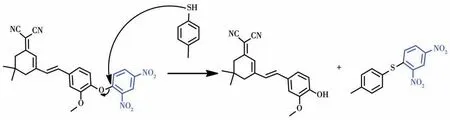
Scheme 2 Response mechanism of probe YC1 for detecting 4-methylthiophenol
2.2 探针YC1识别4-甲基苯硫酚的UV-Vis吸收光谱研究
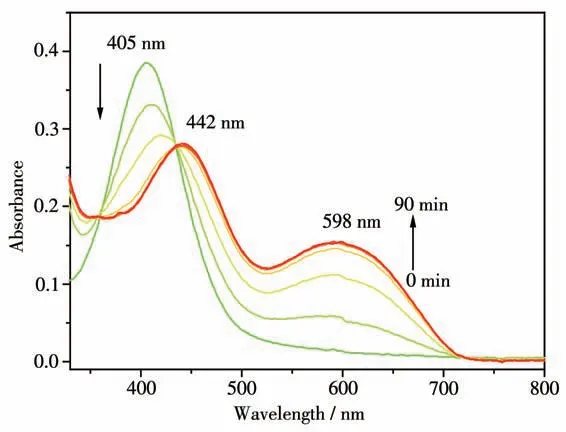
图1 探针YC1检测4-甲基苯硫酚的UV-Vis吸收光谱Fig.1 UV-Vis absorption spectra of YC1 probe for detecting 4-methylthiophenol
探针YC1 检测4-甲基苯硫酚的UV-Vis 吸收光谱如图1 所示。当200 μmol·L-1的4-甲基苯硫酚加入到含有10 μmol·L-1探针YC1 的PBS(磷酸缓冲盐溶液)/DMSO(1∶1,V/V,pH=7.4)体系中,随着时间的增加,405 nm 处的吸收峰值逐渐下降且红移至442 nm 处,同时在598 nm 处出现新的吸收峰且峰值逐渐升高,同时,溶液颜色由浅黄色变为深黄色。二氰基异佛尔酮类荧光团的pKa较高(7.90),在生理条件下会发生部分解离,从而生成2种荧光团:酚形式(主要形式)和酚盐形式(次要形式)。405 nm 为探针自身的吸收峰。当与苯硫酚反应后,生成带有羟基的二氰基异佛尔酮类荧光团,部分解离生成2 种形式的荧光团的酚形式(主要形式)和酚盐形式(次要形式),UV-Vis 光谱中442 nm 为酚形式的吸收,598 nm为酚盐形式的吸收。这说明探针YC1 与4-甲基苯硫酚反应生成了新的化合物,与前述核磁与质谱的结果一致。
2.3 探针YC1识别4-甲基苯硫酚的荧光光谱研究
探针YC1检测4-甲基苯硫酚的荧光光谱如图2所示。探针YC1 在该体系中有较弱的荧光。当30 μmol·L-1的4-甲基苯硫酚加入到含有5 μmol·L-1探针YC1的PBS/DMSO(1∶1,V/V,pH=7.4)体系中,随着时间的增加,594 nm 处出现明显的荧光强度增强。这说明探针YC1 能够用来识别4-甲基苯硫酚,且具有明显的荧光增强(turn-on)响应。
2.4 探针YC1识别4-甲基苯硫酚的动力学研究
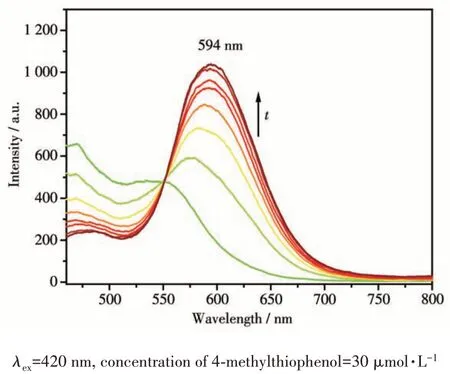
图2 探针YC1检测4-甲基苯硫酚的荧光光谱Fig.2 Fluorescence spectra of YC1 probe for detecting 4-methylthiophenol
探针YC1 检测4-甲基苯硫酚的动力学研究使用的是荧光光谱法,结果如图3 所示。对探针YC1持续光照1.5 h 之后,荧光强度基本不变,说明探针YC1 具有一定的光稳定性。当不同浓度的4-甲基苯硫酚(0、5、10、15、20、25 和30 μmol·L-1)加入到含有5 μmol·L-1探针YC1 的PBS/DMSO(1∶1,V/V,pH=7.4)体系中,可以发现4-甲基苯硫酚的浓度为20 μmol·L-1,时间约90 min 时,荧光响应信号基本达到一个动态平衡状态(激发波长为420 nm,发射波长为594 nm,激发狭缝宽度/发射狭缝宽度:5 nm/5 nm)。

图3 探针YC1检测4-甲基苯硫酚的动力学Fig.3 Kinetic of detecting 4-methylthiophenol by YC1 probe
2.5 探针YC1识别4-甲基苯硫酚的pH体系研究
为了考察探针YC1 识别4-甲基苯硫酚的有效pH 范围,我们研究了不同pH 值(2~10)对探针YC1(5 μmol·L-1)和YC1(5 μmol·L-1)+4-甲基苯硫酚(20 μmol·L-1)荧光性质的影响。从图4 中,我们可以发现强酸以及强碱条件对探针YC1 本身的荧光强度没有影响。而探针YC1 检测4-甲基苯硫酚时,在pH=6.0~8.0范围内荧光响应信号明显。这一结果表明,该探针能够应用于生理环境下检测苯硫酚。
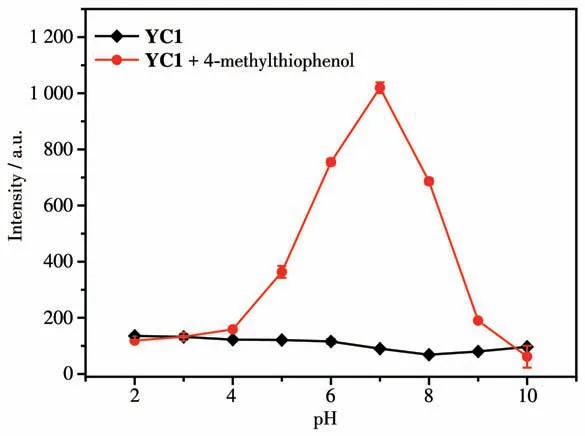
图4 不同pH值下YC1(5 μmol·L-1)和YC1(5 μmol·L-1)+4-甲基苯硫酚(20 μmol·L-1)的荧光强度Fig.4 Fluorescence intensity of YC1(5 μmol·L-1)and YC1(5 μmol·L-1)+4-methylthiophenol(20 μmol·L-1)under different pH values
2.6 探针YC1识别4-甲基苯硫酚的选择性研究
为了研究探针YC1 的选择性,采用荧光光谱考察了探针YC1 对4-甲基苯硫酚的识别性能。在含有5 μmol·L-1探针YC1 的PBS/DMSO(1∶1,V/V,pH=7.4)体系中,先后分别加入100 μmol·L-1各种分析物与20 μmol·L-14-甲基苯硫酚,分别进行检测。各种分析物分为2 组,第1 组如图5a 所示,第2 组如图5b所示。可以看出,探针与其他分析物不能引起YC1在594 nm 处的荧光强度增强,而只有在4-甲基苯硫酚(20 μmol·L-1)存在的情况下,YC1 在594 nm 处的荧光强度才能增强。这些结果表明,探针YC1 可以较好地选择性识别4-甲基苯硫酚,其他分析物的存在不干扰探针YC1对4-甲基苯硫酚的检测。
2.7 探针YC1识别4-甲基苯硫酚的检测限研究
为了研究探针YC1 对4-甲基苯硫酚的灵敏度,我们将不同浓度的4-甲基苯硫酚(2~10 μmol·L-1)分别加入到含有5 μmol·L-1探针YC1 的3 种不同混合体系中,测试其相应的荧光强度。根据594 nm 处的荧光强度变化值与对应的4-甲基苯硫酚浓度得到工作曲线(Y=Ac+B),c的单位为μmol·L-1,测量时的激发波长为420 nm,结果如图6 所示。根据IUPAC规定的检测限公式:LOD=kSb/m[22](其中k为与置信度有关的常数,IUPAC建议取k=3,Sb为空白标准偏差,m为分析标准曲线在低浓度范围内的斜率),可以算出探针YC1 在池塘水、自来水和PBS 中对4-甲基苯硫酚的检测限分别为0.19、0.38和0.65 μmol·L-1,。
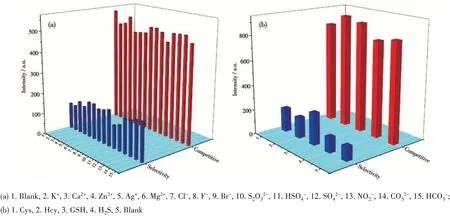
图5 探针YC1对4-甲基苯硫酚的选择性及分析物竞争性Fig.5 Selectivity and analyte competitive of YC1 probe to 4-methylthiophenol
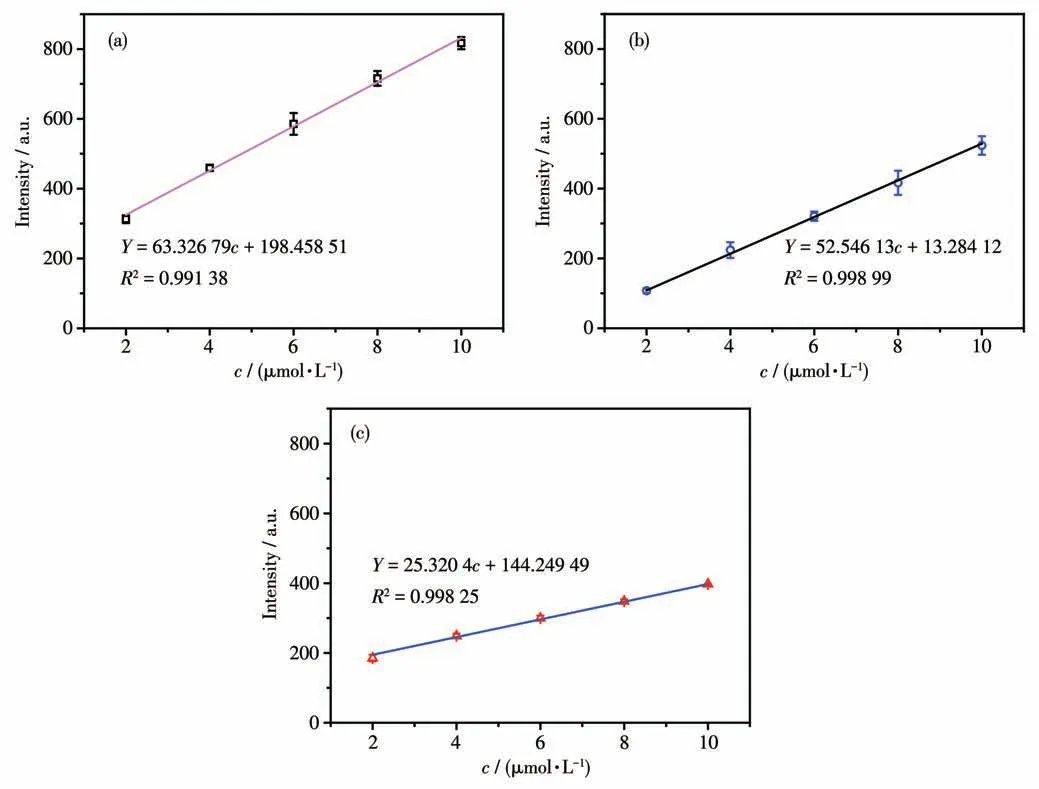
图6 在不同水样中探针YC1荧光强度与4-甲基苯硫酚浓度的线性相关:(a)池塘水、(b)自来水和(c)PBSFig.6 Linear correlation between fluorescence intensity of probe YC1 and 4-methylthiophenol concentration in different water samples:(a)pond water,(b)tap water and(c)PBS
2.8 探针YC1识别4-甲基苯硫酚的细胞成像研究
探针YC1 在活细胞内对4-甲基苯硫酚的成像标记能力通过激光共聚焦显微镜来评估。图7所示的是将5 μmol·L-1探针孵育到HeLa 细胞中,20 min后没有明显的荧光信号;接着将5 μmol·L-1探针孵育到HeLa 细胞中,再孵入20 μmol·L-1的4-甲基苯硫酚,30 min 后产生明显的红色荧光。细胞成像实验表明探针具有较好的细胞膜通透性,并且探针可以用来标记活细胞中外源性的4-甲基苯硫酚。
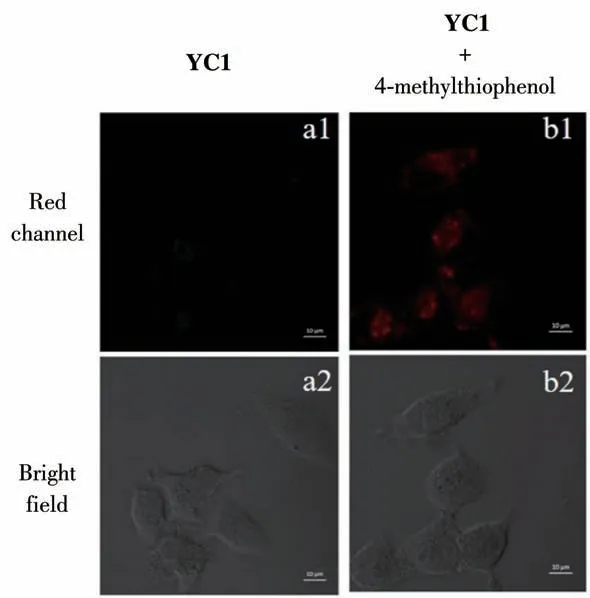
图7 探针YC1对4-甲基苯硫酚的激光共聚焦成像:只有探针的荧光图(a1)和明场图(a2);外源性4-甲基苯硫酚响应荧光图(b1)和明场图(b2)Fig.7 Confocal laser imaging of probe YC1:fluorescence image(a1)and bright field image(a2)of the probe;fluorescence image(b1)and bright field image(b2)of exogenous 4-methylthiophenol response
3 结 论
我们选择具有强吸电子基的2,4-二硝基苯与二氰基异佛尔酮衍生物连接,设计并合成了基于二氰基异佛尔酮的荧光探针YC1 用于特异性检测苯硫酚。苯硫酚通过芳香族亲核取代机制与探针YC1 发生反应,导致2,4-二硝基苯部分离去,随后释放具有明显荧光发射的化合物2,荧光响应信号(594 nm)增强。在PBS/DMSO 的体系中,YC1对苯硫酚的检出限为0.65 μmol·L-1。该方法是基于探针YC1 对4-甲基苯硫酚的识别具有荧光增强(turn-on)的性质。此外,探针还可以在HeLa细胞中实现对外源性4-甲基苯硫酚的荧光成像。该检测方法可以为今后的苯硫酚检测提供一个有用的工具与手段。
Supporting information is available at http://www.wjhxxb.cn

