胃神经内分泌肿瘤的病理学特征及临床意义
郭茹菲,王丰,杜明哲,李珊珊
(郑州大学第一附属医院 病理科,河南 郑州 450052)
神经内分泌肿瘤(neuroendocrine neoplasms,NENs)是一组起源于肽能神经元和神经内分泌细胞的高度异质性肿瘤,可以从缓慢生长的低度恶性发展到高转移、高复发风险的高度恶性[1]。NENs主要发生在胃、肠和胰腺等消化系统中。但在消化系统中,胃神经内分泌肿瘤(gastric neuroendocrine neoplasms,G-NENs)相对少见,约占胃肠道神经内分泌肿瘤的3%和胃恶性肿瘤的0.3%[2]。近年来,G-NENs的检出率升高,可能与内镜的普及以及临床医生对该病认识的加深有关[3]。对于这样一类异质性肿瘤,除了早发现,更重要的是对G-NENs准确的分级、分型,以确定最佳治疗方案。本研究收集并整理了142例G-NENs病例,参照2019年WHO消化系统肿瘤分类[4]和2020年中国胃肠胰神经内分泌肿瘤病理诊断共识[5],对其进行分型分析,以提高病理医生对此类疾病不同分型的认识,为临床医生的分型诊断提供参考。
1 资料与方法
1.1 研究对象收集142例2017年1月至2019年12月郑州大学第一附属医院收治的G-NENs患者的临床资料,内镜活检标本54例,内镜切除标本36例,手术切除标本52例。收集患者的临床特征、血清学检测结果、内镜表现等,分析G-NENs患者的病理特征与临床特征的相关性。
1.2 病理学诊断标准G-NENs的分类、分级和分型参照2019年WHO消化系统肿瘤分类和2020年中国胃肠胰神经内分泌肿瘤病理诊断共识。(1)神经内分泌瘤(neuroendocrine tumor,NET),分为低级(G1)、中级(G2)、和高级(G3);(2)神经内分泌癌 (neuroendocrine carcinoma,NEC),包括大细胞NEC和小细胞NEC;(3)混合性神经内分泌-非神经内分泌肿瘤(mixed neuroendocrine-non-neuroendocrine neoplasm,MiNEN)[一种包括混合性腺神经内分泌癌(mixed adenoneuroendocrine carcinoma,MANEC)的综合分类,此类型肿瘤的两种成分至少各占30%[4]]。见表1。
分型:根据发病机制、胃泌素及胃酸水平、内镜表现、肿瘤组织学特点及周围胃黏膜背景,分化较好的G-NET分为Ⅰ、Ⅱ、Ⅲ型。Ⅰ、Ⅱ型为肠嗜铬样细胞(ECL-细胞)G-NET,通常伴有高胃泌素血症,但病因不同;Ⅲ型胃泌素水平正常,病因尚不完全明确。分化差的G-NEC/MANEC恶性程度较高,预后差,已不再归于Ⅳ型。
1.3 方法
1.3.1临床检验 采用ELISA法测定空腹静脉血胃泌素水平,试剂购自上海江莱生物科技有限公司;胃24 h pH值通过便携式24 h pH监测仪测定,由Digitrapper公司提供;对提示Ⅰ型患者检测其抗胃壁细胞抗体,试剂来自德国欧盟(杭州)医学诊断公司。
1.3.2免疫组织化学 所有标本均经体积分数为3.7%的中性甲醛固定、脱水、石蜡包埋、4 μm切片、免疫组织化学染色并镜下观察。采用Roche BenchMark XT全自动免疫组织化学检测仪,Syn、CgA、Ki-67一抗均购自北京中杉金桥生物技术有限公司。Syn和CgA以细胞质棕黄色为阳性,Ki-67以细胞核棕黄色为阳性。
1.3.3随访 方式为电话随访,内容包括治疗方案、生存状态、肿瘤转移情况。随访结束时间为2020年8月。
1.4 统计学方法应用SPSS 21.0统计软件分析数据。计数资料以频数(n)和率(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 临床病理特征142例G-NENs患者中,Ⅰ型43例(30.28%),Ⅱ型10例(7.04%),Ⅲ型32例(22.54%),NEC 49例(34.51%)、MANEC 8例(5.63%)。首发症状:67.61%(96/142)患者表现为腹部不适(腹痛、腹胀、腹泻),11.97%(17/142)患者表现为恶心呕吐、反酸、烧心,3.52%(5/142)患者体检时发现病变;3.52%(5/142)Ⅲ型和G-NEC/MANEC患者可有呕血、黑便,13.38(19/142)% G-NEC/MANEC患者还可有吞咽困难、进食哽噎及乏力、消瘦等恶病质表现。Ⅰ型、Ⅱ型多见于60岁以下女性,肿瘤多位于胃体,主要表现为多发隆起型病变,最大径多<2 cm。Ⅲ型患者性别、年龄分布无明显差异,肿瘤多位于胃体,肿瘤多单发,主要表现为隆起型病变,2例表现为溃疡型病变(均为NET G3),最大径多<2 cm。G-NEC/MANEC男性多见,主要是老年患者,肿瘤多位于贲门-胃底,主要表现为单发巨大溃疡型病变。不同分型G-NENs在性别、发病年龄、肿瘤部位、肿瘤数目、肿瘤形态及最大径方面存在差异(P<0.05)。见表2。
2.2 病理分级及镜下特点43例Ⅰ型G-NET中,病理分级主要是G1、G2级,无G3级病例,G1占大多数,明显多于G2。10例Ⅱ型G-NET中,病理分级也主要是G1、G2级,无G3级病例,G1多于G2。32例Ⅲ型G-NET中,病理分级以G1、G2级为主,可有G3级。见表2。Ⅰ型、Ⅱ型病理分级均为G1、G2,镜下特点为分化良好的肿瘤细胞呈小梁状/腺样结构排列,胞质丰富嗜酸,细胞核形态单一,圆形/卵圆形,无坏死,核分裂象罕见。两者镜下不同之处在于胃黏膜背景的改变,Ⅰ型周围胃黏膜呈萎缩性胃炎改变,其中假幽门腺化生32例(74.42%),肠上皮化生11例(25.58%)。Ⅱ型中,周围胃黏膜呈肥厚性胃炎改变2例(20.00%)、未见特殊改变8例(80.00%)。Ⅲ型G-NET分级为G1、G2的肿瘤组织学特点与Ⅰ、Ⅱ型类似,分级为G3的肿瘤细胞有一定异型性,核分裂象增多;肿瘤旁胃黏膜背景均无特殊改变。57例G-NEC/MANEC患者中,49例为NEC,8例为MANEC,神经内分泌癌区域镜下特点为分化差的肿瘤细胞弥漫片状分布或排列成器官样、巢状,可见较多坏死,核分裂象多见。
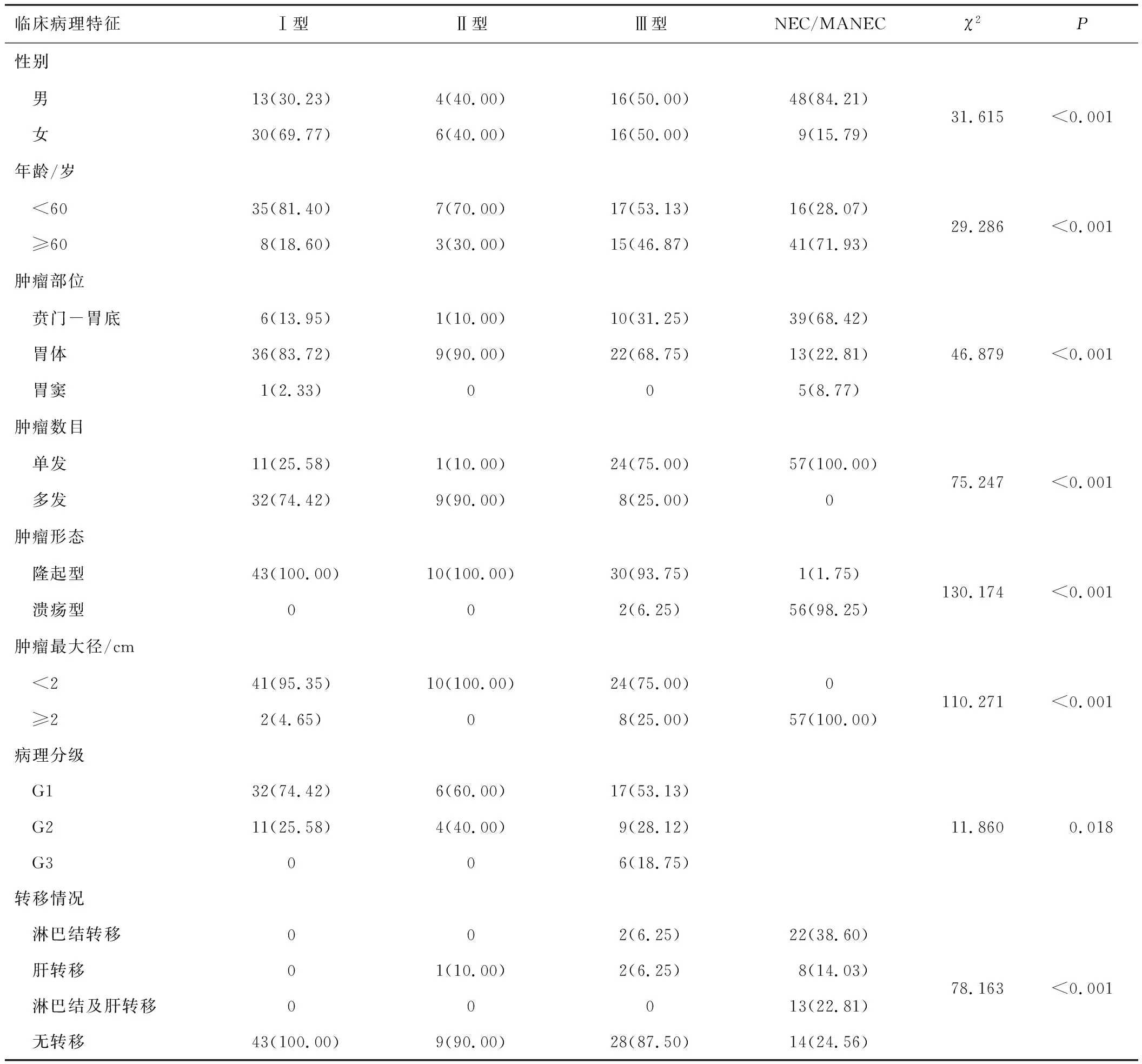
表2 142例G-NENs的临床病理特征[n(%)]
2.3 免疫组织化学结果142例G-NENs Syn均阳性表达(100%)。CgA阳性率67.60%,其中Ⅰ型88.37%(38/43),Ⅱ型 90.00%(9/10),Ⅲ型 75.00%(24/32),G-NEC/MANEC 43.86%(25/57)。
2.4 相关临床检验结果43例Ⅰ型G-NET均接受血清胃泌素检测后显示胃泌素水平升高(150~854 ng·L-1)(正常值25~104 ng·L-1);41例接受胃24 h pH值监测,其中37例(90.24%,37/41)胃酸水平降低;23例接受抗胃壁细胞抗体检测,其中21例结果为阳性(91.30%,21/23)。10例Ⅱ型G-NET接受胃泌素检测后显示胃泌素水平均升高(246~1 156 ng·L-1),胃24 h pH值监测提示胃酸水平升高。32例Ⅲ型G-NET中,26例接受胃泌素检测,结果均在正常范围内(28~68 ng·L-1)。
2.5 临床及随访情况43例Ⅰ型G-NET中,29例(67.44%)接受内镜下切除治疗,4例(9.30%)接受内镜+奥曲肽治疗,2例接受生长抑素受体扫描显示,99Tcm-奥曲肽显像阳性,2例内镜下切除后胃泌素水平仍偏高,1例(2.33%)接受内镜切除+化疗(分级为G2且肿瘤最大径为5 cm),2例(4.65%)接受手术治疗(1例G2级,1例外院内镜活检示胃底腺癌,郑州大学第一附属医院术后病理诊断为NET G1),7例(16.28%)肿瘤最大径<0.5 cm的病例接受动态观察及定期内镜复查。10例Ⅱ型G-NET中,7例(70.00%)接受内镜下治疗,2例(20.00%)接受手术切除治疗,1例(10.00%)接受内镜+奥曲肽治疗(分级为G2且肝转移)。32例Ⅲ型G-NET中,19例(59.38%)接受内镜下切除治疗,11例(34.37%)接受手术治疗(3例G1级、4例G2级、4例G3级,其中 2例 G3级同时接受化疗),2例(6.25%)接受化疗(分级为G3且影像学提示肝转移)。57例G-NEC/MANEC患者,37例(64.91%)接受手术治疗,其中32例接受联合化疗(17例淋巴结转移,4例淋巴结及肝转移);20例(35.09%)接受化疗(其中17例肝转移)。Ⅰ、Ⅱ型随访期间均未死亡(0/53)。Ⅲ型中,2例(6.25%)NET G3随访期间死亡(1例淋巴结转移、1例肝转移)。G-NEC/MANEC中,20例(35.09%)随访期间死亡(8例淋巴结转移,5例肝转移,7例淋巴结及肝转移)。
3 讨论
胃原发性神经内分泌肿瘤是一类罕见的异质性肿瘤,近年来其发病率不断上升,可能与内镜检查的普及、免疫组化染色技术的提高、肿瘤生物标志物的增加以临床医生及对诊断的认识增加有关[6]。
本研究中85例分化较好的G-NET中Ⅰ型最多见(50.59%,43/85),Ⅲ型次之(37.65%,32/85),Ⅱ型罕见(11.76%,10/85)。57例分化差的G-NEC/MANEC约占全部G-NENs的40%。Ⅰ型患者多为女性,G-NEC/MANEC患者多为老年男性。Ⅰ、Ⅱ型为ECL-细胞G-NET,胃泌素水平均升高,肿瘤多发生于胃体,主要表现为多发息肉样隆起。不同之处在于:Ⅰ型胃酸水平降低,肿瘤旁胃黏膜背景呈萎缩性胃炎改变;Ⅱ型胃酸水平升高,肿瘤旁胃黏膜背景呈肥厚性胃炎或无特殊改变。Ⅲ型G-NET主要表现为胃体的单发隆起型病变。胃泌素水平正常,无相关胃黏膜背景改变。G-NEC/MANEC多为贲门-胃底的巨大溃疡型病变。Ⅰ、Ⅱ、Ⅲ型病理分级主要为G1,G-NET中所有G3级病例均为Ⅲ型。Syn、CgA是NENs最常用的免疫组化标志物,本研究142例G-NENs中,Syn阳性率100%,CgA阳性率67.60%,NET中CgA阳性率高于NEC,证实了Syn敏感性较强,而CgA特异性较强[7]。Ⅱ型中1例NET G2发生肝转移;Ⅲ型中2例NET G3发生淋巴结转移,2例发生肝转移;在Ⅲ型中,随着肿瘤分级的增高,发生转移的病例增多。Ⅰ型通常与自身免疫性胃炎有关,由于血清中存在抗胃壁细胞/抗内因子抗体,壁细胞丢失导致胃酸缺乏,从而刺激胃泌素G细胞增生,导致胃泌素水平继发性升高,在高胃泌素环境中,胃底和胃体ECL细胞开始增生[8],这可能是肿瘤发生的必要因素[9]。Ⅱ型多与胃泌素瘤引起的原发性高胃泌素血症相关,胃酸过多,胃泌素水平升高。对于Ⅰ型G-NET,内镜下除了对肿瘤组织进行活检外,还应同时对胃底、胃体、胃窦处非肿瘤性胃黏膜进行多点取材,判断肿瘤周围胃黏膜背景是否呈萎缩性胃炎改变[10-11]。
G-NENs的分级、分型对临床治疗方案的选择和预后判断有重要意义[12]。Ⅰ型G-NET的治疗方法有以下两种:≥0.5 cm的病灶进行内镜下切除,而对较小的病变进行动态观察;≥1 cm的病灶,建议通过超声内镜判断肿瘤在胃壁的浸润深度、局部淋巴结是否累及后再选择内镜下切除或者手术切除。Ⅱ型G-NET主要通过手术切除原发灶治疗。Ⅲ型G-NET治疗原则可参照胃腺癌,如果肿瘤直径<1 cm,选择内镜下治疗。G-NEC/MANEC治疗原则参照胃腺癌,发生远处转移的患者首选铂类化疗[13-14]。本研究中,Ⅰ、Ⅱ、Ⅲ型G-NET患者主要接受内镜下切除治疗。Ⅱ型中发生肝转移的NET G2,接受内镜+奥曲肽治疗。Ⅲ型中的NET G3,主要接受手术或手术+化疗,影像学提示肝转移者接受化疗。G-NEC/MANEC中,淋巴结转移患者主要接受手术联合化疗,肝转移患者接受化疗。随访期间G-NENs死亡率为15.49%(22/142),其中1.41%为Ⅲ型NET G3,14.08%为G-NEC/MANEC,患者均发生淋巴结/肝转移。有研究报道,Ⅲ型早期即可有淋巴结或远处转移,病理分级多为G3级,主要转移到肝脏[15-16]。与Ⅲ型G-NET相比,Ⅰ、Ⅱ型G-NET都是侵袭性较小的肿瘤[17]。多数G-NEC/MANEC患者确诊时已经发生淋巴结或远处转移,远处转移器官主要为肝脏。Ⅰ型和Ⅱ型总体预后较好,Ⅲ型预后较差,G-NEC/MANEC预后最差,提示分级、分型与G-NENs患者预后相关[18]。
综上所述,Ⅰ、Ⅱ型G-NET镜下肿瘤形态无区别,多为分化好的NENs,内镜下应多点取材,了解背景胃黏膜的改变,进一步从病理角度协助G-NET的分型诊断,可提示临床医生做相关检查。Ⅲ型G-NET预后比Ⅰ、Ⅱ型差,且随着分级的增高,转移率也随之增加,临床需重点关注NET G3的处理。

