心泵辅助装置研究进展及动物实验质量控制
崔永春 王小康 周建业 杨伯清 彭鹏 贾六军 孟亮 李彬 罗佳菲 袁卫民 周燕文 杜红 李秋菊 李悦 李巨波 岳广新 王欣 北京协和医学院,心血管植入材料临床前研究评价北京市重点实验室,动物实验中心,阜外医院,中国医学科学院,心血管疾病国家重点实验室 (北京 100037)
内容提要: 心泵辅助装置是目前临床治疗心脏功能不全的常用辅助装置。文章就心泵辅助装置的国内外研究现状,综述了新一代主动脉内球囊反搏、静脉-动脉体外膜式氧合器、左心辅助装置和全人工心脏的结构和功能特点、优点和不足,并对其临床应用现状进行了比较分析。同时,结合文献报道和国家相关标准对植入式心室辅助装置的临床前研究动物实验的质量控制要点进行了阐述,以期为新型心泵辅助装置的研发提供参考与支持。
心泵辅助装置(Heart Pump Assist Device,HPAD)是一类具备辅助心脏泵血功能,并满足人体组织血液灌注要求的装置,主要包括主动脉内球囊反搏(Intra-Aortic Balloon Pump,IABP)、静脉-动脉体外膜式氧合器(Venoarterial Extracorporeal Membrane Oxygenation,ECMO)、左心辅助装置(Left Ventricular Assist Devices,LVAD)和全人工心脏(Total Artificial Heart,TAH)。根据辅助时间长短,又分为一时性辅助和永久性辅助两类。
目前HPAD主要用于急性心肌梗死合并心源性休克、高危经皮冠状动脉介入手术以及外科冠状动脉搭桥手术等首选的循环辅助手段[1-4]。同时,还可用于心脏移植术后功能康复前(Bridge To Recovery,BTR),在获取合适供体心脏前的等待期(Bridge To Transplant,BTT),患者最终进入心脏移植等待名单前的稳定期(Bridge To Candidacy,BTC),在确定进一步治疗方案前的决策期(Bridge To Decision,BTD)的支持治疗以及作为心脏移植患者的终生治疗方法(Destination Therapy,DT)。
1.主动脉内球囊反搏
主动脉内球囊反搏(Intra-Aortic Balloon Pump,IABP)是由动脉系统植入一根带气囊的导管至降主动脉内左锁骨下动脉开口远端,进行与心动周期相应的充盈扩张和排空,使血液在主动脉内发生时相性变化,心脏舒张期球囊充气、主动脉舒张压升高、冠状动脉压升高,使心肌供血供氧增加。心脏收缩前,气囊排气、主动脉压力下降、心脏后负荷下降、心脏射血阻力减小、心肌耗氧量下降,因而增加心排血量[5-7]。IABP因植入简单、较安全,价格低廉,已成为急诊室或病床旁最常用的HPAD[8-12]。不足之处在于:①依赖患者的左心室功能,对于完全性血流动力学崩溃的患者无效[13];②不能长期应用,辅助周期数天;③在小儿中的应用有限。
2.体外膜式氧合器
体外膜式氧合器(Extracorporeal Membrane Oxygenation,ECMO)是一种短期替代肺脏气体交换和心脏泵血功能的辅助装置,可以改善心肺功能严重受损患者的血流动力学,至少可以提供50%以上的心排血量,为急诊患者等待最终诊断和制定有效治疗方案创造条件,降低患者病死率[14-16]。但是,在心脏功能严重受损时,ECMO非搏动性、逆行性灌注可导致左心室后负荷进一步加重,继而人体组织血液灌注不足[17]。
3.人工心脏
人工心脏是指一类用人工材料制造的一种可移植机械装置,以暂时或永久地部分或完全代替心脏功能、推动血液循环。人工心脏分为心室辅助人工心脏(VAD)和全人工心脏(TAH),VAD又分为左心室辅助(LVAD)、右心室辅助(RVAD)和双室辅助(DVAD)。其中左心室辅助装置是临床最常用的HPAD。
左心辅助装置(LVAD)是一个可提供动力的血泵,其效能较IABP高6~8倍,能有效代替心脏工作能力的80%以上,泵血能力可达到10L/min。与IABP相比,IABP仅能改善已存在的循环动力,左心辅助是将左心房或左心室血流引入辅助泵体,经泵体驱动血流进入主动脉,完全替代左心泵血功能。经左心辅助后,左心室室内张力可降低80%,心肌氧需求降低40%,是纠正顽固性心衰和心脏移植前的一种理想治疗手段。在非心脏移植患者在以过渡治疗为目的的情况下,LVAD使用的指征是在已完成满意的畸形或病变手术矫正,代谢紊乱和心电生理异常已控制在较满意水平的前提下,心脏前后负荷调整及正性肌力药物应用无效,IABP使用禁忌或无效时。
根据LVAD的发展历程,LVAD分为3代,详见表1。

表1. 不同类型LVAD的比较
在我国,阜外医院联合苏州同心医疗科技有限公司自主研发的第三代人工心脏China Heart VAD以磁悬浮无接触轴承为特点,具有体积小和生物相容性好的优点,属于世界上最先进的人工心脏之一,目前已经走上临床,开创了国产人工心脏的新纪元。体外和体外溶血试验表明,ChinaHeart VAD血泵具有良好的溶血性能,可以进行动物长期慢性存活试验[28-30]。
现阶段的LVAD已发展为经皮电磁感应传导能源的恒流泵,实现了LVAD的内置化,避免了腹膜袋或腹膜间隙袋。同时高能电池微型化改善了能源的便携性,减少了感染的发生,改善了患者的生活质量[31-33]。如下总结目前临床常用的代表性心室辅助装置特点。
3.1 Impella心室辅助系统
Impella是全球最小的、唯一以介入方式放置的心脏血泵,又称为导管室里的心室辅助装置(见图1)。单一血管入侵点、无需心脏穿刺、不损伤瓣膜,无需依靠与心率同步或促心肌收缩类药物,重建并提高净心排量,降低心肌O2需求,増加心肌O2供应[34]。辅助周期10d左右。长期临床获益高于IABP。目前,临床应用主要有Impella2.5和Impella5.0两种,分别能提供2.5L/min和5.0L/min血流。其中,Impella 2.5因体积较小,介入医生可独立操作,因而在临床上应用更为广泛[35]。
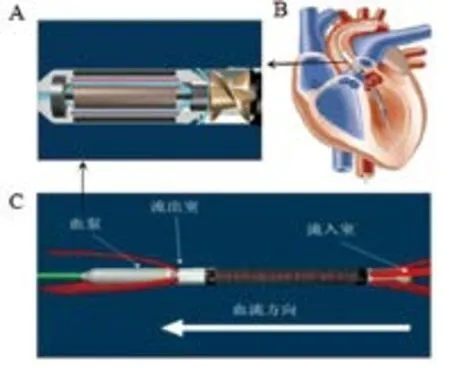
图1. impella 心室辅助系统结构特征(注:1A.血泵;1B.impella左心辅助系统在心脏内位置示意图;1C.impella系统主要构件;黑色箭头所指为血泵。图片来自impella产品说明书。)
3.2 TandemHeart PTVA心室辅助系统
TandemHeart PTVA系统是美国CardiacAssist公司(Pittsburgh,PA,USA)产品,已经获得美国食品药品管理(FDA)批准,在6h之内短期应用。它经由皮肤跨隔膜心室辅助,实现短期循环支持系统,不需要彻底的心肺通路手术。TandemHeart泵(图2A),提供循环动力将氧合血液从左心房中抽吸出来,推进至全身动脉循环系统。TandemHeart套管组件将泵通过2条经皮肤通路腹股沟穿刺点连接起来,跨隔膜插管(图2B)的弯曲远端可在左心房中实现最佳放置,具有14个侧孔,可实现出色的引流;动脉插管(图2C)包括两个必备功能,止动环防止过度插入,缝合线实现在患者身上固定;左心房插管(图2D)是唯一经皮绕过左心室装置,可增加心脏功率输出。TandemHeart替代心脏做工,让左心室获得休息。
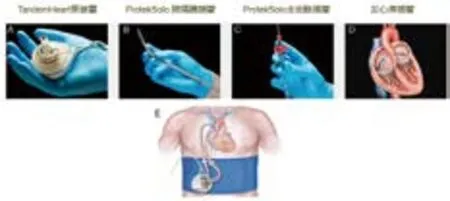
图2. TandemHeart PTVA的组件及植入示意图(2A.泵装置;2B.跨隔膜插管;2C.主动脉插管;2D.左心房插管;2E.TandemHeart PTVA系统植入人体后各组件位置关系示意图。本图引自TandemHeart PTVA厂家产品介绍网站 http://www.tandemlife.com/tandemheart-kit/。)
TandemHeart PTVA与IABP、ECMO、Impella同为临床常用一时性HPAD,但四者亦有区别,见表2。
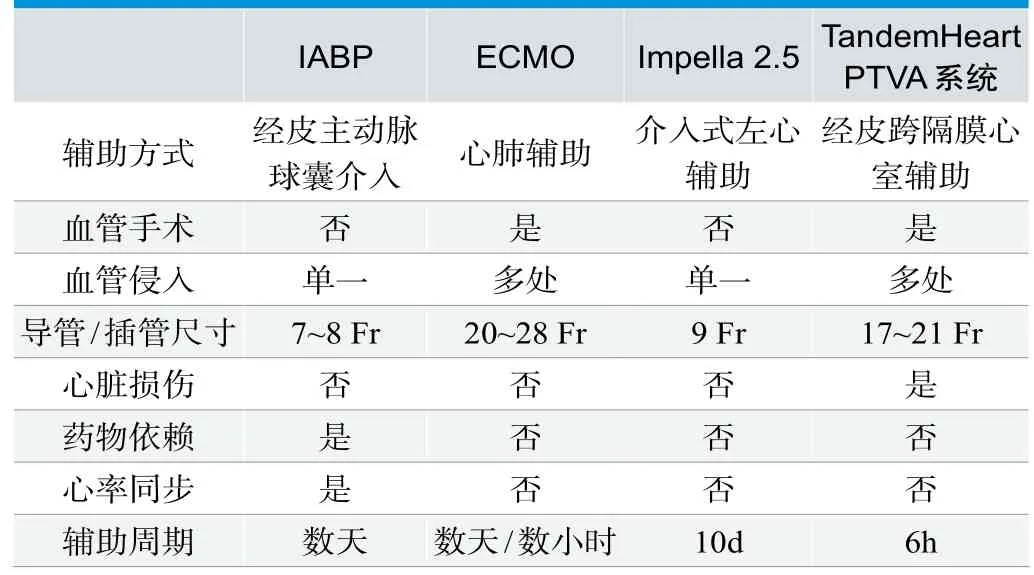
表2. TandemHeart PTVA与其他常用一时性心泵辅助装置比较
3.3 全人工心脏
对重度晚期双室心力衰竭,当所有其他治疗手段失败且没有供体器官时全人工心脏(Total Artificial Heart,TAH)植入是最后的选择。世界上虽已进行了几例完全人工心脏临床应用,证实完全人工心脏能代替自然心脏功能,用其较长维持循环是可行的,其前景是乐观的。已上市代表性全人工心脏见表3。

表3. 已上市代表性全人工心脏
4.植入式心泵辅助装置动物实验及质量控制要点
人工心脏属于高风险的第三类医疗器械产品,技术要求高,是心血管医疗器械中科技含量最高的技术,属于典型多学科交叉渗透的高端产品,性能要求更为精准。国家药品监督管理部门对其实行严格的医疗器械生产企业许可证和产品注册制度,并2019年颁布了《医疗器械动物实验研究技术审查指导原则第一部分:决策原则》,规定“植入式心室辅助装置”研发需进行动物实验研究。动物在体实验的目的是通过活体动物实验获得产品安全性和性能数据,对设计定型的产品进行临床前确认,也是评价其在体可靠性的重要组成部分,是验证其可否进人临床前实验的必要步骤。
4.1 主要评价指标[36-40]
装置性能参数:泵转速、泵流量、平均泵压(U)、电机温度、功率等稳定性等。
对心脏辅助功能:左心室输出量(CO)、平均主动脉收缩压(ASP)、舒张压(ADP)、左心室收缩压(LVSP)、舒张压(LVDP)、左心室压力梯度(Dp/dt)、左心房压(LAP)等。
血液相容性:游离血红蛋白(FHB)、凝血功能、血常规、血生化。
病理解剖:①血泵泵体内、入口和出口流道内有无血栓、感染性赘生物形成;②器械是否有明显的机械性能变化、腐蚀、磨损、密封完整性破坏;③肉眼观察心脏、肺、肝、肾、脾等终末主要脏器有无梗死灶和发生病变,并对其做常规组织学病理切片检查。所有观察结果需进行记录。
4.2 可能并发症
4.2.1 感染
评估包括传动系统引流液培养、血培养以及影像学检查。血培养对于评估隐性血流感染很重要,最常见的病原体是革兰阳性皮肤菌群、真菌和多菌感染[41-43]。
4.2.2 非手术期出血
非手术期出血是LVAD置入术后常见的并发症,也是再入院较常见原因。非手术期出血有多种原因:①抗凝治疗;②获得性血友病,特别是由于高分子量血管性血友病因子(von Willebrand Factor,vWF)多聚体形态变化而导致血小板黏附功能降低的vWF缺乏;③连续血流及相关的血管生成因子的异常调节导致胃肠道、鼻咽、脑或其他组织中动静脉畸形形成[44]。
4.2.3 LVAD机械故障或停转
可由多种原因引起,包括机械泵故障、电路故障和血栓形成[45]。
4.2.4 血栓形成
血泵及人工血管等异物表面直接与血液接触,激活了体内的凝血系统,在血泵内部、人工血管、血泵出入口、吻合口、心尖插管处等易发生血栓。主要表现为血浆游离血红蛋白或乳酸脱氢酶的无症状升高;出凝血指标的变化;机械功率或流量变化导致的装置报警;更严重者出现左心室或双心室衰竭[46,47]。
4.2.5 主动脉瓣关闭不全
最可能发生在由于主动脉瓣开放频率降低引起的主动脉瓣叶融合,来自流出套管的高压连续血流冲击瓣叶,导致其重构和(或)损伤,使瓣膜关闭不全从而形成无效回路,降低LVAD工作效率并导致心衰症状。
4.3 动物实验质量控制要点
为避免或减轻上述植入后并发症,在动物实验中要对如下关键环节进行质量控制。
4.3.1 实验动物选择及植入操作要点
①实验动物应选择心脏大小、主要血管尺寸应以及红细胞机械应力的敏感度与人类相似的实验动物,并排除有出血倾向和凝血机制过度活跃的动物[36]。②植入操作要求术者、麻醉和监护统筹协作、密切配合,每个环节均直接影响实验动物的预后,直接影响实验结果[48-50]。③心尖打孔器的操作及心尖打孔位置的选择至关重要。因实验动物坐卧的特殊性,体位变化是影响装置转速及流量非常重要的因素,需在植入前予以综合考虑。④实验动物个体差异较大,慎重选择装置植入位置,保障良好的同轴性,这是实验动物长期存活的必要条件。⑤装置植入时心尖部吻合需严密,避免缝线撕裂或脱落,缝合过程中需关注流量变化情况,及时调整辅助装置位置,避免装置贴附于心室壁,影响实验结果。⑥心脏有较强的组织修复能力,受损后成纤维细胞大量增殖试图修复受损组织。这就要求VAD植入时血泵入口插入心尖的长度和角度非常精确,血泵入口过短或倾斜贴壁则会给心肌修复组织提供附着点;过长容易在血泵入口与心室壁交界处形成血液流动死区,增加血栓风险;如果手术时血泵入口插入心室角度不良,导致贴壁,修复组织累积增大,加上入口处负压,组织掉进泵体,会导致血泵转子起浮障碍而停转。
4.3.2 护理要点
①术后护理,每日记录实验动物生理参数,包括呼吸频率、心率、体温、每日动物的整体状况、液体出入量[50]。②抗凝初期使用150~200U/mL的肝素持续静脉注射,使ACT维持在1.5~2.0倍于基值(100~200s),术后第3天开始转为饲喂华法林抗凝,保持国际标准化比值(INR)在2.0~3.0,华法林的初始剂量6mg/d,根据INR值进行调整,有效控制血栓和出血并发症。③辅助期间应注意保温,维持有效胶体渗透压,注意伤口无菌处理及预防感染。④LVAD辅助期间须注意纠正低血容量和右心功能不全,必要时酌情使用适量正性肌力药物或少量α受体激动剂提高体循环阻力,使平均动脉压大于70mmHg。⑤需要注意的是实验中所有动物饲喂苜蓿干草,其中含有大量维生素K1,可以拮抗华法林钠的抗凝作用。一些抗生素如羧苄青霉素和先锋霉素则不同程度的增加INR值,这些在指导VAD后期临床实验时都应予以考虑。
5.小结与展望
从脉动排量泵-离心泵-非接触式轴承发展历程,HPAD越来越小型化,可植入性并减少了手术创伤。电池,微处理器技术和(电磁)磁体之类的电气工程技术的进步促使VAD系统的内部和外部组件变得更小,更轻。泵控制和调节更加有效,提高了患者的生活质量。材料和表面处理技术优化,转子和外壳设计改良,改善了血液动力学,大大提高了血液相容性和生物相容性。未来心泵辅助装置将向更微型、更耐久、更稳定、更廉价的方向发展。智能技术得以应用,远程监控系统的实现,将使临床医生可以在线查看患者数据,从而立即为他们提供帮助。患者可能受益于减少常规门诊就诊、早期发现并发症、及时获取安全有效的治疗,节约了医疗成本[45]。

