16 个产地红曲中洛伐他汀及桔霉素测定
齐方圆任 丹黄紫妍秦路平*朱 波*
(1.福建中医药大学药学院,福建 福州350122; 2.浙江中医药大学药学院,浙江 杭州310053; 3.陕西中医药大学药学院,陕西 咸阳712046)
红曲是我国传统中药,用药历史悠久,是药食两用中药的代表药之一[1]。红曲是以稻米为原料,由曲霉科真菌紫色红曲霉Monascus purpureusWent发酵而成,临床上用于治疗高脂血症、降低胆固醇,其主要活性成分洛伐他汀,可作为胆固醇合成途径中3⁃羟基⁃3⁃甲基戊二酸单酰辅酶A(HMG⁃CoA)还原酶的竞争性抑制剂,有效减少胆固醇的合成[2⁃4]。纯天然发酵的红曲产品中,洛伐他汀是以内酯式与酸式2 种形式存在[1],内酯式洛伐他汀需体内产生的羟基酯酶水解成酸式方能发挥药效,酸式洛伐他汀与HMG⁃CoA 还原酶结构更为接近,具有更强的生物活性[5]。2020 年版《中国药典》中关于红曲的质量标准只规定了内酯式洛伐他汀(C24H36O5)不得少于0.22%,且有的研究也仅测定了红曲中内酯式洛伐他汀的含量[6⁃8],忽略了酸式洛伐他汀的存在,因此同时测定红曲中2 种构型洛伐他汀的含量更能反映红曲产品的质量。此外,红曲霉发酵过程中产生的真菌毒素桔霉素[9],具有肝肾毒性[10]、致畸性[11]与致癌性[3,12⁃13],是危及人类、动物健康的潜在威胁,在一定程度上限制了红曲产业的发展。
目前关于同时测定红曲中内酯式洛伐他汀、酸式洛伐他汀与桔霉素的研究鲜有报道,已有报道也仅针对少数产地[14],并不能客观地反映现有市场上红曲产品质量优劣及安全性。综上,本实验收集全国红曲主产区16 个产地红曲样品,以内酯式洛伐他汀、酸式洛伐他汀、桔霉素3 种成分为指标性状,建立HPLC⁃PDA/FLR 法对其进行含量测定,并分析比较其含量差异,以期为红曲药材的质量控制与安全性评价提供参考。
1 材料与方法
1.1 材料 Waters Alliance e2695 型高效液相色谱仪(配置自动进样器、柱恒温箱、PDA 及FLR 双检测器,美国Waters 公司);KQ⁃300DV 型数控超声波清洗器(昆山市超声仪器有限公司);FA2204B 型电子天平(上海天美天平仪器有限公司);超纯水仪(美国Millipore 公司);免疫亲和柱(CitriTestTMHPLC,北京中检维康技术有限公司)。洛伐他汀(B20806)、桔霉素(B25912)对照品均购于上海源叶生物科技有限公司;PBS 缓冲液(上海生工生物工程有限公司)。样品信息见表1。乙腈(色谱纯,美国天地公司);磷酸(色谱纯,上海阿拉丁公司),其余试剂均为分析纯。

表1 样品信息Tab.1 Information of samples
1.2 方法
1.2.1 色谱条件 洛伐他汀,ZORBAX Eclipse C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)⁃0.1%磷酸(B),梯度洗脱(1~5 min,60%~65% A;5~20 min,65% A;20~25 min,65%~90%A;25~30 min,90%~60% A;30~35 min,60%A);柱温28 ℃;体积流量1.0 mL/min;检测波长238 nm;进样量10 μL。桔霉素,ZORBAX Eclipse C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈⁃水(磷酸调pH2.5)(53.5 ∶46.5);柱温28 ℃;体积流量1.0 mL/min;荧光检测器(λex=331 nm,λem=500 nm);进样量20 μL。色谱图见图1。

图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
1.2.2 线性关系考察 精密称取洛伐他汀对照品适量,置于10 mL 量瓶中,用甲醇稀释至刻度,制成206.4 μg/mL 对照品溶液。精密称取内酯式洛伐他汀对照品2 mg,适量甲醇溶解,用0.2 mol/L NaOH溶液超声转化40 min,取出冷却后,用3 mol/L磷酸将pH 调至7.7,甲醇定容至10 mL 量瓶,即得208.9 μg/mL 对照品溶液[14]。精密称取桔霉素对照品1 mg,置于10 mL 量瓶中,加甲醇稀释至刻度,质量浓度为100 μg/mL,于4 ℃冰箱中保存备用。将各对照品溶液用甲醇进行稀释后,在“1.2.1”项条件下进样,以对照品溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,见表2,可知各指标成分在各自范围内线性关系良好。各对照品溶液稀释至不同倍数后,在“1.2.1”项条件下进样,采用信噪比法测定各指标成分的检测限(S/N =3 ∶1)、定量限(S/N =10 ∶1),结果见表2。

表2 各成分线性关系Tab.2 Linear relationships of various constituents
1.2.3 样品含量测定
1.2.3.1 洛伐他汀测定供试品溶液制备 精密称取经充分粉碎均质红曲粉末(红曲米、胶囊及片剂均研磨粉碎后过5 号筛)0.5 g,置于25 mL 具塞锥形瓶中,精密加入25 mL 甲醇,密塞,称定质量,超声(300 W、40 kHz)45 min 后取出,放冷,甲醇补足减失质量,摇匀,离心(4 000 r/min)10 min,取上清液过0.45 μm 微孔有机滤膜,取续滤液,即得。
1.2.3.2 桔霉素供试品溶液制备 精密称取均质红曲粉末(红曲米、胶囊及片剂均研磨粉碎后过5号筛)1.0 g,置于25 mL 具塞锥形瓶中,精密加入20 mL 70%甲醇提取液,摇晃均匀,60 ℃恒温提取30 min,每10 min 摇动30 s。移取1.0 mL 经槽纹滤纸过滤后的滤液,39 mL PBS 溶液稀释、混匀,微纤维滤纸过滤,收集滤液。精密吸取该滤液10 mL,以1~2 滴/s 体积流量全部通过CitriTestTMHPLC 亲和柱直至空气流通。再加入10 mL 0.1%吐温⁃20 PBS 溶液(1~2 滴/s)流经亲合柱,最后加入1.0 mL 甲醇⁃0.1%磷酸(70 ∶30)洗脱液以1 滴/s或者更低的体积流量淋洗CitriTestTMHPLC 亲和柱,收集所有样品淋洗液(1.0 mL)于干净容器中,备用。
1.2.4 精密度试验 分别精密吸取质量浓度为20.02、10.45 μg/mL 的内酯式洛伐他汀、酸式洛伐他汀对照品溶液各10 μL,以及100 ng/mL 桔霉素对照品溶液20 μL,在“1.2.1”项条件下连续进样测定6 次,测得内酯式洛伐他汀、酸式洛伐他汀、桔霉素保留时间RSD 分别为0.11%、0.19%、0.96%,峰面积 RSD 分别为 1.59%、1.38%、1.80%,表明仪器精密度良好。
1.2.5 重复性试验 精密称取浙江SM 样品0.5 g、福建TX 样品1.0 g,按“1.2.3”项下方法分别平行制备6 份供试品溶液,在“1.2.1”项条件下进样,测得内酯式洛伐他汀、酸式洛伐他汀、桔霉素峰面积RSD 分别为1.26%、1.45%、1.63%,含量RSD 分别为1.22%、1.40%、1.67%,表明该方法重复性良好。
1.2.6 稳定性试验 精密称取浙江SM 样品0.5 g、福建TX 样品1.0 g,按“1.2.3”项下方法分别制备供试品溶液,于室温下放置0、1、2、4、6、8 h后在“1.2.1”项条件下进样,测得内酯式洛伐他汀、酸式洛伐他汀、桔霉素峰面积RSD 分别为1.56%、1.26%、1.41%,表明溶液在8 h内稳定性良好。
1.2.7 加样回收率试验 取含量已知的杭州TJT红曲样品6 份,每份精密称定0.5 g,分别加入等量的内酯式洛伐他汀对照品溶液(0.806 5 mg)和酸式洛伐他汀对照品溶液(0.864 5 mg),取含量已知的福建TX 红曲样品6 份,每份精密称定1.0 g,分别加入等量的桔霉素对照品溶液(3.122 μg),按“1.2.3”项下方法分别制备测定洛伐他汀及桔霉素供试品溶液,在“1.2.1”项色谱条件下进样,计算回收率,结果见表3。
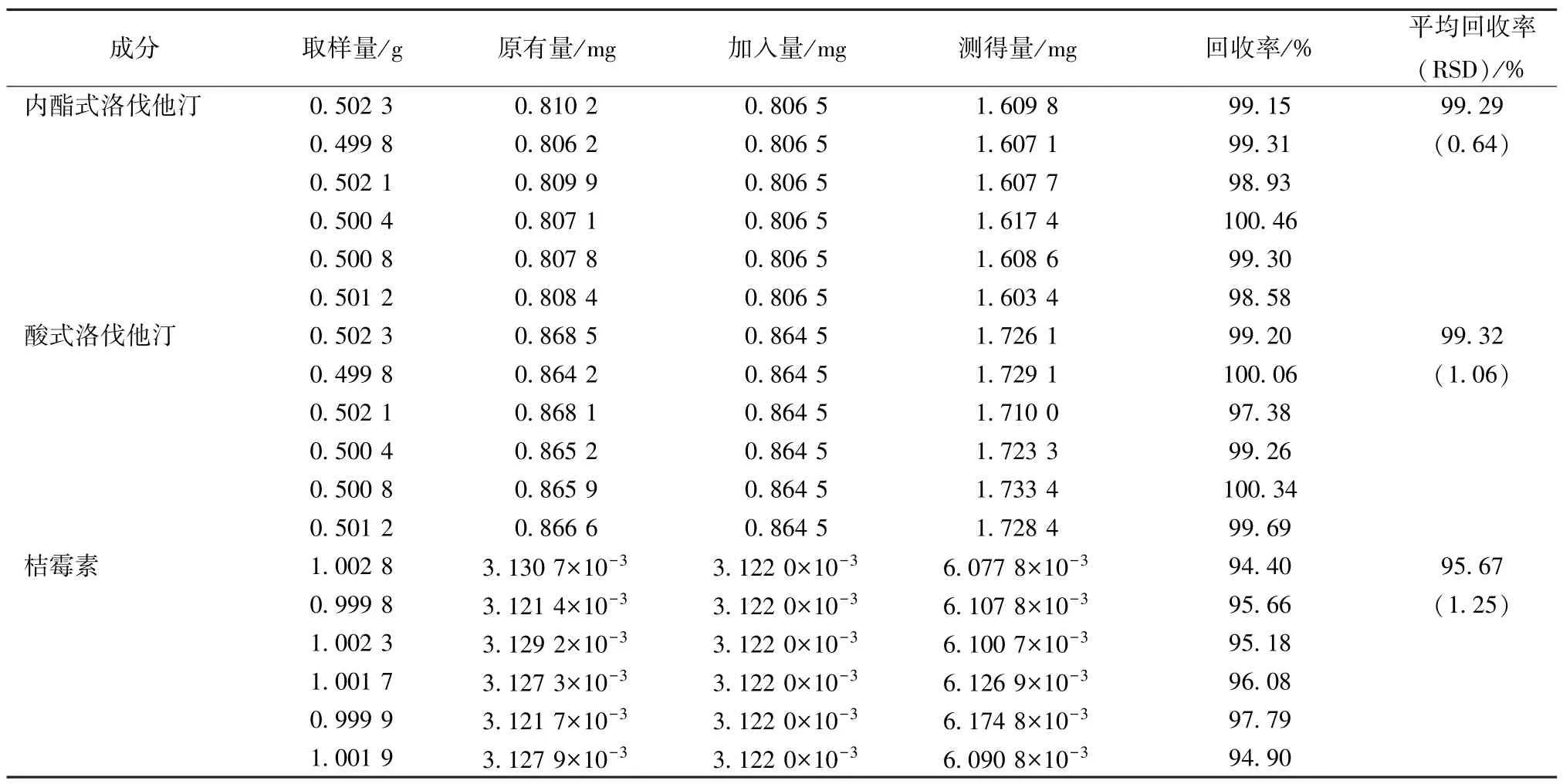
表3 各成分加样回收率试验结果(n=6)Tab.3 Results of recovery tests for various constituents(n=6)
1.3 数据处理与分析 应用SPSS 25.0 软件处理数据,方差分析采用单因素ANOVA,聚类分析采用组间联接法[15]。
2 结果
2.1 洛伐他汀含量比较 16 个产地间红曲中洛伐他汀含量存在统计学差异(P<0.01),见表4,内酯式洛伐他汀、酸式洛伐他汀、总洛伐他汀平均质量分数分别为6.790、1.464、8.254 mg/g。2020年版《中国药典》 红曲质量标准规定,含内酯式洛伐他汀不得少于0.22%,本实验16 批样品中7个产地(浙江建德、浙江宁波、浙江江山、山东滨州、成都高新、北京中关村和北京怀柔)符合质量标准,其中浙江宁波产最高,达(32.611±0.047)mg/g;其他产地(如浙江杭州、浙江丽水、福建古田、福建南平、福建南平、湖北武汉、云南昆明、台湾嘉义)样品以内酯式洛伐他汀含量计,不符合药典标准。
表4 各成分含量测定结果(, n=3)Tab.4 Results of content determination of various constituents(, n=3)

表4 各成分含量测定结果(, n=3)Tab.4 Results of content determination of various constituents(, n=3)
注:**P<0.01。
2.2 桔霉素含量比较 16 个产地间红曲中桔霉素含量存在统计学差异(P<0.01),见表4,平均质量分数为4.895 μg/g。关于桔霉素的限量标准,我国相关规定有所不同,如《中国药典》 红曲质量标准下无桔霉素,而由国家卫生和计划生育委员会与国家食品药品监督管理总局共同发布的国家标准(GB 5009.222⁃2016)[16]中规定,桔霉素定量限为80 μg/kg。表4 显示,本实验16 批样品中部分产地(如浙江建德、浙江丽水、浙江杭州,福建南平、成都高新)均未检测出桔霉素,安全性相对较好,而大多数产品,尤其是福建屏南所产红曲桔霉素含量最高,达(21.854±0.176)μg/g,不符合上述标准。
2.3 聚类分析 以内酯式洛伐他汀、酸式洛伐他汀和总洛伐他汀含量为参考指标,对各批样品进行聚类分析,根据欧氏距离D2=13.12 将不同产地划分为4 个类群,见图2。类群Ⅰ共10 个产地,分别为云南昆明、台湾嘉义、福建古田1、福建南平、福建屏南、福建古田2、湖北武汉、浙江杭州、北京怀柔、浙江丽水,该类群内酯式洛伐他汀、酸式洛伐他汀与总洛伐他汀含量均较低;类群Ⅱ共2 个产地,分别为山东滨州、北京中关村,该类群内酯式洛伐他汀与总洛伐他汀含量较高,但酸式洛伐他汀含量较低;类群Ⅲ为2 个产地,分别为浙江建德、成都高新,该类群内酯式洛伐他汀与总洛伐他汀含量均较高,酸式洛伐他汀含量在所有产地中偏高;类群Ⅳ中2 个产地分别为浙江宁波、浙江江山,两者内酯式洛伐他汀、总洛伐他汀含量在所有产地中偏高,酸式洛伐他汀含量较高。

图2 16 批样品聚类树状图Fig.2 Dendrogram of sixteen batches of samples
3 讨论与结论
本实验用PDA 检测器对内酯式及酸式洛伐他汀对照品溶液在210~400 nm 波长范围下进行扫描,结果表明,酸式和内酯式洛伐他汀对照品溶液的最大吸收波长均为238.2 nm。测定洛伐他汀考察了流动相(甲醇⁃水、乙腈⁃水、甲醇⁃0.1%磷酸、乙腈⁃0.1% 磷酸)、提取溶剂(75% 乙醇、甲醇、乙腈)、超声时间(30、45、60 min)对红曲中洛伐他汀含量的影响,发现在乙腈⁃0.1%磷酸系统下基线相对平稳,峰形相对尖锐,各峰之间分离度良好,甲醇与乙腈的提取效果相对75% 乙醇较好,但两者之间无明显差别,超声45 min 即可提取完全,故选择以乙腈⁃0.1%磷酸为流动相,甲醇提取超声45 min。测定桔霉素考察了流动相乙腈⁃水(磷酸调pH 2.5)比例(60 ∶40、53.5 ∶46.5、50 ∶50、40 ∶60)对桔霉素色谱峰的影响,发现在比例53.5 ∶46.5 条件下,桔霉素保留时间为8.036 min 适宜,与溶剂峰之间能够较好地分离,各峰之间分离度良好。
目前,常用的桔霉素检测方法主要有HPLC法、酶联免疫吸附法和高效毛细管电泳法等,这些方法均需复杂的样品前处理步骤,过程复杂、耗时长,且难以进行痕量检测[17]。本实验采用免疫亲和柱处理的方法直接对红曲中的桔霉素进行富集净化,利用柱内桔霉素的高度特异性抗体吸附,快速特异地将桔霉素从样品中分离出来,并同时完成净化和浓缩步骤,速度快,操作简单,准确性高。
本实验所测16 个产地红曲产品质量存在差异,以浙江产红曲质量较好,而其他产地如福建、云南、台湾等地所产红曲质量次之,这可能是由于各产地红曲菌种、制备条件以及生产加工方式差别而造成的。下一步将利用同一菌种以同一制备条件和生产加工方式在不同产地环境下制备红曲,比较其有效成分含量差异,探索不同产地环境下稳定高产优质红曲的制备工艺,以期为红曲产业发展提供依据。

