Trk-B在促进胶质母细胞瘤失巢凋亡抵抗中的作用及机制研究
林贤宾
(福建医科大学附属第二医院,福建 泉州 362000)
胶质母细胞瘤是中枢神经系统中最常见的恶性肿瘤,根据世界卫生组织神经系统病理可以将胶质母细胞瘤核分裂活跃程度以及临床预后情况分为WHOⅠ、WHOⅡ、WHOⅢ、WHOⅣ4个级别[1]。其中胶质母细胞瘤WHOⅢ、WHOⅣ级较WHOⅠ、WHOⅡ级胶质瘤增殖明显活跃,核分裂相增多,复发率较高。目前主要治疗方法包括手术、放疗、化疗等,均有一定的效果,但对于高级别胶质母细胞瘤预后效果并不理想。因此,研究恶性胶质母细胞瘤增殖的分子病理机制,对于理解胶质母细胞瘤的恶性生物学行为具有重要意义,并且可为恶性胶质母细胞瘤的分子靶向治疗提供理想可靠的治疗靶标,为临床上干预恶性胶质母细胞瘤的发生发展提供坚实的实验依据。相关研究[2]发现,Trk-B可能与NOgo受体复合物在胶质母细胞瘤中存在拮抗作用,能够导致肿瘤细胞快速增长。本文旨在探讨Trk-B在促进胶质母细胞瘤失巢凋亡抵抗中的作用及机制,为临床干预恶性胶质母细胞瘤发生发展提供科学依据。
1 资料与方法
1.1 一般资料 选择4~6周龄雌性胶质母细胞瘤Balb/c裸鼠24只进行研究,将其分为3组,即Trk-B组、对照组、稳定敲低组,每组8只。
1.2 方法 分别将Trk-B过表达细胞、野生型细胞和稳定敲低的Trk-B单细胞悬液注入右侧腋部皮下,比较不同组间肿瘤生长情况。观察终点应用qRT-PCR、免疫组化检测肿瘤组织中Trk-B、Nogo受体和AKT的表达。应用蛋白免疫印迹检测肿瘤组织中Trk-B、Nogo受体和AKT的表达。将未处理细胞移植瘤采用插块法再次接种至裸鼠皮下,分为3组,每组8只,肿瘤长至300 mm3进行干预:空白组、Nogo激活剂和抑制剂治疗组(3组)予以处理。
Trk-B组:Trk-B过表达细胞注射右侧腋部皮下。对照组:野生型细胞注射右侧腋部皮下。稳定敲低组:稳定敲低的Trk-B单细胞悬液注射右侧腋部皮下。干预后28 d处死荷瘤裸鼠,观察肿瘤生长抑制率,应用免疫组化检测肿瘤组织中Trk-B、Nogo受体和AKT的表达情况应用蛋白免疫印迹检测肿瘤组织中Trk-B、Nogo受体和AKT的表达。在临床检测期间,首先进行单层贴壁细胞总蛋白的提取,在提取完成后,对组织中总蛋白进行提取,并将已加药物处理后的贴壁细胞总蛋白进行提取。在实际提取过程中,首先需要将培养液导入至离心管中,在2500 rpm状态下离心5 min,去除上清液后对其进行吹打洗涤,继续在2500 rpm状态下离心5 min,弃上清液后使用PBS进行1次重复洗涤。加入100 μL裂解液实施30 min的冰上裂解处理,并将裂解液混合后,于12000 rpm状态下离心5 min,装于0.5 mL的离心管中,在-20 ℃下保存。将提取完成后的蛋白含量进行测定,首先取1.5 mL离心管,加入4 ℃的考马斯亮蓝溶液1 mL,在室温放置30 min后进行蛋白含量测量。
1.3 评价标准 对比3组细胞凋亡率、肿瘤体积、肿瘤转移率以及裸鼠预后情况。
1.4 统计学方法 将数据纳入SPSS20.0软件中进行统计学分析,计量资料比较采用t检验,并以()表示,计数资料采用χ2检验,并以(n,%)表示,P<0.05为差异显著,有统计学意义。
2 结果
2.1 3组细胞凋亡率、肿瘤体积、肿瘤转移率比较 研究结果显示,Trk-B组的细胞凋亡率明显低于对照组和稳定敲低组,Trk-B组肿瘤体积、肿瘤转移率均明显高于对照组和稳定敲低组,差异均有统计学意义(P<0.05)。见表1。
表1 3组细胞凋亡率、肿瘤体积、肿瘤转移率比较()
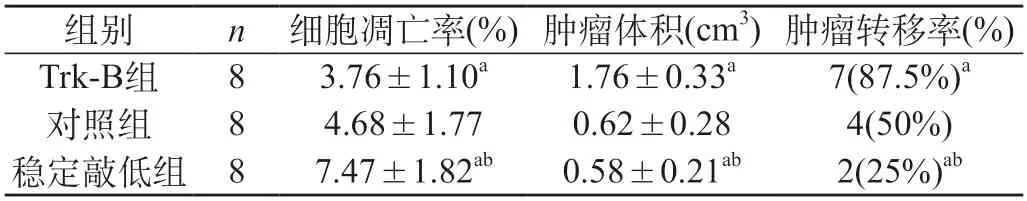
表1 3组细胞凋亡率、肿瘤体积、肿瘤转移率比较()
注:a表示与对照组比较,P<0.05;b表示与对照组比较,P<0.05。
2.2 3组裸鼠预后情况分析 Trk-B组WHOⅢ级和WHOⅣ级共6 例(75.00%)、对照组WHO Ⅲ级和WHO Ⅳ级共3例(37.50%)、稳定敲低组WHOⅢ级和WHOⅣ级共2例(25.00%)。由此可见,Trk-B组WHOⅢ级和WHOⅣ级明显高于对照组和稳定敲低组(χ2=28.571、50.000,均P<0.001)。
3 讨论
胶质母细胞瘤来源于上皮肿瘤,占颅脑肿瘤的40%~50%,统称为脑胶质母细胞瘤,也是最为常见的原发性颅内肿瘤。根据相关研究发现,胶质母细胞瘤年发病率为3~8人/10万人。目前对于高级别胶质母细胞瘤预后情况并未得到有效改善,因此还需要临床不断深入探讨。细胞凋亡是机体生长、分化、发育和病理过程中,由基因编码调控的细胞自发死亡过程,又称程序性死亡[3]。正常的上皮或内皮细胞具有黏附依赖性,其存活依赖于细胞间和细胞与基质间的信号传递,称为锚定依赖。正常上皮细胞或不具备转移性质的实体瘤细胞从原位脱落进入血流后就会引发细胞凋亡,这种在脱离原来生存环境的特殊情况下发生的细胞凋亡称为失巢凋亡[4]。失巢凋亡作为一种特殊的程序化细胞死亡形式,在机体发育、组织自身平衡、疾病发生和肿瘤转移中起重要作用。肿瘤细胞,尤其是一些容易发生远处转移的恶性肿瘤细胞,具有极强的抗失巢凋亡特性,从瘤体上脱落进入循环系统后并不发生凋亡,从而完成转移过程。恶性肿瘤的这种抗失巢凋亡特性已经在肺癌、肠癌、卵巢癌、恶性黑色素瘤、口腔鳞状细胞癌等癌细胞体外培养实验中得到了证实,逐步揭示了失巢凋亡的分子机制[5]。失巢凋亡通过传统的细胞凋亡途径诱导细胞死亡,整合蛋白感知和传导细胞外基质信号而控制细胞的黏附和存活,Bcl-2和某些Bcl-2相关蛋白广泛参与细胞失巢凋亡的调节,多种蛋白激酶信号分子参与失巢凋亡的信号转导[6]。
Trk-B是一种抑制失巢凋亡和诱导肿瘤转移的蛋白,即酪氨酸激酶受体,为失巢凋亡抑制与肿瘤恶性浸润性的关系提供了实验依据[7]。利用基因转染技术培养出高表达Trk-B的小肠上皮细胞,当用这些转染的非肿瘤性细胞进行小鼠鼠尾静脉注射后,小肠上皮细胞在小鼠的肺、肝、肾、心和骨骼迅速形成肿瘤,而注射对照细胞的小鼠均没有肿瘤出现。高表达Trk-B的细胞能够在脱离基质的情况下形成细胞团,通过血管等达到远处转移的目的。有研究表明,Trk-B在胶质母细胞瘤细胞的恶性增殖中起到关键作用,然而在胶质母细胞瘤细胞中,Trk-B是否通过失巢凋亡抵抗来实现细胞恶性增殖目前还没有相关报道[8]。此次研究Trk-B与AKT在胶质母细胞瘤细胞恶性增殖相互关系为切入点,在前期研究工作基础上,提出Trk-B与Nogo受体复合物可能通过调控恶性胶质母细胞瘤细胞失巢凋亡抵抗,促使恶性胶质母细胞瘤细胞增殖和转移实验设想,对胶质母细胞瘤细胞的恶性增殖分子病理机制进行深入探索,目前国内外尚无类似文献报道。当前在我国的研究中已经熟练掌握研究所需的实验技能如免疫组化、PCR、质粒构建和转染、RNAi、Western Blot等,在颅脑肿瘤相关分子靶标筛选和功能鉴定方面做了大量工作,积累了丰富的经验,能够保证研究顺利进行。本研究通过对Trk-B促进胶质母细胞瘤失巢凋亡抵抗中的作用及机制进行分析,发现Trk-B组的细胞凋亡率明显低于对照组和稳定敲低组,肿瘤体积、肿瘤转移率、WHOⅢ级和WHOⅣ级明显高于对照组和稳定敲低组(P<0.05)。证明了Trk-B通过拮抗Nogo受体调控AKT表达,参与胶质母细胞瘤细胞恶性增殖和失巢凋亡抵抗的分子机制及其与胶质母细胞瘤细胞恶性表型的联系,可能为临床上提供潜在的分子靶标并为恶性胶质母细胞瘤的分子干预提供初步实验依据。刘学键等[9]研究发现,Trk-B能够通过促进胶质母细胞瘤失巢凋亡抵抗,导致病灶增殖和转移;胡克琦等[10]研究发现,Trk-B能够促进胶质母细胞失巢凋亡抵抗,均与本研究结果相似。总之,Trk-B会通过促进胶质母细胞瘤失巢凋亡抵抗,导致病灶增殖和转移。

