硼替佐米联合化疗治疗复发难治及高危儿童急性淋巴细胞白血病11例病例系列报告
张智晓 张永湛 陆爱东 吴 珺 左英熹 贾月萍 丁明明 张乐萍
急性淋巴细胞白血病(ALL)是儿童最常见的血液系统恶性疾病。目前儿童ALL的治愈率已达90%,但仍有10%~20%的患儿出现复发或难治,预后不良[1]。复发难治的患儿很难耐受长期强烈的化疗,且目前尚无标准的挽救治疗方案,再诱导缓解率低,尤其对于复发难治的急性T淋巴细胞白血病(T-ALL)的治疗方法非常有限。因此,积极寻找新的治疗手段是临床上的迫切需要。硼替佐米(Bortezomib)作为第一个应用于临床的蛋白酶体抑制剂,主要通过作用于泛素-蛋白酶体通路,抑制核转录因子NF-κB的激活,从而促进肿瘤细胞的凋亡,其不仅适用于多发性骨髓瘤、套细胞淋巴瘤等患者,在治疗ALL方面也显示了一定的优势。研究表明,硼替佐米能够增强恶性肿瘤细胞对化疗的敏感性[2]。来自儿童白血病治疗进展(TACL)的研究显示,硼替佐米联合标准再诱导化疗对复发ALL患儿有效[3-4]。目前国内相关报道较少,本研究对北京大学人民医院(我院)儿科既往应用硼替佐米的病例进行回顾性分析,探讨其对复发难治及高危ALL患儿的疗效。
1 方法
1.1 知情同意 本文患儿的治疗方案均取得家长的知情同意。
1.2 研究对象 纳入2017年9月至2019年9月于我院儿科接受硼替佐米联合化疗的复发难治及高危ALL连续病例。
1.3 诊断标准 根据《血液病诊断及疗效标准》[5],按形态学-免疫学-细胞遗传学-分子生物学进行分型诊断。难治指经常规诱导方案2个疗程未达完全缓解(CR),复发指经常规诱导化疗达CR后骨髓中再现ALL细胞>5%或髓外浸润。
1.4 治疗方案 硼替佐米1.3 mg·m-2,第1、4、8、11 d静脉推注(自2019年1月1日起采用多发性骨髓瘤中优化的每周1次方案[6])。联合化疗方案根据患儿既往治疗情况,选择CAM(环磷酰胺、阿糖胞苷、6-巯基嘌呤)、甲氨蝶呤、去甲氧柔红霉素、异环磷酰胺等不同的化疗方案。治疗过程中记录患儿临床症状、体征,定期监测血常规、肝肾功能及外周血细胞数目及形态学等。
1.5 疗效和不良反应评估 完成硼替佐米1个疗程后,当外周血WBC数目恢复至接近正常时复查骨髓。比较患儿硼替佐米治疗前后骨髓细胞形态及免疫残留判断治疗效果。①CR:骨髓内原始细胞<5%,无髓外病变,外周血细胞恢复(中性粒细胞绝对值≥1 000·μL-1,PLT≥100×109·L-1)。②部分缓解(PR):骨髓内原始细胞~20%。③未缓解(NR):骨髓内原始细胞≥20%。④微小残留病(MRD)阴性:骨髓标本采用多参数流式细胞术检测<0.01%。⑤治疗反应:骨髓形态学CR且MRD低于治疗前的基线水平且无髓外病灶进展判定为治疗有反应;骨髓形态学未CR或MRD高于治疗前基线水平,或髓外病灶进展,判定为治疗无反应。总反应率(ORR)定义:治疗有反应的人数占总人数的百分比。⑥不良反应评估:采用不良事件通用术语标准(CTCAE) Version 5.0进行分级。
1.6 随访 通过电话及门诊随访患儿长期生存情况。本研究随访截止日期为2020年9月1日。无事件生存(EFS)中的事件指治疗无反应、复发或死亡。总生存(OS)指从硼替佐米治疗开始至任何原因的死亡。
1.7 临床资料截取 从我院病历资料中截取以下信息用于本文分析。①一般情况:性别,诊断时年龄;②临床资料:首发症状,首次血常规,肝、脾、淋巴结浸润情况;③辅助检查:骨髓形态学表现,免疫残留,融合基因及突变检测,染色体核型分析;④治疗:治疗方案,疗效评估,不良反应,移植状态;⑤随访。
1.8 统计学方法 采用SPSS 25.0软件进行统计分析。计数资料以例(%)表示;符合正态分布的计量资料以均数±标准差表示,非正态分布的计量资料以中位数(四分位间距)表示。采用Kaplan-Meier生存分析评估患儿的EFS和OS率。生存时间从硼替佐米治疗的时间开始计算。
2 结果
2.1 一般资料 11例患儿纳入本文分析(表1),男9例,女2例,诊断中位年龄10(3~15)岁。7例T-ALL,2例T淋巴母细胞性淋巴瘤(T-LBL)Ⅳ期,2例B-ALL。
2.2 分子生物学特征 表1显示,WT1阳性4例,NOTCH1突变2例,4例基因及突变均阴性。染色体:正常核型7例,+6 1例,t(11;14)1例,2例未见分裂相。
2.3 疾病状态 复发2例,难治4例,高危5例。诱导期使用硼替佐米4例(例2、4、5、10),巩固期使用硼替佐米7例。例1合并中枢神经系统白血病。
2.4 治疗反应 11例均完成1个疗程的硼替佐米联合化疗。ORR为72.7%(8/11),其中B-ALL 1例,T-ALL 7例;治疗前NR 3例,PR 4例,治疗后CR率85.7%(6/7);治疗前MRD阳性10例,治疗后均有下降,其中1例(例6)MRD转阴(表2)。
2.5 不良反应 11例均观察到3级或4级血液系统不良反应。7例发热,6例重症肺炎或其他肺部感染,4例消化道感染,2例口腔感染,2例甲沟炎,1例大肠埃希菌败血症,经积极抗感染治疗,感染均得到有效控制。恶心、呕吐、腹痛为主要的胃肠道反应,分别有5例、4例和4例。
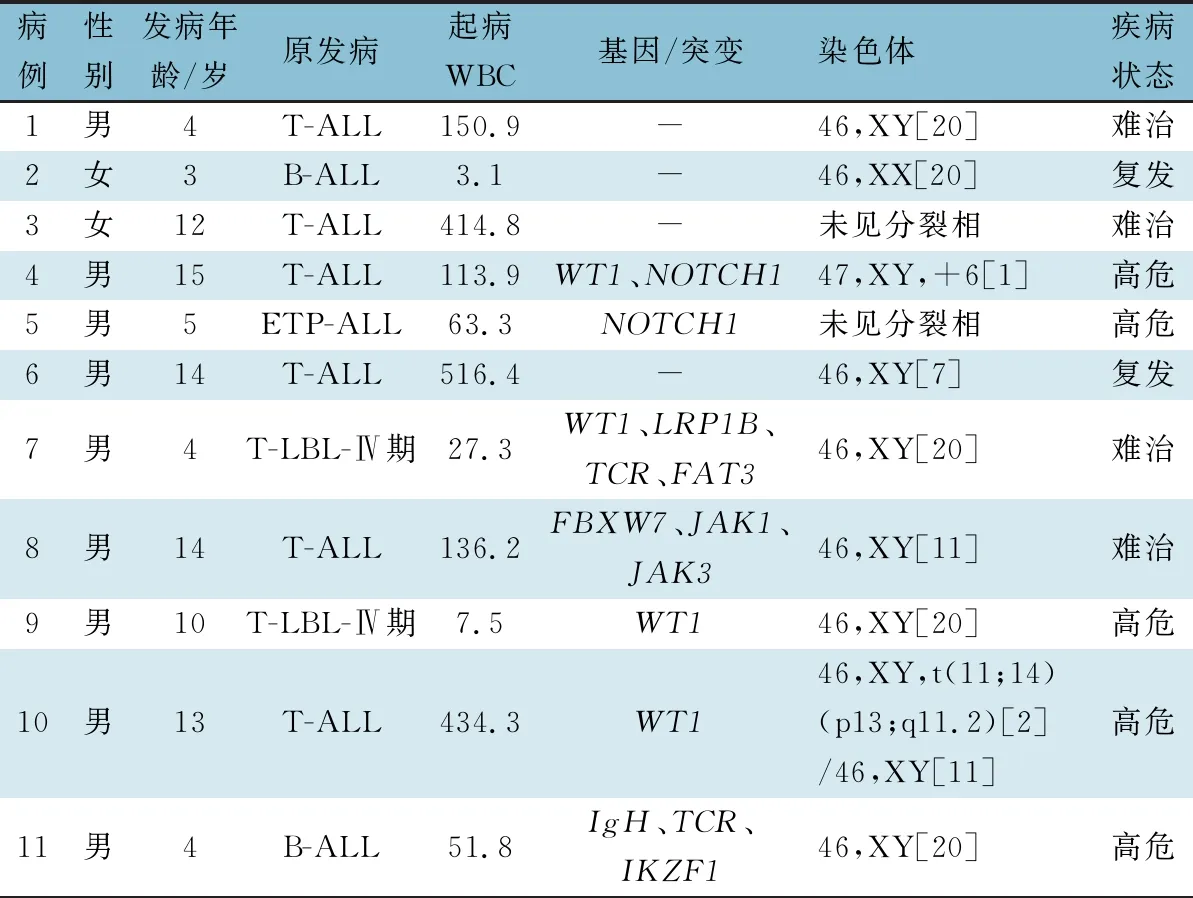
表1 11例患儿的临床和生物学特点
6例出现血清转氨酶和/或胆红素升高,4例1级,1例2级,1例4级,给予保肝治疗后均恢复正常。1例在接受硼替佐米治疗后观察到明显的周围神经病变,予维生素B1、B6、B12和加巴喷丁等对症支持治疗后好转。无化疗相关死亡病例。
2.6 转归 9例行异基因造血干细胞移植治疗,其中7例无病存活,2例死于移植后复发;2例患儿继续化疗,长期随访均死亡,其中1例死于重症肺部感染,1例原因不详。图1显示,中位随访时间15(2~29)个月,2年EFS为(45.5±15)%,2年OS为(63.6±14.5)%。
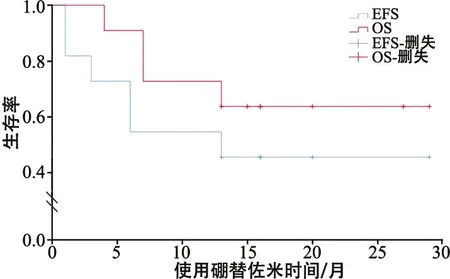
图1 11例患儿的EFS和OS

表2 11例患儿的治疗及预后
3 讨论
硼替佐米在ALL中应用最早的临床证据来自病例报告[7],1例8岁的ALL患儿经历5次复发,对地塞米松和大多数标准抗白血病药物治疗均无效。对其上颌窦组织的病理学检查显示其NF-κB表达上调,予地塞米松联合硼替佐米1.2 mg·m-2,第1、4、8、11 d治疗后,成功诱导白血病细胞凋亡,疗效显著。
随后的Ⅰ期临床研究发现,硼替佐米单药治疗难治复发ALL疗效并不满意。来自儿童肿瘤协作组(COG)的Ⅰ期研究,包括9例ALL和3例急性髓系白血病(AML),采用硼替佐米1.3 mg·m-2,每周2次,连续2周,休息1周。结果显示,硼替佐米在抑制NF-κB活性方面有效,但作为单一药物使用并没有产生临床应答。其中1例患儿在硼替佐米治疗后接受地塞米松、阿霉素和长春新碱化疗,达到CR[8]。临床前研究的数据,包括体外细胞培养及小鼠体内实验都表明,硼替佐米对ALL有抗肿瘤活性,促使对该药物联合常规化疗的探索[9]。
来自TACL协会的Ⅰ期试验,纳入经过多次化疗的复发ALL儿童(9例B-ALL,1例T-ALL),在地塞米松、长春新碱、阿霉素、培门冬酶联合的基础上,分别在第1、4、8和11 d加入硼替佐米1或1.3 mg·m-2。10例中,1例死于弥漫性接合菌感染,余9例中6例(66.6%)获得了CR,另1例骨髓CR但合并持续性中枢神经系统白血病。不良反应可接受,并且在1和1.3 mg·m-2的剂量水平不良反应分布没有明显差异[3]。TACL协会的Ⅱ期试验,纳入22例复发ALL患儿,包括前体B-ALL 20例、T-ALL 2例,先前2~3次治疗无效。结果显示,73%(16/22)的患儿实现了CR或CR但血细胞未恢复(CRi),较历史对照40%的CR率有了显著改善。值得注意的是,在这项研究中,前体B-ALL患者对该方案有反应,而T-ALL患者均无反应[4]。
此后,硼替佐米联合不同化疗方案的研究[10-17]不断涌现,本研究进行了文献汇总(表3)。目前为止最大宗的数来自COG Ⅱ期研究,探讨硼替佐米联合化疗是否可提高复发儿童的二次完全缓解率(CR2)[17],该研究纳入确诊后3年内首次复发的患儿135例,其中B-ALL 103例,T-ALL 22例,T-LBL 10例。结果显示,首次复发B-ALL和T-ALL患儿CR2率分别为(68±5)%(68/100例)和(68±10)%(15/22例),与历史对照试验AALL01P2中非常有限的数据(5/7的T-ALL患者在诱导结束时未能达到CR2)相比,在VPLD中加入硼替佐米CR2率更高。10例T-LBL 患者ORR 70%。该研究硼替佐米总体耐受性良好,血液学毒性常见,非血液学毒性包括感染并发症和代谢异常、胃肠道症状等。美国国家癌症研究所(NCI)赞助的COG Ⅲ期研究AALL1231(NCT 02112916)将新诊断的T-ALL患儿随机分为标准诱导疗法和硼替佐米联合标准疗法组,其研究结果值得期待。
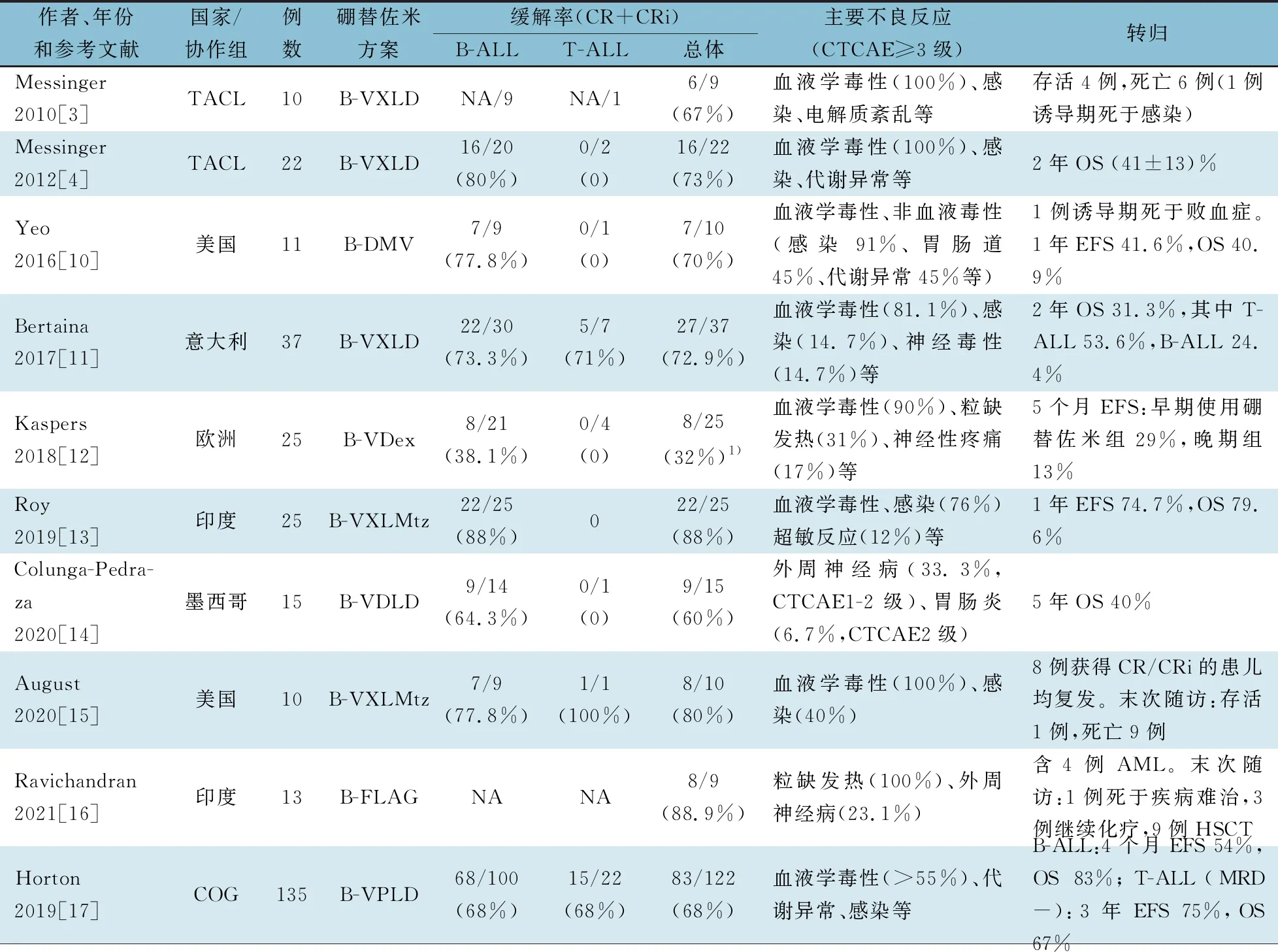
表3 硼替佐米联合化疗治疗儿童复发/难治性ALL的临床研究汇总
基于文献回顾可以看到,对于儿童复发难治性ALL,硼替佐米单药治疗的结果并不满意,建议联合标准白血病化疗方案。硼替佐米作为化疗增敏剂,联合的化疗方案很重要。虽然文献报道的联合方案不一,但总体有效缓解率60%~88.9%,不良反应(骨髓抑制、感染、神经毒性、胃肠道反应等)可耐受。
本研究显示,对于复发难治性以及高危ALL患儿,硼替佐米联合化疗的ORR为72.7%,与文献报道一致。不良反应主要表现为联合化疗所致的血液学毒性、感染等。
随着CD19和CD22-嵌合抗原受体T细胞(CAR T)免疫治疗及免疫靶向药物blinatumomab、inotuzumab等的应用,复发/难治性B-ALL的治疗前景发生了巨大变化。但对于T-ALL,可用的治疗手段较局限,复发患儿预后极差。我院积极将硼替佐米应用于T-ALL的治疗中,旨在提高这部分患儿的疗效,77.8%(7/9例)的T-ALL患儿治疗有效,为后续桥接异基因造血干细胞移植治疗创造了条件。研究表明,硼替佐米不但能抑制NF-κB的活性,同时还能明显抑制Notch1受体的活化,而Notch1的活化以及过表达是T-ALL强有力的诱导因子,因此可明显抑制白血病细胞在体内的生长、增殖。可见硼替佐米的抗T-ALL作用与其对Notch1信号通路以及NF-κB信号通路的协同抑制作用有关[18,19]。
本研究的不足之处:①本文为病例系列报告,患儿在接受硼替佐米治疗前的疾病状态不均一,联合化疗的方案亦不统一;②不良反应的观察基于病历的提取;③纳入分析的病例为单中心且例数较少。

