新生儿起病的钼辅因子缺乏症3例病例报告
徐素华 张 鹏 杨 琳 曹 云 周文浩 程国强
1 病例资料
1.1 病例报告
例1,男,4日龄,因“皮肤黄染3 d,突然青紫1次”于2018年2月至复旦大学附属儿科医院(我院)就诊。患儿系G1P1,足月顺产,出生体重3 100 g,5和10 min Apgar评分均为10分。生后第2 d无明显诱因出现皮肤黄染,进行性加重,出现2次双眼上翻,持续2~3 s后自行缓解,无发热、少吃、少哭、少动等,当地医院检测经皮胆红素(TcB)150 mg·L-1、CRP 110 mg·L-1,予抗感染治疗和光疗,期间出现面色发绀,经皮血氧饱和度(SPO2)下降至83%,无呼吸暂停、抽搐、呕吐等,血糖5 mmol·L-1,故转入我院新生儿科病房。其母孕产史未见异常报告 ,否认近亲婚配及家族相关遗传病史。查体:面容未见异常,反应稍差。鼻导管吸氧下,呼吸平稳,SPO2正常。皮肤中度黄染,四肢肌张力正常。入院第2 d出现反复口唇紫绀,呼吸不规则,高流量辅助通气下,SPO2最低可至60%,每次持续10 s至1 min,期间出现四肢抖动、双眼凝视,疑似角弓反张,反应及胃纳差。
辅助检查:血气分析乳酸2.3~4.5 mmol·L-1,BE -6.3~-7.2 mmol·L-1;血生化检查肌酐71 μmol·L-1,尿素8.2 mmol·L-1,TBIL 213.1 μmol·L-1,DBIL 10.7 μmol·L-1,ALT 37 U·L-1,AST 56 U·L-1,尿酸287 μmol·L-1,CK 1 343 U·L-1,血氨57.9 μmol·L-1。血常规和分类、CRP、脑脊液检查(常规、生化和病原学)、TORCH、血培养、血氨基酸、血酰基肉碱谱和尿有机酸谱检测均未见异常。8日龄头颅MR(图1 A~D)显示,双侧额颞顶枕叶、基底节及脑干广泛异常信号灶。视频脑电图(vEEG)显示,背景活动中度不连续伴多灶性放电。新生儿听力筛查通过。
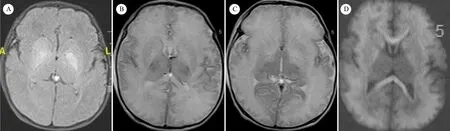
图1 例1(生后8 d)头颅MR
例2,男,3月6 d,因“反复抽搐2月余”于2019年8月至我院首次就诊并住院。患儿系G1P1,足月顺产,出生体重2 950 g。生后7 d外院诊断“新生儿高胆红素血症”,行血串联质谱和尿气相色谱质谱检测未见异常,心超提示房间隔缺损。新生儿后期无明显诱因出现抽搐,表现为双上肢上举或拥抱样动作,多在入睡前发生,每天1~2次,持续数十秒自行缓解,清醒时四肢肌张力增高,家属未予重视。3月龄体检发现头围小,外院行头颅MR显示,大脑半球多发软化灶,两侧侧脑室增宽,大枕大池,胼胝体菲薄。其母孕产史未见异常报告,否认近亲婚配及家族相关遗传病史。查体:尖颅,头围38 cm,前囟0.3 cm×0.3 cm;追听、追视欠佳,抬头不稳,四肢肌张力显著增高,腱反射活跃。
辅助检查:血生化检查肌酐18 μmol·L-1,尿素1.1 mmol·L-1,TBIL 13.7 μmol·L-1,DBIL 4.1 μmol·L-1,ALT 38.8 U·L-1,AST 57.3 U·L-1,尿酸6 μmol·L-1,CK 236 U·L-1,血氨82 μmol·L-1。TORCH检查CMV-IgM、IgG阳性;血CMV-DNA阴性。血常规、CD系列、免疫球蛋白等未见异常。血氨基酸、酰基肉碱谱检测,甲硫氨酸、精氨酸略升高;尿有机酸谱检测,2-酮戊二酸、柠檬酸、乌头酸显著升高。听力及眼底检查未见异常。视觉诱发电位,有双侧波形可引出,分化差。vEEG显示,醒睡大量广泛及多灶性棘波、尖慢波、多棘慢波发放,右侧颞区及双侧后头部显著,睡眠时显著,家长指认抽动事件不伴同步异常放电。
例3,男,10月龄,因“生后发育落后”于2015年7月至我院神经内科门诊就诊。患儿生后即出现发育落后,6月龄抬头,不能独坐。8月龄因“肠道感染”后出现抽搐,大发作,经治疗(具体不详)后,抽搐未再发作,但双眼向上凝视。外院血串联质谱检测未见异常;EEG:两侧适量尖波、尖慢波、棘慢波发放伴阵发,两前额部明显;头颅MR:双侧基底节、丘脑、脑白质异常信号;考虑“线粒体脑病(Leigh’s)待排除”,故至我院就诊。患儿系G1P1,足月顺产,出生体重3 600 g,其母孕产史未见异常报告,否认近亲婚配及家族相关遗传病史。查体:反应差,前额突出,双眼向上凝视,无眼球震颤,四肢肌张力增高明显,病理征阴性。
1.2 基因检测 在取得患儿父母的知情同意后对3例患儿及其父母行基因检测,例1行新生儿panel检测,例2和3均行家系WES测序,根据我院高通量测序数据分析流程[1]进行分析,并行Sanger测序验证。表1显示,3例患儿均经基因诊断为钼辅因子缺乏症(MoCD,MIM:252150),例1和2为A型,例3为B型。例1检测到MOCS1基因的2个杂合突变c.45delG(p.A17Qfs*79)和c.199C>T(p.R67W),c.199C>T为人类基因突变数据库(HGMD)已收录的致病突变位点,错义突变,来自患儿母亲;c.45delG为新发现的突变,移码突变,来自患儿父亲。例2检测到MOCS1基因的2个杂合突变c.203delinsCGGCA(p.Q68Pfs*122)和c.646-2A>G,均为新发现的突变位点。c.203delinsCGGCA为移码突变,来自患儿母亲;c.646-2A>G为剪切突变,来自患儿父亲。例3检测到1个MOCS2基因的纯合无义突变,位于1号外显子的c.16C>T(p.Q6X),是HGMD已收录的致病突变位点。
1.3 治疗和随访 例1予禁食、补液、机械通气、止惊、改善循环等治疗后,病情好转,自主呼吸平稳,无青紫、惊厥发作,喂养耐受。生后15 d随访血尿酸49 μmol·L-1,余指标未见异常。出院后门诊随访,基因明确诊断后家属放弃治疗。患儿1月龄起出现四肢肌张力增高,频繁四肢抽动,喂养困难,生长发育迟缓,随访清醒脑电图提示多量尖波、尖慢波发放。后反复发热,极度消瘦,18月龄死亡。

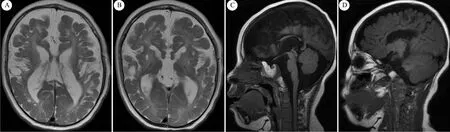
图2 例2(11月龄)头颅MR
2 讨论
钼辅因子(MoCo)的生物合成途径高度保守。从遗传学上,可将MoCD分为3种类型(图3A)。A型MoCD(MIM:603707)因MOCS1基因变异导致MoCo合成的中间代谢产物环吡喃蝶呤单磷酸(cPMP)缺乏所致,占MoCD大多数;B型MoCD(MIM:603708)因编码含硫基因的钼蝶呤(MPT)合成酶亚基的MOCS2基因变异,或编码MOCS3硫酸化酶的MOCS3基因变异,导致MPT合成障碍所致;C型MoCD(MIM:603930)由编码催化钼与硫基团结合的桥尾蛋白的GPHN基因变异所致,目前仅有2例GPHN致病变异引起MoCD的报告[2, 3]。
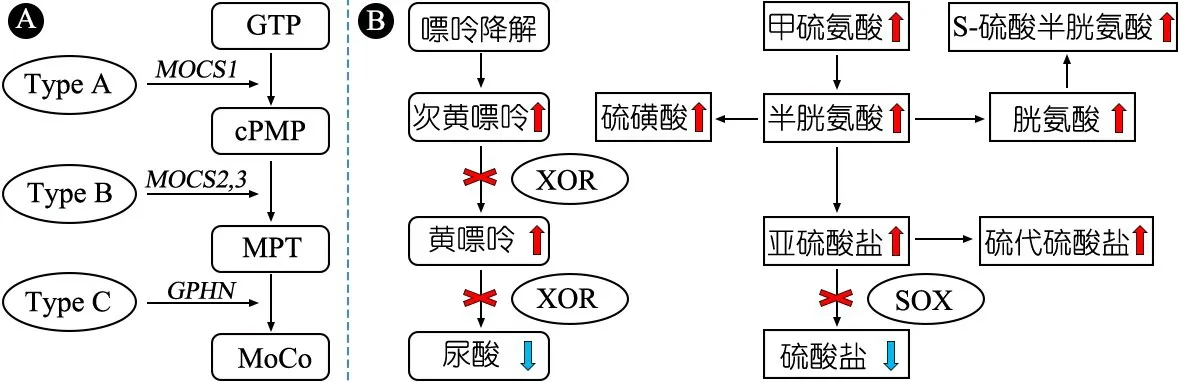
图3 钼辅因子(MoCo)合成途径(A)及钼辅因子缺乏症(MoCD)引起代谢异常(B)

体内MoCo依赖酶包括:亚硫酸钠氧化酶(SOX)、黄嘌呤氧化还原酶(XOR)、线粒体偕胺肟还原组分和醛氧化酶。SOX参与蛋氨酸和半胱氨酸等硫化氨基酸降解途径(图3B),其活性降低可导致蛋氨酸、半胱胺酸、亚硫酸盐、硫代硫酸盐、牛磺酸和S-磺酸半胱氨酸等代谢产物堆积,其中亚硫酸盐和S-磺酸半胱氨酸水平升高可导致神经系统进行性损害[5]。高效液相色谱法对检测尿液中亚硫酸盐和S-磺酸半胱氨酸有较高敏感度[6],可协助MoCD的诊断。XOR参与嘌呤代谢,其活性异常可导致尿酸生成减少、黄嘌呤水平升高(图3B)。因MoCD临床症状与影像学表现与亚硫酸氧化酶缺乏症(MIM:272300)十分相似,故血、尿液中尿酸下降、黄嘌呤水平升高,有助于两类疾病的鉴别。因对该类疾病的了解不够,在基因明确诊断以前,虽然本文例1和2病程中血尿酸有显著降低,但并未进一步检测尿亚硫酸盐、S-磺酸半胱氨酸、黄嘌呤等代谢产物。

MoCD患儿头颅MR异常表现似乎按时间顺序发展,疾病早期可见全面性脑梗死所致脑水肿和扩散加权受限改变,基底神经节、丘脑等受累也较早可见,最终进展为严重的囊性脑软化;还可观察到胼胝体发育不良、皮质下囊肿、小脑脑萎缩、脑干发育不良等其他异常[11-14]。本文中例1生后8 d头颅MR病变以弥漫性脑水肿为主,例2在3月龄及12月龄随访时头颅MR可见脑内多发软化灶形成。MoCD早期影像学发现易与严重HIE混淆,尤其是当患儿存在明确围生期窒息史时。越来越多的证据表明,部分病例在胎儿期头颅影像学已发生改变,目前确诊的病例中最早见于孕26周,胎儿B超见巨枕大池和第六脑室[8, 15]。
cPMP是MoCo最直接、最稳定的前体,目前研究已表明,A型MoCD患儿采用cPMP替代治疗安全且有效[16],在脑病发生前即予以替代治疗,患儿长期神经系统发育良好,但不能逆转已经产生的脑损伤。然而,cPMP目前仍处于临床试验性阶段。其他类型的MoCD尚缺乏特异性治疗,以对症支持治疗为主。
综上所述,MoCD是一种罕见的遗传代谢病,主要临床症状为顽固性新生儿惊厥发作、喂养困难、肌张力异常、发育迟缓、面部畸形,其临床症状和影像学表现易与HIE、氨基酸代谢异常等混淆;血中尿酸水平下降,尿液中亚硫酸盐、S-磺酸半胱氨酸、黄嘌呤等水平升高,可协助诊断;及时基因诊断对确诊及产前诊断至关重要。

