人工栽培桑黄不同生长期子实体的主要活性成分测定比较
张文隽 吴亚召 雷 萍* 马婧嘉 贾 静 张 欢
(1陕西省微生物研究所,陕西西安 710043;2陕西崇德生物技术发展有限公司,陕西西安 710201)
桑黄(Sanghuangporusspp.)隶属担子菌亚门(Basidiomycotina)层菌纲(Hymenomycetes)非褶菌目(Polyporales)锈革孔菌科(Hymenochaetaceae)桑黄孔菌属(Sanghuangporus),是多年生大型药用真菌,因其通常生长于桑属植物上,子实体为黄褐色而得名[1]。《本草纲目》详细记载了桑黄的药性:“味甘、性平。主治女子漏下赤白,血病腹内凝块,肿痛,阴阳寒热,不孕。疗月经不调。”[2]民间用于治疗肝腹水、肝硬化等症。现代研究表明,桑黄有效活性成分有多糖类、黄酮类、三萜类、甾类、多酚类、吡喃类及生物碱等,具有显著的医疗保健功效及较高的营养价值[3]。桑黄多糖类物质是桑黄主要有效成分之一,具有免疫调节、抗肿瘤、抗氧化、抗疲劳、抗炎、护肝、降血糖血脂等广泛的药理作用[4]。黄酮类化合物是桑黄具有抗氧化、抗肿瘤、抗病毒、抗菌、增强心血管系统等作用的重要药理成分[5]。桑黄含有的三萜类化合物具有显著的抗肿瘤、抗氧化、抗菌、抗炎等药用功效[6-10]。不同生长发育期的药用真菌子实体活性有效成分含量差异较大[11-13]。故药用菌采收时间直接影响其有效成分及药效。研究药用菌生长期有效成分含量变化,对探索其适宜的采收期尤为重要。目前关于桑黄多糖、总黄酮和总三萜的研究报道主要集中在提取测定、分离纯化和药理药效等方面,对不同生长期桑黄子实体中三种活性成分含量变化研究报道较少,为此笔者进行人工栽培桑黄不同生长期子实体的(以下称桑黄子实体)多糖、总黄酮、三萜测定,以期为桑黄子实体的适时采收及质量控制提供科学依据。
1 材料与方法
1.1 供试材料
桑黄桑-S子实体为2019年6月中旬至8月下旬采集自陕西省微生物研究所试验基地,分别为原基发生后生长30 d、40 d、50 d、60 d、70 d、80 d、90 d、100 d。采收后桑黄子实体由鼓风干燥箱68℃烘干2.5 h,粉碎后过孔径为0.85 mm筛,备用。
试剂:葡萄糖、芦丁、齐墩果酸(均为标准品),美国Sigma;无水乙醇、苯酚、硫酸、亚硝酸钠、硝酸铝、氢氧化钠、氯仿、香草醛、冰乙酸、高氯酸(均为分析纯)。仪器:WGL-65B鼓风干燥箱(天津泰斯特仪器有限公司),FW177型中草药粉碎机(天津市泰斯特仪器有限公司),RE-5299旋转蒸发器(巩义市英峪予华仪器厂),TG16高速离心机(上海卢湘仪离心机仪器有限公司),LGJ-18S型冷冻干燥机(北京松源华兴有限公司),TU-1901型双光束紫外-可见分光光度计。
1.2 多糖测定方法
1.2.1 样品制备
分别精确称取待测桑黄样品2.0 g,加入蒸馏水100 mL充分混匀,70℃水浴提取2 h,真空抽滤,收集滤渣按上述操作重复1次,合并滤液,旋转蒸发浓缩至原体积1/5,加入无水乙醇至乙醇终浓度达80%,置于4℃冰箱静置过夜,3 000 r/min转速离心15 min,用80%乙醇洗涤沉淀,离心,此操作重复2次,沉淀用蒸馏水溶解定容至250 mL,即得多糖测定供试液。
1.2.2 标准曲线绘制
精确称取105℃条件下干燥至恒重的无水葡萄糖对照品20 mg,于100 mL容量瓶中溶解定容,配制成0.2 mg/mL的葡萄糖标准溶液。分别吸取标准溶液0、0.1 mL、0.2 mL、0.3 mL、0.4 mL、0.5 mL、0.6 mL、0.7 mL、0.8 mL于25 mL具塞试管,加入蒸馏水至1 mL。然后加入5%苯酚溶液2 mL,振荡摇匀,再加入浓硫酸7 mL,充分摇匀,静置显色30 min,于490 nm波长处测定吸光值,计算并绘制标准曲线。
1.2.3 供试液多糖含量的测定
吸取供试液0.5 mL,按照标准曲线制作方法操作,测定吸光值并计算不同生长期桑黄样品中多糖含量。
1.3 总黄酮测定方法[14]
1.3.1 样品制备
精确称取待测桑黄样品粉末10.0 g,加入70%乙醇200 mL,于室温下浸提24 h,真空抽滤,收集滤渣按上述操作重复1次,合并滤液,真空浓缩回收乙醇,浓缩液中加水继续浓缩以挥发残留的乙醇,水液冷冻干燥,得桑黄提取物。准确称取桑黄提取物17.3 mg于25 mL容量瓶中,用70%乙醇定容,即得总黄酮测定供试液。
1.3.2 标准曲线绘制
精确称取芦丁对照品23.2 mg,于50 mL容量瓶中用70%乙醇溶解定容,配制成0.464 mg/mL的芦丁标准溶液。分别吸取标准溶液0、0.5 mL、1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL于25 mL容量瓶,加入5%NaNO2溶液1 mL,充分摇匀后放置6 min,然后加入10%Al(NO3)3溶液1 mL,振荡摇匀放置6 min,再加入4%NaOH溶液10 mL,摇匀后用70%乙醇定容,静置显色10 min,于510 nm波长处测吸光值,计算并绘制标准曲线。
1.3.3 供试液总黄酮含量的测定
吸取供试液3 mL,按照标准曲线制作方法操作,测定吸光值并计算不同生长期桑黄样品中总黄酮含量。
1.4 总三萜含量测定方法
1.4.1 样品制备
准确称取待测桑黄样品粉末0.2 g,置于100 mL具塞磨口三角瓶,加入氯仿50 mL,超声处理60 min,放冷,移至100 mL容量瓶中,用氯仿洗涤三角瓶3次,洗涤液合并入同一容量瓶中,并加入氯仿定容至100 mL,摇匀,即得总三萜测定供试液[15-16]。
1.4.2 标准曲线绘制
精确称取95℃干燥2 h齐墩果酸标准品10.0 mg,于100 mL容量瓶中用氯仿溶解定容,配制成0.1 mg/mL的齐墩果酸标准溶液。分别吸取齐墩果酸标准溶液0、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL于5 mL具塞试管中,常压下60℃水浴蒸干溶剂。依次加入新配制的5%香草醛-冰乙酸溶液0.2 mL、高氯酸0.8 mL,摇匀,70℃水浴加热15 min,取出,立即冰浴冷却5 min,再水浴调至室温。用冰乙酸定容至5 mL,摇匀后于30 min内在548 nm波长处测吸光度值,计算并绘制标准曲线。
1.4.3 供试液总三萜含量的测定
吸取供试液1 mL,按照标准曲线制作方法操作,测定吸光值并计算样品中总三萜含量。
1.5 数据统计与分析
采用Excel 2013和SPSS 17.0进行数据统计学分析与绘图。
2 结果与分析
2.1 标准品回归方程与相关系数
分别绘制多糖、总黄酮和总三萜测定的标准曲线,计算线性回归方程与相关系数,结果见表1。由表1可知,相关系数均为0.99以上,符合检测的要求。
2.2 不同生长期桑黄子实体的多糖、总黄酮、总三萜质量分数
不同生长时期桑黄子实体的多糖、总黄酮、总三萜质量分数及变化见表2、图1、图2。
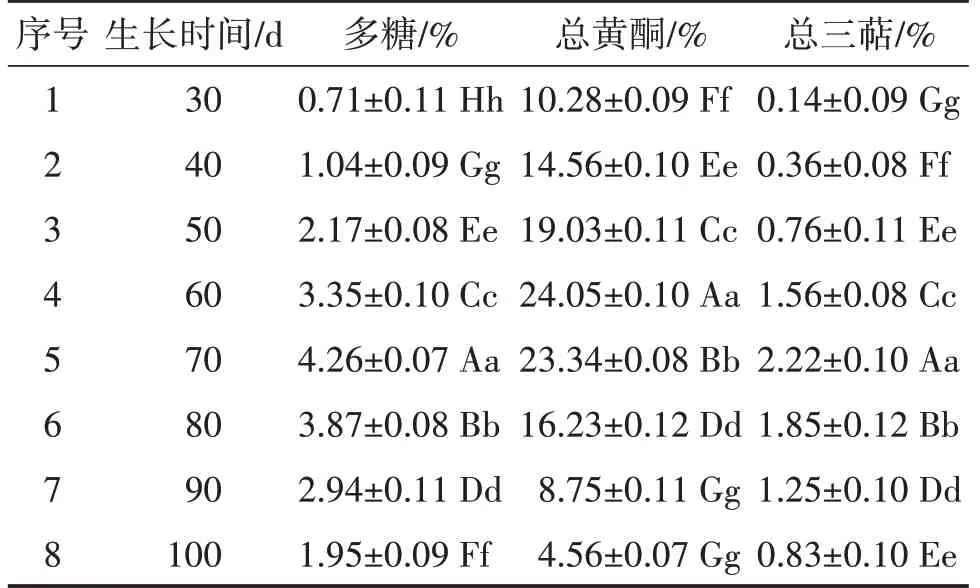
表2 不同生长期桑黄子实体多糖、总黄酮、总三萜质量分数

图1 不同生长期桑黄子实体的多糖、总三萜质量分数变化趋势

图2 不同生长期桑黄子实体的总黄酮质量分数变化趋势
由表2、图1和图2可以看出,多糖、总黄酮、总三萜质量分数随着桑黄子实体生长时间的递增逐渐升高,分别在生长60 d、70 d时达最高,随后又逐渐下降。
多糖、总三萜质量分数变化趋势一致,在子实体生长30~70 d逐渐上升,70 d时达最大值,为4.26%、2.22%,之后又逐渐降低;总黄酮质量分数在子实体生长30~60 d快速上升,至60 d时达最高值(24.05%),生长70 d之后下降迅速。
3 小结
对桑黄的三种活性成分测定结果表明:人工栽培桑黄子实体生长70 d时,其多糖和总三萜质量分数达最高,为4.26%、2.22%,生长80 d次之,为3.87%、1.85%;生长60 d时总黄酮质量分数达最高,为24.05%,生长70 d时总黄酮质量分数仅次于60 d,为23.34%。综合考虑这3种主要有效成分质量分数,再结合实际生产中的子实体产量,桑黄子实体生长70 d时应为最佳采收期,此时采收可有效保障活性成分含量,为市场提供更为优质的桑黄产品。

