乌黄润肠丸治疗阿片相关性便秘的药效及安全性研究
李显勇 陈露 蒋祺 唐平 周旭峰 代沙 周露 兰海 阮秀娟 顾国栋 李琪
疼痛是肿瘤患者第五大体征,依据世界卫生组织(WHO)癌痛三阶梯止痛指南,阿片类药物是治疗中重度疼痛重要药物,而阿片类药物相关性便秘(opioidinduced constipation,OIC)是最常见的阿片类药物相关性胃肠道不良反应。既往研究显示,OIC 可导致肿瘤患者治疗和生活质量下降。OIC 比疼痛更易导致患者抑郁情绪,致使患者宁愿忍受疼痛,并放弃长期使用阿片类药物止痛治疗,从而间接影响癌痛治疗的依从 性[1]。OIC 发生机制与神经末梢的μ-受体抑制有关,阿片类药物作用于中枢神经系统及胃肠道的阿片类受体,削弱肠道运动,减慢肠道蠕动,肠液分泌减少吸收增多,延迟粪便的排泄,抑制神经兴奋性,但增强肠道单个相性收缩和摆动,增加肠壁平滑肌的张力,抑制协调性蠕动,使非蠕动性收缩增加,从而延缓肠内容物通过时间[2]。乌黄润肠丸是一种用于治疗OIC 的中药复方制剂。相关研究报道,何首乌所含成分二苯乙烯苷能降低肝中醋酸可的松所致甘油三酯积累,调节肝脏的脂代谢,预防乙型肝炎。降低四氯化碳所引发的肝肿大,阻碍肝脏微粒体中的脂质过氧化,降低血清游离脂肪酸,是保肝的有效成分,含有的二苯乙烯苷、蒽醌类、黄酮类等多种成分,在抗衰老、抗肿瘤、保护神经以及改善血管功能等方面具有显著效果[3,4]。本研究使用阿片类药物复方地芬诺酯建立OIC 小鼠模型,研究不同给药剂量的乌黄润肠丸对便秘小鼠排便时间、排便重量和排便粒数的影响,并考察制剂安全性,为该制剂治疗阿片类药物致便提供临床理论依据和参考。
1 实验材料
1.1 药材及试剂 乌黄润肠丸由成都复兴医院与攀枝花市农林科学研究院联合研究开发及制备。熟地黄(蒸制)、知母、枳壳、当归、黄芩、黄柏购于四川千方中药股份有限公司;“首乌1 号”为攀枝花农林科学院育出的新品系,经攀枝花市食品药品检验所检测,何首乌块根总灰分3.6%,二苯乙烯苷含量4.4%,结合蒽醌含量0.21%,符合《中国药典》(2015 版,一部)规定。复方地芬诺酯片(国药准字H41020205,规格:每片含盐酸地芬诺酯2.5 mg、硫酸阿托品0.025 mg);麻仁丸(国药准字Z42020417)。溶血剂(V-28CFL);稀释剂(M-3D);清洗液(V-28R);丙氨酸氨基转移酶(140119002)。
1.2 仪器 BSA124S 万分之一电子天平(赛多利斯科学仪器有限公司);电子天平(JM-B2002);兽用全自动血液细胞分析仪(BC-2800Vet,深圳迈瑞生物医疗电子股份有限公司);兽用生化分析仪(BC-240VET,深圳迈瑞生物医疗电子股份有限公司)。
1.3 实验动物 昆明小鼠56 只,SPF 级,雌雄各半。实验单位使用许可证编号:SYXK(川)2016-202,由成都达硕实验动物有限公司提供。
2 实验方法
2.1 乌黄润肠丸对阿片类药物致便秘小鼠通便的作用
2.1.1 复方地芬诺酯混悬液配制 取复方地芬诺酯片2 片(每片含盐酸地芬诺酯2.5 mg、硫酸阿托品 0.025 mg),加RO 水至10 ml,质量浓度为0.5 g/L,振荡溶解混匀,临用前配制[6]。
2.1.2 墨汁配制 准确称取阿拉伯树胶100 g,加RO水800 ml,煮沸至溶液透明,称取活性炭(粉末)100 g加至上述溶液中煮沸3 次,待溶液凉后加RO 水定容至1000 ml,于4℃储存[7]。
2.1.3 动物分组 40 只昆明小鼠随机分为空白对照组、阴性实验组、阳性对照组、实验低剂量组、实验高剂量组,每组8 只,雌雄各半。另选16 只昆明小鼠,随机分为给药组和对照组,每组8 只,雌雄各半。
2.1.4 排便实验 试验前一天下午各组小鼠禁食不禁水16 h,于次日测定时,除空白对照组外,其余各组小鼠灌胃给予复方地芬诺酯混悬液(5 mg/kg),空白对照组给予等容量RO 水;60 min 后分别灌胃阳性对照组(麻仁丸0.6 g/kg)、实验低剂量组(乌黄润肠丸0.4 g/kg)、实验高剂量组(乌黄润肠丸1.2 g/kg)小鼠相应受试药物,空白对照组和阴性实验组分别给予等容量RO 水;20 min 后给予碳粉液指示剂。从灌墨汁开始记录每只动物排首粒黑便时间和在6 h 内排黑便的粒数及黑便质量。
2.2 乌黄润肠丸单次给药毒性 给药组采用小鼠最大给药量法,以乌黄润肠丸最大给药浓度2.4 g/kg,最大给药体积1.0 ml,24 h 内经口灌服1 次,对照组给予等体积的RO水,观察14 d。试验期间观察小鼠体重、饮食、外观、行为、分泌物、排泄物、死亡情况及中毒反应等,到期时眼球采血和大体解剖,组织行病理学检查,眼球血用于血常规和血生化检测[8]。
3 统计学方法
采用SPSS17.0 统计学软件处理数据。计量资料以均数±标准差()表示,多组间比较采用单因素方差分析,两组间比较采用t 检验。P<0.05 表示差异有统计学意义。
4 结果
4.1 各组小鼠排首粒黑便时间、6 h 内排便粒数、6 h排便净重量比较 阳性对照组、实验低剂量组、实验高剂量组排首粒黑便时间均短于空白对照组与阴性实验组,差异均具有统计学意义(P<0.05)。实验高剂量组6 h 内排便粒数多于空白对照组与阴性实验组,实验低剂量组多于阴性实验组,差异有统计学意义(P<0.05)。实验高剂量组6 h 排便净重量高于空白对照组与阴性实验组,差异有统计学意义(P<0.05)。实验低剂量组与阳性对照组的6 h 内排便粒数与6 h 排便净重量比较,差异无统计学意义(P>0.05)。见表1。
表1 各组小鼠排首粒黑便时间、6 h 内排便粒数、6 h 排便净重量比较()

表1 各组小鼠排首粒黑便时间、6 h 内排便粒数、6 h 排便净重量比较()
注:与空白对照组比较,aP<0.05;与阴性实验组比较,bP<0.05
4.2 乌黄润肠丸安全性
4.2.1 对照组与给药组单次给药第0、4、7、14 天体重比较 对照组与给药组小鼠单次给药第0、4、7、14 天的体重比较,差异无统计学意义(P>0.05)。见表2。
表2 对照组与给药组单次给药第0、4、7、14 天体重比较(,g)

表2 对照组与给药组单次给药第0、4、7、14 天体重比较(,g)
注:两组比较,P>0.05
4.2.2 对照组与给药组小鼠血常规检验结果比较 对照组与给药组血小板、红细胞、血红蛋白、白细胞水平比较,差异无统计学意义(P>0.05)。见表3。
表3 对照组与给药组小鼠血常规检验结果比较()

表3 对照组与给药组小鼠血常规检验结果比较()
注:两组比较,P>0.05
4.2.3 对照组与给药组小鼠血生化检验结果比较 对 照组与给药组的肌酐和天门冬氨酸氨基转移酶水平比较,差异无统计学意义(P>0.05)。给药组的丙氨酸氨基转移酶低于对照组,差异有统计学意义(P<0.05)。见 表4。
表4 对照组与给药组小鼠血生化检验结果比较()
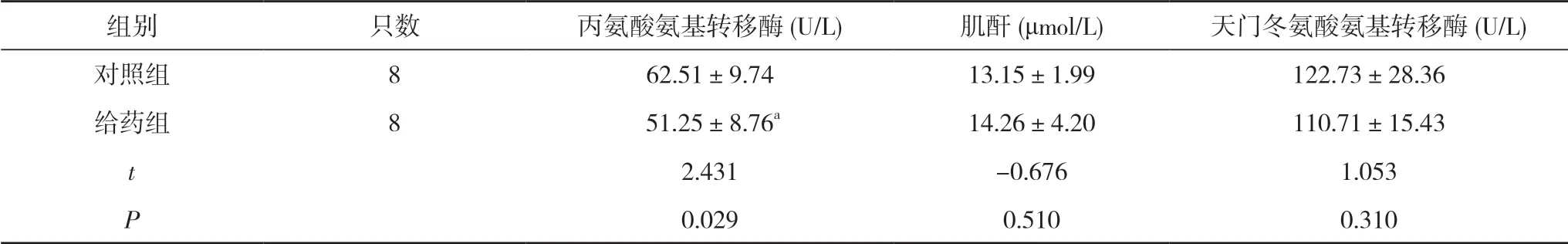
表4 对照组与给药组小鼠血生化检验结果比较()
注:与对照组比较,aP<0.05
4.2.4 乌黄润肠丸对小鼠器官的毒副作用 给药组小鼠肝、肾、肠组织病理学苏木素-伊红(HE)染色结果显示:肠道黏膜未见明显水肿肠黏膜结构清晰,肝脏组织内未见肝细胞明显水肿及脂肪样变,肾脏组织未见肾脏细胞明显水肿及肾小球结构完整。结果表明乌黄润肠丸对小鼠的肝、肾、肠等器官无毒副作用。见图1。
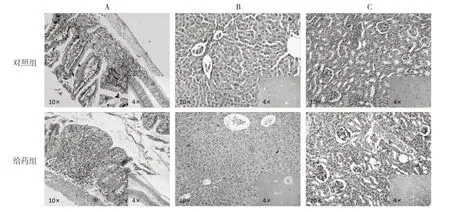
图1 小鼠肠(A)、肝(B)、肾(C)组织病理学HE 染色结果
5 讨论
既往研究发现,内源性阿片肽可通过阻滞肠道神经元的活动继而阻止肠道的推性蠕动和腺体的分泌[9,10];因此,当外源性阿片与受体结合,阻止兴奋性和抑制性神经递质的分泌,将影响肠道节律性收缩、增加肠道水分重吸收,最终导致胃肠道功能紊乱、大便干结及排便困难[11]。因此,阿片类药物导致的胃排空延迟、腹绞痛、腹胀、肠排空延迟、大便干结等症状,可再次加重恶心、呕吐、排便困难、排便疼痛、排便不尽感、排便梗阻感等[12]。目前,减少阿片类用量、控制阿片类药物引起的不良反应、更换阿片类药物、改变给药途径是降低阿片类不良反应的主要手段,但对部分OIC 患者效果不佳。同时,阿片类药物减量将导致癌痛得不到有效控制,有违于WHO 提出的癌痛控制目标。美国国立综合癌症网络(NCCN)疼痛指南中推荐预防性使用泻药治疗OIC,如聚乙二醇、乳果糖、纳络酮缓释剂、甲基纳曲酮、阿维莫潘等,国内常用中药制剂麻仁丸对症治疗[13]。
除阿片药物直接导致的胃肠道功能紊乱性排便困难,癌症晚期患者多并发脱水、电解质紊乱、肿瘤相关性机械性梗阻及精神紧张等便秘相关危险因素。因此,不仅需要改善便秘症状,纠正肠道功能紊乱,同时需要改善机体状态,从而缓解OIC。本组方及制剂根据阿片类药物致便秘的特点和机制,并结合改善全身机体组方,以何首乌、柏子仁、当归、大黄等具有具润肠通便和刺激性作用的泻下类药物改善便秘症状为君药,佐以养阴生津类药物熟地黄、知母等,调节交感神经和内分泌的功能,使代谢亢进状态有所缓解,并能促进淋巴母细胞的转化,增加白细胞及血小板,从而提高机体免疫功能[14];再辅以清热解毒药物黄芩、黄柏等,对于热毒蕴结的肿瘤患者,通过抑菌、对抗多种微生物毒素及其他毒素,改善肠道菌群微环境,维持及保护肠道功能[15]。实验结果表明,乌黄润肠丸可以明显缩短阿片类药物致小鼠便秘的小鼠首次排便时间,并且明显增加小鼠排便次数和排便重量,治疗效果优于麻仁丸阳性对照组;同时,单次给药急性毒性实验研究结果表明,在剂量范围内,乌黄润肠丸对小鼠的肝、肾、肠均无明显的毒副作用。
综上所述,乌黄润肠丸是一种能有效改善OIC 的复方中药制剂,本研究为进一步中药制剂转化及临床应用提供了支撑。

