生物模板法制备磁性中空微球的方法和应用
黄冠华,刘序彦,房晨曦,顾庆峰,雷浩
(中国矿业大学化工学院,江苏徐州221116)
纳米中空磁性微球因具有独特的磁响应性、比表面积大、中空结构可容纳特定物质、微球壳面可进行功能化修饰等特点,在物质分离和纯化、材料学和医学等领域有较广泛的应用,具体应用场景有功能性吸附剂[1-2]、固定化酶载体[3]、药物的缓释载体[4-5]、靶向药物治疗等[6-8]。
传统制备纳米磁性微球的方法主要是非生物模板法,其又分为硬模板法、软模板法和自模板法,这3种方法各有优劣,硬模板法制备出的微球成型率高且形状完整,但模板不易去除,易造成残留[9-10]。软模板法的模板易于去除,但制备出的微球破损严重[11]。自模板法虽然不需要模板,操作步骤较少,但需要精确控制反应时间和反应过程中pH的改变,较为困难[12]。相比之下,生物模板法以天然的生物材料为模板,用物理和化学的方法进行处理制备纳米磁性中空微球,制备过程操作简单,所用化学试剂的数量和毒性均比非生物模板要低。制得的微球形状完整,成形率高,而且若采用软模板法,因生物材料可通过高温热解炭化挥发,生物模板易于去除并且无残留[13]。生物材料的表面还带有丰富的活性基团,可以通过一系列反应引入特定的官能团,丰富微球的特定功能,这显著拓宽了生物模板法制备的纳米磁性微球在功能吸附、酶固定载体、物质的控释、靶向给药等方面的应用前景。
1 磁性中空微球的结构特点
根据磁性物质在中空微球所处的位置不同将其分为:①核磁型中空微球(karyotype magnetic hollow microspheres),磁性颗粒游离于中空微球的空腔部位,呈分散状态[图1(a)];②壳磁型中空微球(shelltype magnetic hollow microspheres),磁性颗粒掺杂在其他材料表面[图1(b)]。这两种构型的磁性中空微球分别由不同的工艺制备而成。核磁型中空微球主要通过将磁性前体物质渗透分布到模板材料的空腔内,再通过液相高温水热反应生成磁性物质。而壳磁型中空微球是通过将磁性物质吸附或嵌合在模板材料的表面上形成,又或者是磁性物质的前体吸附或嵌合在模板材料的表面后经过固相高温反应生成掺合于模板材料中的磁性物质。这两种制备方法都可以生产具有磁性和特殊官能团的中空微球。这两种构型的磁性中空微球都具备良好的顺磁性,在外加磁场下能够被其吸引,而在撤掉外加磁场后又能够很好地分散。目前常用的磁性粒子主要有铁的氧化物(Fe3O4、γ-Fe2O3)[14-15]、金属合金(FePt、CoPt3)[16-17]、尖晶石型的磁铁物质(Mg-Fe2O4、MnFe2O4、CoFe2O4)[18]等。其 中,Fe3O4是应用最广泛的磁性粒子,因为其可通过水溶性铁盐的化学反应制备,且可以通过调节反应条件制备不同粒度的磁球。
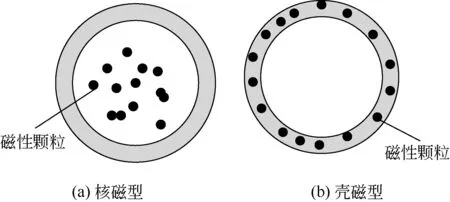
图1 磁性中空微球
2 生物模板法制备磁性中空微球工艺
利用生物质材料作为模板制备功能性纳米中空微球具有广泛的发展空间,其相对于传统制备方法具有更多的优势。首先,生物质材料具有来源广泛、可再生性强、成本低廉等优势。自然界存在多种多样的微纳米结构的生物材料,这些生物材料不仅形态大小均一,而且生物量巨大,可直接从外界环境中收集或者培养获得,如具有微纳米球形特征的花粉孢子、酵母微生物等陆生生物材料和微藻类水生生物材料,可通过大规模的种植和培养得到[19],而传统的化学材料的合成需要大量的化学试剂,会排放对环境产生巨大危害的污染物。其次,生物材料带有丰富的活性官能团,可通过化学反应修饰,如微藻细胞、酵母细胞壁通常由纤维素、甘露聚糖、葡聚糖等构成,含有丰富的糖苷键和羟基官能团,可进行一系列聚合反应引入特定的官能团或通过化学反应转换成新的活性基团[20-22],天然形成的官能团避免了使用繁琐的化学合成步骤。再次,生物材料热稳定性差,可通过高温热解炭化挥发,无残留[23-25],如利用软模板法将酵母在高温下煅烧可以得到无酵母残留的CeO2空心微球[25]。最后,如作为药物缓释载体,材料本身对身体无毒无害,生物相容性好。Diego-Taboada等[26]研究发现孢粉素微胶囊对人体内皮细胞无毒害效应。生物模板法制备磁性中空微球的设计思路分为两类:其一,以生物材料为模板引入磁性材料后去除,如通过高温煅烧,得到具有“空腔”结构的磁性微球,此方法为“生物软模板法”;其二,以生物材料自身为载体负载和引入磁性物质,而生物材料结构和外形不被破坏,以水热碳化法和高温厌氧法制备居多,此方法为“生物自模板法”。生物模板法制备的磁性中空微球主要在吸附材料、酶固定化载体、物质的封装与控释等领域有较突出的应用,本文将会一一介绍。
2.1 生物软模板法
以生物材料为模板介导制备的磁性中空微球可以在高温炭化过程中保持和生物材料一样完整的物理外形和尺寸,而生物基质会被炭化除去,无残留。如Zhao等[27]将酵母细胞浸渍于混合盐溶液中[Ce(NO3)3·6H2O,Fe(NO3)3·9H2O],并在室温下搅拌1h后再加入NaOH溶液,该混合体系在室温下静止数小时后沉淀,离心,用蒸馏水和乙醇洗涤后,沉淀物在80℃干燥6h,最后升温至600℃高温炭化2h,得到Fe掺杂的壳型CeO2中空微球。还可以将生物模板材料在高温炭化下制备中空磁壳微球后,进一步通过水热反应制备复合性磁微球。如Lu等[13]将松花粉在Fe(NO3)3溶液中浸泡一段时间,将浸泡溶胀后的松花粉在80℃下干燥2h后,在300~600℃下炭化1h,制备出γ-Fe2O3型中空磁微球。随后,将γ-Fe2O3型中空磁微球加入到含MgSO4和尿素的混合溶液中,磁力搅拌30min后密封于高压反应釜中,在160℃下反应10h,最后在室温下慢慢冷却形成的MgFe2O4/γ-Fe2O3中空微球(图2、图3)。一种多孔磁性微球ZnFe2O4/MgAl-LDH也可通过类似的方法制备。Sun等[28]将松花粉于Fe(NO3)3和Zn(NO3)2的乙二醇溶液中混合超声20min,然后将混合液在室温下静止10h,将沉淀物过滤后600℃炭化1h得到ZnFe2O4复合物。溶解一定量的MgSO4·7H2O和Al(NO3)3·9H2O于 蒸 馏 水 中,再 加 入ZnFe2O4复 合物,混合物在140℃高压釜中反应10h,冷却至室温后慢慢形成ZnFe2O4/MgAl-LDH中空微球。综上所述,利用生物模板法制备磁性中空微球的基本工艺流程可归纳为图4。

图2 利用松花粉制备MgFe2O4/γ-Fe2O3多孔微球的工艺流程

图3 SEM图及TEM图
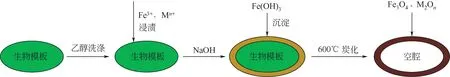
图4 生物软模板法的磁性中空微球制备工艺
2.2 生物自模板法
由于天然生物材料,如酵母、花粉孢子、微藻等具有天然的球形外观、具有耐酸碱的细胞壁[29]、其内容物可通过物理化学方法除去等特点,且生物材料表面具有的丰富天然活性基团,如羟基、羧基、氨基和酰胺官能团可与一些小分子化合物结合或与生物活性物质(酶、抗体、核酸等)反应,这些都有利于其自身作为模板材料使用。
2.2.1 浸渍-高温炭化法
将微生物类材料浸渍于含铁盐溶液中,使其表面吸附含铁离子,再通过惰性气体保护下的高温炭化形成表面具有磁性颗粒的中空炭化微球。孙予罕等[30]在水热反应釜中加入微藻和水配置成微藻悬浮液,并依次加入铁盐、有机酸和催化剂,密封后通入保护性气体置换反应釜内的空气,然后将吸附铁盐的微藻置于烘箱中炭化,获得壳磁性中空碳微球。王东升等[31]将微藻分散于4%硝酸铁水溶液中,充分搅拌12h后离心分离藻细胞,然后使用超纯水反复洗涤除去过量的硝酸铁,将清洗后的藻细胞分散至6%NaOH溶液中加热至105℃,冷凝回流2h。反应结束后将离心分离的藻细胞用超纯水洗涤数次,最后置于石英舟中在氮气气氛下600℃煅烧,获得壳磁性中空碳微球。浸渍高温炭化法的基本工艺流程可归纳为图5。
2.2.2 水热碳化法
水热碳化法是将生物材料置于密闭的水热反应釜中,以水为反应介质,在反应温度为200~300℃的亚临界水中加速有机物的水解和碳化,形成具有两亲性特点的材质[31-33]。毕磊等[29]采用绿藻藻粉和3价铁前体水溶液充分混合一段时间后,用蒸馏水充分清洗藻细胞,再将分离后的藻细胞分散后于氢氧化钠碱性溶液中105℃处理1~2h,将充分洗涤后的材料置于水热反应釜中200℃反应4h,最终得到内含多个Fe3O4磁性纳米内核的铃铛结构多孔微球(RMMCMs),平均粒径在30nm左右,球壁上存在15nm的孔道,微球内部的容积率达到80%,而且依据不同pH条件下磁性内核与BSA的可控释放的特点,使得该微球有望应用于物质的封装、磁分离以及磁操控下的靶向给药领域(图6、图7)。Cai等[34]利用Fe(NO3)3、Co(Ac)2、尿素和NH4F的水热反应,得到蒲公英花粉状多孔CoFeO4微球,微球直径为1μm左右,球表面孔尺寸为100~200nm,可负载抗肿瘤药物盐酸阿霉素后利用交变磁场下的磁效应实现对该药物的可控释放。水热碳化法的基本工艺流程可归纳为图8。
2.2.3 常温吸附法
常温吸附法制备磁性微球可将磁性纳米颗粒和中空微球的制备分开进行,再将高浓度磁性纳米颗粒吸附于中空微球上制备高磁性的磁性中空微球。如李黎明[35]将FeCl3·6H2O、FeSO4·7H2O和NH3·H2O利用共沉淀法制备磁性纳米Fe3O4,而后制得水基磁流体,最后利用表面吸附法使微藻与磁流体结合,使其藻细胞表面负载磁性纳米颗粒。
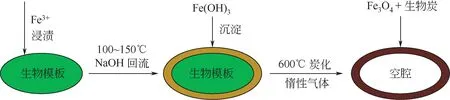
图5 浸渍-高温炭化法的磁性中空微球制备工艺
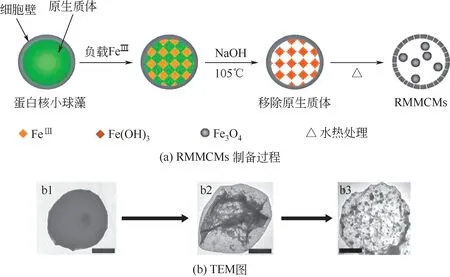
图6 RMMCMs的制备过程及TEM图

图7 RMMCMS的电镜图
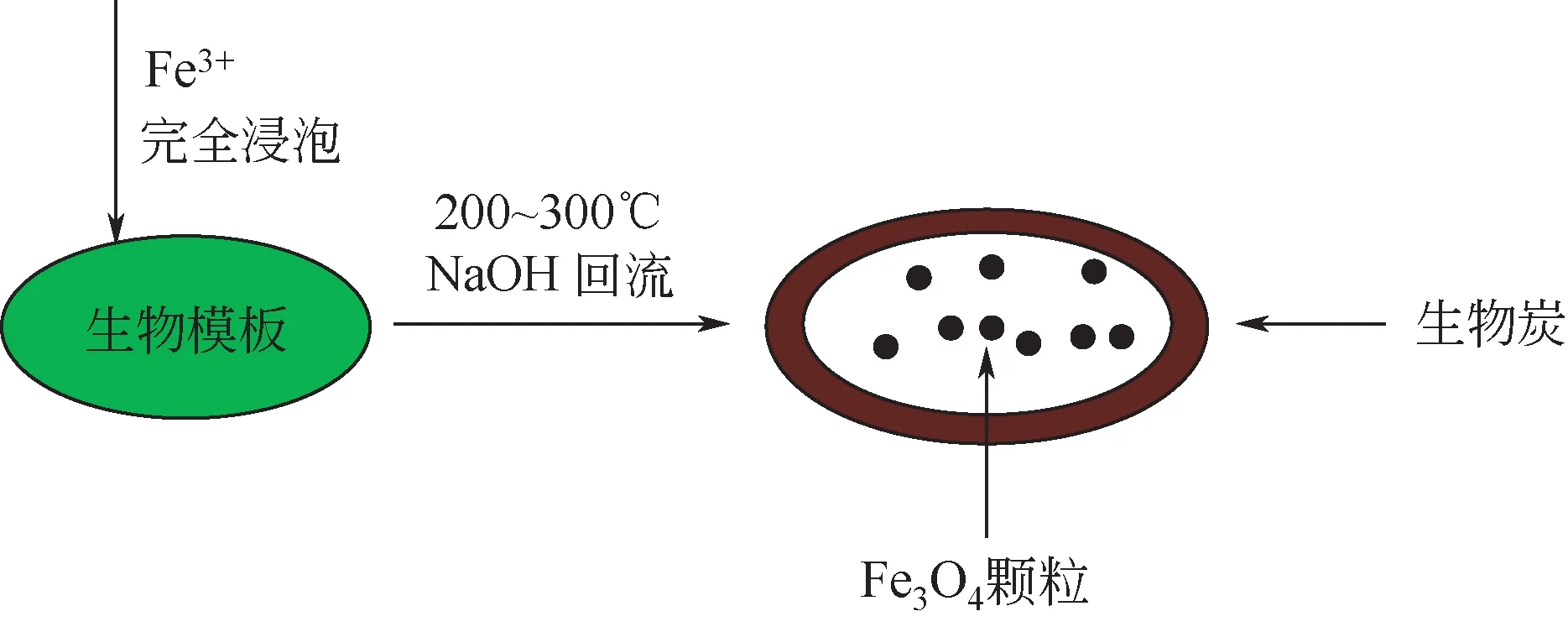
图8 水热炭化法的磁性中空微球制备工艺
(1)吸附-共沉淀法利用微藻吸附-共沉淀法可以制备磁性生物材料,而后进一步制备成磁性中空微球。李晨等[36-37]将FeCl3、FeSO4和盐酸混合配制成酸性铁盐溶液,然后加入20%的氨水,搅拌均匀得到棕色沉淀,将沉淀离心、洗涤、过滤,冷冻干燥后得到Fe3O4纳米粒子。磁性纳米粒子经过硫酸氢甲酯氨解预处理后,在表面生成一层无定形物质,能够增加其对生物细胞的吸附力。将磁性纳米粒子加入微藻培养液中混合振荡2~4天,完成微藻对磁性纳米粒子的吸附固定,得到磁性微藻生物吸附剂,用该磁性吸附剂对废水中的铅离子进行吸附,研究发现在合适的吸附条件下,最高可以除去95.7%的铅离子和93.5%的镉离子。通过类似的微藻吸附-共沉淀法可制备微藻基磁性石墨烯和生物炭。如路晏红等[38]在常温下将石墨烯超声分散在蒸馏水中并加入含Fe3+的溶液搅拌数分钟,然后在氮气保护下加入含Fe2+的溶液并搅拌,之后加入氨水溶液并搅拌2h,使溶液pH≥10,得到磁性石墨烯,干燥备用。之后将磁性石墨烯、还原剂、偶联剂分散在有机醇水溶液中并加入一定量生物炭,磁力搅拌1~2h,然后在真空下干燥备用。而后将所得混合物在500~700℃的氮气下高温裂解2h,洗涤后真空干燥备用。最后,将培养好的微藻与磁性石墨烯和生物炭按照一定比例混合,静止3~8h,得到微藻基磁性石墨烯和生物炭。吸附-共沉淀法制备磁性中空微球基本工艺流程可归纳为图9。
(2)高温炭化-共沉淀法王珏玉[39]将生物模板高温炭化后形成一定形貌的中空微球,再利用磁性颗粒的共沉淀方法制备磁性中空微球。如将灵芝孢子在马弗炉中于600℃、氮气保护下炭化4h制备中空微球,然后将其置于含Fe3+和Fe2+的盐溶液中,滴加氨水,40℃恒温过夜,共沉淀法制备灵芝孢子磁性中空微球。高温炭化-共沉淀法的基本工艺流程可归纳为图10。
微生物具有天然空腔和细胞壁结构,可以省去制备空腔的诸多步骤,相比以其他糖类物质为模板制备磁性中空微球具有显著的优势。主要通过软模板法和自模板法制备微生物磁性中空微球(表1)。软模板法以生物材料为模板,使其表面沉积和吸附可溶性磁性物质前体,再通过高温炭化除去生物模板材料,并形成磁壳性中空微球;自模板法利用生物材料本身吸附磁性物质,或在其表面或内部吸附和负载可溶性磁性前体物质,再通过高温炭化或水热碳化将其转变成磁性物质,与此同时,生物模板材料本身所带官能团得到修饰和转化。
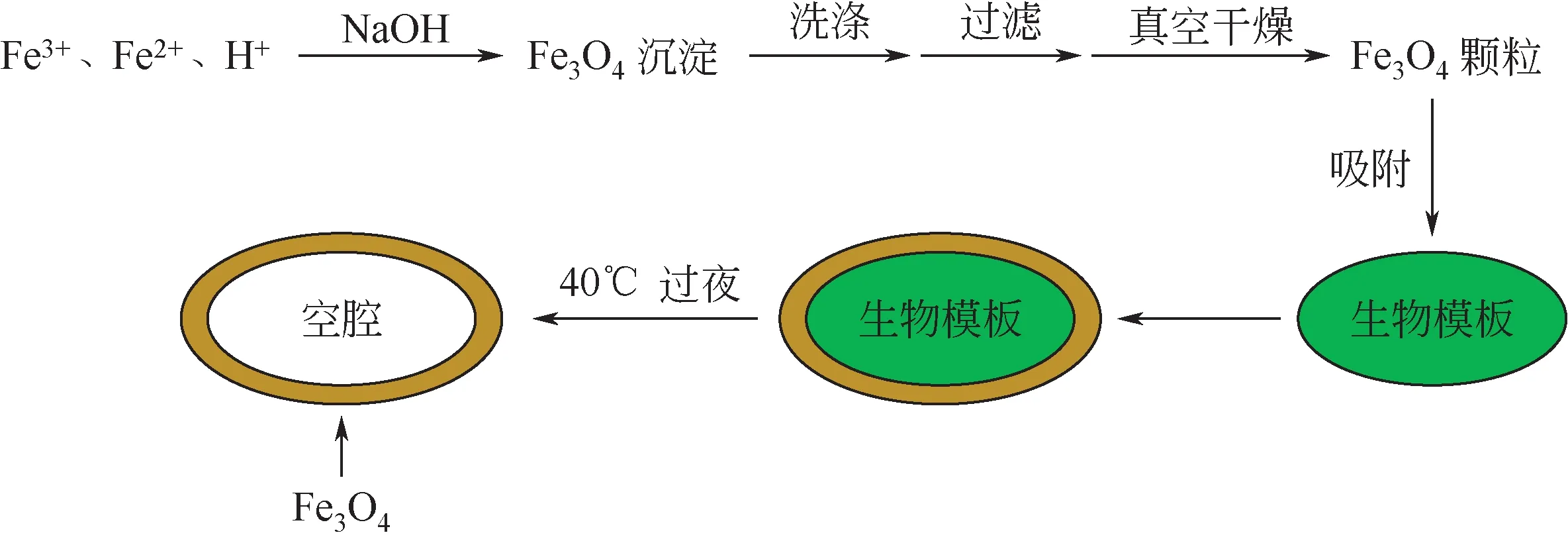
图9 吸附-共沉淀法的磁性中空微球制备工艺
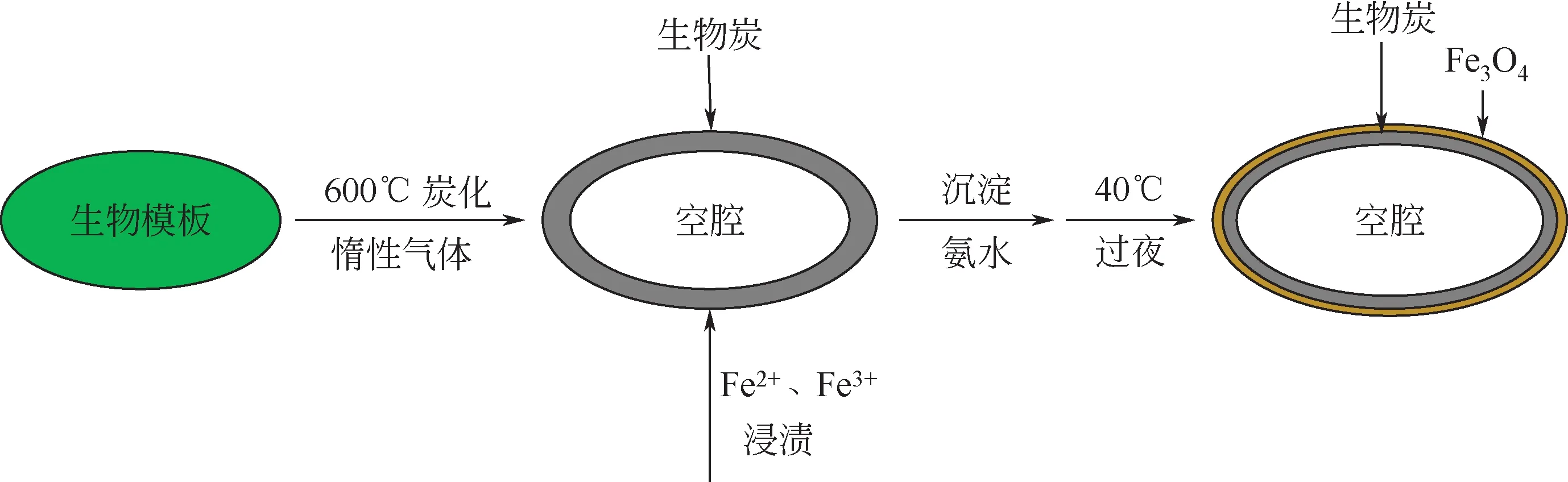
图10 高温炭化-共沉淀法的磁性中空微球制备工艺

表1 生物模板法制备磁性中空微球工艺特点
非生物类硬模板法制备磁性中空微球以壳核结构二氧化硅磁性纳米微球的研究居多,可采用两种策略(表2)。一种是以无机材料模板吸附表面活性剂,然后在模板粒子表面生长含磁性物质壳层,最后除去模板粒子以及表面活性剂,得到壳层具有磁性、内部空心的磁性中空微球[10]。另一种是以磁性颗粒为核,并在其表面包覆SiO2形成模板,再在模板上继续包覆功能性材料,通过除去模板形成内部磁性夹层空心的复合磁性中空微球[9-10]。以无机SiO2为硬模板的制备方法主要通过酸蚀或碱蚀破坏SiO2模板,从而达到一定中空结构的空间构象。
非生物软模板法可通过表面活性剂形成的囊泡、胶团和高分子组织等利用分子间的弱相互作用形成具有一定空间结构特征的簇集体,但这类软模板结构的稳定性较差,模板效率不够高[11,41-42]。欧阳兆辉等[41]以NiFe2O4纳米粒子作为磁性载体,钛酸丁酯做钛源,十二烷基磺酸钠和聚乙烯吡咯烷酮作模板剂,掺杂Co和Ce离子,惰性气氛下高温煅烧除去模板,制备得到(Co,Ce)-TiO2-SiO2/NiFe2O4磁性介孔微球。
非生物自模板法一般通过酸蚀和碱蚀无机材料制备多孔中空微球,然后通过吸附和负载磁性物质制备磁性中空微球。佟若菲等[46]将实心的二氧化硅微球用过碱性碳酸钠进行蚀刻反应,除去实心部分得到中空微球。周田等[12]通过共沉淀法将尖晶石铁氧体MeFe2O4包覆在中空微球表面制备SiO2/MeFe2O4中空复合微球。

表2 模板法制备磁性中空微球的技术特点
总之,以生物模板法和非生物模板法制备磁性中空微球各有优劣(表3)。非生物模板法制备中空磁性微球可选择多种无机和有机模板材料,材料来源广泛,操作过程繁琐复杂;模板材料和化学试剂的大量消耗提高了微球的制造成本,也对环境造成了污染;非生物模板材料在去除的过程中条件较为苛刻,常导致微球结构的破坏或模板去除不完全。而生物模板材料正好可弥补非生物模板材料的缺点,如生物材料对环境友好,模板材料易除去且无残留,并且由于其具备天然的中空球状结构,可以减少工艺流程中的制备步骤[47-48],但是生物模板材料需要进行大规模的培养和收集,材料来源受限。
3 磁性中空微球的开发和应用
功能性磁性中空微球比表面积大,中空结构可实现物质的装载和释放,具有优异的电化学性能和磁响应特性,便于产品的富集、分离,可在外加磁场的作用下移动到特定药物靶点,在生物分离工程、物质的封装与控释、酶催化剂载体开发等领域发挥了重要作用。
3.1 吸附材料的应用
生物模板磁性微球具备较大的比表面积,具有优异的吸附能力,并且由于微球具有铁磁性,在吸附完成后很容易实现固液分离,因此在物质的吸附、分离和作为酶催化剂的开发和应用方面具有广泛的应用。李黎明[35]经研究发现,磁性小球藻细胞壁含有的蛋白质和多糖的功能基团能与染料分子结合,具有吸附剂的特质,可用作染料废水的脱色剂,对刚果红和亚甲基蓝的吸附量分别可达169mg/g和216mg/g,而吸附后的磁性小球藻可通过磁铁的吸引而快速分离(图11)。
3.2 酶固定化载体的应用
利用生物磁性微球所携带的疏水区域可以吸附酶的非功能疏水区而进行酶的固定化,利用微球的磁性特征可以将所吸附的酶快速分离和回收,减少离心分离时间和能耗,利用磁性中空微球易通过磁场进行固液分离的特性可将其作为固定化载体进行酶催化剂的吸附,便于酶的分离和回收。以一种介孔SiO2/Fe3O4磁性复合微球为固定化酶载体物理吸附漆酶,吸附量可达280.7mg/g。固定化漆酶的热稳定性和pH稳定性都明显高于游离漆酶[45]。利用分散聚合法制备的多孔中空微球Fe3O4/P(GMADVB-St)本身带有环氧功能基,可直接与酶分子上的氨基连接,共价固定化假丝酵母脂肪酶,固定效率达到了95.92%,具有良好的pH和温度耐受性,固定化酶的活力回收高达73.25%,重复使用10次后活力保留约80%,具有较大的工业应用价值[49]。孢粉素微胶囊也可作为酶的固定化载体并将脂肪酶封装于其内部,封装的脂肪酶表现出对底物硝基苯棕榈酸酯更高的水解效率和更强的选择性水解萘普生的能力,而且固定化酶的重复利用率也大幅提高[50]。刘潇[44]将Fe3O4/SiO2微球进行表面改性,使微球表面羟基被硅烷偶联剂的氨基所取代,氨基再与甲基壳聚糖(CMCS)表面的羧基反应制备中空Fe3O4/SiO2@CMCS磁性复合微球。该微球作为果胶酶固定化载体具有很好的pH和温度稳定性,载酶量高达231.5mg/g,在4℃下放置40天后活性是游离酶的4倍。

表3 生物模板法和非生物模板法制备磁性中空微球技术指标对比

图11 磁性小球藻吸附刚果红后的磁分离过程
3.3 物质的封装与控释
磁性中空微球因其具有多孔中空的结构和磁响应特性,具有选择性容纳和释放某一特定尺寸物质的能力[45,49]。毕磊等[29]将一种蛋白核小球藻经过水热碳化后制备的多磁核中空微球进行牛血清白蛋白的控释,研究发现,当溶液中pH为5时,中空微球里的蛋白含量远远大于溶液中的蛋白含量,蛋白容载能力大于600mg/g;当溶液pH调至7时,蛋白逐步从微球中释放到溶液中;继续将溶液的pH调至9时,绝大部分的蛋白都逃逸至溶液中,此现象可解释为在不同pH下蛋白和磁性中空微球之间的静电相互作用的变化引起的。徐雪[9]制备得到的两种类型的Fe2O3/TiO2磁性复合中空微球可作为药物布洛芬的缓释材料,载药量分别达到33.1mg/g和92.7mg/g,并在24h内药物的释放率分别为70%和100%。刘潇[44]制备的中空Fe3O4@SiO2@CMCS磁性复合微球在pH=7.4时可对药物顺铂进行缓释,在释放的100h内,释放量可达90%。Zhao等[51]制备了介孔SiO2包覆的磁性微球,并用作药物载体,在模拟的体液环境中前24h释放较快,70h内可以释放87%的药物。
利用生物软模板法制备的磁性中空微球和传统方法制备的磁性中空微球在结构上相比无明显差别,但生物软模板法制备工艺比传统方法更为简便,制备条件更容易控制。而利用生物自模板法具有更明显的优势。首先,因其具有很好的生物相容性,对人体无毒无害;其次,由于生物材料具有的亲水官能团易于被化学修饰,从而可以通过改变微球的亲疏水特性轻松实现对物质的封装与控释。如经过表面加乙酰基改性的孢粉素微胶囊可以从油水乳浊液中高效分离和富集油脂,通过简单的碾压又可以实现油脂的再释放[52]。再次,可通过水热碳化法设计合成具有特定两亲性的磁性中空微球,实现在特定的pH环境中选择性封存和释放药物。Guan等[33]发现,这种两亲性中空碳微球中主要存在烷基类碳和芳香类碳两种类型的含碳物质,烷基类碳主要来源于非碳化有机物(可离子化官能团的主要贡献者),而芳香类碳则主要来源于碳化有机物(疏水性片段的主要贡献者)。通过调节pH可实现可离子化官能团的质子化和去质子化过程,从而调节磁性中空微球的亲疏水性。而这两种类型的含碳物质在微球中的比例则可以通过控制水热时间和温度来加以调节。所以,可以通过合成特定成分的磁性中空微球来实现对不同pH的响应,使其通过磁场到达病症部位时释放药物,实现磁性靶向治疗的目的。
4 结语
相比于其他化学模板材料,微生物模板材料兼具硬模板材料较稳定的物理构型和软模板材料易于碳化挥发除去的特点,是较理想的功能性微球的模板材料。特别是微生物模板材料具有天然的中空结构[47-48]且其细胞壁含有丰富的可修饰官能团,可通过化学反应接上特殊官能团或改变其亲疏水性制备符合需要的两亲性中空微球[21,32]。利用微生物模板材料制备磁性微球条件较为温和、无污染,制备的磁性中空微球具有无毒和体内不易分解的特性[53],特别适合于在食品、医药等行业的应用,具有很好的生产应用前景。
虽然生物材料作为模板具有如上所述比传统材料在某些方面更优异的性能,但作为工业化应用材料,其生产成本和使用寿命还需要进行很好的评估。首先,如作为物质吸附和酶的固定化材料,生物模板材料在多次循环使用下是否有较长寿命而具备可观的经济性,需通过试验进行生产评估,但如作为靶向给药和药物缓释等一次性载体,可不受重复使用条件的限制。其次,可制备特定尺寸微球的生物材料来源有限,需要大规模制备微生物细胞,这需要相关的微生物培养技术和设备支持;最后,微球的制备工艺受限于生物模板材料的尺寸和组成成分。不同的生物材料尺寸和组成成分各有不同,即使是同一种类生物材料,在不同的培养条件下,组成也有所差别,因此,利用生物材料为模板制备磁性中空微球的工艺要实时监控和改进,这需要在生产过程中进行全程监测和控制。总之,生物模板材料因具有某些其他模板材料不可替代的优势受到越来越普遍的关注,将在特定的应用场景中发挥重要作用。

