前循环大血管闭塞患者机械取栓后脑水肿严重程度及预后影响因素分析
张梦柯, 石秋艳, 杨 斌, 王 迪, 张春阳, 孙 原, 高敬华
急性缺血性脑卒中(acute ischemic stroke,AIS)具有发病率高、致残率高、死亡率高的特点,其中大血管闭塞性脑梗死(large vessel occlusion,LVO)会明显增加不良预后及90 d的死亡率,而大约80%的LVO-AIS发生在前循环[1]。机械取栓治疗可以快速开通血管,及时挽救缺血半暗带区。大血管闭塞往往会伴随严重血脑屏障损伤,导致脑组织肿胀,恶性脑水肿会使患者临床症状迅速恶化,患者几天内的死亡率接近80%[2]。目前临床研究对LVO-AIS机械取栓术后脑水肿的研究相对较少,本研究想探讨机械取栓后LVO-AIS患者脑水肿严重程度的预测因素,及脑水肿程度与相关因素对临床预后的影响。
1 资料与方法
1.1 一般资料 纳入标准:(1)通过影像学明确前循环大血管闭塞的急性缺血性脑卒中患者,年龄≥18岁;(2)卒中前改良Rinkin Scale量表(Modified Rankin Scale,mRS)评分0分~1分;(3)美国国立卫生研究院卒中量表(The National Institutes of Health Stroke Scale,NIHSS)评分≥6分;(4)发病时间在24 h内,超过6 h的患者通过核磁共振DWI或CT灌注评估存在临床症状严重程度与梗死体积不匹配;(5)患者家属对手术及术后风险知情并签署知情同意书。排除标准:(1)近期合并颅内或椎管内手术;(2)合并急性出血倾向;(3)合并血流动力学不稳定。选择2018年1月-2020年7月在我院行机械取栓术的急性前循环大血管闭塞的缺血性脑卒中患者共83例,其中男性53例,女性30例,年龄在41~86岁之间,平均年龄为(63.28±9.38)岁。
1.2 研究方法 符合超早期静脉溶栓适应证的患者给予阿替普酶静脉溶栓治疗。超过静脉溶栓时间窗、静脉溶栓后患者神经功能缺损症状改善不明显或进一步恶化,以及存在静脉溶栓禁忌证的大血管闭塞患者进入导管室行机械取栓治疗。具体操作:采用改良Seldinger技术穿刺股动脉,置入8F主动脉鞘,行主动脉弓及全脑血管造影术,发现闭塞部位,送入6F导引导管及泥鳅导丝,路径图指引下沿导引导管送入微导丝及微导管,穿过闭塞部位,沿微导管送入取栓支架,进行取栓,取栓结束后再行造影明确血管再通情况。
1.3 观察指标 患者年龄、性别、是否合并高血压、糖尿病、冠心病、房颤病史、TOAST分型、入院NIHSS评分、抗血小板药物使用史、吸烟史、饮酒史、闭塞血管的部位(分为颈内动脉(Internal Carotid Artery,ICA)闭塞、大脑中动脉(Middle Cerebral Artery,MCA)MI段闭塞、大脑中动脉M2段及远端闭塞、是否给予静脉溶栓治疗,闭塞血管是否成功再通,发病到手术的时间、入院到手术时间、股动脉穿刺到手术完成时间、侧支循环评分。再通定义:通过改良脑梗死溶栓血流分级系统(Thrombosis in Cerebral Ischemia Grade,mTICI)进行评价,血管再通定义为mTICI为2b级或3级[ 3]。侧支循环评分:采用Souza等人[4]提出的侧支循环评估方法对CTA图像上的侧支血管进行评估,0级:无侧支血管的面积>50%MCA~M2段某一支供血区域;1级:侧支血管减少面积>50%MCA~M2段某一支供血区域; 2级:侧支血管减少面积<50%MCA~M2段某一支供血区域;3级或4级:与对侧相同或比对侧增多。将侧支循环0级~1级定义为较差侧支循环;2级~4级定义为良好侧支循环。
1.4 主要结果指标
1.4.1 脑水肿严重程度 脑梗死患者发病48 h左右复查头部CT,我们将轻度脑水肿(Cerebral Edema,CED)定义为局灶性脑肿胀小于半球的三分之一 ;中度CED 定义为局灶性脑肿胀大于半球的三分之一 ;重度CED定义为局灶性脑肿胀伴中线移位[5,6]。所有影像学结果由两位有经验的影像学医师(有5 y以上的工作经验),采用双盲法对所有影像资料进行分析,结果不一致时经协商后达成一致。
1.4.2 电话随访患者3个月的预后 使用改良Rankin评分量表判定预后,3个月后mRS≤3分认为预后良好;mRS 4分~6分认为预后不良[7]。
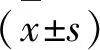
2 结 果
2.1 不同程度脑水肿患者一般资料比较 3组不同程度脑水肿患者在高血压病史、闭塞部位、入院NIHSS评分、侧支循环程度、血管再通率比较差异有统计学意义(P<0.05)(见表1)。
2.2 脑水肿影响因素的有序Logistic回归分析 将高血压病史、闭塞部位、入院NIHSS评分、侧支循环状态、血管是否再通等影响因素纳入有序Logistic回归分析。对变量进行赋值:预后(不良=0、良好=1);脑水肿程度(轻度=0、中度=1、重度=2);高血压(无=0、有=1),闭塞部位(颈内动脉=0、大脑中动脉MI段=1、大脑中动脉M2段及远端=2),NHISS评分(NHISS评分≤15分=0,NHISS评分>15分=1);侧支循环(较差=0、良好=1);有无血管再通(否=0、是=1)。有高血压病史、基线NHISS评分>15分与脑水肿严重程度呈正相关,血管M2段及远端闭塞、成功血管再通与脑水肿严重程度呈负相关(见表2)。
2.3 机械取栓后急性脑梗死患者预后单因素资料分析 两组在高血压史、脑血管闭塞部位、入院NIHSS评分、侧支循环状态、有无血管再通、脑水肿严重程度之间有明显差异(P<0.05)(见表3)。
2.4 机械取栓后急性脑梗死患者预后影响因素二分类Logistic回归分析 将脑水肿严重程度、入院NIHSS评分、侧支循环状态、有无血管再通、脑血管闭塞部位纳入机械取栓后患者预后影响因素Logistic回归分析。因素赋值同前。重度脑水肿及基线NHISS评分>15分与LVO-AIS机械取栓后3个月良好预后负相关,良好侧支循环及成功血管再通与良好预后正相关(见表4)。
表1 行机械取栓术后不同程度脑水肿患者一般资料比较
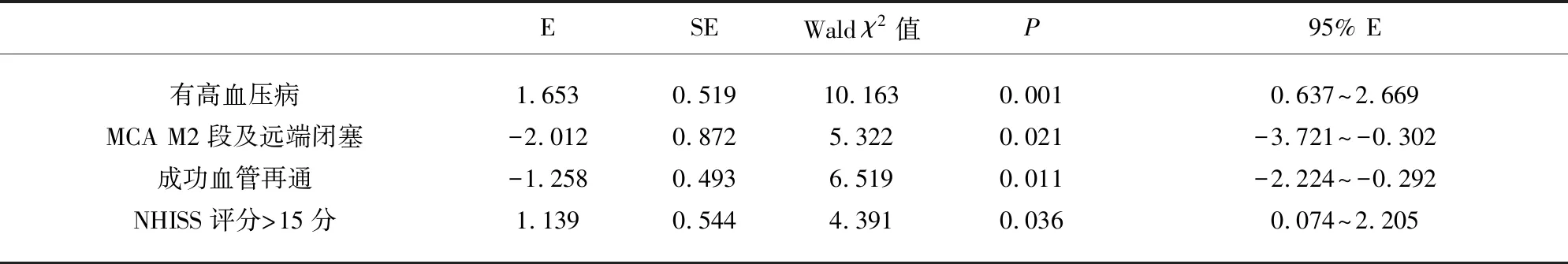
表2 行机械取栓后脑水肿的影响因素多因素Logistic回归分析
表3 机械取栓后急性脑梗死患者预后单因素分析
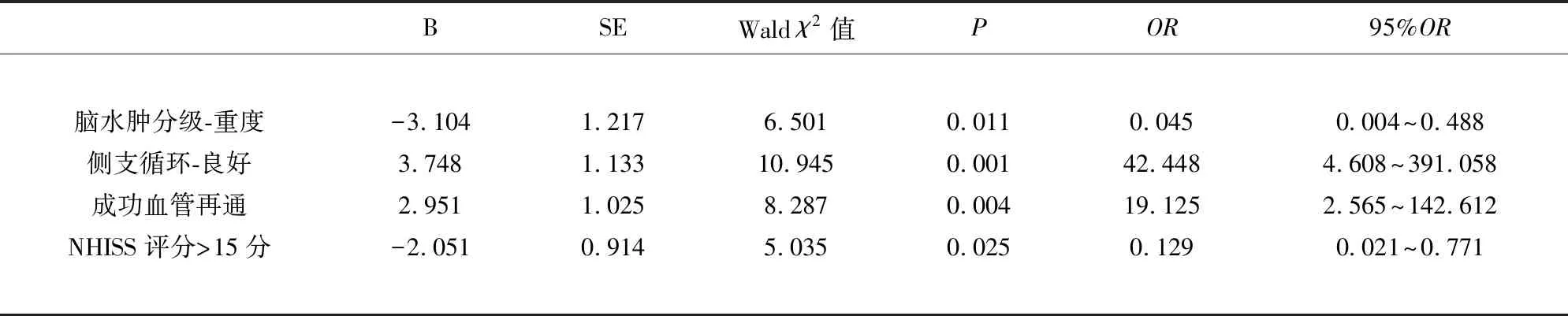
表4 机械取栓后患者预后多因素Logistic回归分析
3 讨 论
既往有研究认为血管再通,缺血的脑组织恢复血供后,一些炎症因子生成及氧化应激等机制会加重脑组织损伤,因此也会加重脑水肿[8]。而最近一项大型研究表明,静脉溶栓术后再通的患者中度及重度脑水肿的发生率明显低于非再通的患者[9],也有一项单中心研究发现机械取栓术后成功的再通,减少了72 h内脑组织中线移位≥5 mm 的发生[10 ]。而本次研究刚好也验证了血管再通可以减轻脑水肿的严重程度,脑水肿是由于血脑屏障通透性逐渐增加和损伤的这一过程而引起,而血管再通、血流恢复会减轻血脑屏障继续损伤。
有研究证明基线NIHSS评分、高密度动脉体征、基线血糖、意识障碍和影像学急性梗死体征是急性脑梗死静脉溶栓后脑水肿严重程度的独立预测因子[6]。由于观察指标不同,本研究多因素回归分析结果示基线NIHSS评分>15分、高血压病史、血管无再通、脑血管闭塞部位为前循环大血管闭塞患者机械取栓后脑水肿严重程度的独立预测因素。基线NIHSS评分分数越高,提示患者脑组织损伤越重,毛细血管内皮功能障碍也就越严重,因此基线NIHSS评分>15分提示患者取栓术后脑水肿严重程度较高。高血压病会伴随脑血管内皮损害、粥样硬化严重及小血管玻璃样变[11],一旦发生脑缺血事件,脑血管损伤会更严重,本研究结果示有高血压预示取栓后较严重水肿的发生。本研究发现脑水肿严重程度还与脑血管闭塞部位相关,与颈内动脉与大脑中动脉M1段相比(P>0.05),而大脑中动脉M2段及远端闭塞脑水肿严重程度较低(P<0.05),颈内动脉及大脑中动脉M1段闭塞往往导致脑梗死面积相对较大,同时侧支循环供应血流较差,虽然本研究表明侧支循环与脑组织水肿程度不独立相关,这可能由于样本量不足导致,文献发现较差的侧支循环会增加不良梗死的进展[10]。
德国一项大型回顾性研究发现年龄、无院内转移、基线NIHSS评分、脑梗死面积及成功再通率为神经功能预后的预测因子[12]。本研究分析证明,重度脑水肿、NIHSS评分>15分机械取栓后预后不良的独立预测因素,良好侧支循环及成功血管再通为预后良好的独立预测因素。既往研究表明恶性脑水肿回导致机械取栓患者功能独立率低,90 d死亡率明显增高,而本研究的结果发现中度脑水肿与轻度脑水肿对预后影响无明显差异,重度水肿会导致90 d不良神经功能恢复状态发生率增加。
综上所述,基线NIHSS评分>15分、高血压病史、血管无再通、脑血管闭塞部位为前循环大血管闭塞患者机械取栓后急性期脑水肿严重程度的预测因素。脑水肿严重程度、基线NIHSS评分、是否血管再通及侧支循环状态为90 d后神经功能恢复的预测因素。

